以乏力为表现的肝豆状核变性1例
周俊 贺学强 熊红 申秋艳 黄应文 莫春荣 邓园园
患者,男性,25岁,因发现肝功能异常8年余,乏力1周入院。患者8年前发现“转氨酶高”,曾多次就诊当地医院,完善肝炎分型、腹部彩超等相关检查,未见明显异常,予护肝治疗后病情缓解。1年前因腹痛就诊我院,诊断为“胆囊多发结石并胆囊炎;肝硬化失代偿期、食管静脉曲张(F3CbLsRC++E-,重度)、慢性肝衰竭、门脉高压性胃病、脾亢、腹水、电解质紊乱(低钾、低钠、低钙) ”,予抗感染、护肝、输注血浆等治疗后病情好转出院,出院后继续保肝、利尿等对症治疗。患者此后分别因消化道出血(解黑便)于2020年11月15日、2021年3月10日在我科住院,期间行食管静脉曲张套扎止血等对症治疗,症状缓解后带药出院。1周前患者无明显诱因出现乏力,且患者家属诉患者行走步态与往常不一样,故再次入院复查。否认疫区接触史,否认外伤,无过敏史。无烟酒嗜好,无肝炎、结核等传染病病史,否认家族遗传病病史。入院时查体:体温36.5℃,脉搏82次/min,呼吸20次/min,血压132/70 mmHg(1 mmHg=0.133 kPa),体重80kg,身高170cm。神志清楚。浅表淋巴结无肿大。颈静脉未见怒张,数字结点试验阴性,双肺呼吸音清,未闻及干湿性啰音。心律齐,各瓣膜听诊区未闻及病理性杂音。腹膨隆,上腹轻压痛,无反跳痛及肌紧张,肝脾肋下未扪及,墨菲氏征阴性,肠鸣音5次/min,移动性浊音阳性。双下肢轻度水肿。
辅助检查
血常规:血小板总数 56×109/L。肝功能:总胆红素 88.2 μmol/L、直接胆红素 27.5 μmol/L、谷草转氨酶 68 U/L、总胆汁酸 36.6 μmol/L、白蛋白 27.5 g/L。凝血功能:凝血酶原时间 18.5 s、凝血酶原活动度 40.9%、国际标准化比值 1.57、纤维蛋白原 1.77 g/L。肝炎病毒分型、免疫I组、风湿三项、抗核抗体、抗平滑肌抗体、微量元素七项(铜、锌、铁、钙、镁、铅、汞)未见异常。多次大便寄生虫虫卵(-)、血浆氨正常。腹部CT(图1):①肝硬化、脾大、少量腹水;②肝内多发再生结节。患者入院后有步态异常,结合相关病史,考虑肝性脑病可能性大,故积极护肝、灌肠、抗肝性脑病、护胃等对症处理,但患者乏力无明显改善,且反复表现步态异常。故予查头颅MRI(图2、图3):考虑肝豆状核变性,请结合临床。眼科角膜检查:可见K-F环(图4)。进一步完善铜蓝蛋白 43.7 mg/L。24 h尿铜 115.1 μmol/L。患者及家属拒绝行肝活检测定,但临床表现、MRI表现、眼底检测符合肝豆状核变性诊断。
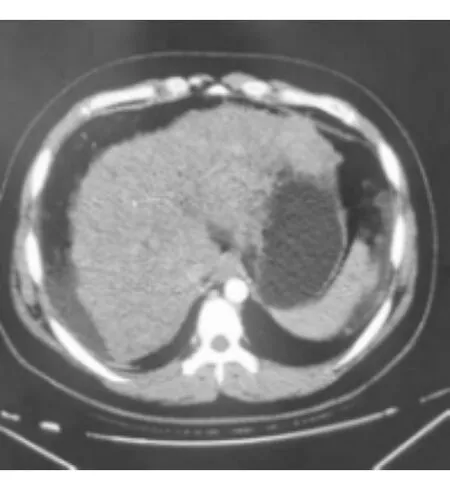
图1 腹部CT
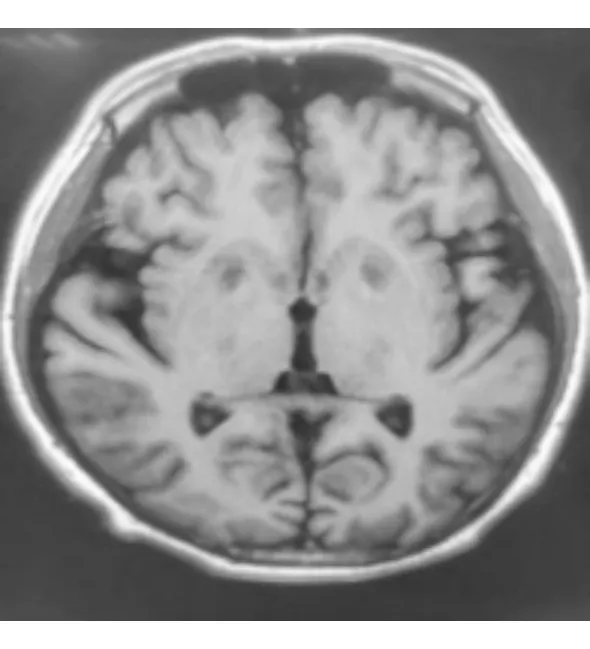
图2 头颅MRT
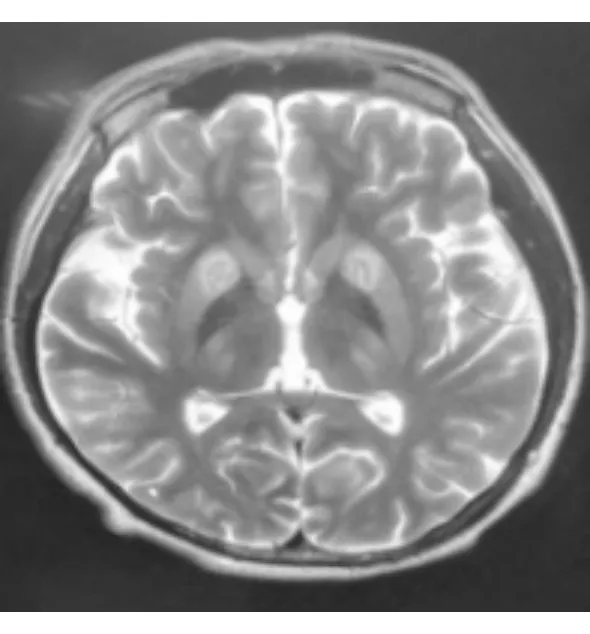
图3 头颅MRT
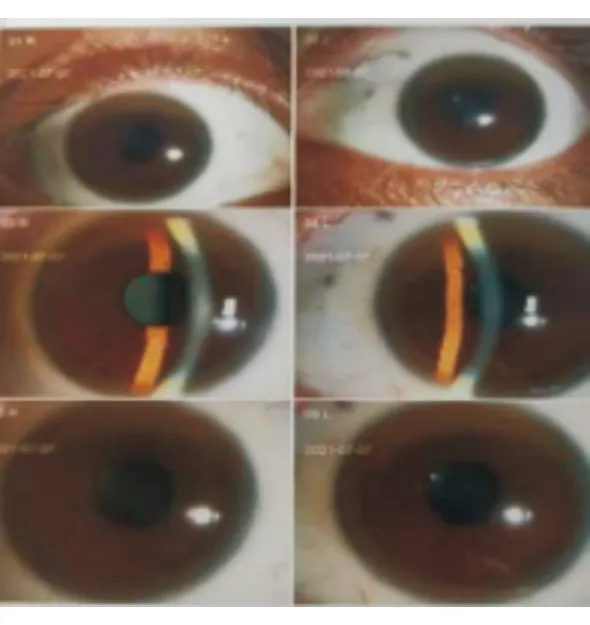
图4 眼科角膜检查
诊断与治疗:Wilson病,治疗上予低铜饮食、驱铜、护肝等对症治疗。
出院后随访:患者目前驱铜治疗过程中,近3个月无乏力、精神行为异常等表现。
讨论肝豆状核变性(hepatolenticular degeneration,HLD)也称Wilson病(WD),是一种罕见的常染色体隐性遗传的铜代谢异常疾病,分为脑型、肝型、其他类型及混合型,主要临床表现为进行性加重的肝硬化、精神症状及角膜色素(Kayser- F1eischer ring, K-F) 环等。全球的发病率约1/3000~1/100 000,致病基因携带者约为1/90[1]。国外一项流行病学统计发现该病年平均发病率为3.8/百万人,患病率为38.7/百万人,且呈逐渐上升趋势[2]。该病早期影响肝脏,临床症状不明显,后期主要表现神经精神症状,而在青少年人群中,早期可仅为情绪波动、性格改变、学习能力下降等,甚至无症状,易被忽视,从而漏诊、误诊[3-4]。而作为最精准的诊治手段——全基因组测序分析,发现其遗传患病率高于临床流行率,分析可能存在不完全的外显或有尚未确定的修饰基因有关[5],这种明显的差异也解释了高漏诊率的原因。
在本病例中,一位没有肝病、精神疾病家族史的青年患者,因表现出肝硬化、乏力、步态异常,完善各方面检查,排除各种常见急慢性肝炎(病毒性、自身免疫性、药物性、酒精性等)、癫痫、帕金森病、韦尼克脑病、慢性溶血等常见病因,且充分抗肝性脑病治疗后仍效果欠佳,最终经头颅MRI、眼底K-F环确诊,血铜蓝蛋白测定佐证,驱铜、限铜等对症治疗,患者症状逐渐缓解。通过这个临床病例,我们强调在不典型病因下肝功能受损患者,在排除相关并发症后需高度警惕罕见病。肝豆状核变性与许多神经代谢疾病不同,临床表现多样,故诊断困难。
头颅磁共振成像(magnetic resonance imaging, MRI)具有分析大脑解剖图像、功能信息和代谢信息等研究的重要价值。近年MRI被用来研究WD的发生原因、诊疗,且获得显著成果,敏感性优于CT,如典型的MRI发现脑桥、中脑和基底神经节的T2加权成像中存在对称高强度或混合强度(图4),已列为临床诊断标准之一[6]。同时T2加权成像的高、低信号可反应铜沉积于脑部的病理、生理过程,且随着病情的治疗,病灶可逐渐变小、变浅,对评估疾病的病因和演变有着重要意义[7]。无症状患者中有20%~30%,肝病型中有40%~75%可发现脑部MRI改变[8]。最新指南提出头颅MRI可作为监测疾病严重程度和治疗效果的重要方法,我国是WD高发国家,筛查高频致病的ATP7B基因及查全长编码区及其侧翼序列的致病变异[3, 9],相比头颅MRI对评估疾病的病因和演变,后者无创、更实用、更减轻疾病经济负担及减少医疗资源消耗[10],且对于基层医院无法完善铜蓝蛋白测定、尿铜排泄、肝活检铜定量检查时,影像学检查对于提高该病的确诊率显得尤为重要[3],而头颅MRI作为非侵入性、全面的技术,价格便宜而被广泛应用到临床,并且为确定WD的潜在机制和较早诊断提供了新思路。
利益冲突声明:所有作者均声明不存在利益冲突。

