高效液相色谱—荧光法检测鸡蛋中氟喹诺酮类药物的残留量
韦 伟,刘付祥,王文涛
(清镇市农产品质量检测站/清镇市农业产业服务中心/清镇市农业广播电视学校,贵州 清镇 551400)
氟喹诺酮类药物(FQS)是第3代哇诺酮药物,主要包括恩诺沙星(ENR)、达氟沙星(DAN)、环丙沙星(CIP)、沙拉沙星(SFX)等。由于养殖行业对农产品质量安全的责任意识不强,存在部分违规使用兽药、抗生素及违禁药品和不严格执行休药期规定等诸多问题,使得动物性产品中兽药残留超标[1-2]。生活中,当过多食用含有药物残留的动物性食品后,通常不表现为急性毒性,而是药物在人体不断蓄积,对人体神经系统、消化系统、泌尿系统等多个系统造成损害[3],更容易诱导人类致病菌对其耐药性的增强,不利于该类药物对人类疾病的治疗[4]。农业部于2002年已发布第235号公告《动物性食品中兽药最高残留限量》中规定环丙沙星、达氟沙星、恩诺沙星、沙拉沙星在鸡蛋中不得检出。因此,不断提高食品安全监管能力和水平,利用有效检测技术测定动物性食品中兽药残留,对坚决捍卫人民群众舌尖上的安全尤为重要。
近年来,国内外已有诸多有关FQS残留在动物组织中的测定方法的报道[5-8]。主要有高效液相色谱法(HPLC)、液相色谱-串联质谱法(HPLC-MS/MS)及酶联免疫分析法(ELISA)等。其中,HPLC法具有应用范围广、分离能力强、检测工作成本低、样品易回收等特点,在实际工作中更具推广性和实用性,但因仪器设备、环境条件等不同导致相关测定方法与行业标准偏离较大,且回收率不稳定。因此,本试验针对县级检验检测机构常用的《农业部781号公告-6-2006 鸡蛋中氟喹诺酮类药物残留量的测定 高效液相色谱法》检测过程进行优化,通过标准曲线、回收率试验、检出限试验和精密度试验等,以期为鸡蛋中氟喹诺酮类药物残留量的测定提供参考。
1 材料与方法
1.1 仪器设备
试验主要仪器设备:高效液相色谱仪(UiMate3000-FLD,Thermo Scientific,美国)、酸度计(PHS-3C,上海)、高速离心机(Thermo Scientific,美国)、组织匀浆器(Equl-kinematica,瑞士)、固相萃取柱(300 mg/mL)、有机滤膜(0.22 μm)及电子天平(0.01 g)等。
1.2 试剂材料
环丙沙星(C17H18FN3O3)、达氟沙星(CI9H20FN3O3)、恩诺沙星(C18R20FN3O3)、沙拉沙星(C20R17F2N3O3)标准样品,标准值均为100 μg/mL(农业部环境保护科研监测所);乙腈(色谱纯,美国BCR色谱试剂)、三乙胺(纯度≥99.0%,广东)、磷酸二氢钾(分析纯,纯度≥85.0%,北京)。
1.3 色谱条件
色谱柱:Thermo C18柱,参数4.6×250 mm。检测波长:激发波长280 nm;发射波长450 nm。流速:1.0 mL/min。柱温:35 ℃。进样量:20 μm。流动相:0.05 mol/L磷酸/三乙胺溶液-乙腈(81+19),使用前过0.22 μm滤膜。
1.4 样品制备
按标准称取样品(2±0.05)g,置于匀浆杯中,加提取液磷酸2.0 mL,搅匀振荡10 min,5000 r/min 离心10 min。取上清液立即转入另一离心管中。再用提取液磷酸盐2.0 mL重复提取一次,洗残渣,搅匀,振荡和离心。然后,合并两次提取的上层清液于同一离心管中,加入水饱和的正己烷10 mL,振荡5 min,5000 r/min离心10 min,用吸管将上层正己烷絮凝状固体仔细吸净弃去,在下层溶液中再次加入水饱和正己烷10 mL,振荡,离心。同样,再弃去上层正己烷,下层为备用液。然后,将C18固相萃取柱(300 mg/mL)安装于固相萃取装置,并依次用乙腈5 mL,乙腈(30%)-缓冲液5 mL和磷酸盐提取液5 mL润洗过柱,取备用液全部过柱,再用水5 mL过柱冲洗。加1 mL流动相洗脱过柱,收集洗脱液作为试样溶液,溶液过滤膜(0.25 μm)后供高效液相色谱分析。试验中,对《农业部781号公告-6-2006鸡蛋中氟喹诺酮类药物残留量的测定 高效液相色谱法》检测过程进行优化,磷酸取液体积调整为20 mL,分两次提取;备用液过柱分取5 mL;流动相洗脱过柱的流动相中乙腈比例调整为35%。
1.5 结果计算
2 结果与分析
2.1 样品提取与净化
本试验结合农业部781号公告-6-2006鸡蛋中氟喹诺酮类药物残留量的测定方法,并在前期的"鸡蛋中氟喹诺酮类药物残留量检测方法"相关研究报道基础上[9-12],进一步提高环丙沙星、达氟沙星、恩诺沙星、沙拉沙星的检测灵敏度继续进行方法确认和验证。研究表明,多数喹诺酮类在C-3含有酸性的羧基,C-7位连接有含氮碱性的哌嗪基等,属酸碱两性化合物,易溶于酸性或碱性溶剂,通过实验对比甲醇、乙腈和磷酸盐三种提取液,磷酸盐提取液杂质少、回收率高,效果最佳[10]。此次试验,结合相关研究成果以及实验室试验研究,对农业部781号公告-6-2006鸡蛋中氟喹诺酮类药物残留量的测定方法前处理中提取液体积、备用液分取体积和洗脱液中乙腈的比例进行了研究试验。样品前处理中,提取液体积分别量取2 mL和10 mL磷酸盐提取液重复2次提取;备用液分取体积分别为全部和分取5 mL过柱;洗脱液体积分别量取1 mL的乙腈(19%)-缓冲液和1 mL的乙腈(35%)-缓冲液洗脱开展对比试验。结果表明,按照农业部781号公告-6-2006检测方法磷酸提取液4 mL、备用液全部过柱和乙腈(19%)-缓冲液洗脱的处理方法添加回收率只能达到25.12%~36.20%;优化后的20 mL磷酸提取液,备用液分取5 mL过柱和乙腈(35%)-缓冲液洗脱的处理方法添加回收率提高50%以上,达到90.40%~96.15%,氟喹诺酮类药物残留量的测定回收率得到大幅度提升。
2.2 校准曲线与线性范围
校准曲线的数学方程式以及校准曲线的工作范围,浓度范围尽可能覆盖一个数量级,至少作5个检测点(不包括空白)。此次试验,结合实验室经验积累以及操作便利性对农业部781号公告-6-2006检测方法中校准曲线梯度做了优化。精确量取适量100 μg/mL环丙沙星、恩诺沙星和沙拉沙星标准工作液,用流动相稀释成浓度为5、10、 20、100、500 ng/mL的环丙沙星、恩诺沙星和沙拉沙星标准溶液,精确量取适量达氟沙星标准工作液,用流动相稀释成浓度为1、2、4、20、100 ng/mL达氟沙星标准溶液。供高效液相色谱分析(强制过原点)。由表1可知,4种喹诺酮类药物的回归方程(强制过原点)及相关系数,在5~500 ng/g 范围内线性良好,其中达氟沙星为1~100 ng/g,相关系数R2均达到0.9999以上。
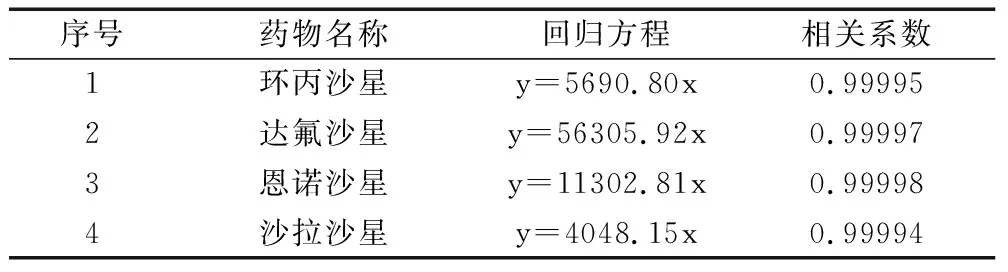
表1 喹诺酮类药物的回归方程、相关系数Tab.1 Regression equation and correlation coefficient of quinolones
2.3 方法准确度、回收率和检出限
此次试验,取适量试样添加溶液和相应的标准工作溶液,作多点校准,以色谱峰面积积分值定量。标准工作液及试样溶液中的环丙沙星、达氟沙星、恩诺沙星和沙拉沙星响应值均应在仪器检测的线性范围之内。采用标准添加法,在空白鸡蛋样品中添加10 ng/mL的环丙沙星、达氟沙星、恩诺沙星、沙拉沙星进行回收率试验,平行试验2个。在上述色谱条件下,药物的出峰先后顺序依次为环丙沙星、达氟沙星、恩诺沙星和沙拉沙星,空白溶液、标准溶液和试样添加溶液的液相色谱图见图1、图2和图3。由此可见,4种氟喹诺酮类药物分离效果好,基线平滑,峰形尖锐,对称性好,且经计算回收率均达到了90%以上(表2),相对标准偏差均小于等于10%。通过优化后的前处理方法,在标准色谱条件下,药物不同浓度样品试验,以信噪比S/N=3确定检出限。结果表明,环丙沙星、恩诺沙星和沙拉沙星检出限为5 ng/mL,达氟沙星检出限为1 ng/mL。
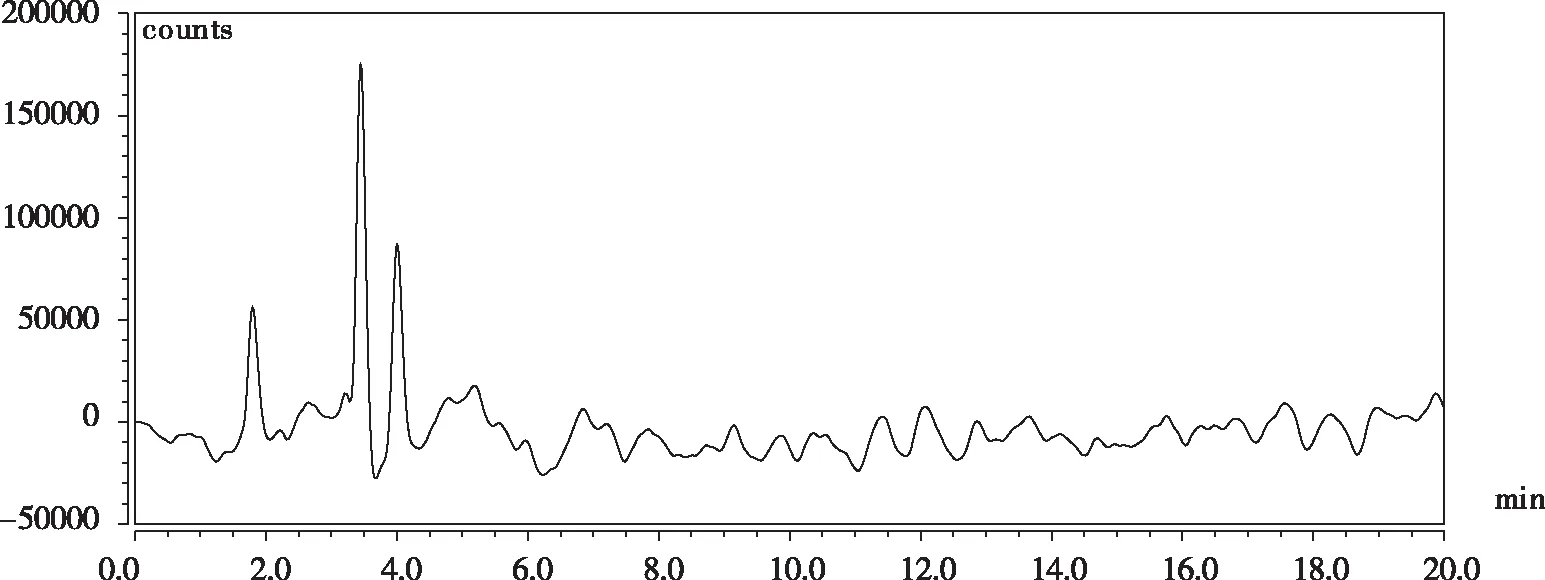
图1 鸡蛋试样中空白样品色谱图Fig.1 Liquid chromatogram of blank sample in eggs

图2 氟喹诺酮类药物混合标准品色谱图(20 ng/mL,4 ng/mL)Fig.2 Liquid chromatogram of Fluoroquinolones mixed standard substances

图3 鸡蛋中空白添加样品色谱图(10 ng/mL,2 ng/mL)Fig.3 Liquid chromatogram of blank addition sample eggs

表2 鸡蛋中4种氟喹诺酮类药物添加回收率(补充每个重复的回收率)Tab.2 Additive recovery of 4 fluoroquinolones in eggs
3 结论与讨论
此研究针对县(市)级农产品质量安全检验检测机构常用的检测标准《农业部781号公告-6-2006 鸡蛋中氟喹诺酮类药物残留量的测定—高效液相色谱法》[16]进行方法优化,在最大限度遵循该参考标准基础上进行了研究试验,并参考了近年来国内外诸多有关氟喹诺酮类药物残留在动物组织中的测定方法的报道[13-16]。经试验研究发现,标准中提取条件、色谱条件等影响因子不变,仅需对标准中关键部分优化,即校准曲线浓度梯度、磷酸盐提取液体积调整为20 mL,洗脱液调整为乙腈(35%)-缓冲液,在UiMate3000-FLD高效液相色谱仪分析下鸡蛋中氟喹诺酮类药物残留量的添加回收率达到90%以上,符合县(市)级检验检测机构对动物性食品(鸡蛋)中氟喹诺酮类药物残留量的测定要求。

