Q235钢表面涂覆含碳酸钙和石墨烯无机富锌涂层的耐蚀性能
石文龙,赵 野,吴青华,杨 意,何 壮,陈羽阳,罗 瑶,黄莹莹,刘 畅,李宇春
(长沙理工大学化学与食品工程学院,湖南 长沙 410114)
0 前 言
由于海洋环境比较复杂且海水本身具有腐蚀性,金属设施在海洋环境使用过程中将会被腐蚀从而造成巨大损失。如果全部使用耐蚀效果极佳的钢材如316L和317L钢,将导致工程成本太高,所以从经济角度考虑,碳钢还是工程施工中的最优选择。但由于碳钢的耐蚀性能较差,使用涂层对碳钢进行保护就显得尤为重要。
在海洋领域,富锌涂料是最常用的防腐导电涂料,在富锌涂料中大量的锌粉用作牺牲阳极,但是如果加入过多的锌粉,不仅会提高成本,也会影响涂层的附着力,使其与中间漆的粘合力大大降低。大量研究表明,在富锌涂料中能起阴极保护作用的锌粉只占锌粉总量的25%左右,其余大部分的锌粉只起导电作用。而且涂层中的锌粉反应速率很快,提供阴极保护的时间很短,虽然锌粉反应后的产物可以覆盖在微孔表面降低涂层的孔隙率,保护涂层的完整性,但是其腐蚀产物并不稳定,在碱性环境下容易分解,所以涂层的使用寿命较短。
石墨烯作为一种新型材料具有很多独特的性能和特质,如优异的电学性能,在室温条件下,石墨烯的电子迁移率可以达到1.5×104cm2/(V·s);优异的力学性能,如在理想状态下其杨氏模量可以达到1 TPa,固有的拉伸强度可以达到130 GPa[1];优异的光学性能,其可见光区域的透光率≥97%;石墨烯还具有很高的比表面积,其比表面积可达2 630 m2/g[2]。石墨烯本身是二维层状结构,对腐蚀性物质能够产生一定的屏蔽作用[3]。刑玉雷等[4]通过研究发现,石墨烯能够对腐蚀性物质形成一道物理隔离层屏障,可以抑制金属的腐蚀。石墨烯还能够在一定程度上对镀层金属起到钝化保护作用,可以进一步提高涂层的防腐蚀性能[5]。Mallick等[6]通过阴极电泳沉积(EPD)在镍钛诺基底上制备了石墨烯涂层,并在模拟的体液环境中进行了电位动力学极化试验,发现其腐蚀电位正移,表明石墨烯涂层改善了镍钛诺基材的耐腐蚀性能。但在无机富锌涂料中添加石墨烯和碳酸钙的研究未见报道。本工作首次探究研发了一种添加石墨烯和碳酸钙的新型无机富锌涂料,并就其对Q235钢的耐蚀性能进行了测试分析。
1 试 验
1.1 气溶胶模拟环境
选取6块边长为50 cm的正方形透明钢化玻璃,将其制作成边长为50 cm的正方体盐雾箱,在箱体的玻璃璧上打2个孔径为2 cm的小圆孔用于雾化器和恒温加热器的电源连接。将超声雾化器放入模拟的海水溶液中,模拟海水盛放在圆底烧杯中,液面高度高出传感器3~5 cm,通过变压器将220 V电压转换为24 V并连接超声雾化器进行超声雾化,通过压电陶瓷的谐振作用将能量传输出来击碎模拟海水溶液,使模拟海水溶液可以长时间处于悬浮颗粒的雾化状态,通过恒温加热装置保持模拟液的温度为40 ℃,通过在模拟箱底层加入饱和氯化钾溶液控制相对湿度为 85%~90%。制作该透明玻璃箱体有助于观察模拟箱内涂有涂料的试片表面变化情况,模拟箱的上封玻璃盖可以取下来,模拟箱中放入1根玻璃支架,用于悬挂试片(如图1所示)。
1.2 海水模拟液及试验材料
海水模拟液的主要化学成分如表1所示,海水的pH值为8.0左右[7,8]。

表1 海水模拟溶液主要化学成分
试验材料为Q235钢,其主要成分见表2,用线切割加工成50 mm×25 mm×2 mm的试样,试验前依次用200~1 000目金相砂纸打磨试样表面,然后用蒸馏水、乙醇、丙酮清洗,吹干,放入干燥箱内,干燥后用电子天平称重记录。
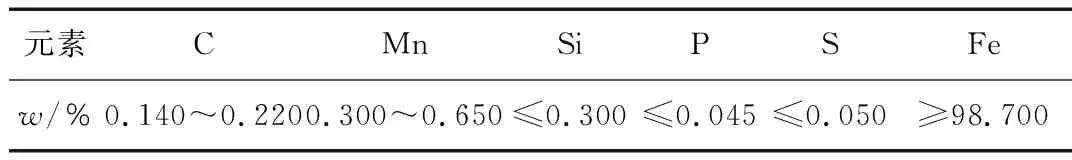
表2 Q235钢的化学成分 (质量分数) %
1.3 无机富锌涂料的制备
1.3.1 涂料粘合剂的制备
所选用的涂料粘合剂是正硅酸乙酯,其水解液中各组分含量(质量分数)分别为:正硅酸乙酯50.0%~70.0%,无水乙醇20.0%~40.0%,去离子水10.0%~20.0%,浓H2SO40.2%~0.4%。
将三颈瓶放入可以磁力搅拌的水浴加热装置中,三颈烧瓶的左右2个瓶口先用橡胶塞堵住,在中间瓶口上方用回流冷凝管搭建回流装置。将一定量的正硅酸乙酯和乙醇依次加入三颈烧瓶中,开启磁力搅拌并使其水浴温度升至35 ℃。
将浓度为98%的浓H2SO4加入到自制的去离子水中并搅拌使其混合均匀,然后滴加到三颈烧瓶中进行水解反应,滴加时间尽量控制在1~2 h。待滴加完毕后,将水浴升温至50~70 ℃继续反应2~3 h。反应完毕停止加热,待其温度冷却至室温后将所得的硅酸乙酯水解液倒入事先准备好的容器中,加盖密封待用。
1.3.2 涂料主剂的制备
无机富锌涂料的主剂即锌粉浆中的主要成分(质量分数)为3.0%聚乙烯醇缩丁醛、12.0%乙醇、80.0%锌粉、2.5%磷铁粉、2.5%乙二醇乙醚醋酸酯和不同比例(0和2%)的碳酸钙、石墨烯。配制方法:先用一定量的乙醇溶解一定量的聚乙烯醇缩丁醛,直至其完全溶解,之后再向溶解好的混合物中按事先确定的比例依次加入其他主要成分,并开始搅拌,搅拌完成后,将配制好的锌粉浆主剂放入超声设备中使其分散更加均匀。
将制备好的主剂与粘合剂按质量比2∶1混合,然后将其放入搅拌器中搅拌20 min,使其充分搅拌均匀。用板刷将涂料均匀地涂刷在Q235试片表面。
1.4 测试表征
1.4.1 涂层耐腐蚀性能
气溶胶挂片腐蚀试验。设定超声雾化频率为3.4 MHz,雾化量200 mL/h,温度40 ℃(温度通过恒温加热器控制),相对湿度85%~90%(通过在模拟箱底层加入饱和氯化钾溶液控制)。将涂有涂层的Q235钢试片悬挂于模拟箱中,设定所有试验条件后将模拟箱密封,试验时间为2 000 h。
模拟海水浸泡试验。用水浴锅控制温度为40 ℃,将涂有涂层的Q235钢试片浸泡在加入模拟海水的烧杯中,为防止溶液浓度变化过大,每3 d换1次溶液,试验时间同样为2 000 h。
采用CHI660电化学工作站进行开路电位、极化曲线和电化学阻抗谱(EIS)测试,采用三电极体系,工作电极为涂有涂层的Q235试片,饱和甘汞电极(SCE)为参比电极,辅助电极为铂电极。电解液成分和雾化溶液相同。Tafel极化试验,扫描范围为相对开路电位-0.25~0.25 V。EIS测试扰动电位为10 mV,频率测试范围为1.0×(10-2~105) Hz。
1.4.2 涂层和腐蚀产物组织结构
采用FEG250型扫描电镜(SEM)分析涂层、腐蚀产物的形貌和成分。
采用D/max - 2500/PC型X射线衍射仪(XRD)分析腐蚀产物的物相组成。
2 结果与分析
2.1 气溶胶试验
图2为涂有不同无机富锌涂料的Q235钢试片腐蚀前及在40 ℃模拟海水气溶胶环境下腐蚀2 000 h的SEM形貌。从图2可以看出,原始配方涂料(未添加石墨烯和碳酸钙的无机富锌涂料,下同)涂层在没有腐蚀之前其表面比较平整,锌粉颗粒分散得比较均匀并且将基材完整的包裹住(图2a)。原始配方涂料涂层经过40 ℃模拟海水气溶胶环境腐蚀2 000 h后,涂层表面的锌被腐蚀,生成大量腐蚀产物附着在涂层表面,继续保护金属基体不被腐蚀,但是生成的腐蚀产物之间不够致密(图2b)。原始配方涂料基础上添加了2%石墨烯和2%碳酸钙的涂层腐蚀前表面比较平整,虽然添加石墨烯和碳酸钙后使得锌粉颗粒的间距变得比较大,但是并不影响涂料对基材的包裹性(图2c)。添加了2%石墨烯和2%碳酸钙的涂层经过40 ℃气溶胶环境下腐蚀2 000 h后,其表面的锌粉被大量腐蚀并且生成了更加致密(相对图2b)的腐蚀产物(图2d),这表明石墨烯和碳酸钙的添加增大了涂层中锌粉的腐蚀反应参与度,同时生成的致密腐蚀产物也可以更好地保护基材[9]。
2.2 海水浸泡试验
图3为涂有不同无机富锌涂料的Q235钢试片腐蚀前及在40 ℃模拟海水浸泡环境下腐蚀2 000 h的SEM形貌。从图3可以看出,原始配方涂料的涂层经过40 ℃模拟海水环境下腐蚀2 000 h后,其表面的锌被腐蚀,生成了少量的腐蚀产物附着在涂层表面(图3b)。原始配方涂料基础上添加了2%石墨烯和2%碳酸钙的涂层经过40 ℃模拟海水环境下腐蚀2 000 h后,其表面生成的腐蚀产物填充到涂层的缝隙中,使涂层更加耐蚀,提高了涂层表面的致密性(图3d)。该结果与气溶胶腐蚀结果一致。
2.3 电化学分析
2.3.1 开路电位(EOCP)
图4为涂有原始配方涂料的Q235钢在模拟海水浸泡环境下其开路电位随时间的变化,图5为涂有原始配方涂料+2%石墨烯+2%碳酸钙的Q235钢在模拟海水浸泡环境下其开路电位随时间的变化。通过对比图4和图5可以看出,添加了石墨烯和碳酸钙的涂层在模拟海水中浸泡21 d后的开路电位明显更低,其耐蚀性能也更加优异[10]。
2.3.2 极化曲线
图6为涂有原始配方涂料的Q235钢在模拟海水浸泡环境下随时间变化的Tafel极化曲线, 其相应的腐蚀数据见表3。图7为涂有原始配方+2%石墨烯+2%碳酸钙涂料的Q235钢在模拟海水浸泡环境下随时间变化的Tafel极化曲线,其相应的腐蚀数据见表4。

表3 涂有原始配方涂料的Q235钢随时间变化的腐蚀数据
从图6、表3和图7、表4可以看出,添加了石墨烯和碳酸钙的涂层的腐蚀速率更慢,其耐蚀性更好,因为其涂层表面在腐蚀过程中生成了致密的腐蚀产物,这些腐蚀产物填充了涂层表面的空隙,从而降低了腐蚀速率。随着反应时间的延长,腐蚀电流密度逐渐降低,腐蚀反应速率变慢;在同样反应21 d后,添加了2%石墨烯+2%碳酸钙的涂层的腐蚀电位(-0.936 0 V)比未添加的(-0.765 9 V)更负,说明其具有更好的耐蚀性能。

表4 涂有原始配方+2%石墨烯+2%碳酸钙涂料的Q235钢随时间变化的腐蚀数据
2.3.3 EIS
根据电化学理论可知[11],电荷及传质阻力的大小由EIS的容抗弧大小决定,容抗弧越大,表明电荷及传质阻力越大,越耐腐蚀,反之表明电荷及传质阻力越小。图8为时间梯度下电化学阻抗的等效电路。图 9~图12为涂有原始配方涂料及其添加2%石墨烯+2%碳酸钙的Q235钢在不同时间下的Nyquist谱和Bode谱,表5和表6为相应的EIS拟合结果。
等效电路模型可以用来描述涂层的腐蚀机理。其中,可以通过溶液电阻Rsol,双层电容Cdl以及电荷转移电阻Rt等参数反映出锌粉参与反应的情况。由于存在弥散效应,在对阻抗数据进行拟合时,会使涂层的电容偏离理想电容,对该体系下的电容响应使用恒定相位元素Qdl代替Cdl,Qdl为涂层与界面间的双层电容,Qc为涂层电容,Rpo为涂层的电阻,涂层电容反映了涂层的屏蔽性能。Prasai等[12]、Liu等[13]发现层状填料会阻碍氧气的扩散,并提高涂层的防腐性能,石墨烯起到一种填充剂的作用。图9~图12表明,随着时间的推移,试片腐蚀程度加剧,但涂有2%石墨烯+2%碳酸钙涂料的Q235钢的容抗弧更大,其抗腐蚀性更强。
在模拟海水环境下随着时间的不断延长涂层表面生成了许多腐蚀产物,涂层表面的耐溶液侵蚀性不断增强,涂层表面的电阻不断增大,电荷转移的电阻也在不断增大。

表5 涂有原始配方的Q235钢随时间变化的EIS拟合结果
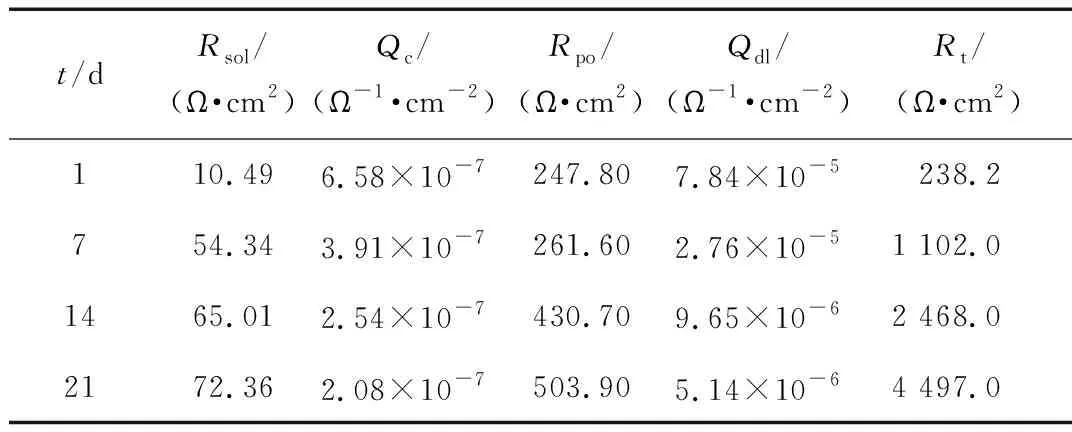
表6 涂有原始配方+2%石墨烯+2%碳酸钙涂料的Q235钢随时间变化的EIS拟合结果
2.4 涂层氧化产物及形成
图13为涂有原始配方+2%石墨烯+2%碳酸钙涂料的Q235钢在模拟海水气溶胶环境下腐蚀2 000 h后的XRD谱,由图13可知,涂层表面的氧化产物主要包含ZnO、Zn(OH)2、碱式锌盐、碱式复盐以及ZnSO4等物质。
Zn的标准电位为-0.762 V低于钢铁的(-0.409 V),故在微电池体系中更容易失电子作为阳极,钢铁作为微电池的阴极被保护起来。阴极区,钢铁不断得到电子被保护;阳极区,Zn失去电子被氧化,变成Zn2+。腐蚀过程如下:
阴极区:
O2+2H2O+4e→4OH-
(1)
阳极区:
Zn-2e→Zn2+
(2)
由于模拟海水中存在大量的Cl-和SO42-,失去电子的锌粉会与环境中的Cl-结合生成ZnCl2和ZnSO4,此外涂层中大量的锌粉还会与水分子结合生成不溶于水的Zn(OH)2,由于氧化产物的不断积累导致Zn(OH)2不断增多,再加上涂料中含有CaCO3,CaCO3会与Zn(OH)2生成更难溶解的碱式碳酸盐、碱式复盐等,这些物质都很稳定且极难溶解,会填充到涂层被腐蚀后的微小空隙中并沉积在基材的表面,对水、氧以及一些盐类起到屏蔽作用,保护基体不被侵蚀[14,15],附着在涂层表面的产物生成路径如式(3)~(7):
Zn2++2Cl-→ZnCl2
(3)
Zn2++SO42-→ZnSO4
(4)
Zn+2H2O→Zn(OH)2+H2
(5)
5Zn(OH)2+2CaCO3→Zn5(CO3)2(OH)6+2Ca(OH)2
(6)
4Zn(OH)2+ZnCl2+H2O→Zn5(OH)8Cl2·H2O
(7)
3 结 论
(1)通过SEM对涂层进行表面形貌分析可知,添加了2%石墨烯+2%碳酸钙的涂层表面相较原始配方涂料涂层,其锌粉的腐蚀反应参与度更大,其表面生成了较多的保护性产物,基体表面涂层更加致密,对基体包裹性更好,耐蚀性能更优。
(2)通过电化学试验可知,腐蚀反应21 d后添加了2%石墨烯+2%碳酸钙的涂层的腐蚀电位(-0.936 0 V)仍比原始配方涂层的腐蚀电位(-0.765 9 V)更负,其腐蚀电流密度接近,这说明添加了2%石墨烯+2%碳酸钙的涂层耐蚀性能更好。
(3)结合XRD分析可知,添加了2%石墨烯+2%碳酸钙的涂层表面较原始配方涂层中参与反应的锌粉颗粒能够生成较多的腐蚀产物保护涂层不被进一步侵蚀,在腐蚀相同时间后添加了2%石墨烯+2%碳酸钙的涂层中保留了更多的锌粉颗粒,耐蚀性能更加优异。

