早卵泡期长效长方案与拮抗剂方案在卵巢正常反应患者中的应用效果比较
马紫玮,南 燕,王 慧,于 莲,李玉洁
(新乡医学院第三附属医院生殖医学科,河南 新乡 453003)
随着社会飞速发展,女性角色发生转变,面对生活及精神双重压力,女性生育能力也受到了影响,不孕症发生率逐年上升,成为继肿瘤及心血管疾病的第三大疾病[1]。辅助生殖技术(assisted reproductive technology,ART)是治疗不孕不育的重要治疗手段,而提高不孕症患者的妊娠率是ART的难题之一。控制性超促排卵(controlled ovarian hyperstimulation,COH)是体外受精/单精子卵泡胞质内注射-胚胎移植(invitrofertilization/intracytoplasmic sperm injection and embryo transfer,IVF/ICSI-ET)的基础,选择合适的促排卵方案不仅可以改善患者的获卵情况及胚胎质量,还可能影响其妊娠结局。促性腺激素释放激素拮抗剂(gonadotrophin-releasing hormone antagonist,GnRH-ant)方案与促性腺激素释放激素激动剂(gonadotrop-releasing hormone agonist,GnRH-a)方案是2种常用的促排卵方案,既往卵巢正常反应(normal ovarian response,NOR)患者多应用激动剂促排卵方案,随着拮抗剂促排卵方案的不断发展完善,目前拮抗剂促排卵方案在NOR患者中也取得良好的效果。但目前2种方案的临床效果存在争议。有研究表明,早卵泡期长效长方案可以改善盆腔内环境及子宫内膜容受性,提高新鲜周期着床率及妊娠率[2];但也有很多学者认为,拮抗剂促排卵与激动剂促排卵方案具有相似的妊娠率[3-4]。基于此,本研究通过比较早卵泡期长效长方案与拮抗剂促排卵方案在NOR患者COH过程中的临床指标、新鲜胚胎移植周期及首次冻融胚胎移植(frozen-thawed embryo transfer,FET)周期临床结局,探讨这2种促排卵反应在NOR患者中应用的临床效果,以期为临床NOR患者行IVF/ICSI-ET助孕中COH方案的选择提供依据。
1 资料与方法
1.1 一般资料选择2017年4月至2021年1月于新乡医学院第三附属医院生殖医学科行IVF/ICSI-ET助孕治疗的NOR患者为研究对象。病例纳入标准:(1)促排卵方案采用早卵泡期长效长方案或拮抗剂方案;(2)卵巢储备功能良好,即窦卵泡数6~15枚,抗苗勒管素 1.1~4.4 μg·L-1,基础血清卵泡刺激素(follicle stimulating hormone,FSH)<10 U·L-1;(3)年龄≤35岁;(4)既往无卵巢低反应或高反应的体外受精周期取消史。排除标准:(1)夫妻任一方染色体异常;(2)多囊卵巢综合征患者;(3)合并糖尿病、甲状腺功能异常等其他代谢性疾病者;(4)畸形子宫患者;(5)患有卵巢肿瘤等肿瘤疾病患者。本研究共纳入241 例NOR患者,根据促排卵方案分为长效长方案组和拮抗剂方案组。长效长方案组164例,年龄23~35(30.18±3.38)岁,不孕年限 0.5~15.0(3.81±3.00)a,体质量指数(body mass index,BMI)15.6~30.4(23.04±3.49)kg·m-2,月经期2~5 d基础性激素水平:FSH 2.7~9.8(8.67±4.88)U·L-1,黄体生成素(luteinizing hormone,LH)0.6~14.0(4.07±1.98)U·L-1,雌二醇(estradiol,E2)12.6~91.0(37.83±16.06)ng·L-1,黄体酮(progesterone,P)0.41~7.90(0.99±0.83)μg·L-1,AFC 6~15(12.51±3.97)枚。拮抗剂方案组77例,年龄25~35(30.86±2.91)岁,不孕年限0.17~15.0(4.18±3.39)a,BMI 19.0~31.4(23.95±3.38)kg·m-2,月经期2~5 d基础性激素:FSH 3.1~9.87(8.37±2.54)U·L-1,LH 0.2~11.48(4.00±1.45)U·L-1,E216.0~82.5(37.81±15.07)ng·L-1,P 0.24~4.73(0.94±0.79)μg·L-1,AFC 6~15(11.39±5.49)枚。2组患者的年龄、不孕年限、BMI、基础性激素水平及AFC比较差异均无统计学意义(P>0.05),具有可比性。本研究经新乡医学院第三附属医院医学伦理委员会批准,患者知情同意并签署知情同意书。
1.2 促排卵方案
1.2.1 长效长方案组患者行早卵泡期长效长方案,具体治疗措施:患者于月经周期第2~4天,根据阴道超声及性激素检查在早卵泡期单次皮下注射3.75 mg长效GnRH-a[辉凌制药(中国)有限公司,进口药品注册证号 H20140123],注射28~40 d达到降调标准(FSH<5 U·L-1,LH<1 U·L-1,E2<30 ng·L-1,阴道超声检测卵泡直径3~5 mm)[5]后每日皮下注射注射用重组人促性腺激素(gonadotrophin,Gn)(默克雪兰诺有限公司,进口药品注册证号 S20160039)促排卵,Gn起始剂量依据患者年龄、BMI或既往周期使用药物情况决定。注射Gn 4 d后应用阴道超声观察卵泡发育情况,并检测血FSH、LH、E2、P水平,酌情调整Gn注射剂量,之后间隔1~3 d监测以上指标,依据卵泡大小及血激素水平调整Gn注射剂量直至人绒毛膜促性腺激素(human chorionic gonadotrophin,HCG)注射日(HCG日)。当2~3个主导卵泡直径≥18 mm、3个优势卵泡直径≥17 mm或≥16 mm卵泡超过60%时,结合血E2水平给予重组HCG(默克雪兰诺有限公司,进口药品注册证号 S20130091)250 μg 联合HCG(马鞍山丰原制药有限公司,国药准字 H34023585)2 000 U进行扳机,36~38 h后行超声引导下穿刺取卵术。
1.2.2 拮抗剂方案组患者行拮抗剂促排卵方案,具体治疗措施:患者于月经周期第2~3天开始每日皮下注射Gn,Gn起始剂量依据年龄、BMI或既往周期使用药物情况决定。4~5 d后开始监测卵泡发育及血FSH、LH、E2、P水平,酌情调整Gn剂量,于Gn注射第5~6 天或优势卵泡直径达12~14 mm或LH≥10 U·L-1时每日皮下注射短效GnRH-ant(默克雪兰诺有限公司,进口药品注册证号 H20140476)0.25 mg直至HCG日,依据卵泡监测情况及血激素水平及时调整Gn用量。当2个主导卵泡直径≥18 mm 或3个主导卵泡直径≥17 mm时结合E2和P水平,使用重组HCG 250 μg 联合HCG 2 000 U进行扳机,34~36 h后行超声引导下穿刺取卵术。
1.3 受精和胚胎移植2组患者取卵后根据男方精液质量或既往周期治疗情况选择合适的受精方式。根据胚胎发育情况,在受精后第3天进行卵裂期胚胎移植,2组患者共行新鲜胚胎移植137例,其中长效长方案组移植119例,拮抗剂方案组移植18例。不符合新鲜移植标准者行全胚冷冻,然后行FET;首次行FET(包括全胚冷冻后首次解冻移植周期和新鲜胚胎移植未孕后首次解冻移植周期)共162例,其中长效长方案组95例,拮抗剂方案组67例。移植后给予地屈孕酮片[荷兰苏威制药(上海)有限公司,进口药品注册证号 H20170221]10 mg口服,每日2次;黄体支持采用黄体酮阴道缓释凝胶(默克雪兰诺有限公司,进口药品注册证号 H20140552)阴道给药,每日1次,共 14 d。胚胎移植后14 d,查血HCG>5 U·L-1为生化妊娠,35 d阴道超声检查见宫腔内孕囊为临床妊娠。
1.4 观察指标
1.4.1 促排卵指标(1)Gn总量及Gn天数:统计促排卵期间Gn使用总量及Gn使用天数;(2)HCG日内膜厚度:于HCG日应用Prosound SSD-3500彩色超声诊断仪(上海阿洛卡医用仪器有限公司)检测子宫内膜厚度;(3)HCG日LH、E2、P水平:于HCG日应用Access全自动微粒子化学发光免疫系统(美国贝克曼库尔特有限公司)检测患者空腹静脉血LH、E2、P水平。(3)记录获卵数、第2次减数分裂(metaphase Ⅱ,MⅡ)卵母细胞数、双原核(double pronucleus,2PN)数、可移植胚胎数、优质胚胎数,计算优质胚胎率(优质胚胎数/2PN数×100%)。
1.4.2 新鲜胚胎移植周期临床结局指标统计2组患者全胚冷冻周期数、取消周期数、中重度卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)发生例数、孕囊数、生化妊娠周期数、临床妊娠周期数、早期流产例数、持续妊娠(妊娠≥20周)数、活产(单胎、双胎及双胎以上活产均记为1次活产)数,计算全胚冷冻率、周期取消率、中重度OHSS发生率、胚胎着床率、生化妊娠率、临床妊娠率、早期流产率、持续妊娠率、活产率。全胚冷冻率=全胚冷冻周期数/有可移植胚胎的周期数×100%,周期取消率=取消周期数/启动周期治疗的周期数×100%,中重度OHSS发生率=中重度OHSS发生例数/启动周期数×100%,胚胎着床率=孕囊数/总移植胚胎数×100%,生化妊娠率=生化妊娠周期数/移植周期数×100%,临床妊娠率=临床妊娠周期数/移植周期数×100%,早期流产率=早期流产例数/临床妊娠周期数×100%,持续妊娠率=妊娠≥20周周期数/胚胎移植周期数×100%,活产率=活产数/胚胎移植周期数×100%。
1.4.3 FET周期实验室及临床结局指标(1)FET日内膜厚度:FET周期移植当天应用Prosound SSD-3500彩色超声诊断仪(上海阿洛卡医用仪器有限公司)检测子宫内膜厚度;(2)计算FET周期中胚胎着床率、生化妊娠率、临床妊娠率、早期流产率、持续妊娠率、活产率,按“1.4.2”项相关计算公式计算。
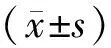
2 结果
2.1 2组患者COH过程中临床指标比较结果见表1。长效长方案组Gn天数、HCG日内膜厚度、获卵数、MⅡ卵数、2PN数、可移植胚胎数、优质胚胎数均显著高于拮抗剂方案组,HCG日LH值显著低于拮抗剂方案组,差异有统计学意义(P<0.05);长效长方案组与拮抗剂方案组Gn总量、HCG日E2水平、HCG日P水平、优质胚胎率比较差异无统计学意义(P>0.05)。

表1 2组患者COH过程中临床指标比较
2.2 2组新鲜胚胎移植周期临床结局指标比较结果见表2。长效长方案组全胚冷冻率显著低于拮抗剂方案组,差异有统计学意义(P<0.05);长效长方案组与拮抗剂方案组中重度OHSS发生率、周期取消率、胚胎着床率、临床妊娠率、生化妊娠率、早期流产率、持续妊娠率及活产率比较差异均无统计学意义(P>0.05)。
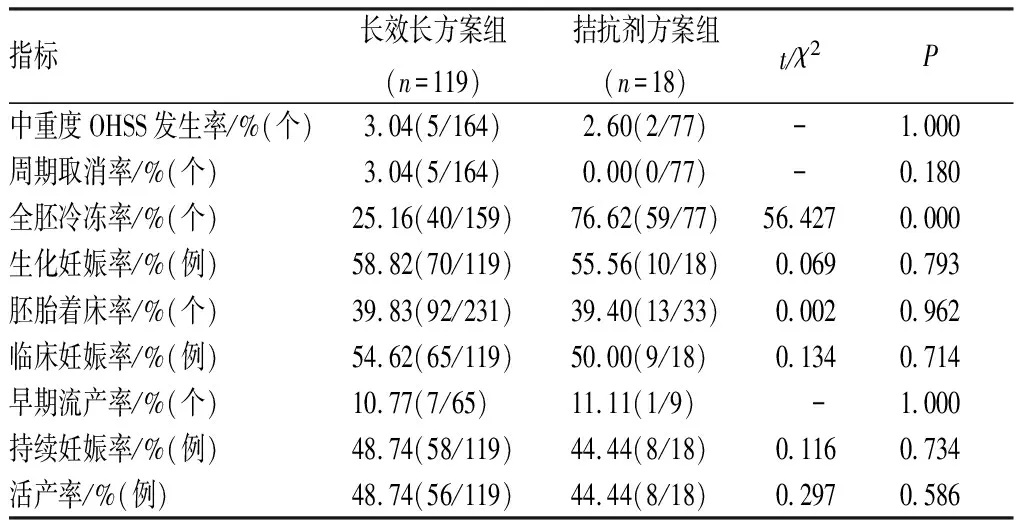
表2 2组新鲜胚胎移植周期临床结局指标比较
2.3 2组患者首次FET周期临床结局指标比较结果见表3。长效长方案组与拮抗剂方案组FET日内膜厚度、生化妊娠率、临床妊娠率、持续妊娠率、早期流产率比较差异均无统计学意义(P>0.05);长效长方案组胚胎着床率显著高于拮抗剂方案组,差异有统计学意义(P<0.05)。

表3 2组患者首次FET周期临床结局对比
3 讨论
ART临床工作中根据卵巢反应性选择合适的COH 可以保证促排卵治疗效果并减少促排卵过程中的并发症。既往NOR患者多采用GnRH-a方案,早卵泡期长效长方案是临床上常用的GnRH-a方案;近年来,有研究表明,GnRH-ant方案可应用于NOR患者并获得与GnRH-a方案相似的临床结局[3-4]。但是,目前2种方案应用于NOR患者的效果仍存有争议。
早卵泡期长效长方案是于卵泡早期应用长效GnRH-a进行垂体降调节,使用初期GnRH-a与促性腺激素释放激素受体结合,可促进垂体短期内分泌FSH、LH,产生“flare-up”效应;而且GnRH-a半衰期长,随着促性腺激素释放激素受体对GnRH-a敏感性逐渐减弱,患者的垂体功能也逐渐被抑制,内源性Gn分泌减少,从而避免早发LH峰的出现,达到降调效果,在避免卵巢黄素化的同时增加卵泡的募集[6-7]。此时,添加外源性Gn可促进同期募集卵泡同步发育,但也会降低对Gn的敏感性,增加Gn用量[8]。研究表明,高浓度的LH可使卵泡闭锁,垂体的降调节作用可以降低GnRH-a方案中的LH水平,减少卵泡闭锁,增加Gn用量及Gn使用天数,增加获卵数及MⅡ卵母细胞数[9];且可通过降低白细胞介素-1、白细胞介素-8、血管内皮生长因子水平,改善卵母细胞及胚胎质量[10-11]。有学者提出,卵泡期单剂量GnRH-a注射可诱导子宫内膜表达整合素,改善子宫内膜容受性,有利于胚胎着床[12]。拮抗剂方案同样于早卵泡期应用外源性Gn促进卵泡募集及生长,但不涉及垂体降调节,早期内源性FSH的分泌使卵泡发育同步性欠佳;GnRH-ant与内源性促性腺激素释放激素竞争结合促性腺激素释放激素受体,可迅速抑制LH,并无“flare-up”效应,可缩短周期治疗时间、减少并发症。但有研究报道,应用GnRH-ant会影响子宫内膜容受性[13-14],其原因可能与子宫内膜间质细胞表达的同源框基因A10(homeoboxA10,HOXA10)有关。HOXA10是子宫内膜容受性的标志物,有研究发现,GnRH-a方案中子宫内膜中的HOXA10表达显著高于GnRH-ant方案[15]。本研究结果显示,长效长方案组患者COH过程中的Gn天数、HCG日内膜厚度、获卵数、MⅡ卵母细胞数、2PN数、可移植胚胎数、优质胚胎数均显著高于拮抗剂方案组,HCG日LH值显著低于拮抗剂方案组;而长效长方案组与拮抗剂方案组患者Gn用量、HCG日E2水平、HCG日P水平、优胚率比较差异无统计学意义;这与既往研究结果一致[8-9]。以上结果说明,早卵泡期长效长方案于卵泡早期应用长效GnRH-a进行垂体降调节可降低HCG日LH值,但增加了Gn天数;另外,早卵泡期长效长方案通过降低卵泡液中炎症细胞因子水平增加了卵母细胞、胚胎数量并改善了子宫内膜容受性[11,16],从而可获得较高的获卵数、MII卵母细胞数、2PN数、可移植胚胎数及优质胚胎数。
既往对于早卵泡期长效长方案与拮抗剂方案应用于NOR患者的着床率、妊娠率等研究结果有争议,如:YANG等[17]一项纳入11项研究的Meta分析指出,早卵泡期长效长方案组患者的临床妊娠率和胚胎种植率、活产率均高于拮抗剂方案组;但YING等[8]研究报道,拮抗剂与激动剂方案对于NOR患者可产生相似的妊娠率。本研究结果显示,长效长方案组与拮抗剂方案组患者的周期取消率、胚胎着床率、临床妊娠率、生化妊娠率、早期流产率、持续妊娠率及活产率比较差异均无统计学意义,说明2种方案均适用于NOR不孕症人群且不会影响其妊娠率。OHSS是促性腺激素诱发排卵过程中的医源性并发症。激动剂方案中同步性发育卵泡数目多、促排时间长等是诱发OHSS的因素之一。有研究指出,拮抗剂方案可通过较少刺激天数及Gn用量来减少OHSS的发生[18]。但本研究结果显示,长效长方案组与拮抗剂方案组患者中重度OHSS发生率比较差异并无统计学意义,与李娜[19]研究结果一致;说明,现临床阶段拮抗剂方案可降低OHSS发生率的观点尚未达成共识,仍需大样本、多中心研究证实。此外,本研究结果显示,长效长方案组患者全胚冷冻率显著低于拮抗剂方案组,这可能是因为拮抗剂方案中出现子宫内膜不同步、早发LH峰或者P水平提前升高等情况而取消新鲜移植[20],从而使全胚冷冻率高于早卵泡期长效长方案组。
本研究对2种方案中行全胚冷冻患者首次FET周期的临床结局的指标进行了比较,结果显示,长效长方案组与拮抗剂方案组患者FET日内膜厚度、生化妊娠率、临床妊娠率、持续妊娠率、早期流产率比较差异均无统计学意义,这与既往XIA等[10]和WANG等[21]的研究结果一致。这说明,NOR患者应用早卵泡期长方案或拮抗剂方案时并不影响后续FET周期的临床结局。本研究结果也发现,长效长方案组中胚胎着床率高于拮抗剂方案组,考虑可能是长效长方案通过垂体降调节作用改善了卵母细胞及胚胎质量从而提高冻融周期的胚胎着床率;且本研究中早卵泡期长效长方案中优质胚胎数多于拮抗剂方案组也证实了这一点。
综上所述,早卵泡期长效长方案与拮抗剂方案均适用于NOR患者,且新鲜周期及冻融周期中的妊娠结局并无明显差异。拮抗剂方案中Gn使用天数少、周期短,患者依从性好,可节约患者的时间成本及经济成本,但其获卵及优质胚胎数少于早卵泡期长效长方案,全胚冷冻率高、新鲜移植机会少;早卵泡期长效长方案虽延长周期治疗时间,但并未增加中重度OHSS的发生率且在改善胚胎质量及子宫内膜容受性方面有优势。因此,对于NOR患者可优先选择拮抗剂方案,若既往取卵周期中胚胎质量即子宫内膜容受性欠佳时可考虑选择早卵泡期长效长方案。

