中枢神经系统孤立性纤维瘤11例的回顾性分析
李 伟 王业忠 胡 滨 姬云翔 柯炎斌 黄 观
1 广州医科大学附属第二医院神经外科(广州 510260)
2 广州医科大学附属第二医院病案科(广州 510260)
孤立性纤维瘤(solitary fibrous tumors,SFT),是一种罕见的来源于间叶组织的梭形细胞肿瘤[1]。大多数SFT为良性,生长缓慢;少部分为恶性,具有侵袭、转移性。其可发生于中枢神经系统、泌尿系统、消化系统等多个系统的器官或组织[2- 6]。中枢神经系统SFT发病率极低,Bisceglia Michele等[2]统计自1996—2011年仅有220例见诸于文献报道,而且多为个位数的病例报告或数十例的单中心小样本数据分析[2- 3,8- 9]。
本文通过回顾性分析2013—2021年期间广州医科大学附属第二医院神经外科接受手术并经病理检查证实SFT的11例患者的临床资料,旨在总结对该病的诊治经验,以期提高诊治水平。
1 资料与方法
1.1 研究对象
回顾性收集2013—2021年期间广州医科大学附属第二医院神经外科接受手术并经病理检查证实SFT的11例患者的临床资料。其中男6例,女5例。年龄范围:17~60岁,平均年龄(44.18±15.34)岁。研究方案经医院伦理委员会审批通过(伦理批件号:2022-hg-ks-10)。
1.2 研究方法
回顾11例SFT患者病历资料,记录患者入院时主诉及查体情况、术中所见。复习患者术前磁共振成像(magnetic resonance imaging,MRI)检查资料,记录病灶MRI平扫的信号特征及增强的表现。在病理科医师指导下查阅病灶标本的HE和免疫组化染色切片。通过定期来院复诊或电话询问的方式对本组病例进行术后随访。
1.3 统计方法

2 结 果
2.1 SFT患者的临床特征
本组病例11例,6例以头痛或头晕为主要症状;1例以双眼畏光、视物重影为主要症状,同时伴有头晕、头痛。4例以肢体乏力或麻木或不自主运动为主要症状。
2.2 SFT患者影像学表现特点
所有患者都接受了MRI检查。见表1及图1。10例颅内SFT,其中9例发生于幕上,1例发生于幕下。其中7例MRI提示为脑膜瘤,1例MRI提示脑膜瘤与SFT鉴别,1例MRI提示胶质母细胞瘤与脑膜瘤相鉴别,1例MRI提示多形性胶质母细胞瘤、恶性脑膜瘤、间变性室管膜瘤可能。1例发病部位为第7~8胸椎椎管内,MRI提示为神经鞘瘤。
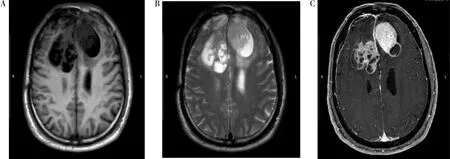
图1 SFT患者双侧额叶病灶的MRI图像

表1 11例SFT13个病灶的影像学特征 (n,%)
MRI平扫:9例为单发病灶,2例为多发病灶。报告主要提及13个主要病灶。61.54%(8/13)病灶最大直径≥5 cm,38.46%(5/13)病灶最大直径<5 cm。T1WI:46.15%(6/13)病灶表现为等-低信号,38.46%(5/13)病灶表现为低或稍低信号,15.39%(2/13)病灶表现为等信号。T2WI:46.15%(6/13)病灶表现为混杂信号或等-稍高信号;38.46%(5/13)病灶表现为高信号或稍高信号,15.39%(2/13)病灶表现为低信号。
MRI增强:13个病灶实性部分均可见不同程度的强化。3个病灶有明显的“脑膜尾征”。
2.3 SFT患者病理学表现特点
2.3.1 HE染色切片的镜下特点 肿瘤细胞呈梭形、圆形,细胞疏密不一,排列呈编织状、旋涡状或束状。间质可见胶原纤维组织。见图2。

图2 SFT标本HE染色切片,梭形的肿瘤细胞排列呈漩涡状(×100)
2.3.2 免疫组织组化检测结果特点 在本组病例中,11例检测信号转导及转录激活蛋白6(signal transducer and activator of transcription 6,STAT6)表达,均为阳性。11例检测分化抗原簇34(cluster of differentiation 34,CD34)表达,其中9例阳性,2例阴性(注:这2例CD34阴性,但是STAT6阳性)。6例检测分化抗原簇99(cluster of differentiation 99,CD99)表达,均为阳性。7例检测淋巴细胞瘤- 2(B-cell lymphoma- 2,Bcl- 2)表达,其中6例为阳性,1例为阴性。6例检测胶质纤维酸性蛋白(blial fibrillary acidic protein,GFAP)表达,均为阴性。11例检测上皮细胞膜抗原(epithelial membrane antigen,EMA)表达,均为阴性。11例检测孕激素受体(progesterone-receptor,PR)表达,其中7例阳性,4例阴性。 6例检测生长抑素受体2(recombinant somatostatin receptor 2,SSTR2)表达,均为阴性。1例检测SSTR2a表达为阴性。10例检测P53表达,其中8例阳性,2例阴性。10例检测细胞增殖核抗原Ki- 67表达,热点1%~15%,其中热点<10% 2例,=10% 5例,>10% 3例。见表2及图3。

图3 SFT标本肿瘤细胞STAT6(图A)、CD34(图B)免疫组化染色阳性(×100)。
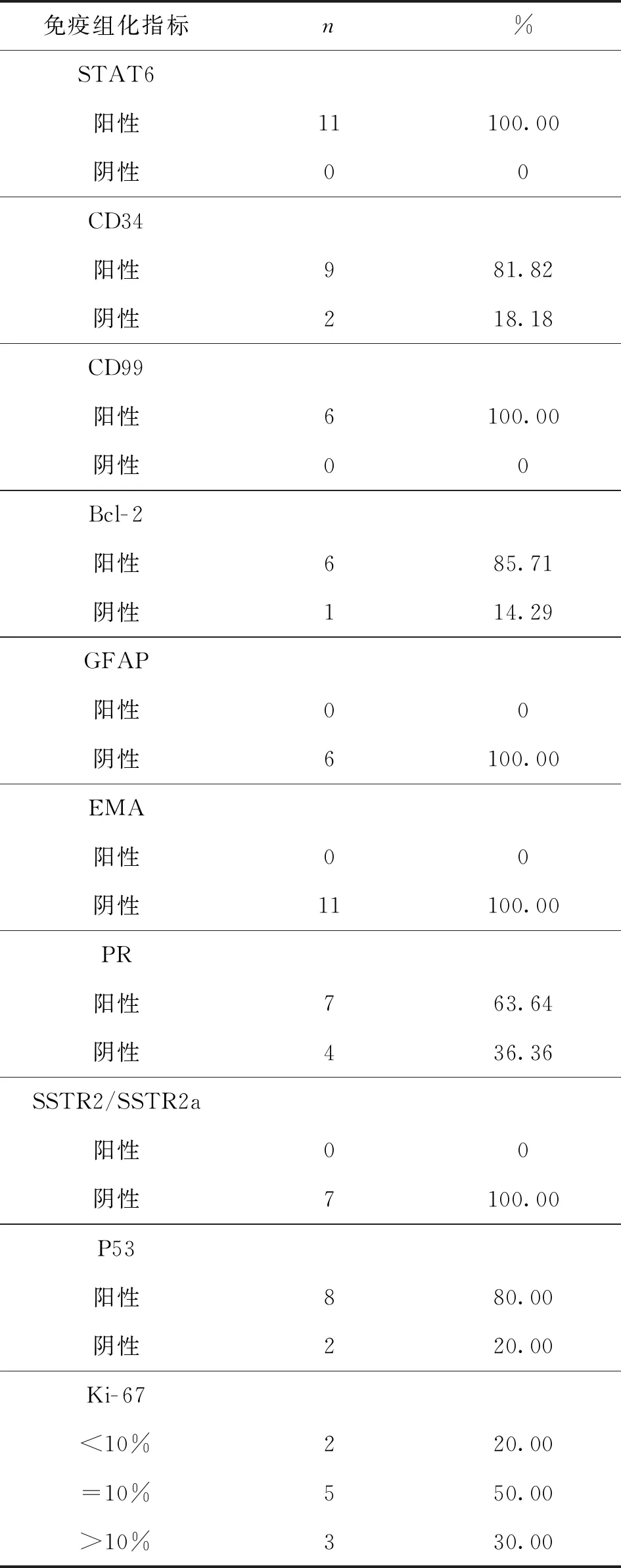
表2 11例SFT的免疫组化指标特点
2.4 SFT患者治疗方案
本组11例患者均接受手术治疗,其中10例病灶行全部切除,1例因病灶与矢状窦粘连行次全切除。术后1例进行放疗及伽马刀治疗,3例进行伽马刀治疗。
2.5 SFT患者随访结果
本组11例患者均成功进行了随访。随访时间范围5~103月,随访时间中位数为27个月。9例全切除病灶患者未见肿瘤复发。2例复发,其中1例既往有颅内SFT手术病史,第一次复发行病灶全切除手术(本次手术),术后约8个月出现第二次复发;1例为接受病灶次全切除术的患者。11例患者均未出现CNS 内外转移。
3 讨 论
1996年,Carneiro等[7]首次报道了颅内SFT。而后,国内外文献陆续报道了CNS SFT的病例,病例数量多为个位数至二十余例的单中心小样本数据[2- 3,8- 9]。本组病例年龄范围:17~60岁,发病年龄范围大;平均年龄(44.18±15.34)岁,主要集中在中年发病。男女性别比为1.2:1,无明显的性别差异。81.8%(9/11)发生于幕上,9.09%(1/11)发生于幕下,9.09%(1/11)发生于椎管内。本组病例就诊的主要症状为颅内压升高引起的头痛、头晕或神经功能障碍引起肢体麻木、乏力或不自主运动等。起病症状没有特异性,主要与病变所在部位密切相关。
在组织病理学上,典型的SFT在镜下表现为梭形、圆形肿瘤细胞疏密不一,富细胞区、少细胞区呈编织状、旋涡状或束状交替排列;间质可见胶原纤维增生。在此基础上,检测免疫组化标志物有助于SFT的诊断及鉴别诊断。在本组病例中,81.82%(9/11)病例CD34阳性。舒凯等[9]报道,在27例CNS SFT病例中,检测CD34表达均为阳性,其中78%(21/27)病例表现为弥漫性阳性,22%(6/27)病例表现为局灶阳性。尽管大量国内外文献报道[3,8-10]及本组病例SFT CD34检测阳性,但CD34表达也可存在于神经纤维瘤、脑膜瘤以及血管和神经肿瘤等病变中[11],因此,CD34不能作为诊断SFT的特异性标志物,但在鉴别诊断中起到一定的作用。近年来,随着分子病理学的发展,研究表明[12-13]:当基因突变时,位于染色体第12位q13带存在两个相邻基因:转录抑制因子NAB2和转录激活因子STAT6,通过产生基因融合NAB2-STAT6诱导细胞增殖,激活EGR1靶基因及其启动子,促进相关基因的表达。在2021年第五版WHO中枢神经系统肿瘤分类标准中,明确提出NAB2-STAT6是SFT发病的关键性基因[1]。Cheah AL等[14]收集54例不同部位的SFT标本以及99例组织形态相似的软组织肿瘤标本,通过免疫组化检测到100% SFT病例的细胞核STAT6染色阳性,并且与SFT标本的来源部位或CD34表达无关。因此,检测STAT6表达在诊断或鉴别诊断SFT时具有一定的特异性,有助于提高诊断的准确性。在本组病例中,11例检测了STAT6,均为阳性(注:其中2例为CD34阴性、STAT6阳性),验证了在SFT病例检测STAT6表达具有较好的特异性及敏感度。
研究表明,在MRI T2序列中,SFT细胞密集区表现为高信号,瘤内胶原纤维成分表现为低信号,因此,T2WI典型信号表现为高低混杂信号,又称为“黑白征”、“阴阳征”[15-16]。本组病例46.15%(6/13)病灶T2WI表现为混杂信号或等-稍高信号。本组病例T2WI信号主要特征与国内外研究报道基本一致[15-16]。
本组病例颅内SFT最容易误诊为脑膜瘤。主要有以下鉴别点[16-18]:①好发部位:脑膜瘤好发于大脑的凸面或矢状窦旁。②MRI:脑膜瘤平扫T1WI、T2WI信号与脑实质信号基本一致;增强常见“脑膜尾征”。③脑膜瘤一般无或轻微瘤周水肿。本组病例椎管内SFT误诊为神经鞘瘤。主要鉴别点[19- 20]:①好发部位:神经鞘瘤好发于神经根鞘部。②病灶影像学典型表现为“哑铃状”,即神经根鞘处病变穿过椎间孔向硬膜外延伸,常伴随椎骨骨质破坏。病灶容易出现囊性变。③MRI:神经鞘瘤T2WI常表现为高信号。
当前,CNS SFT的治疗首选手术最大程度地切除肿瘤病灶,对其临床预后起着至关重要的作用。丁大领等[8]对14例CNS SFT患者进行了6~49月随访,其中12例病灶全切除未出现复发,2例病灶部分切除均出现复发。舒凯等[9]对27例CNS SFT患者进行了平均38个月随访,成功随访接受26例手术治疗的患者(除1例活检未手术),其中21例病灶全切除及1例次全切除术后均未出现复发,5例病灶次全切除术后3例出现复发。在本组病例中,11例均接受手术治疗,其中10例病灶行全部切除,1例因病灶与矢状窦粘连行次全切除。2例复发,其中1例本次接受手术为颅内SFT第一次复发进行手术全切除,1例为接受病灶次全切除术的患者。11例患者均未出现CNS 内外转移。
综上,中枢神经系统SFT是一种罕见的软组织肿瘤,由于临床表现及影像学特点缺乏特异性,难以在术前做出精准的诊断。手术最大程度地切除肿瘤是首选的治疗方法。通过病理组织学检查观察镜下肿瘤细胞形态,以及免疫组化检测相关分子表达(尤其检测到STAT6表达),有助于诊断及鉴别诊断。

