瓜蒌皮注射液中细菌内毒素检查法的建立
王琪 周建华
(上海上药第一生化药业有限公司 上海 200240)
瓜蒌皮注射液为棕黄色的澄明液体,主要成分为瓜蒌皮提取液和注射用水。临床上主要用于行气除满、开胸除痹、痰浊阻络之冠心病、稳定性心绞痛治疗。作为中药注射剂,其质量标准中未制定细菌内毒素的检查项。参考《中国药典》2020版四部9301注射剂安全性检查法应用指导原则,为加强临床使用的安全性和制剂质量的可控性,应考虑设细菌内毒素检查项[1]。
1 材料和方法
1.1 仪器
ET-96细菌内毒素凝胶法测定仪(天津市天大天发科技有限公司);BET-48G6细菌内毒素测定仪(天津市天大天发科技有限公司);XW-80A漩涡混旋器(上海沪西分析仪器厂有限公司);微量移液器(20~200 μL、100~1000 μL,Eppendorf公司);无热原吸咀(250 μL、1000 μL,湛江安度斯生物有限公司);试验所用玻璃仪器均经250 ℃干热灭菌1 h以上。
1.2 试剂
瓜蒌皮注射液(批号1906201、1906202、1906203、1910201、1911201、1912201、2002201、2003201,规格4 mL,上海上药第一生化药业有限公司);细菌内毒素工作标准品(CSE,批号150601-201784,规格80 EU/支,中国食品药品检定研究院);鲎试剂[TAL,批号1903151,规格0.25 EU(0.1 mL);批号1905241,规格0.125 EU(0.1 mL);批号1804200,规格10~0.01 EU(1.35 mL)]、细菌内毒素检查用水(BET,批号1806120,规格5 mL/支)(湛江安度斯生物有限公司);鲎试剂[TAL,批号1809292,规格0.125 EU(0.1 mL)]、细菌内毒素检查用水(BET,批号1811160,规格2 mL/支)(湛江博康海洋生物有限公司)。
1.3 实验方法
1.3.1 细菌内毒素限值(L)的确定
参照《中国药典》细菌内毒素限值L计算方法,L=K/M,注射剂K为5 EU/(kg·h),M为每1 kg体质量每1 h瓜蒌皮注射液最大静脉滴注剂量(12 mL),人均体质量按60 kg计算,则成人理论L=5/(12/60)=25 EU/mL。依据《中国药典》2020版四部通则9301注射剂安全性检查法应用指导原则,限值设定可适当严控至计算值的1/3~1/2,而欧美等国常以计算值的1/4作为标准,从使用安全性角度考虑,则将限值设定为<6.25 EU/mL[1]。
1.3.2 确定最大有效稀释倍数(MVD)
参照中国药典最大有效稀释倍数MVD=cL/λ的计算公式,则c为供试品溶液浓度等于1.0 mL/mL,在凝胶法中λ为鲎试剂的标示灵敏度,最高为0.03 EU/mL,则MVD=1.0×6.25/0.03=208;在动态浊度法中λ为所使用的标准曲线上最低的细菌内毒素浓度0.01 EU/mL,则MVD=1.0×6.25/0.01=625[1]178-181。故确定采用凝胶法时瓜蒌皮注射液的最大有效稀释倍数为208,采用动态浊度法时则最大有效稀释倍数为625,验证时的稀释倍数不应超过其最大有效稀释倍数。
1.3.3 凝胶法干扰试验
1)干扰预实验 选择λ=0.25 EU/mL的低灵敏度鲎试剂进行干扰预实验。取瓜蒌皮注射液用BET制成25、50、100、200倍稀释浓度的供试品溶液,各浓度取0.1 mL,分别加入鲎试剂0.1 mL,每一浓度平行做2次,作为供试品阴性对照(NPC);同时用各稀释倍数下的供试品溶液同比例加入1.0 EU/mL细菌内毒素工作标准品制成含细菌内毒素0.5 EU/mL的溶液,各取0.1 mL,分别加入鲎试剂0.1 mL,每一浓度平行做2次,作为供试品阳性对照(PPC);另取2支鲎试剂,加入BET水作为阴性对照(NC);取2支,加入0.5 EU/mL的细菌内毒素工作标准品溶液作为阳性对照(PC),混匀,用封口膜封口,置于凝胶仪中于37 ℃孵育60 min[2-3]。
2)干扰试验 选择预实验下的无干扰稀释倍数下的供试品溶液和BET,分别将细菌内毒素工作标准品稀释成2.0λ、1.0λ、0.5λ、0.25λ(EU/mL)的系列溶液,用2批来自不同厂家的TAL进行试验,每一浓度平行做4管[3-4]。同时做阴性对照和供试品对照各2管。λC可根据公式λC=antilg(∑lgX/n)计算,式中X为反应终点浓度,n为每个浓度的平行管数。
3)样品细菌内毒素检查 另取5个不同生产批号的瓜蒌皮注射液,用BET将瓜蒌皮注射液稀释成由干扰试验确定的稀释倍数下的供试液,按《中国药典》2020版第四部通则1143的方法进行细菌内毒素检查。
1.3.4 光度测定法——动态浊度法
1)标准曲线可靠性试验 取1支细菌内毒素标准品,加入1 mL BET水,漩涡15 min,用BET水依次稀释制成1.0、0.1、0.01 EU/mL系列浓度的标准品溶液,每个浓度平行做3管,并以BET水作为阴性对照,进行自动检测[2-3]。
2)干扰试验 根据凝胶法确定的MVD,把瓜蒌皮注射液稀释50倍后作为供试液,平行做2管;将瓜蒌皮注射液稀释25倍,与浓度为0.2 EU/mL的细菌内毒素标准品溶液1∶1混合得含细菌内毒素0.1 EU/mL的供试品阳性对照液(稀释倍数为50倍),平行做2管。
2 结果
2.1 凝胶法干扰试验
采用TAL 1903151的预实验结果表明,将瓜蒌皮注射液稀释50、100、200倍时,2管NPC均为阴性,2管PPC均为阳性,则可认为在这些稀释倍数下均无干扰;而稀释25倍时,有时会有干扰(表1)。为操作方便和准确,选择供试品的最小不干扰稀释倍数为50,并以此进行干扰试验。

表1 干扰预实验
分别使用湛江安度斯生物有限公司和湛江博康海洋生物有限公司灵敏度(λ)=0.125 EU/mL的鲎试剂进行干扰试验。试验结果表明不同厂家的鲎试剂,鲎试剂λc均在0.5λ~2.0λ(即0.063~0.250 EU/mL)范围内,鲎试剂灵敏度试验符合要求,瓜蒌皮注射液在稀释50倍时,λc亦在0.5λ~2.0λ范围内,干扰试验有效,认为供试品在该稀释倍数下不存在干扰作用(表2)。
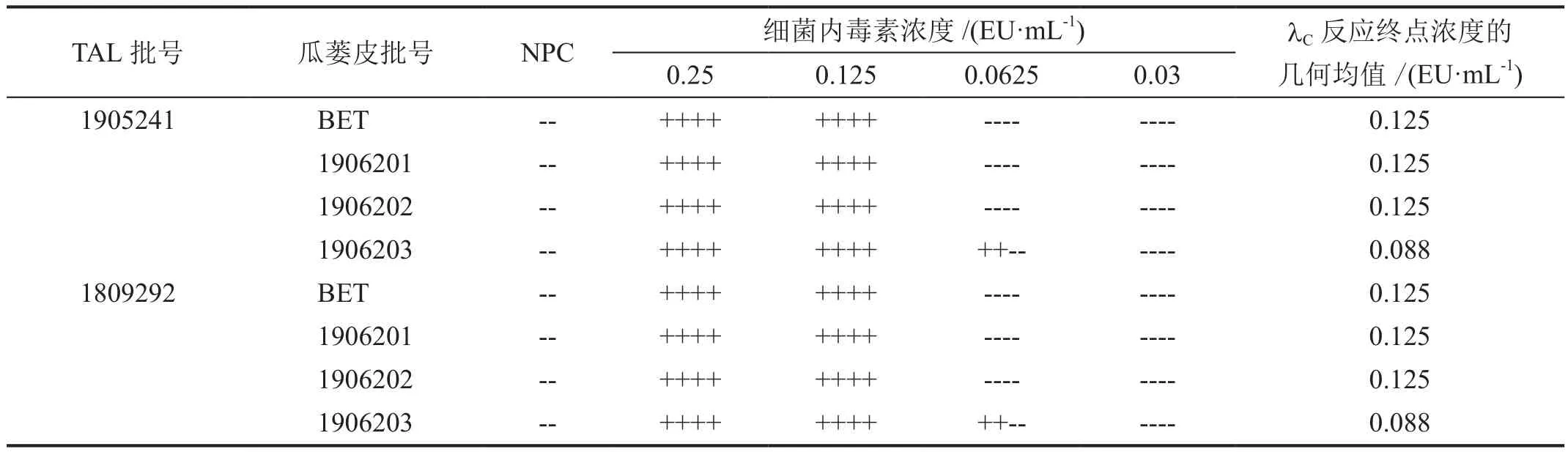
表2 瓜蒌皮注射液稀释50倍后的干扰试验
依据干扰试验确定的条件另取5批其他批号的瓜蒌皮注射液进行细菌内毒素检查,结果均符合规定(表3)。
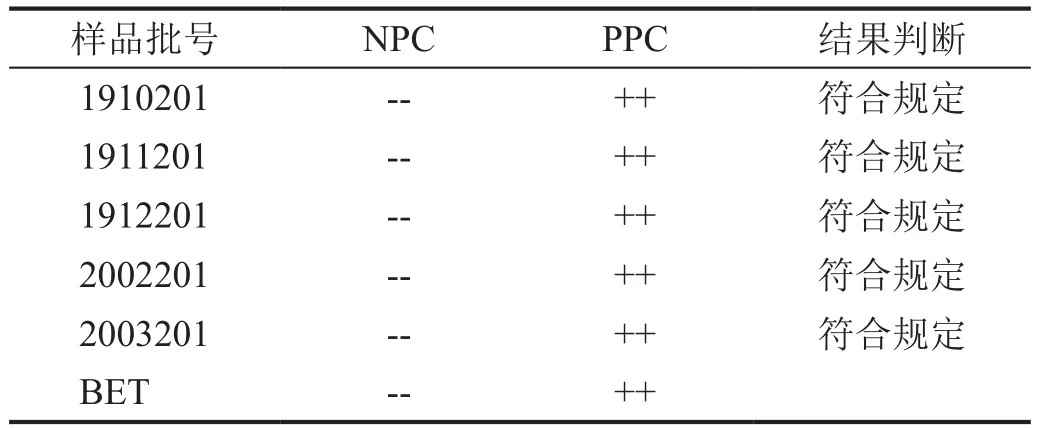
表3 瓜蒌皮注射液细菌内毒素检查结果
综合凝胶法干扰试验结果,瓜蒌皮注射液按上述实验条件可确立该样品的细菌内毒素检查法。瓜蒌皮注射液稀释50倍后试验反应物不干扰,可选择灵敏度为0.125~0.03 EU/mL的鲎试剂作为日常的凝胶法细菌内毒素检测[4-5]。
2.2 动态浊度法标准曲线可靠性试验及干扰试验
根据试验结果,标准曲线lgT=2.663 93-0.276 75lgC,相关系数r=-0.999 9,相关系数绝对值大于0.980;阴性对照的反应时间均大于标准曲线最低浓度的反应时间;变异系数均小于10%;供试品阳性对照的细菌内毒素回收率均在50%~200%[6-7]。这些结果表明,标准曲线是可靠的。选用灵敏度为10~0.01 EU/mL的鲎试剂,供试品溶液稀释至50倍,供试品在此试验条件下不存在干扰作用,干扰试验有效(表4)。
动态浊度法的检测结果表明,3批瓜蒌皮注射液在稀释了50倍后供试液中细菌内毒素的含量分别为0.008 4、0.014 4 EU/mL及未检出,折合原液中细菌内毒素含量为0.42、0.72 EU/mL,均小于限值6.25 EU/mL,符合相关规定(表4)。
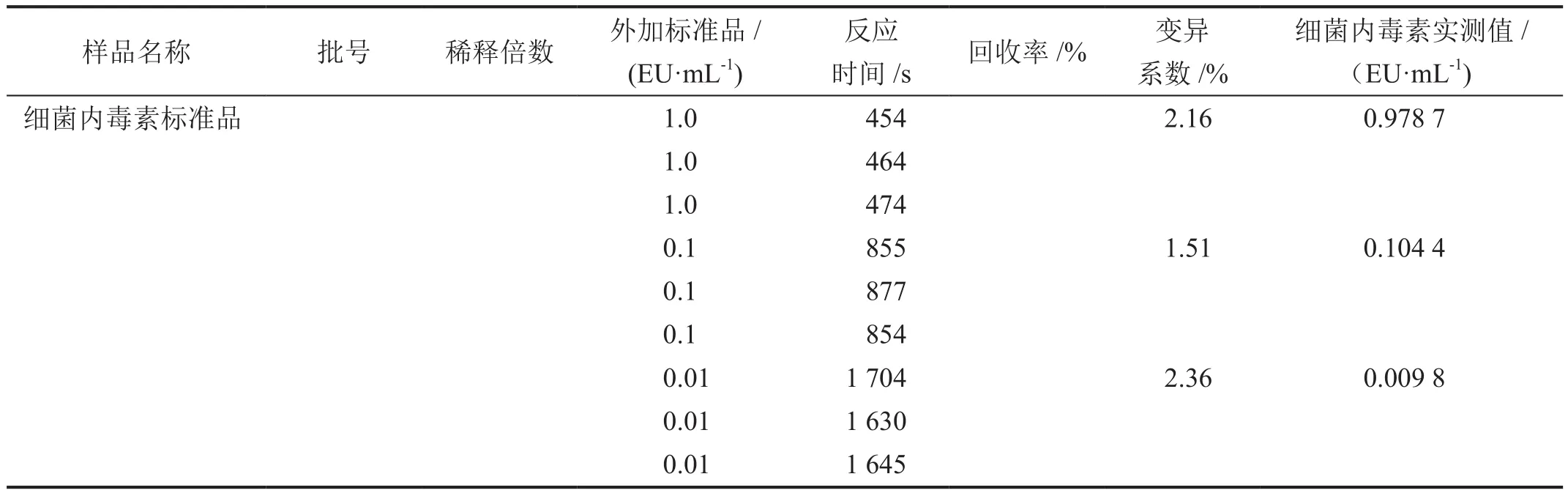
表4 标准曲线可靠性试验及样品干扰试验

(续表4)
从凝胶法和动态浊度法的干扰试验结果来看,瓜蒌皮注射液在稀释50倍后无干扰作用,两种方法试验结果一致。两种方法均可进行瓜蒌皮注射液的细菌内毒素的检查,日常检验可任选其一。
3 讨论
类似瓜蒌皮注射液等的中药制剂,其成分相对复杂,易受到原料产地、生产工艺等干扰因素影响,控制其细菌内毒素对于人体用药安全有重要意义[8-9]。采用动态浊度法可较为准确地检测出样品中真实的细菌内毒素含量,但根据现行中国药典规定,当测定结果有争议时,目前尚以凝胶法的结果为准,故本研究建立的两种方法可为互补。然而,鲎作为国家二级保护动物,堪称海洋里的远古遗民,有“生物活化石”之称,考虑到现在国家对于海洋动物鲎的保护,一些细菌内毒素检测的新方法也有报道,如重组C因子法等[10],以减少鲎试剂的使用量。但目前各厂家重组C因子质量差异较大,还须进行深入的研究才能作为国标用于注射液的细菌内毒素检测。

