糖尿病领域研发态势分析
张丽雯,阮梅花,刘加兰,贺彩红,3,于建荣,3
领域动态
糖尿病领域研发态势分析
张丽雯1,阮梅花1,刘加兰2,贺彩红1,3,于建荣1,3
1.中国科学院上海生命科学信息中心,中国科学院上海营养与健康研究所,上海 200031 2.中国科学院昆明动物研究所,昆明 650201 3.中国科学院大学,北京 100049
糖尿病(diabetes mellitus)是由胰岛素分泌缺乏和/或胰岛素抵抗引起的以高血糖为特征的一类代谢性疾病,已成为威胁全球人类健康的重大疾病之一。本文从论文、专利、药物、产业发展等方面分析了糖尿病领域国内外研发态势,旨在为我国糖尿病领域研究及相关产业发展提供决策参考。结果表明,论文发表方面,糖尿病领域研究的论文数量稳步增长,研究热点主要包括并发症及流行病学研究;技术开发方面,比利时杨森制药、美国礼来制药、德国勃林格殷格翰公司等大型制药企业在糖尿病诊断、治疗、管理等方面积极探索;药物研发方面,截至2022年3月23日,已有207个药物上市,还有大量药物处于临床前及临床阶段;产业发展方面,国内外市场潜力巨大,糖尿病数字化管理快速发展。我国在糖尿病研究和技术开发方面拥有一定的实力,未来需要采取措施加强研究成果转化与产品开发,以满足我国庞大的糖尿病诊疗与管理需求。
糖尿病;研究现状;药物研发;产业发展
根据世界卫生组织(World Health Organization, WHO)的定义,糖尿病(diabetes mellitus)指一组在没有治疗干预的情况下以高血糖为特征的代谢性疾病,由胰岛素分泌缺乏和/或胰岛素抵抗引起。据2022年2月发布的《糖尿病分型诊断中国专家共识》,将糖尿病分为1型糖尿病(type 1 diabetes mellitus, T1DM)、2型糖尿病(type 2 diabetes mellitus, T2DM)、单基因糖尿病、继发性糖尿病、妊娠期糖尿病(gestational diabetes mellitus, GDM)和未定型糖尿病6种类型[1]。
糖尿病已成为威胁人类健康的重大疾病之一。2021年12月,国际糖尿病联盟发布“全球糖尿病地图第10版”(IDF Diabetes Atlas 10th edition),指出2021年全球20~79岁糖尿病患者有5.37亿,约占该年龄段全球人口的10.5%;预计到2030年,这一数值将增长到6.43亿,2045年达到7.83亿。2021年,约1/3的糖尿病死亡发生在60岁以下人群;排除与COVID-19相关的死亡风险,约有670万20~79岁人群死于糖尿病或并发症,占该年龄组全球死亡人数的12.2%。我国也面临着严峻的糖尿病防控形势。2021年,我国20~79岁糖尿病患者总数、未被诊断糖尿病患者数量、因糖尿病导致的死亡人数均排名全球第一,20~79岁群体因糖尿病产生的医疗费用排名全球第二。据估计,2045年我国20~79岁成年人患糖尿病人数将上升到1.744亿人,仍将排名全球第一。
随着糖尿病患者人数的逐年增加,为国家、医疗系统、患者及其家庭带来巨大经济负担。据“全球糖尿病地图第10版”,全球医疗支出中,20~79岁糖尿病患者相关费用从2007年的2320亿美元增加到2021年的9660亿美元,预计到2030年,将达到1万亿美元[2]。因此,糖尿病及其并发症的防治已迫在眉睫。本文基于杂志为纪念胰岛素发现100周年推出的“糖尿病”专题,梳理了糖尿病领域研发历程,并从研究论文、专利、药物研发和产业发展整个创新链角度阐述糖尿病领域的研发态势,分析了我国的研发实力,并提出建议,促进我国糖尿病领域的发展,以满足巨大医疗需求,助力“健康中国2030”目标实现。
1 糖尿病研究历程
根据杂志为纪念胰岛素发现100周年推出的“糖尿病”专题,梳理了及其系列期刊发表的糖尿病相关论文,通过分析100年来的糖尿病研究发展历程中的里程碑事件,发现糖尿病机制研究以及糖尿病干预一直是全球研究的重点[3]。下面重点对T1DM和T2DM的机制、干预、管理等进行论述①以下内容主要整理自Nature杂志推出的“糖尿病”专题文章。。
1.1 糖尿病发病机制被深入探索
在T1DM发病机制方面,1974年,研究人员就认识到T1DM受到遗传因素的强烈影响,存在多基因遗传模式。后续多项研究进一步证明了遗传变异的重要性,并确定了相关重要等位基因的确切位置;2019年,研究人员开发了更新版的T1DM遗传风险评分。20世纪八九十年代,研究人员探索了白介素-1 (interleukin-1, IL-1)、干扰素-γ (interferon-γ, IFNγ)、肿瘤坏死因子(tumor necrosis factor, TNF)等多种与T1DM直接相关的细胞因子的作用机制。同时,青少年糖尿病环境决定因素(the environmental determinants of diabetes in the young, TEDDY)项目对与T1DM相关的肠道微生物组进行了广泛表征,确定了具有保护作用的、与短链脂肪酸(short chain fatty acids, SCFA)发酵和生物合成相关的基因,并研究了肠道微生物群的早期定植以及母乳喂养、分娩方式和其他因素的影响。2019年,发现较高水平的链球菌属、乳球菌属和较低水平的阿克曼菌属可以改变T1DM风险婴儿体内的微生物组,参与T1DM的发展,T1DM受病毒感染的影响成为T1DM病因学的研究前沿。
在T2DM发病机制方面,研究人员探索了肠促胰岛素效应及遗传因素的影响。1987年发现胰高血糖素样肽1 (glucagon-like peptides 1, GLP1)是胰岛素分泌的调节剂。除了增加葡萄糖刺激的胰岛素分泌外,GLP1还具有抑制胰高血糖素分泌、胃排空和食物摄入,以及刺激β细胞增殖等多种功能。1988年,研究人员发现葡萄糖转运蛋白4 (glucose transporters 4, GLUT4)的细胞内转运受胰岛素信号转导调控,之后多项研究揭示GLUT4在T2DM中发挥重要作用。同时,基因组测序技术的发展推动了T2DM相关致病基因的发现。2000年,研究人员通过全基因组关联研究(genome-wide association study, GWAS)评估了16种与T2DM相关的基因;2007年3项GWAS研究确定了和或其附近的T2DM易感基因座。此外,研究人员探索了T2DM中的胰岛炎症机制、免疫介导的胰岛炎症过程等。
其他糖尿病的发病机制研究方面,目前已在多个基因中发现青年发病型糖尿病(maturity-onset diabetes of the young, MODY)的相关突变,包括和。GDM被认为是遗传基因、炎症因子与脂肪细胞因子、胰岛素抵抗和氧化应激等多种因素共同作用的结果[4]。在相关研究中,动物模型发挥了重要作用。目前糖尿病动物模型主要有胰腺部分切除动物模型、自发性遗传动物模型、药物/食物诱导型动物模型和基因编辑动物模型等[5],未来需要开发能用于指导转化和更准确地预测糖尿病治疗结果的模型。
1.2 糖尿病干预措施不断改进
百年来,糖尿病治疗与干预不断取得进步。从1922年开始用动物来源胰岛素治疗,1965年中国科学家在世界上首次人工合成结晶牛胰岛素,到20世纪70年代末利用DNA重组与合成技术合成升级版的胰岛素(人工合成人胰岛素),目前胰岛素已经成为糖尿病尤其是T1DM治疗的常规药物。成功合成人胰岛素是糖尿病治疗向前迈出的重要一步,为美国食品药品监督管理局(U.S. Food and Drug Administration, FDA)批准更多治疗性重组蛋白(已批准100多种)奠定了基础。
T1DM治疗与干预主要包括单克隆抗体、干细胞疗法和免疫疗法三类。20世纪90年代,CD3特异性单克隆抗体研发获得进展,2002年一项临床试验首次证明免疫调节CD3特异性抗体能减缓T1DM患者β细胞功能的丧失。未来CD3特异性单克隆抗体试验,包括与其他免疫调节药物联合使用的试验,在保护β细胞功能和恢复T1DM的免疫耐受方面具有巨大潜力。糖尿病干细胞疗法始于1998年,到21世纪初该领域受益于模式生物胚胎研究,取得一些突破,2010年以后加速发展。但是,目前仍然没有针对T1DM的β细胞替代疗法。该领域需要进一步优化成熟β细胞生产的效率,需要解决保护移植的干细胞衍生β细胞免受免疫排斥并确保其纯度等重要问题。免疫细胞疗法方面,Marek-Trzonkowska等[6,7]于2012年和2014年发表了调节性T细胞(regulatory T cell, Treg)在T1DM治疗中的临床试验结果,证明了Treg治疗的安全性及耐受性。此外,研究人员使用基因工程开发胰岛特异性Treg细胞,使用嵌合抗原受体或转基因T细胞受体开发糖尿病免疫疗法。
针对T2DM致病机制,研究人员探索了手术、药物、饮食和运动等多种干预措施。1995年研究人员发现减重手术可以延缓T2DM的作用机制。2006年,发现接受胃旁路手术(Roux-en-Y gastric bypass, RYGB)有助于改善血糖控制,这一发现在2010年和2013年的研究中被进一步证实;2014年,发现垂直袖状胃切除术通过增加循环胆汁酸水平和改变肠道微生物群落对血糖控制产生积极影响。药物开发方面,研究人员开发出针对肠促胰岛素的药物,2017年随着GLP1类似物Semaglutide的3期临床试验结果公布,这类药物受到关注[8]。GLP1受体激动剂(GLP1 receptor agonists, GLP1RA)是一类多肽药物,耐受性良好,尽管会加剧低血糖,但与其他降糖药(如短效胰岛素)相比,不良事件的风险降低;GLP1RA还可以降低T2DM患者发生动脉粥样硬化性心血管疾病和肾脏疾病的风险,对肥胖和胰岛素抵抗相关的其他疾病也有治疗益处。同时,新一代降糖疗法如empagliflozin(一种钠–葡萄糖协同转运蛋白2抑制剂,SGLT2i),除了能控制血糖水平,还能显著减少心力衰竭和慢性肾病等并发症的发生。目前T2DM的常见药物有胰岛素、二甲双胍、噻唑烷二酮类、磺酰脲类、GLP-受体激动剂等[9]。此外,饮食和运动等行为干预也可以降低T2DM发病率。
近年来,大数据和人工智能等新技术、新方法的应用,为糖尿病治疗带来变革。例如2014年,El-Khatib等[10]报告了在门诊中使用闭环双激素输送系统。与传统胰岛素泵治疗相比,使用闭环双激素输送系统能使平均血浆葡萄糖水平持续降低。目前,已有少数混合闭环系统获准在欧洲和美国上市,另有大型试验正在进行中,未来将有更多的闭环系统被批准上市。此外,人工智能为糖尿病患者制定个性化饮食等糖尿病管理方面也取得突破。例如上海市第六人民医院与上海交通大学联合研发了一款健康饮食分析软件Dimax,不仅能够自动识别食物种类及其营养成分,也能够帮助糖尿病患者建立良好的饮食习惯,加强患者的自我管理[11]。
1.3 有效管理糖尿病及其并发症是改善患者生活质量的根本
由于长期以来没有有效的治愈疗法,研究人员转变研究思路,将糖尿病作为重要慢性病来加强管理,重点在血糖管理和糖尿病并发症的管理。20世纪中叶,糖尿病与神经病变、视网膜病变和肾病等退行性疾病之间的联系已经得到证实。但直到比利时Jean Pirrat医生1978年发表其开创性的纵向研究结果后,糖尿病并发症与血糖控制之间的确切关系才被充分认识。到1983年,糖尿病控制与并发症试验(DCCT)招募患者以研究强化治疗②指用外部泵或每天注射3次或更多次胰岛素,目标是实现血糖控制接近于尽可能安全的非糖尿病范围。是否可以改善1型糖尿病患者的预后,研究结果于1993年发表,标志着糖尿病管理的新时代到来。20世纪80年代开始的我国大庆启动的大规模随机对照试验,通过行为干预③健康饮食和/或运动。降低T2DM发病率。经过长期的纵向队列研究表明,通过健康饮食和加强运动等物理手段,可以改善糖尿病患者生活质量。在糖尿病并发症的药物研发方面,主要包括醛糖还原酶抑制剂、血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂、内皮素受体拮抗剂、他汀类降脂药、抗氧剂、抗血小板药、钙拮抗剂等[12]。
糖尿病百年研究里程碑事件见图1。
2 从文献看糖尿病研究现状
利用Web of Science数据库对糖尿病研究现状进行分析。2017~2021年,Web of Science数据库共收录了糖尿病研究论文180,080篇,进一步从年度趋势、国家/地区分布、主要机构以及研究热点等方面对这些论文进行分析④检索式:ts=(diabete$ or diabetic or prediabete$ or prediabetic) and py=(2017-2021),文献类型:Article+Review;检索日期:2022-03-24,数据库更新日期:2022-03-23。。
2.1 近年来糖尿病论文量稳步增长
近年来,糖尿病领域论文量持续稳定增长,从2017年的30,574篇增长到2021年的43,547篇,增长了42.43% (图2)。
2.2 美国发表论文量遥遥领先
美国发表论文量最多,其ESI (Essential Science Indicators, 基本科学指标)高水平论文量⑤ESI高水平论文量是指ESI高被引论文与ESI热点论文之和。也远高于其他国家,ESI高水平论文量占比为2.83%;中国论文量排名第二,ESI高水平论文量在论文量排名前10位国家中排名第三,ESI高水平论文量占比较低,在论文量排名前10位国家中排名第10位(表1)。
2.3 国内机构研究实力与国际相比存在一定差距
美国哈佛大学、加拿大多伦多大学、丹麦哥本哈根大学等机构在糖尿病研究中表现突出,全球论文量排名前10位的机构中,欧洲的机构有5所,占50%;美洲的机构4所,澳洲的机构1所,表明欧洲机构在糖尿病研究领域有较强实力。
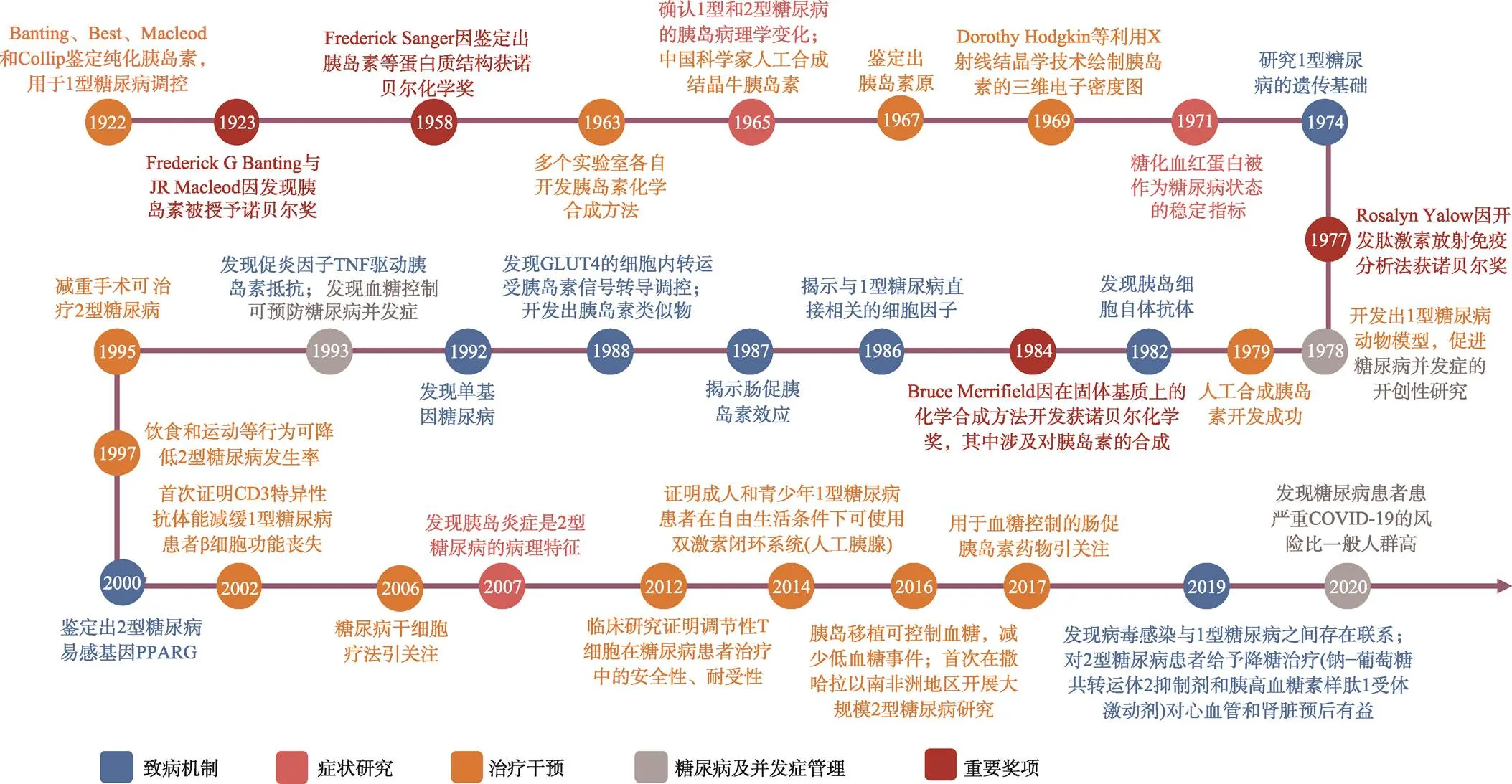
图1 过去100年糖尿病研究里程碑事件⑥整理自Nature杂志为纪念胰岛素发现100周年推出的“糖尿病”专题。
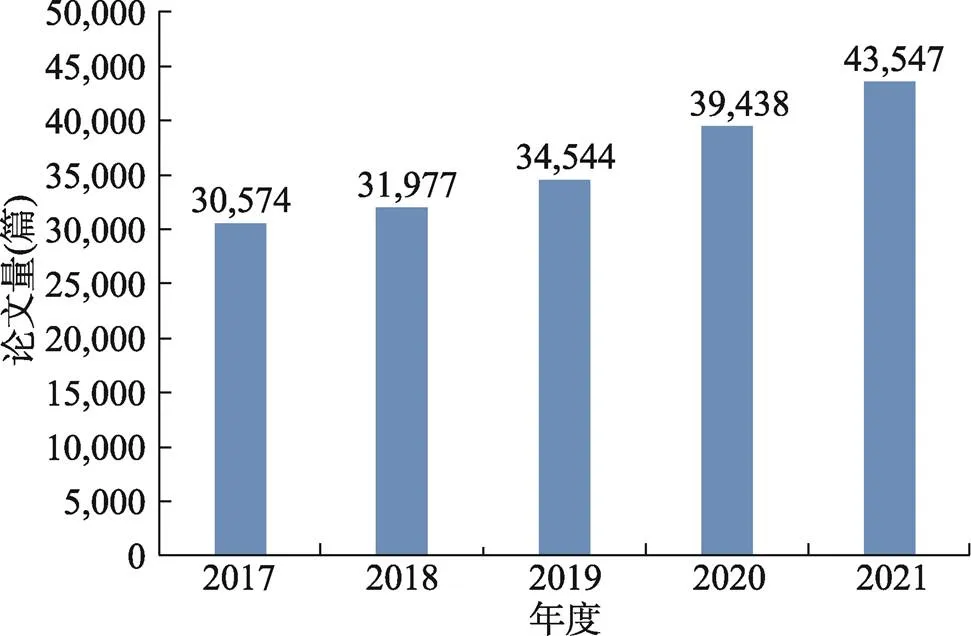
图2 2017~2021年糖尿病领域论文量
比较论文量排名前10位的国际国内机构,国际机构的论文量、ESI高水平论文量及其占比都高于中国机构。ESI高水平论文量及其占比可以从一定程度上反映研究质量。ESI高水平论文量国际机构大部分超过100篇,我国机构大部分在20~40篇之间;ESI高水平论文量占比指标,国际机构主要在4%~6%之间,而我国多数在1%~3%之间,有一定的差距(表2)。

表1 2017~2021年糖尿病领域论文量排名前10位国家及ESI高水平论文量情况
2.4 糖尿病并发症及流行病学是近年来研究热点
利用VOSviewer软件对糖尿病领域2020~2021年67,877篇论文⑦文献类型限定到Article。进行关键词聚类,以显示糖尿病领域目前的研究热点(图3)。

表2 论文量排名前10位国际机构与中国机构
(1)糖尿病并发症发病机制研究(红色聚类)
糖尿病并发症主要可能原因包括氧化应激、炎症、各种功能紊乱或障碍等。例如氧化应激导致葡萄糖自身氧化造成线粒体超负荷,活性氧(ROS)增多,细胞内抗氧化的还原型辅酶Ⅱ(NADPH)量不足,促进肾小球细胞外基质合成增多、降解减少,导致小球纤维化,最终诱发糖尿病肾病[13];炎症方面,过多的自由基使得体内的炎症细胞因子和化学引诱物增多,同时释放的氧自由基对β细胞造成一定的损害,从而抑制了胰岛素的释放,并且炎症过程也会抑制机体对胰岛素的吸收,T2DM通过上调炎症细胞的水平,包括IL-6、IL-1b、COX-2,从而影响神经系统,导致焦虑、抑郁等症状。氧化应激、炎症反应和内皮功能的紊乱与心血管疾病发病相互影响,互为相关因素[14]。
(2)糖尿病与新冠病毒关系研究(绿色聚类)
主要分为两类:第一类:糖尿病患者感染新冠病毒死亡率显著提高。在新冠患者中,糖尿病患者死亡率达7%,排名第二,仅次于心脏病患者,其机制是SARS-CoV-2病毒在与B类1型清道夫受体(scavenger receptor, class B type 1,SR-B1)结合时,可以粘附在胆固醇分子上,促进病原体在体内定植、感染细胞[15];第二类:新冠患者患糖尿病概率显著提高。感染新冠病毒后,人体内β细胞中的胰岛素分泌量减少,出现胰岛素不耐受、血糖水平升高等情况,而且,新冠病毒可能导致促炎症信号物质(细胞因子)的强烈释放,损害胰岛素的有效性,从而导致新冠患者患糖尿病概率显著提升[16]。
(3)糖尿病流行调研与管理(蓝色聚类)
包括主要发生成儿童和青少年的1型糖尿病[17],主要发生在成年人的2型糖尿病和单基因型糖尿病的流行病学研究,并通过加强老年糖尿病患者教育以提高糖尿病并发症管理效果[18]。
(4)妊娠期糖尿病研究(黄色聚类)
妊娠期糖尿病主要是由于妊娠期母体发生了一系列生理变化导致的。妊娠期糖尿病对于孕妇、胎儿和新生儿都有极大影响。如:对孕妇,会使胚胎发育异常甚至死亡、羊水过多发生率提高、易发生糖尿病酮症酸中毒;对胎儿,使巨大胎儿发生率提高、胎儿生长受限、易早产流产;对新生儿,会使新生儿呼吸窘迫综合征发生率增高等[19]。
(5)糖尿病治疗药物研究(紫色聚类)
包括各类药物的研究,如:钠依赖的葡萄糖转运蛋白2(sodium-dependent glucose transporters 2, SGLT-2)抑制剂,其可以抑制肾脏对葡萄糖的重吸收,使过量的葡萄糖从尿液中排出,降低血糖[20]。
(6)糖尿病视网膜病变机制及治疗研究(淡蓝色聚类)
糖尿病视网膜病变(diabetic retinopathy, DR)是糖尿病最常见的微血管并发症之一。DR以是否有从视网膜发出的异常新生血管作为判断标准,可分为增殖性糖尿病视网膜病变和非增殖性糖尿病视网膜病变。近年来,人工智能技术应用分析眼科疾病的影像,使AI可对糖尿病视网膜病变进行自动分析和辅助诊断[21],促进了该领域的迅速发展。
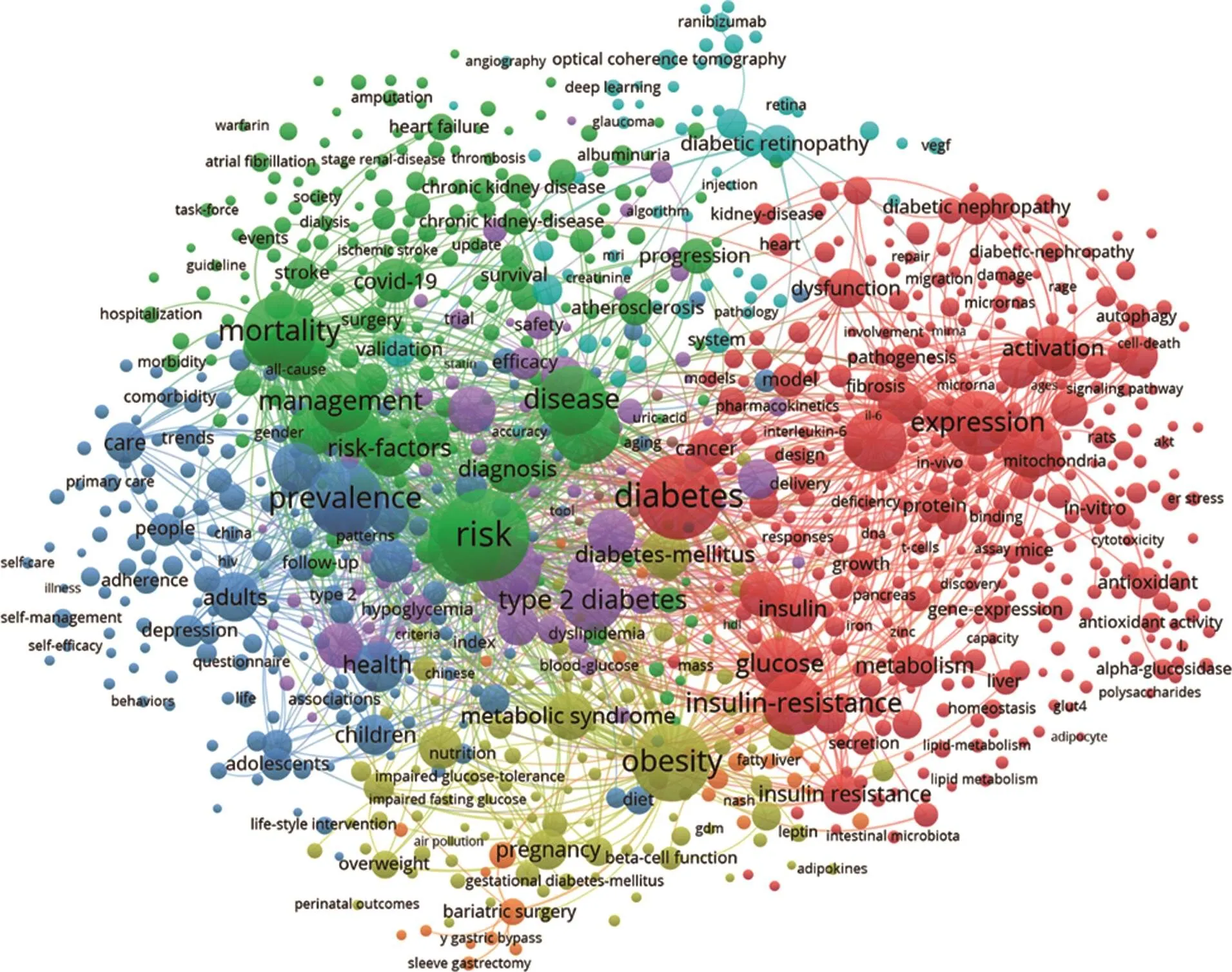
图3 2020~2021年糖尿病领域研究热点
3 从专利看糖尿病技术研发进展
利用incoPat数据库对2017~2021年糖尿病领域专利数据进行检索、分析,截至2022年3月27日,共检索到相关专利25,792件(合并申请号)。进一步从申请/公开趋势、专利申请来源国家/地区、重要国际国内机构、专利技术重点等进行分析。
3.1 全球专利申请量稍有下降,公开量持续增长
2017~2021年,全球糖尿病领域专利申请量稍有下降,专利公开量呈不断增长趋势。由2017年的1644件上升到2021年的7344件,表明该领域有越来越多的专利通过评审后公开(图4)。
3.2 中国专利申请量居全球首位,占全球比例逐年提升
从专利申请来源国看,2017~2021年糖尿病领域相关专利申请量排名前10的国家分别为:中国、美国、韩国、日本、印度、英国、瑞士、德国、比利时、丹麦,主要分布在亚洲及欧美地区。其中,仅中国(10,833件)专利申请量超过1万件,占该领域全球专利申请总量的42.00% (图5)。
2017~2021年,中国专利申请量略有下降,占全球的比例呈不断上升趋势。2017~2019年比例维持在40%左右,尤其是2021年达60.20%(由于专利申请公开滞后等原因,数据供参考),一定程度呈现出我国在糖尿病研究领域的创新活力(图6)。
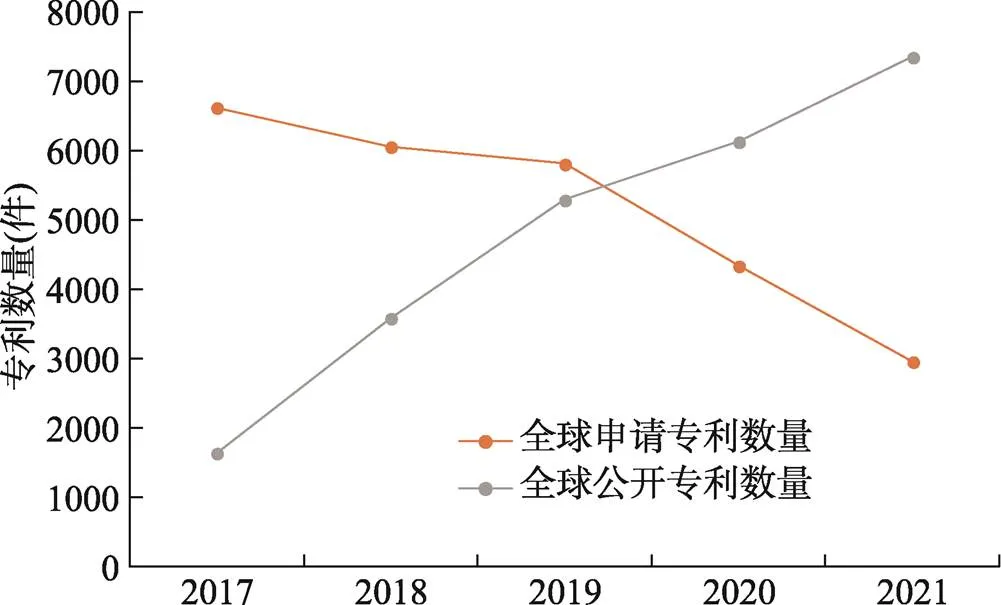
图4 2017~2021年糖尿病领域专利申请与公开量趋势
专利公开和专利申请相比有一定滞后,近两年数据仅供参考。一般发明专利在申请后3~18个月公开,实用新型专利和外观设计专利在申请后1~15个月公开。
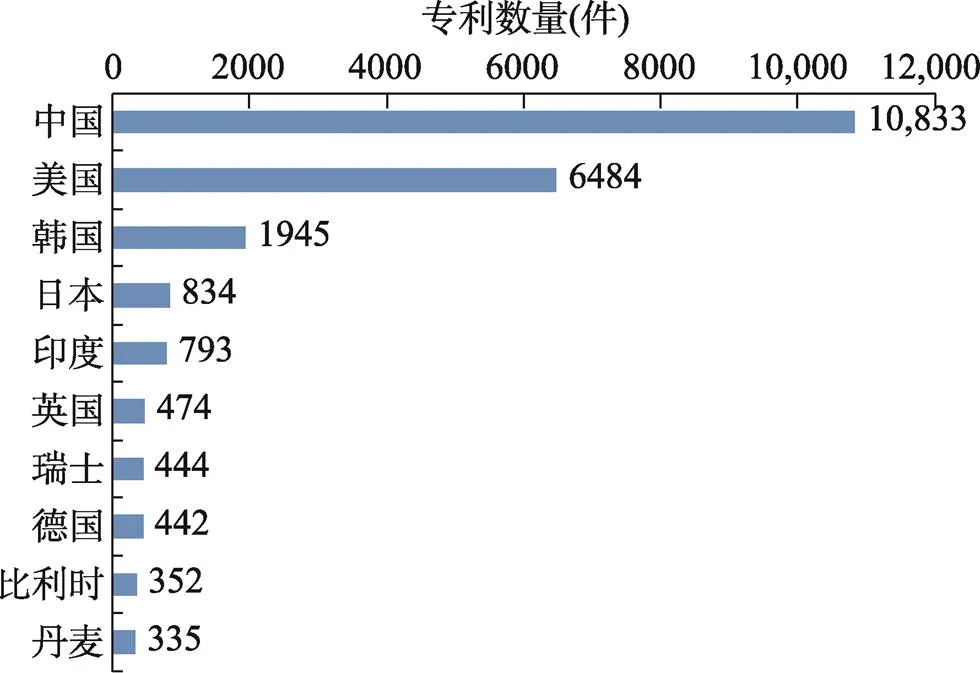
图5 2017~2021年糖尿病领域专利量前10的专利申请来源国
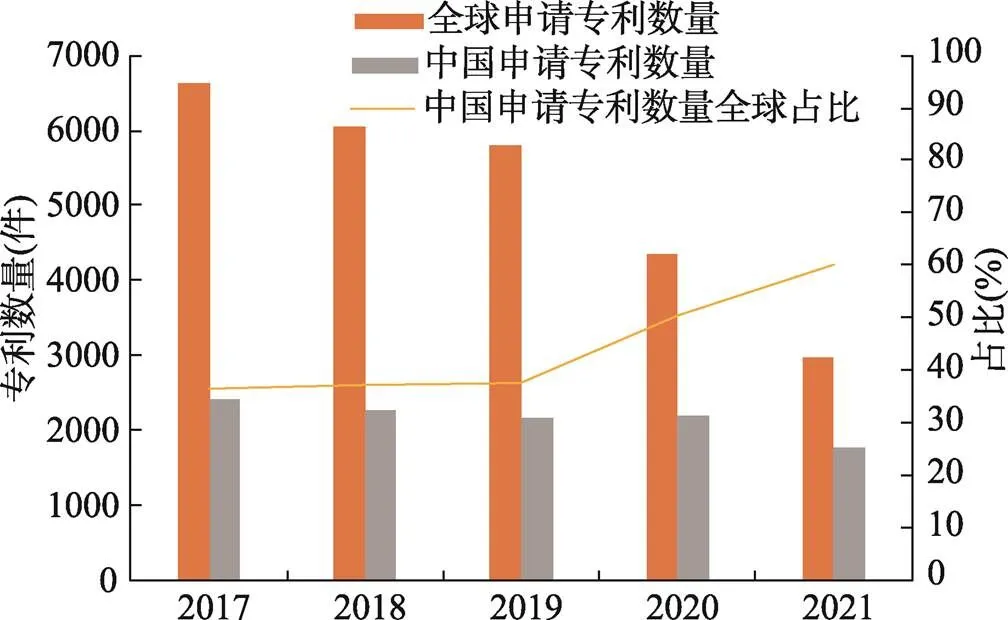
图6 2017~2021年中国糖尿病领域专利申请全球占比情况
3.3 制药企业是全球糖尿病领域专利申请主体
对糖尿病领域专利申请人进行分析,发现国外制药企业是糖尿病专利申请主体。全球Top10申请机构分别为:比利时杨森制药(292件)、美国礼来制药(172件)、德国勃林格殷格翰公司(104件)、丹麦诺和诺德公司(91件)、中国药科大学(86件)、美国默沙东(85件)、美国德克斯康公司(82件)、瑞士罗氏公司(78件)、美国安进公司(76件)、美国MD Healthcare公司(70件)。除中国药科大学,其他9家均为企业。
对于我国糖尿病领域专利,申请主体为高校及科研院所。我国Top10申请机构分别为:中国药科大学(86件)、江南大学(59件)、浙江大学(53件)、中山大学(36件)、吉林大学(35件)、中国科学院上海药物研究所(30件)、四川大学(28件)、复旦大学(28件)、天津科技大学(28件)、上海齐鲁锐格医药研发有限公司(27件)。除上海齐鲁锐格医药研发有限公司,其他9个均为高校或科研院所。
3.4 药物活性成分研发是糖尿病专利技术重点
利用incoPat数据库对全球专利进行聚类分析,可以发现全球糖尿病技术领域研究热点分布在糖尿病诊断、治疗、管理的各个方面(图7)。
(1)肽类化合物及衍生物、胰岛素及类似物、酶抑制剂等糖尿病预防、治疗药物开发。例如,一种短链胜肽组合物可以增加血管内皮生长因子,促进伤口修复愈合(尤其是糖尿病患者难愈的伤口) (TW109124127);一种由SEQ ID NO:1的氨基酸序列组成的新型肽,可有效治疗或预防1型糖尿病(CN202080018425.9);蛋白酪氨酸磷酸酶1B (PTP1B抑制剂)在糖尿病治疗中有良好效果(JP2021009651);研究人员制备的一种新的二取代吡唑化合物可作为己酮糖激酶抑制剂,在2型糖尿病、糖尿病肾病等代谢性疾病治疗中发挥重要作用(WOUS20037894)。
(2)糖苷类、双胍类、脂肪酸类、黄酮类降糖药物及组合制剂开发,包括对蒲黄、野生核桃、红树等可降低血糖水平的植物提取物的研究。研究人员利用新方法得到的C-糖苷类衍生物具有良好的稳定性、溶出性,能有效起到治疗糖尿病、降低血糖的疗效(CN113045525B);研究人员通过用不同溶剂提取泡囊酸模叶并用色谱法分离得到黄酮类化合物,具有一定的抗糖尿病活性(IN202141060142);达帕利嗪L-脯氨酸和二甲双胍的组合制剂的储存稳定性和性质稳定性高,溶解速率快,给药方便,可用于预防或治疗糖尿病或糖尿病并发症(PH12020500532)。在植物提取物相关研究方面,研究人员从红树植物BURGUIERA SEXANGULA的树皮中分离得到Bruguierin C化合物(AU2021106724),可用于控制高血糖和治疗非胰岛素依赖型糖尿病。
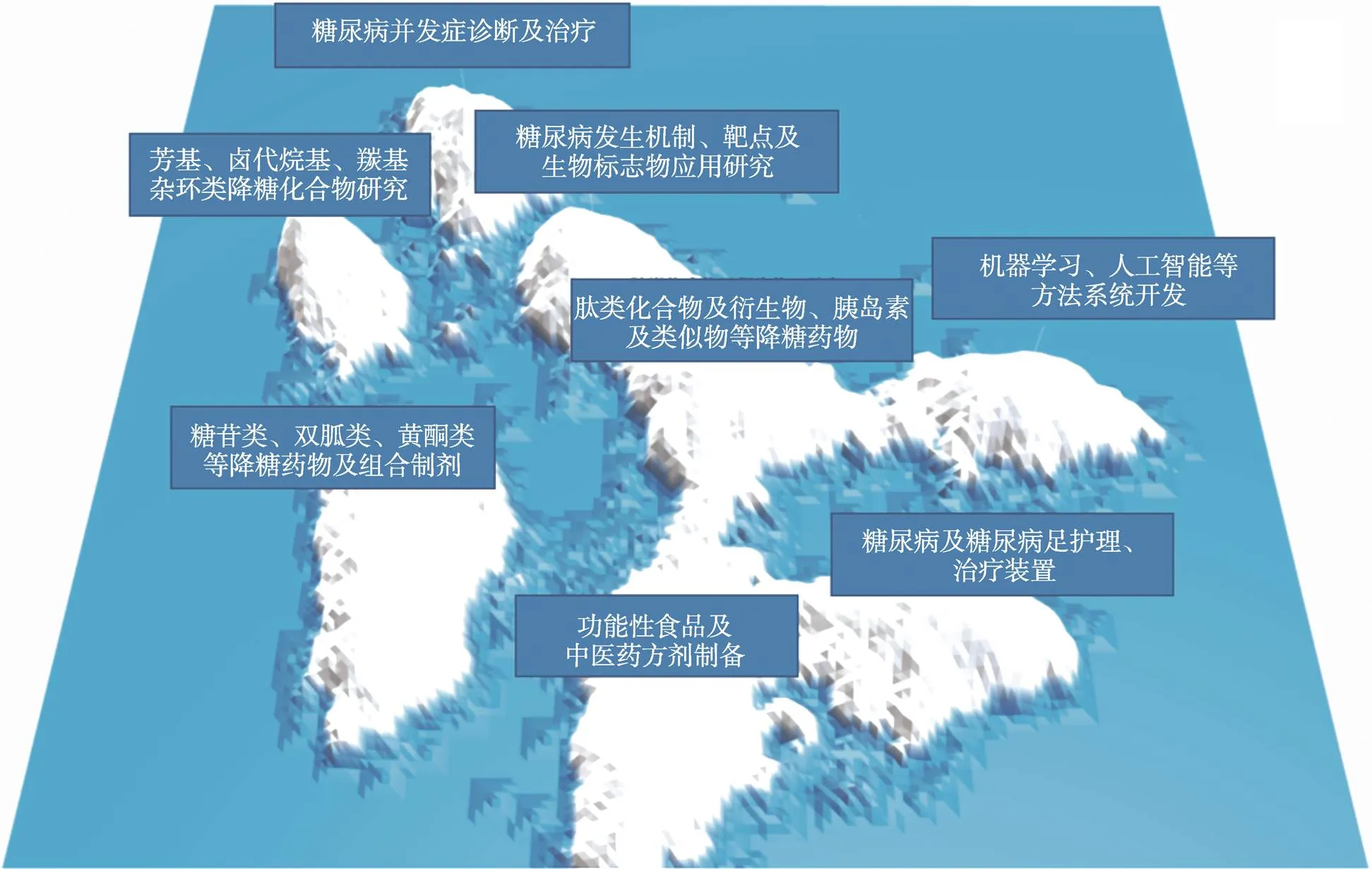
图7 全球糖尿病领域专利技术重点
(3)杂芳基、卤代烷基、磺酰胺类、羰基杂环类降糖化合物及衍生物研究。例如,可用于治疗糖尿病的新的6-芳基-4-(吗啉-4-基)-1H-吡啶-2-酮化合物(HRP20201400);作为ALK4/5抑制剂的稠环杂芳基化合物可用于肥胖症、糖尿病、非酒精性脂肪性肝炎等(IN202127036322);一种羰基杂环类化合物可以用于治疗自身免疫性疾病、糖尿病等(CN202111101581.4);咪唑并杂芳基类衍生物作为GLP-1受体激动剂,可用于制备治疗和/或预防糖尿病的药物(CN202110659950.5)。
(4)糖尿病发生机制、靶点及生物标志物应用研究,包括诊断试剂盒开发、治疗性抗体研究等。例如,一种检测糖尿病肾病易感性的试剂盒可根据扩增产物解读糖尿病肾病易感性基因型(CN202010817155.X);一种可用于快速检测新生儿糖尿病ABCC8 c.1686C>CT位点突变情况的引物,检测结果准确,在临床鉴别诊断上有重要参考意义(CN201911199221.5)。在治疗性抗体研究方面,研究人员公开了一种制备ALK7结合蛋白的方法,发现靶向ALK7治疗糖尿病的有效性(US17350608);抗CXCR3抗体可用于在1型糖尿病的诊断和治疗中(IL271697)。
(5)控制血糖的相关功能性食品及中医药方剂制备等,主要为中国专利。例如,一种含有苦瓜提取物的微生物代谢产物的组合物,能够使抗氧化作用和降血糖作用最大化(KR1020210018340);由水和天然材料制成的集成粥(植物+海藻+鱼+坚果+肉+杂粮),可以降低钠含量及血糖水平(US17293022);具有防治糖尿病功效的组合物包括大豆肽、苦瓜肽、葫芦巴种子提取物、仙人掌提取物、人参提取物、罗汉果甜苷等多个组分,实现了组分间的协同增效,适合糖尿病人群长期使用(CN201911332439.3);一种纯中医药治疗糖尿病的组合物采用多种中药组合,包括柴胡、郁金、白芍、黄芩、香附、陈皮、枳壳、党参、白术、山药、茯苓、生地、知母、天花粉、黄精、泽泻、茵陈丹参、白桦茸菌、甘草、绞股蓝等,可以有效改善糖尿病的症状(CN202111196112.5)。
(6)糖尿病及糖尿病足患者护理、治疗等装置开发,主要为中国专利。例如,一种新型的胰岛素注射笔具有定量注射的优点,可避免因注射胰岛素剂量不准确而对身体造成的负面影响,方便中老年糖尿病患者使用(CN202120597950.2);针对糖尿病足患者开发的一种糖尿病足创面的护理装置设置了脚面按摩组件,能够对患者脚面进行按摩,并对患者脚部进行加热,解决了现有装置不能对患者脚面进行护理的问题(CN201910994838.X);研究人员研发的一种中医糖尿病足治疗装置包括足疗箱本体和药草盒,可避免足疗箱本体箱内的水分热量过大烫伤到患者脚部,减轻了护理人员的工作负担,具有一定的实用性(CN202021594901.5)。
(7)糖尿病并发症诊断及治疗研究。例如,研究人员开发了一种能够特异性诊断糖尿病肾病的生物标志物miRNA-125b-5p和/或miRNA-181b-5p (JP2020551094);一种或多种特异性结合活性血浆激肽释放酶(例如人血浆激肽释放酶)的抗体的组合物,可用于治疗糖尿病性黄斑水肿(IN202118028473);基于糖尿病性肝损伤的治疗靶点,香叶基香叶基转移酶(GGTase 1)抑制剂的特定剂型可作为抗糖尿病性肝损伤的肝保护剂(IN202011036305);用于治疗肾功能损伤的糖尿病的葡糖激酶激活剂(GKA)可用于预防或改善糖尿病合并慢性肾脏病(US17338555)。
(8)机器学习、人工智能等方法及系统开发,用于糖尿病诊断、管理、评估及监测。例如,基于人工智能的语音命令葡萄糖监测和确定系统,可在通过输入的语音识别患者的葡萄糖水平后,学习和确定对患者的胰岛素可输送量,并进一步在用户设备上提供数字音频输出(IN202121019989);研究人员研发出一种智能的糖尿病管理系统,可以跟踪/确定糖尿病患者的位置,以及时向医护人员、家人、朋友等提供相关信息(US17450865);一种基于k-meas方法的糖尿病风险预警系统改进了聚类中心方法,从糖尿病数据集特征出发,建立了糖尿病分段函数预警模型,提高了糖尿病预警能力,有助于提供准确的糖尿病预防与治疗措施(WOCN20080251)。
4 糖尿病药物研发现状
利用Cortellis数据库对糖尿病领域的药物研发情况进行分析⑧Indication中用diabetes检索,获得的适应症,不考虑Diabetic angiopathy糖尿病血管病并发症,因并发症中的药很多是治疗其他疾病,顺便治疗糖尿病并发症的,干扰比较大,所以不要。检索日期:2022-03-23。。结果表明,糖尿病及其并发症领域目前有效的在研药物1285个⑨去除无进展报道、中止、撤回的药物。。
4.1 已上市一定数量的药物,大部分处于临床前阶段
在糖尿病领域,已有上市药物207个,注册阶段的药物15个,注册前18个,临床3期62个;处于临床前阶段的有502个,发现阶段171个。可以看出,糖尿病领域虽然是一个重要的慢性疾病领域之一,已经有一定数量的药物上市,但是仍有约一半的新药处于临床前及发现阶段,表明这个领域未来仍将快速发展,将有较多药物上市(图8)。
4.2 美国研发药物数量最多
研发药物数量最多的美国,共计开发了667个;中国排名第二,共开发了392个药物(包括跨国制药公司在中国开发的药物);排名第三的是韩国,为227个(图9)。
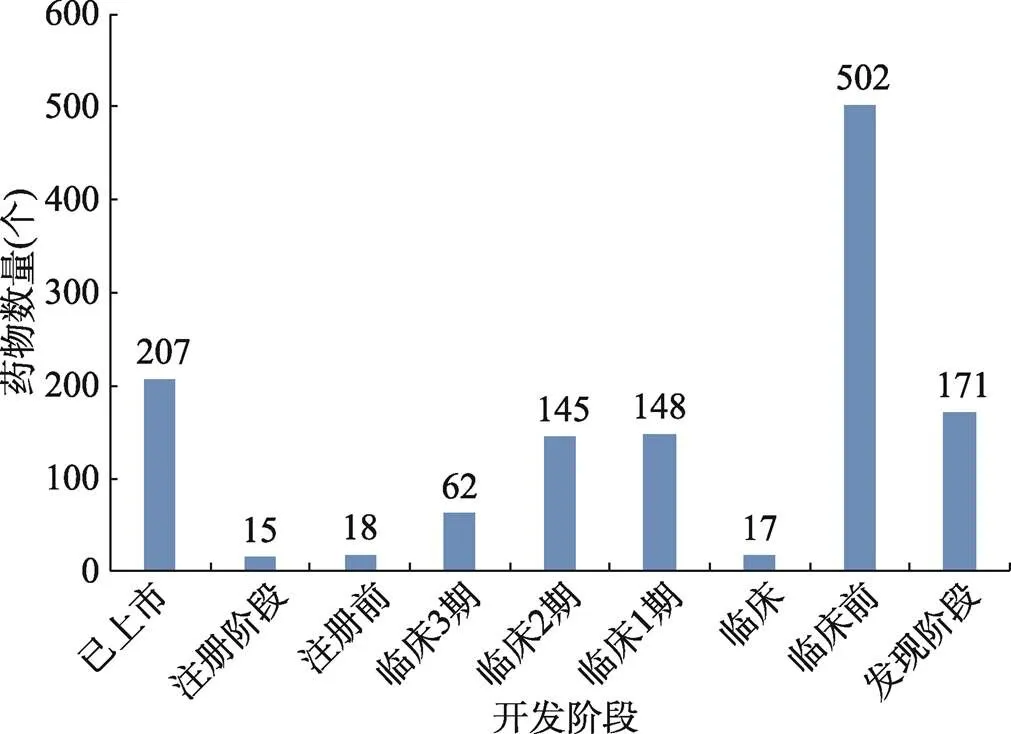
图8 糖尿病领域处于各研发阶段的药物数量
临床指报道中未指明处于临床几期、只称处于临床的药物。
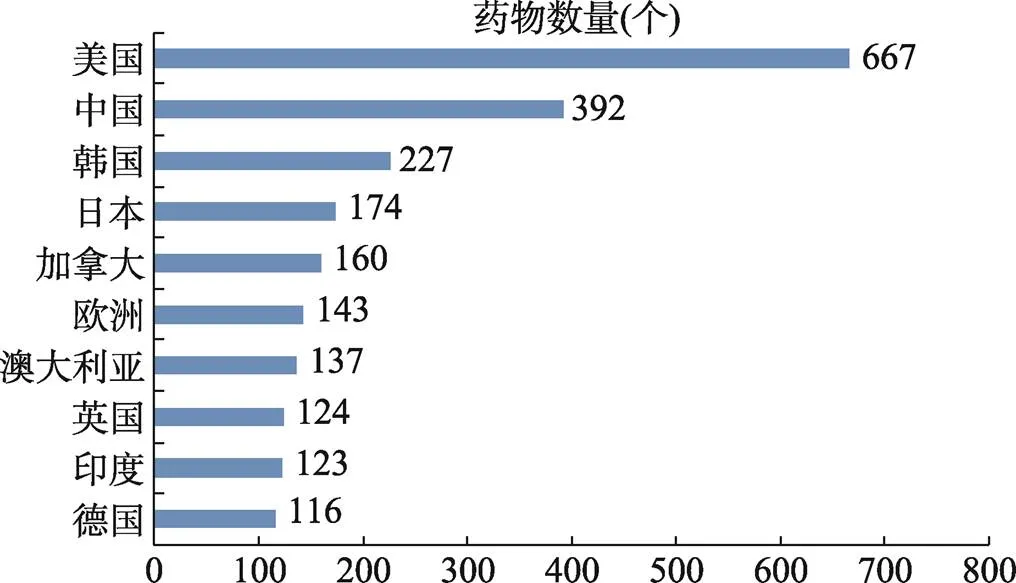
图9 糖尿病领域研发药物数量排名前10位的国家/地区
欧洲的药品管理分2层,即欧盟层面和国家层面。欧洲医药局批准的药物可以在全欧洲范围内销售,图中欧洲的143个药是指通过欧洲医药局审批、监管的药物。
4.3 大型跨国制药公司引领糖尿病药物研发
糖尿病领域,研发药物数量排名前10位的机构都是大型制药公司;而研发药物4个及以上的国内机构中,有中国科学院上海药物研究所、中国药科大学,其他都是企业,表明我国的企业在糖尿病药物研发方面也有一定的实力(表3)。
国际公司中,礼来公司拥有胰岛素、BAQSIMI等多个糖尿病药物,还与罗氏等公司联合开发了数字糖尿病护理管理系统,通过自动化的数据收集、跟踪糖尿病剂量优化糖尿病护理管理[22]。赛诺菲公司聚焦于1型糖尿病,经过近百年的努力,通过开发新疗法,包括多靶标生物制药、免疫调节剂和蛋白功能调节剂,来治疗糖尿病等代谢性疾病,并加强患者教育,提供集治疗、服务与数据分析为一一体的整合方案[23]。诺和诺德公司则是将糖尿病作为主要疾病领域的大型制药公司,该公司研发管线中,拥有4个临床1期、2个临床2期、3个临床3期以及1个处于注册阶段的糖尿病药物;既有DNA免疫疗法、胰岛素治疗1型糖尿病,也有胰淀素(amylin)类似物和GLP-1类似物semaglutide的组合产品CagriSema治疗2型糖尿病[24]。阿斯利康公司的研发管线中,拥有处于临床2期的2型糖尿病、肥胖、糖尿病肾病药物cotadutide及另外2个2型糖尿病新药[25]。2型糖尿病是辉瑞公司的重要治疗领域之一。
国内机构中,通化东宝药业股份有限公司[26]主要产品有重组人胰岛素“甘舒霖”、甘精胰岛素“平舒霖”、门冬胰岛素“锐舒霖”等系列产品,致力于糖尿病治疗领域的研发,成立了通化东宝药物研究院,并与法国阿多西亚公司合作共同推进第四代胰岛素——超速效赖脯胰岛素的研发,其全球首个SGLT1/SGLT2/DPP4三靶点抑制剂已于2021年6月获得临床批准。甘李药业股份有限公司是我国第一家掌握产业化生产重组胰岛素类似物技术的公司,在研发生产生物合成人胰岛素及其类似物方面处于中国糖尿病市场的领先地位[27]。联邦制药位于中国香港,拥有多家分公司,在珠海和中山建立了大型的人胰岛素及类似物生产基地,实现了糖尿病生物制药领域产研一体化,上市产品有人胰岛素注射液“优思灵USLIN®”系列产品(R、N、30R、50R)、甘精胰岛素注射液“联邦优乐灵®USLEN®”、联邦优倍灵®UBLIN®门冬胰岛素注射液和门冬胰岛素30注射液,是国内第一家同时拥有第二代和第三代胰岛素生产能力的企业[28]。三生制药集团与阿斯利康订立独家许可协议,获得Byetta在中国的商业化权利,用于改善2型糖尿病患者的血糖控制,适用于单用二甲双胍、磺酰脲类以及二甲双胍合用磺酰脲类、血糖仍控制不佳的患者[29]。
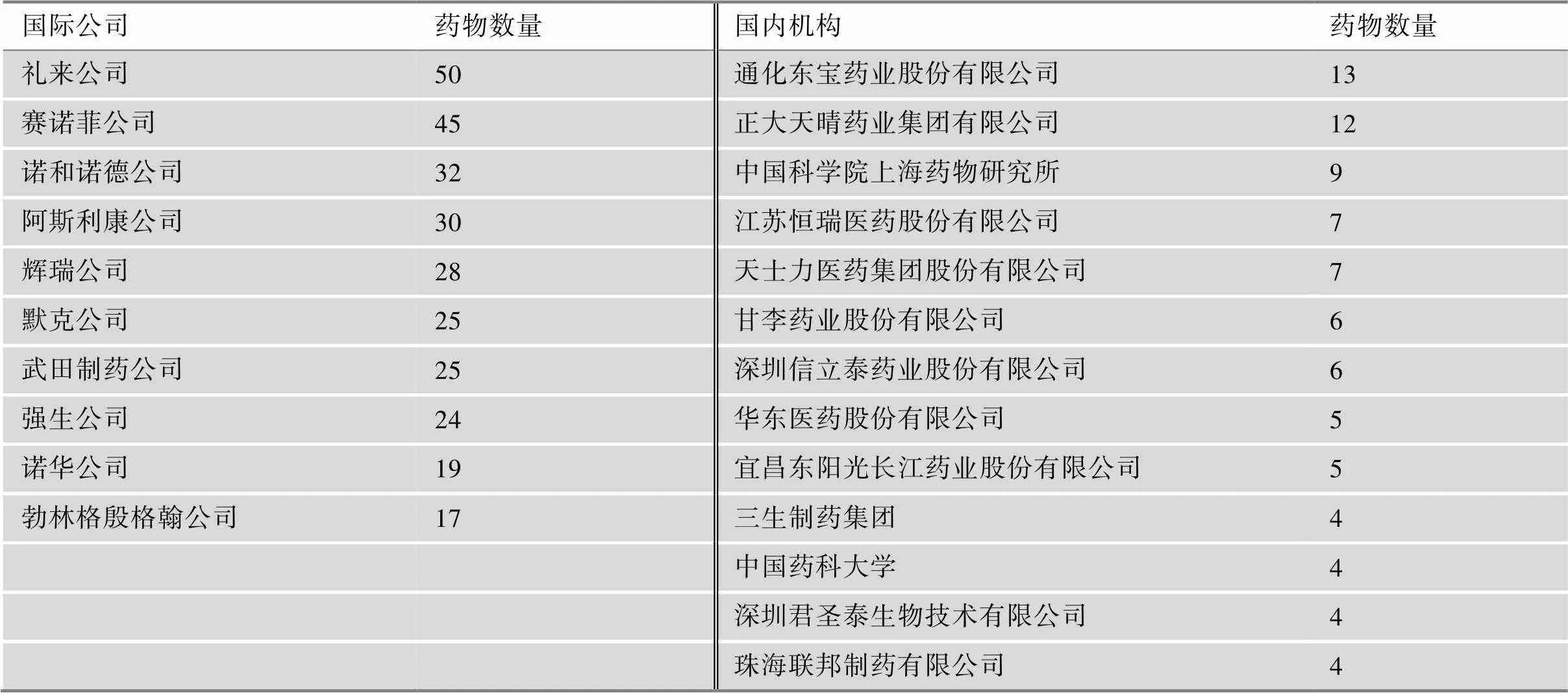
表3 糖尿病领域研发药物数量排名前10位的国际机构与中国机构
4.4 胰岛素受体及胰高血糖素样肽1受体等是糖尿病药物重要的作用靶标
从作用靶标看,最多的是胰岛素受体及胰高血糖素样肽1受体,这两种分别对应1型糖尿病和2型糖尿病。其他重要的靶标包括AMP活化蛋白激酶、钠葡萄糖转运蛋白-2等(图10)。
5 糖尿病相关产业发展
糖尿病市场主要包括智能血糖仪市场、个性化服务市场、口服降糖药市场和胰岛素药物市场。随着数字化技术在糖尿病管理方面的应用,糖尿病数字化管理可以覆盖到整个糖尿病市场,市场规模可期。
5.1 糖尿病领域国内外市场潜力巨大
全球糖尿病患者人数众多,市场规模较大。2016~2020年全球糖尿病市场规模逐年上升,2020年全球糖尿病市场规模达697亿美元,同比上升1.46%。全球糖尿病市场的快速发展,主要动力来自于降糖药物新品种的不断推出(图11)。其中部分药物具有全新的作用机制,例如胰岛素胰高糖素样肽-1受体激动剂(GLP-1RA)、钠–葡萄糖共转运蛋白-2抑制剂(SGLT-2i)。从糖尿病药物细分市场来看,2020年胰岛素及其类似物在全球糖尿病药物中的占比排名第一,达39.0%;其次是GLP-1RA,凭借其在临床上表现出的优异疗效,安全性和多重获益的特点,市场份额超过131亿美元,占比为18.8%。
我国是全球糖尿病第一大国,患者数量居全球第一,市场空间广阔。随着我国糖尿病患者的支付能力的增加、医保制度的完善和糖尿病创新药物的不断发展,我国糖尿病用药市场规模呈逐年增长态势,但2020年中国糖尿病药物市场有小幅度下降,降至632亿元,同比减少3.36% (图12)。从糖尿病药物细分市场来看,我国糖尿病药物市场以胰岛素及其类似物、双胍类和α-糖苷酶抑制剂类等已上市几十年的传统药物为主流,分别占比45.1%、13.2%、12.1%;由于新型药物GLP-1受体激动剂、DPP-4抑制剂和SGLT-2抑制剂进入中国市场的时间较晚,带来的销售收入比例远不及全球其他发达国家,但市场潜力较大。2021年10月,诺和益(德谷胰岛素利拉鲁肽注射液)在国内上市,这是全球首个基础胰岛素GLP-1RA注射液,适用于血糖控制不佳的成人T2DM患者,在饮食和运动基础上联合其他口服降糖药物,改善血糖控制,将助力我国T2DM患者实现高质量血糖达标。
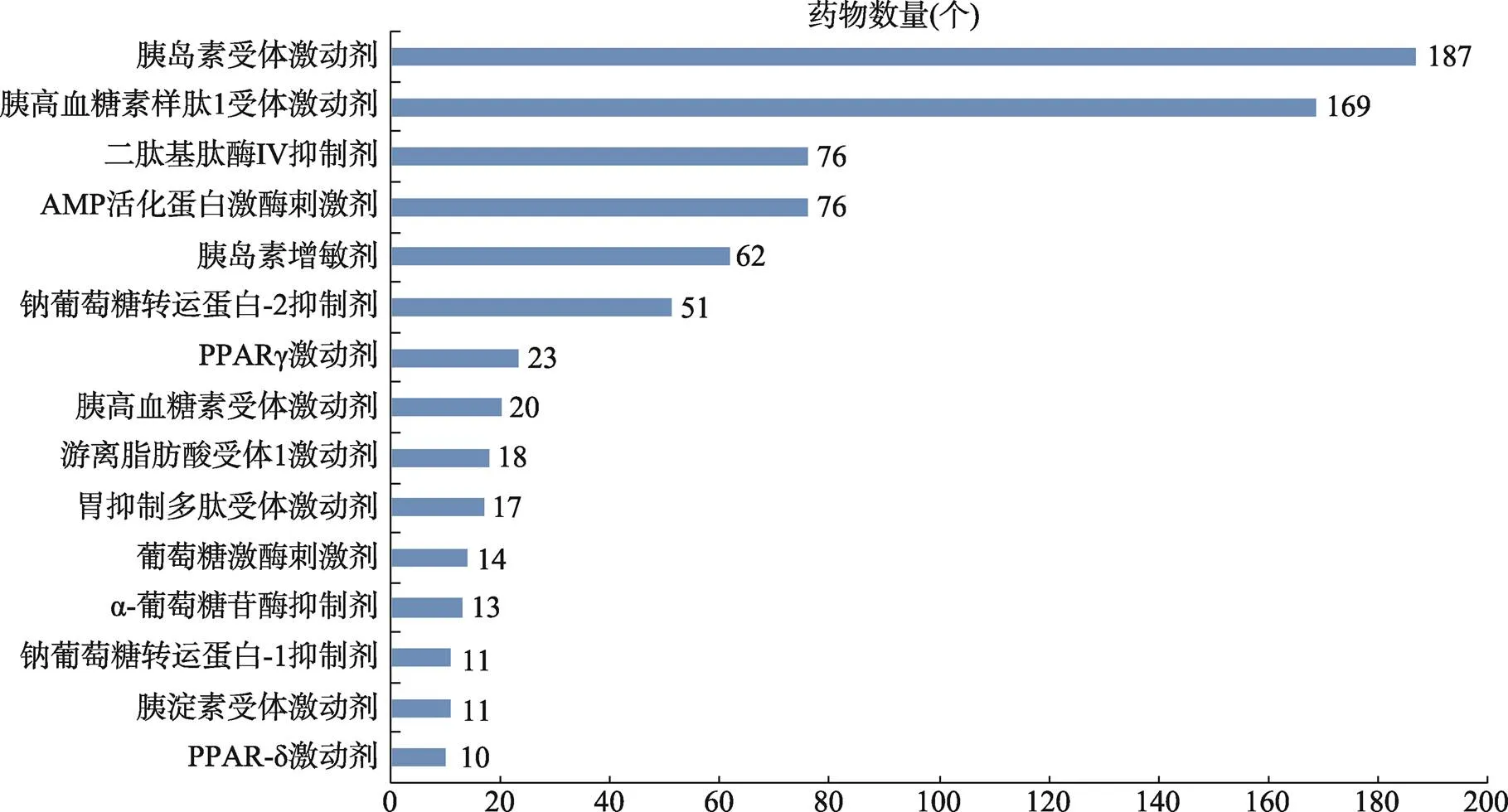
图10 糖尿病领域研发药物数量为10个及以上的靶标作用机制

图11 2016~2020年全球糖尿病市场规模[30]

图12 2016~2020年我国糖尿病市场规模
5.2 糖尿病数字化管理赛道投融资快速成长
慢病管理作为医疗健康产业的重要组成部分,数字化技术将会重塑慢病管理生态。而糖尿病是慢病管理的主要病种之一,需要契合数字化发展大势,主动求新突变,构建糖尿病数字化管理生态。随着互联网、大数据、人工智能等数字技术的发展,为糖尿病数字化管理奠定了技术基础。2013~2020年间共有12家企业完成27起融资,累计实现融资22亿元,借助糖尿病数字化管理软件和智能硬件对糖尿病人群(包括糖尿病患者和糖尿病前期人群)进行远程干预,或者糖尿病人群利用相关数字化工具进行自我管理,达到控制病情、防治恶化的医学行为过程,主要包括健康教育、在线咨询、血糖实时监测、胰岛素给药控制、用药智能管理、医生工具、患者教育、饮食管理、患者社群、运动管理等。截至2020年,糖尿病数字化管理行业的投融资事件基本信息如表4。
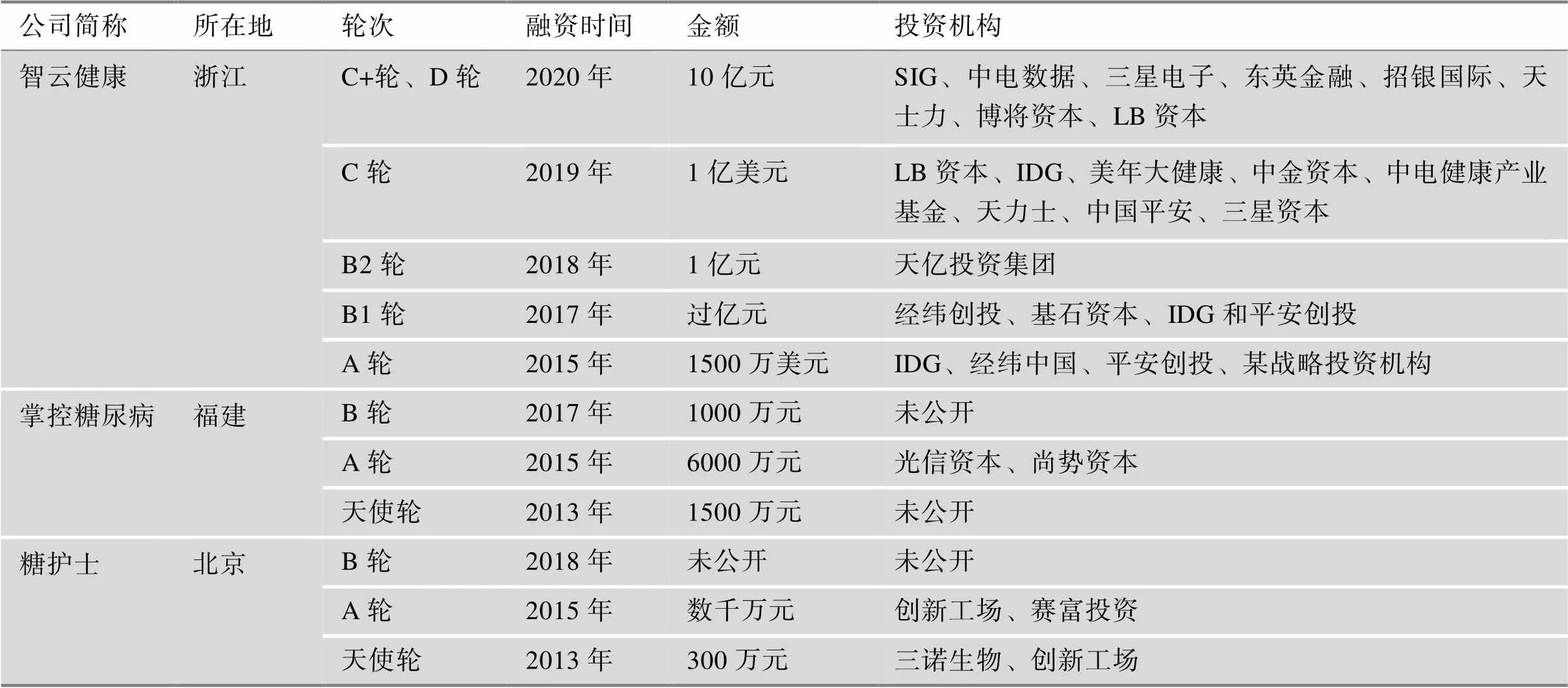
表4 糖尿病数字化管理行业投融资情况
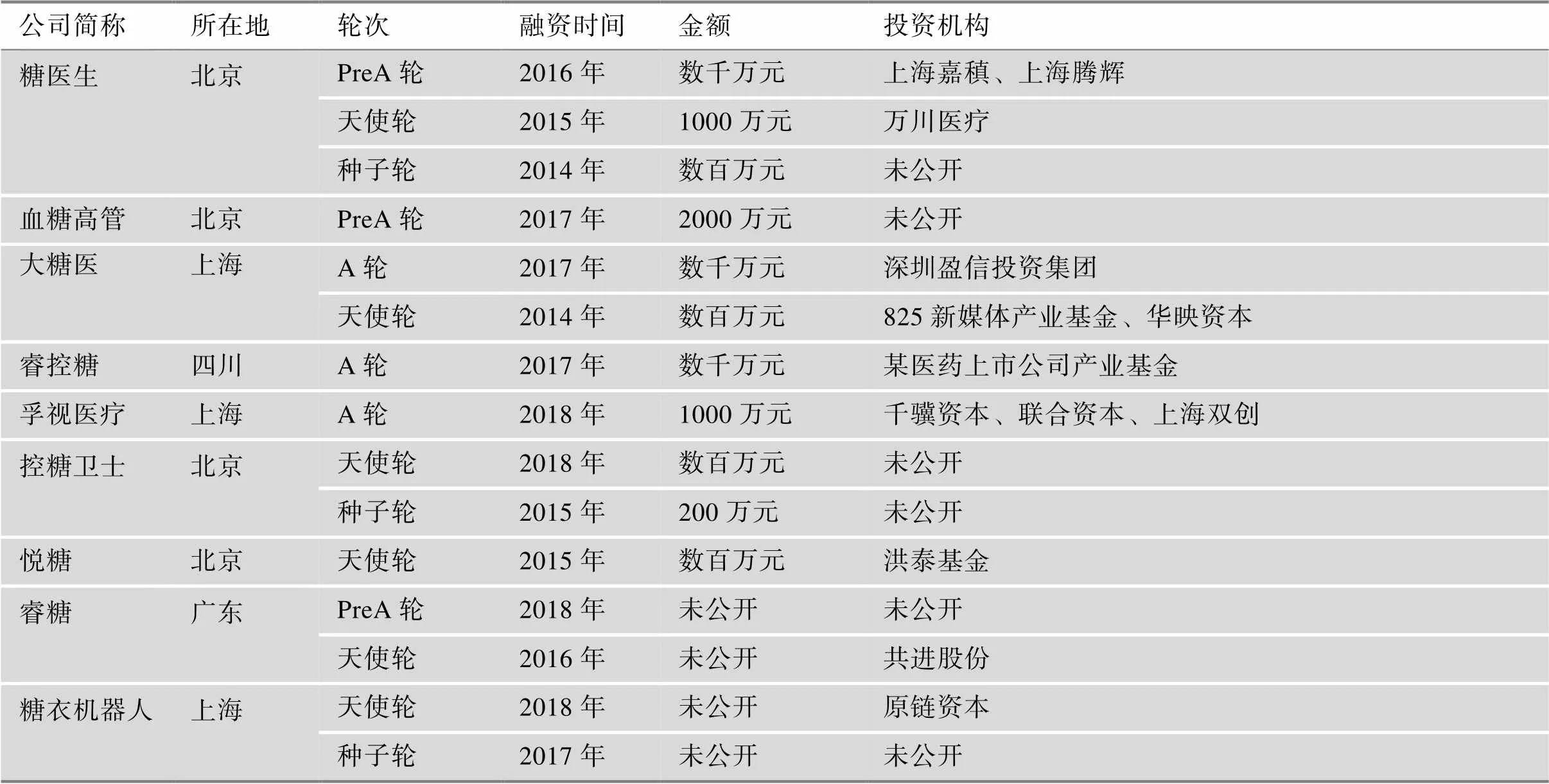
续表
6 结语与展望
总结以上分析可以看出,百年来,研究人员致力于导致糖尿病的遗传与环境因素的发病机制探索;在此基础上开发出各类疗法和干预措施,从最开始的动物提取胰岛素,重组与合成胰岛素,到后来的单克隆抗体、干细胞疗法及免疫细胞疗法。基于发病机制的糖尿病分型与诊断被进一步细化,由原先的大致分成T1DM、T2DM,到现在的4种、6种甚至更多种类型,根据分型采取不同的治疗和干预措施,例如针对单基因糖尿病的基因疗法等。尽管并不是所有类型的糖尿病都有治愈药物,但是已经实现糖尿病的长期、有效管理,尤其是近年来运用大数据与人工智能技术开发闭环双激素输送系统等,极大地提升了糖尿病管理质量和效率。
全球和我国糖尿病患者数量庞大,海量的治疗和干预需求未被满足,并带来巨大的经济社会负担。目前该领域研究论文和专利量在稳定增长;研究热点有糖尿病及并发症的机制研究及干预措施开发、相关流行病学研究等;技术重点在糖尿病的诊断、治疗、管理技术开发;已有一定数量的药物上市,但约有一半新药处于临床前及发现阶段,表明糖尿病领域新药研发管线丰富;糖尿病市场潜力巨大,糖尿病数字化管理成为近年来快速增长的投融资方向,这与该方向取得的研究与技术突破密切相关。
未来,随着基因编辑和人工智能技术等的广泛应用,将为糖尿病领域带来巨大变革,主要表现在:(1)糖尿病及其并发症的发生机制研究不断深入,如T2DM的生活方式因素[31]及与抑郁症[32]、心血管疾病[33]等的关系,将实现更精确的分型诊断。(2)疾病治疗与干预手段将更加多样化:药物研发方面,长效化糖尿病药物将持续发展,降糖药物将加快升级换代,并将更多地关注多重临床获益[34];此外,针对T2DM的减肥手术治疗[35],以及针对T1DM的恢复功能性β细胞的胰岛/干细胞移植[36]、针对T1DM和单基因糖尿病的基因治疗等正处于研发阶段的新兴疗法将取得突破,极大地丰富糖尿病治疗手段。(3)近年来人工智能技术应用于糖尿病领域,已经产生人工胰腺系统等专业型设备,以及手机血糖仪、胰岛素注射剂量计数器等可广覆盖的设备,极大地提升糖尿病患者相关指标的监测与自我管理能力[37],未来,随着可穿戴设备和人工智能技术的深入应用,糖尿病管理将实现数字化、智能化和个性化。总之,未来糖尿病领域将获得持续长足发展,从而更好地预防、诊断和管理,并最终实现治愈这一目标。
比较国际国内糖尿病领域发展现状可以看出,基础研究方面,我国的论文总量较高,但ESI高水平论文量占比较低;与国际重要机构相比,我国的重要机构论文量、ESI高水平论文量及其占比都有一定差距。技术开发方面,我国的专利申请量已达全球第一,国际专利申请机构主要是大型制药公司,而我国主要是高校及科研院所;糖尿病新药研发仍然是大型跨国制药公司引领,通化东宝药业股份有限公司、正大天晴药业集团有限公司、江苏恒瑞医药股份有限公司等企业,以及中国科学院上海药物研究所、中国药科大学等大学和研究院所有一定的开发实力。因此,我国在研究和技术开发方面有一定的实力,未来需要采取措施加强研究成果转化与产品开发,来满足我国庞大的糖尿病诊疗与管理需求。
感谢中国科学院上海营养与健康研究所的陈雁研究员在文章专业方面给予的指导和帮助。
[1] Endocrine Metabolic Branch of Chinese Medical Doctor Association, National Clinical Medical Research Center for Metabolic Diseases. Classification of diabetes mellitus in China: an expert consensus statement., 2022, 14(2): 120–139.
中国医师协会内分泌代谢科医师分会, 国家代谢性疾病临床医学研究中心. 糖尿病分型诊断中国专家共识. 中华糖尿病杂志, 2022, 14(2): 120–139.
[2] International Diabetes Federation. IDF Diabetes Atlas 10th edition. [2022-04-20]. https://diabetesatlas.org/atlas/ tenth-edition/.
[3] Nature Milestones in Diabetes. (2021-10-29)[2022-03-20]. https://www.nature.com/collections/aecjgdhadg/.
[4] Ma N, Zhu YN. Pathogenesis and recent research progress of gestational diabetes mellitus., 2019, 5(22): 62–64, 67.
马宁, 朱永宁. 妊娠期糖尿病的发病机制和最新研究进展. 智慧健康, 2019, 5(22): 62–64, 67.
[5] SongD, RanLY, Jiang RJ, Wu YJ. Animal models in diabetes mellitus research, 2016, 26(9): 83–87.
宋丹, 冉丽媛, 姜如娇, 吴英杰. 糖尿病研究中的动物模型进展. 中国比较医学杂志, 2016, 26(9): 83–87.
[6] Marek-Trzonkowska N, Myśliwiec MŁ, Dobyszuk A, Grabowska M, Techmańska I, Juścińskad J, Wujtewicz MA, Witkowski P, Młynarski W, Balcerska A, Myśliwska J, Trzonkowski P. Administration of CD4+ CD25highCD127− regulatory T cells preserves β-cell function in type 1 diabetes in children., 2012, 35(9): 1817– 1820.
[7] Marek-Trzonkowska N, Myśliwiec ML, Dobyszuk A, Grabowska M, Derkowskab I, Juścińskad J, Owczuke R, Szadkowskaf A, Witkowskig P, Młynarskif W, Jarosz- Choboth P, Bossowskii A, Sieberta J, Trzonkowskic P. Therapy of type 1 diabetes with CD4+ CD25highCD127- regulatory T cells prolongs survival of pancreatic islets— results of one year follow-up., 2014, 153(1): 23–30.
[8] Sorli C, Harashima SI, Tsoukas GM, Unger J, Karsbøl JD, Hansen T, Bain SC. Efficacy and safety of once-weekly semaglutide monotherapy versus placebo in patients with type 2 diabetes (SUSTAIN 1): a double-blind, randomised, placebo-controlled, parallel-group, multinational, multicentre phase 3a trial., 2017, 5(4): 251–260.
[9] Chinese Diabetes Society. Guideline for the prevention and treatment of type 2 diabetes mellitus in China (2020 edition)., 2021, 13(4): 315–409.
中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020年版). 中华糖尿病杂志, 2021, 13(4): 315–409.
[10] El-Khatib FH, Balliro C, Hillard MA, Magyar KL, Ekhlaspour L, Sinha M, Mondesir D, Esmaeili A, Hartigan C, Thompson MJ, Malkani S, Lock JP, Harlan DM, Clinton P, Frank E, Wilson DM, DeSalvo D, Norlander L, Ly T, Buckingham BA, Diner J, Dezube M, Young LA, Goley A, Kirkman MS, Buse JB, Zheng H, Selagamsetty RR, Damiano ER, Russell SJ. Home use of a bihormonal bionic pancreas versus insulin pump therapy in adults with type 1 diabetes: a multicentre randomised crossover trial.. 2017, 389(10067): 369–380.
[11] Cai C, Jia WP. Application and challenge of artificial intelligence in continuous Diabetes management., 2021, 35(1): 104–109.
蔡淳, 贾伟平. 人工智能在糖尿病全程健康管理的应用与挑战. 中国科学基金, 2021, 35(1): 104–109.
[12] Shen S, Liu HF, Xu XY, Yu JN. Research progress of drugs for Diabetic complication treatment.2012, 26(8): 906–910.
申升, 刘宏飞, 徐希明, 余江南. 治疗糖尿病并发症药物的研究进展. 中国药事, 2012, 26(8): 906–910.
[13] Alanazi AZ, Mohany M, Alasmari F, Mothana RAA, Alshehri AOA, Alhazzani K, Ahmed MM, Al-Rejaie SS. Amelioration of diabetes-induced nephropathy by loranthus regularis: implication of oxidative stress, inflammation and hyperlipidaemia., 2021, 11(10): 4548.
[14] Kotova JA, Zuikova AA, Pashko AN, Strahova NV, Krasnorutskaya ON, Shevzova VI, Esina EY. Markers of endothelial damage, inflammation, oxidative and cellular stress in patients with coronary artery disease and type 2 diabetes., 2020, 10(2): 104–107.
[15] Gupta A, Nayan N, Nair R, Kumar K, Joshi A, Sharma S, Singh J, Kapoor R. Diabetes mellitus and hypertension increase risk of death in novel corona virus patients irrespective of age: a prospective observational study of co-morbidities and COVID-19 from India., 2021, 3(4): 937–944.
[16] Rajpal A, Rahimi L, Ismail-Beigi F. Factors leading to high morbidity and mortality of COVID-19 in patients with type 2 diabetes., 2020, 12(12): 895–908.
[17] Van Name MA, Cheng P, Gal RL, Kollman C, Lynch J, Nelson B, Tamborlane WV, Pediatric Diabetes Consortium. Children and adolescents with type 1 and type 2 diabetes mellitus in the Pediatric Diabetes Consortium Registries: comparing clinical characteristics and glycaemic control., 2020, 37(5): 863–867.
[18] Mobley-Bukstein W, Reece SM, Hebdon K. Special considerations in the management and education of older persons with diabetes., 2021, 9(4): 30–42.
[19] Minschart C, De Weerdt K, Elegeert A, Van Crombrugge P, Moyson C, Verhaeghe J, Vandeginste S, Verlaenen H, Vercammen C, Maes T, Dufraimont E, De Block C, Jacquemyn Y, Mekahli F, De Clippel K, Van Den Bruel A, Loccufier A, Laenen A, Devlieger R, Mathieu C, Benhalima K . Antenatal depression and risk of gestational diabetes, adverse pregnancy outcomes, and postpartum quality of life., 2021, 106(8): e3110–e3124.
[20] Yamada T, Wakabayashi M, Bhalla A, Chopra N, Miyashita H, Mikami T, Ueyama H, Fujisaki T, Saigusa Y, Yamaji T, Azushima K, Urate S, Suzuki T, Abe E, Wakui H, Tamura K. Cardiovascular and renal outcomes with SGLT-2 inhibitors versus GLP-1 receptor agonists in patients with type 2 diabetes mellitus and chronic kidney disease: a systematic review and network meta-analysis., 2021, 20(1): 14.
[21] Math L, Fatima R. Adaptive machine learning classification for diabetic retinopathy.2021, 80: 5173–5186.
[22] McGrail S. Eli Lilly takes on digital diabetes care management. (2021-05-12)[2022-05-15]. https://pharmanewsintel.com/news/eli-lilly-takes-on-digital-diabetes-care- management.
[23] Sanofi. A broad range of innovative medicines. (2019- 06-14)[2022-05-13]. https://www.sanofi.com/en/about-us/ our-stories/pushing-the-science-for-better-diabetes-care-tomorrow#.
[24] Novo Nordisk. R&D pipeline. [2022-05-15]. https://www. novonordisk.com/science-and-technology/r-d-pipeline.html.
[25] AstraZeneca. Pipeline. (2022-03-22)[2022-05-15]. https:// www.astrazeneca.com/our-therapy-areas/pipeline. html#.
[26] 通化东宝药业股份有限公司. 企业简介. [2022-05-15]. http://www.thdb.com/companyprofile-list.html.
[27] 甘李药业股份有限公司. 企业介绍. [2022-05-15]. https://www.ganlee.com.cn/about_company.html.
[28] 联邦制药国际控股有限公司. 集团简介. [2022-05-15]. http://www.tul.com.cn/cn/guanyulianbang.
[29] 三生制药. [2022-05-15]. http://www.3sbio.com/field/ index.aspx?cid=72620543991349248.
[30] 华经情报网. 2021-2026年中国糖尿病药品市场供需现状及投资战略研究报告. (2021-01-12)[2022-06-15]. https://m.huaon.com/detail/679936.html.
[31] Yuan S, Gill D, Giovannucci EL, Larsson SC. Obesity, type 2 diabetes, lifestyle factors, and risk of gallstone disease: a mendelian randomization investigation., 2022, 20(3): e529–e537.
[32] Repple J, König A, de Lange SC, Opel N, Redlich R, Meinert S, Grotegerd D, Mauritz M, Hahn T, Borgers T, Leehr EJ, Winter N, Goltermann J, Enneking V, Fingas SM, Lemke H, Waltemate L, Dohm K, Richter M, Mehler DMA, Holstein V, Gruber M, Nenadic I, Krug A, Brosch K, Schmitt S, Stein F, Meller T, Jansen A, Steinsträter O, Amare AT, Kircher T, Baune BT, van den Heuvel MP, Dannlowski U. Association between genetic risk for type 2 diabetes and structural brain connectivity in major depressive disorder., 2022, 7(3): 333–340.
[33] Cinkajzlová A, Mráz M, Haluzík M. Adipose tissue immune cells in obesity, type 2 diabetes mellitus and cardiovascular diseases., 2021, 252(1): R1–R22.
[34] 华经情报网. 2020年糖尿病药物行业现状及趋势分析, 降糖药物将加快升级换代. (2021-09-09)[2022-03-24]. https://www.huaon.com/channel/trend/746990.html.
[35] Lingvay I, Sumithran P, Cohen RV, le Roux CW. Obesity management as a primary treatment goal for type 2 diabetes: time to reframe the conversation., 2022, 399(10322): 394-405.
[36] Guo LX. 2021 annual review of major progress in diabetes., 2022, 14(1): 1–8.
郭立新. 2021年糖尿病领域年度重大进展回顾. 中华糖尿病杂志, 2022, 14(1): 1–8.
[37] 动脉网. 智能设备成为糖尿病数字化管理基本前提, 关键创新点有哪些?(2021-01-06)[2022-03-24]. https:// www.cn-healthcare.com/articlewm/20210106/content-1178242.html.
Progress on research and development in diabetes mellitus
Liwen Zhang1, Meihua Ruan1, Jialan Liu2, Caihong He1,3, Jianrong Yu1,3
Diabetes mellitus is a kind of metabolic disease characterized by hyperglycemia resulting from insulin insufficiency and insulin resistance. It has become one of the major diseases threatening human health. In this paper, we analyze the current R&D status of diabetes from the aspects of papers, patents, drugs and industrial development. The results show that scientific outcomes are increasing steadily and the hot topics are diabetic complications and epidemiological research. In terms of technology development, large pharmaceutical companies, such as Janssen Pharmaceutical, Lilly pharmaceutical, Boehringer Ingelheim, are actively engaged in diagnosis, treatment and management of diabetes. By March 23 2022, 207 drugs have been launched and a large number of candidate drugs are in the pre-clinical and clinical stage. In terms of industrial development, the potential diabetes market is huge and the digital management of diabetes is developing rapidly.China has certain strength in diabetes research and development. In the future, measures should be taken to strengthen the transformation of research outcomes, and promote product development to meet China’s huge needs of diabetes cares.
diabetes mellitus; research status; drug development; industrial development
2022-08-15;
2022-09-30;
2022-10-12
国家自然科学基金专项项目(编号:L1924031)资助[Supported by the National Natural Science Foundation of China (No. L1924031)]
张丽雯,硕士,馆员,研究方向:生物情报。E-mail: zhangliwen@sinh.ac.cn
阮梅花,硕士,研究馆员,研究方向:慢病防控、脑科学等领域的战略情报研究。E-mail: mhruan@sinh.ac.cn
张丽雯和阮梅花并列第一作者。
于建荣,硕士,研究馆员,研究方向:科技情报。E-mail: jryu@sinh.ac.cn
10.16288/j.yczz.22-272
(责任编委: 孟卓贤)

