基于真实情境下的创新试题命制
——第二届命题征集活动优质创新试题选登
山东 刘 刚 黑龙江 孙秀民 河北 王晓宁 陕西 鱼春萌


图1
( )
A.正反应为吸热反应
B.a、b、c三点,b点v(逆)最大

D.b点时向密闭容器内再充入0.5 mol H2,反应速率增大,达到平衡时Kp增大
【参考答案】B
【命题意图】本题以化学平衡图像为试题情境,对化学平衡的移动的判断、图像的分析、平衡常数的计算与应用等知识进行考查,培养学生平衡思想和科学探究意识。
【解题思路】从图像看,转化率80%的曲线先达到平衡,反应速率较快,所以温度较高,为520 K,即升高温度,转化率降低,所以正反应为放热反应,A项错误;a、b、c三点,b点转化率最大,产物浓度最大,且温度为520 K,所以b点v(逆)最大,B项正确;520 K时,若容器内起始压强为p0,根据转化率为80%可得:

起始量 1 2
转化量 0.8 1.6 0.8
平衡量 0.2 0.4 0.8

【创新点分析】1.题干材料设置和题型选择,以水煤气合成甲醇的反应为试题情境,选材符合“碳中和”绿色化学思想,以传统的化学平衡知识为考查载体,借用图像对平衡移动的判断、分压平衡常数的判断进行考查。
2.创新/设问考查角度,创新设问体现在选项B、C上,选项B是问v(逆)的大小判断,需要综合考虑温度、浓度等条件影响。选项C看似需要复杂的计算,实际考生通过观察可快速进行判断,考查学生审题、提取信息、分析信息、快速判断的能力,增强答题的技术性,这也是新高考所要求考生具备的综合素养之一。
3.考查维度,从近几年高考试题来看,利用图像为载体对化学反应速率和化学平衡相关知识进行考查的题目属于必考题型,并且处于几个选择题中的压轴题之一,该题型主要培养学生变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识等化学学科素养,所以命题者在设计设问角度时需兼顾传统知识考点并创新思维考点。
【点评】试题的图像分析思路好,考查知识点多样,信息给予全面。
2.R、Y、G、X为原子半径依次增大的四种短周期元素,Y与G同周期,X与Y同主族。甲、乙、丙、丁、戊为由这四种元素构成的化合物,其转化关系如图2所示。下列说法中正确的是

图2
( )
A.Y与其他三种元素均能形成至少两种二元化合物
B.G的最高价氧化物的水化物的酸性比X强
C.将丁滴入乙中会发生放热反应
D.①与②、③与④的反应类型相同
【参考答案】A
【命题意图】本题是元素及物质结构推断题,主要考查学生的读图、识图、辨图和析图能力,考查学生理解与辨析能力、分析与推测能力。考查学生的宏观辨识与微观探析、证据推理和模型认知、变化观念与平衡思想的化学学科核心素养。
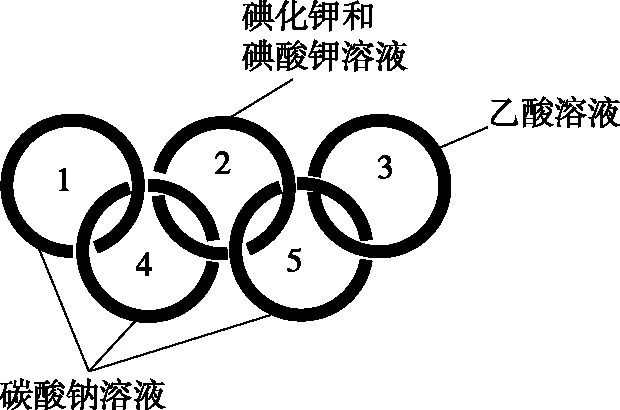
【解题思路】根据题意可推出R为H元素,Y为O元素,G为C元素,X为S元素。氧原子与氢原子可形成H2O和H2O2、氧原子与碳原子可形成CO和CO2、氧原子与硫原子可形成SO2和SO3,选项A正确;根据非金属性C 【创新点分析】本题以元素推断和物质转化关系为情境素材设计成反应机理图,题目呈现方式新颖。在设问上,既有元素化合物的组成、物质的结构和性质的考查,又有反应的热效应及根据反应机理推测化学反应类型的考查,知识点覆盖面较广、信息量大,符合新高考的命题趋势。 【点评】本题以反应机理图为试题情境呈现形式,考查元素推断和物质性质等知识,将元素周期表和元素周期律及有机结构式联合起来,素材呈现较新,情境新颖,选项创新性较高。 3.航天员通过化学反应让奥运五环在中国空间站上飘浮。如图3所示,1号环中加入溴百里酚蓝(一种酸碱指示剂,遇碱性物质变蓝)呈现出鲜亮的蓝色;2号环中加入淀粉和乙酸溶液后生成了碘单质,变成了深如黑色的深蓝色。3号环中加入甲基橙呈现出橙色,4号环中加入甲基橙后呈现鲜亮的黄色,5号环中加入甲基橙和溴百里酚后呈现绿色。 图3 下列叙述错误的是 ( ) C.用标准氢氧化钠溶液滴定3号环中乙酸溶液,选择甲基橙作指示剂,测得的乙酸浓度会偏低 D.若3号环与5号环中的溶液以溶质物质的量之比2∶1 混合反应,反应后溶液中离子浓度大小排序:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)(不考虑生成气体的溶解) 【参考答案】B 【命题意图】本题选择天宫课堂太空奥运五环中的化学反应为试题背景,进行了试题情境素材上的创新;从水溶液中离子之间的相互作用定性考查水解平衡和离子方程式的书写,定量考查酸碱滴定反应指示剂选择和离子浓度大小的比较,体现对宏观辨识与微观探析、变化观念与平衡思想的学科核心素养的考查。 【创新点分析】题干材料设置为中国空间站奥运五环中的化学反应,创新命题素材,考查学生在新情境中解决问题的能力。设问考查角度集合水解平衡、氧化还原反应、酸碱中和滴定和离子浓度大小排序等,实现基本理论在水溶液中离子平衡的综合应用以及定性和定量相结合的考查。 【点评】试题素材新颖,设问综合性强,同时对激发学生家国情怀、增强民族自豪感有重要意义。 4.电化学合成是合成领域的有效手段之一。制备碘仿(CHI3)的一种方式就是通过电化学方法合成,实验步骤如下: Ⅰ.将一个150 mL烧杯作为电解槽,用2个石墨棒分别作为阴阳电极,并接到直流电源(如图4)。在烧杯中加入100 mL蒸馏水和6 g碘化钾,固体溶解后加入1 mL丙酮(CH3COCH3)。将烧杯放在电磁搅拌器上慢慢搅拌,接通电源,烧杯中立即有棕黄色物质析出,电解一段时间,切断电源,停止反应。 图4 Ⅱ.将电解液过滤,用水将电极和烧杯壁上黏附的碘仿冲洗到漏斗中,过滤,水洗,干燥。 Ⅲ.将Ⅱ中获得的固体用适量的乙醇在加热搅拌回流的条件下溶解,趁热过滤,冷却结晶,过滤,干燥并称量,固体质量为1.2 g。 已知:a.电解槽中发生的反应: b.纯碘仿为黄色晶体,几乎不溶于水,能溶于醇、三氯甲烷等有机溶剂。 回答下列问题: (1)步骤Ⅰ中使用电磁搅拌器对溶液搅拌(图4),也可用图5的仪器替代,其名称为________。 图5 (2)电解实验中,制备1 mol碘仿实际消耗的电量________理论消耗的电量(填“>”“<”或“=”),主要原因是____________________________________________。 (3)请补充完整下列离子反应: (4)步骤Ⅲ的分离提纯方法为________。该步骤中乙醇的用量是使碘仿恰好溶解,待固体完全溶解后,再加入1 mL 乙醇,则加入1 mL乙醇的作用是____________________________________________。 (5)请设计实验方案证明碘仿中含有碘元素:____________________________________________。 (6)本实验的电源为电流为2 A的直流稳压电源,电解时长为30 min,求反应结束后碘仿的产率________%。(保留一位有效数字)(1 mol电子的电量为9.6×104库仑,CHI3的摩尔质量为394 g/mol) 【参考答案】 (1)环形玻璃搅拌棒或玻璃搅拌器 (2)>;电解反应中存在副反应,会消耗部分IO-,所以实际消耗的电量多。 (4)重结晶;防止趁热过滤过程中,碘仿析出,使产率降低。 (5)取少量碘仿固体,加入氢氧化钠溶液并加热,充分反应后加入过量的硝酸,再加入硝酸银溶液,若产生黄色沉淀,说明含有碘元素。 (6)48.7 【命题意图】本试题为有机合成实验,但是方法为高中罕见的电化学合成方法。在合成碘仿的过程中,即涉及了电极反应又包含溶液中的反应,合成方法和反应过程易懂,并且实验步骤、操作过程和结果分析适合对高中生学科素养和关键能力的考查。 【解题思路】 (1)考查学生对常规仪器的认识和了解。环形玻璃搅拌棒常见于中和热测定实验。 (2)理论电路上的电子与碘仿的关系:2I2~6e-~3IO-~CHI3,但是溶液中存在副反应,会使部分IO-没有生成CHI3,即电路中电子转化为碘仿的转化率小于100%,因此实际消耗的电量多。 (3)根据元素守恒,在IO-前配3,再根据电荷守恒可写出2OH-。 (4)考查重结晶的定义。提纯碘仿实际过程就是得到热的饱和溶液,再趁热过滤除去不溶性杂质,最后冷却结晶,本设问考查得到热的饱和溶液额外多加少量乙醇的作用。其作用是因为在趁热过滤时,温度会略降低,若是饱和溶液温度降低会有碘仿析出,额外加入少量乙醇可以使溶液接近饱和,从而防止趁热过滤时温度降低产物析出。 (5)考查卤代烃中卤素原子的检验方法。利用卤代烃的取代反应,再结合卤化银的颜色即可检验。 【创新点分析】题干材料的创新点是高中少见的电化学合成有机物为背景材料。设问考查角度的创新点是将电路中的电量与产物的产率相关联。考查维度的创新点是自主设计方案检验物质中的元素。 【点评】本题以电化学合成有机物为试题情境素材,考查实验装置推断、物质性质和检验等知识,情境新颖,选项创新性较高。