核心素养视域下“正负电荷相互吸引”的有机化学教学应用
北京 徐晓斌
基于化学键视角预测和解释有机化合物的性质,对于学生建立“组成、结构决定性质”的核心观念、发展高级思维具有重要意义。无论是在《普通高中化学课程标准(2017年版2020年修订)》(以下简称《课程标准》),还是在人教版新教材《有机化学基础》(以下简称新教材)中都对化学键视角进行了强化。但是,仅仅基于这些认识角度,学生虽然能准确预测或解释断键部位,但是分析新化学键形成时仍然会面临困惑。例如,新教材83页“资料卡片”介绍了羟醛缩合反应。
学生基于化学键视角,能够预测可能的断键位置分别为图1中①处的碳氧双键、图1中②处的醛基邻位碳原子(α-C)上的氢原子(α-H)之间的化学键。紧接着,在分析产物时,学生可能得到如图2a和b所示的两种不同的结果。

图1 羟醛缩合反应中反应物可能的断键

图2 羟醛缩合反应中可能的成键方式
其实,这一问题本质是在追问有机物在成键时应遵循什么样的原则,这是基于化学键视角认识有机物不可缺少的环节,然而,这一问题却没有引起教师的关注,很多教师在教学中没有介绍,致使学生认知造成障碍。
1.引入成键规律,建构认知模型
1.1 明晰有机物成键规律
有机物在成键时要遵循“正亲负、负亲正”的基本规律。以卤代烃(RCH2Br)的取代反应为例,由于溴原子和碳原子的电负性差异,形成一个极性较强的共价键:Cδ+—Brδ-,碳原子(Cδ+)与带负电荷的—OH结合形成醇。类似地,分析如图3所示的乙醇的取代反应,可以发现,总是δ+和δ-的原子连接形成新的化学键,这就是有机化学中的“正负电荷相互吸引”。
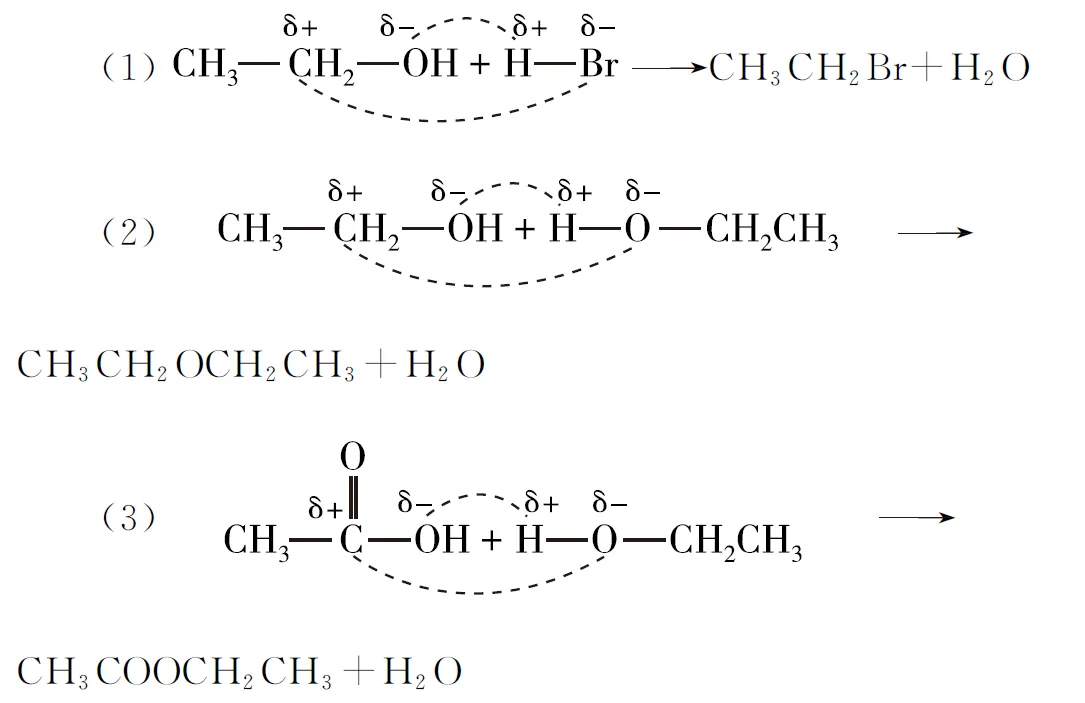
图3 乙醇的取代反应中的“正负电荷相互吸引”
1.2 有机物成键规律是有机化学反应本质的外显
有机化学中的“正负电荷相互吸引”不是巧合,而是由反应机理决定的。按照反应时化学键断裂和生成的方式,有机反应分为以下3大类。
(1)离子型反应。仍以卤代烃(RCH2Br)的取代反应为例,如图4所示,OH-对原子核有显著亲和力,与卤代烃中带部分正电的原子(Cδ+)相互吸引、接近,经历过渡态然后再成键,同时生成Br-。像OH-这种供给电子的试剂(δ-)进攻有机物中的正碳中心(Cδ+)而发生的反应称为亲核反应。相反地,由缺少电子的试剂(δ+)进攻有机物中的负碳中心(Cδ-)而发生的反应称为亲电反应。亲电反应和亲核反应在反应过程中伴随着化学键的异裂,统称为离子型反应。

图4 卤代烃的取代反应机理
(2)自由基反应。常常对应着化学键的均裂,成键的一对电子平均分给两个原子或原子团,生成自由基。典型的反应如甲烷和氯气的取代反应,是由Cl·进攻CH4实现链增长。
(3)协同反应。
因为高中所学的绝大多数反应属于离子型反应,如碳碳双键、碳碳三键的加成,苯环的取代,卤代烃的水解和消去,醇的取代和消去,酯化和酯的水解等,所以“正负电荷相互吸引”这一规律具有极强的普适性。
1.3 建构有机化合物的认知模型
基于有机反应的成键规律,通过文献梳理、结合教学实践,构建了如图5所示的基于化学键视角认识有机化合物的认知模型。在分析结构时,首先关注有机物的不饱和度和化学键的极性(需要考虑成键原子的电负性差值、邻近基团对化学键的影响),从而分析断键部位,根据“正负电荷相互吸引”的原则,推测或解释新键形成的原理。

图5 有机化合物的认知模型
1.4 应用有机化合物的认知模型解释问题


图6 羟醛缩合反应的断成键分析
2.应用模型,突破有机合成难点
有机化合物的认知模型不仅能用于解释教材中出现的反应,更有价值的是,可以应用于分析难度较大的陌生反应。对学生而言,学业水平考试的难点之一是分析碳链的增长。造成这一困难的原因在于课内较少介绍碳链增长的反应,学生只是通过试题提供的新信息才对其有所了解。这种碎片化的学习方式容易使知识体系缺乏系统性。《课程标准》要求“认识有机合成的关键是碳骨架的构建和官能团的转化”,凸显了有机合成在有机化学学习中的关键地位。因此,利用有机化合物的认知模型,理解概括出有机合成、尤其是碳链增长反应的规律和本质,有助于学生突破认知障碍。
2.1 应用模型探寻碳链增长的规律和实质


(R1、R2代表烃基,下同)
2.2 应用碳链增长的规律突破难点
基于碳链增长反应规律和有机化合物的认知模型,可以解决陌生复杂的问题。
2017年北京卷的25题部分合成路线如图8,本题已知E为乙酸乙酯,需推断F的结构。由于这个反应新颖,给考生造成困扰,甚至出现部分考生已经推导出F的结构但是不敢确信这种成键方式是否合理的情况。

图8
应用有机物的认知模型进行分析。如图9所示,因为产物中有乙醇,所以确定A中的断键位置,分子A中羰基碳为正碳中心;而B分子中有3种氢,考生困惑的是哪个碳氢键断裂。考虑邻近基团对化学键极性的影响,可以发现,因为酯基的存在,α-C和α-H之间的共价键极性较强,易于断裂,断裂后形成负碳中心;正碳中心可以和负碳中心连接成键,实现碳链的增长。

图9 乙酸乙酯的缩合反应
事实上,可以将该反应推广到一般,两分子酯可以发生缩合反应。


图10

图11 E→F的成键分析
推广至一般,如下图所示,A分子中的α-C分别与羰基和酯基相连,α-C两侧均为吸电子基团,使得α-C和α-H 原子之间的共价键极性较强,更容易发生断裂,α-C成为负碳中心。在卤代烃B中,α-C是正碳中心,和A的负碳中心连接成键,同时生成HBr。



除了碳链增长反应,有机化合物的认知模型还可以用于设计有机合成路线、预测未知反应等。
总而言之,构建认识有机物的认知模型,有助于学生深刻地体会“结构决定性质”这一有机化学学科核心思想、发展证据推理与模型认知的化学学科核心素养。第一,基于学习进阶理论,学生认识有机反应的思维层级应该从单点结构水平的物质视角,发展至多元和关联结构水平的官能团视角,最终发展至抽象结构水平的化学键视角。从化学键视角去分析有机物结构,既要通过分析化学键的极性和饱和程度确定断键部位,还要根据“正负电荷相互吸引”分析新化学物质的形成。依据这一认知模型,学生能在化学键的认识层级分析有机化合物的结构以预测和解释有机化合物的性质,通过分析有机化合物性质有效推理和论证有机化合物的结构,发展宏观辨识、微观探析的化学学科核心素养。第二,构建模型、应用模型的过程是思维发展的过程。通过分析、推理、抽象、概括,逐步深化认知,自我构建有机化合物认知范式,并进一步运用模型预测和解释有机化合物的化学性质,能在陌生情境的解决问题过程中检验学习成果,将认识方法内化为学生的元认知,不断加深对有机反应的本质特征认识,促进证据推理与模型认知化学学科核心素养的发展。

