QuEChERS结合超高效液相色谱-四极杆/静电场轨道阱高分辨质谱法同时测定全血中10种新型合成大麻素
张志远,宋 辉*,李 想,许英健,朱 昱*,王 磊
(1.中国刑事警察学院 刑事科学技术学院,辽宁 沈阳 110854;2.新疆喀什市公安局,新疆 喀什 844000)
合成大麻素(Synthetic cannabinoids,SCs)是一类能够与人体内源性大麻素受体CB1或CB2结合产生生理活性的人工合成化合物,其作用与天然大麻中的四氢大麻酚相似甚至更强,是目前品种最多、数量最大的新精神活性物质(New psychoactive substance,NPS)[1-2]。合成大麻素在世界各地快速蔓延态势日趋严重,且新品种和新物质层出不穷、种类繁多。资料显示[3],截至2020年底,全世界范围内已鉴定和报告给联合国毒品和犯罪问题办公室(UNODC)的新精神活性物质数量达1 047种,而合成大麻素类化合物数量已达794种,远超芬太尼类(398种)[4]。吸食合成大麻素易产生心跳过速、血压升高、胸痛、口齿不清、幻觉亢奋等副作用,出现自伤自残等暴力行为[5-7],甚至会导致心肌梗塞或器官衰竭造成死亡[8]。为坚决遏制和严厉打击新型合成大麻素违法犯罪,我国自2021年7月1日起对合成大麻素类新精神活性物质实行整类列管[9]。
血液样本是滥用药物检测最常用的生物检材之一,色谱-质谱联用技术是目前体内药物毒物分析最重要的检测手段。Ong等[10]建立了液相色谱-串联质谱同时分析全血中29种合成大麻素的方法,目标物主要包括吲哚、吲唑酰胺和萘酰吲哚类合成大麻素,方法检出限为0.1~6.0 ng/mL;王冠翔等[11]建立了超高效液相色谱-串联质谱分析血液中吲唑酰胺类合成大麻素的方法,其中6种合成大麻素的检出限为0.01~0.05 ng/mL;Krotulski等[12]采用液相色谱-质谱分析了血清中84种合成大麻素的冻融稳定性和长期稳定性,发现大多数合成大麻素的血清样本在-20℃下可至少稳定1个月;徐恩宇等[13]分别建立了气相色谱-质谱和液相色谱-串联质谱快速鉴别血液中4种新型合成大麻素的方法,其中ABCHMINACA等4种新型合成大麻素采用液相色谱-串联质谱法的检出限为0.1~0.5 ng/mL,气相色谱-质谱法需用时21 min,而液相色谱-串联质谱法仅需5 min,表明液相色谱-质谱联用技术更适合血液中合成大麻素的定性及定量检测。
QuEChERS是一种针对复杂基质快速、简单、廉价、有效、可靠和安全的前处理方法,比单一的乙腈沉淀蛋白、固相萃取等方法具有更好的提取与净化效果[14-15]。基于四极杆/静电场轨道阱高分辨质谱的平行反应监测(PRM)模式能够以高精度和高分辨率监测目标物前体离子的所有碎片离子,同时具有可靠的定性分析和准确的定量分析功能,且具有较强的去除背景干扰能力,能够显著提高复杂背景下目标物的灵敏度[16]。本文建立了QuEChERS法结合超高效液相色谱-四极杆/静电场轨道阱高分辨质谱(UPLC-QE-Orbitrap MS)同时测定全血中10种新型合成大麻素的分析方法,其中ADB-BINACA(N-(1-氨基-3,3-二甲基-1-氧代丁-2-基)-1-苄基-1H-吲唑-3-甲酰胺)、ADB-BICA(N-(1-氨基-3,3-二甲基-1-氧代丁-2-基)-1-苄基-1H-吲哚-3-甲酰胺)、AB-FUBICA(N-(1-氨基-3-甲基-1-氧代丁-2-基)-1-(4-氟苄基)-1H-吲哚-3-甲酰胺)等物质尚未见相关报道。
1 实验部分
1.1 仪器与设备
UltiMate 3000高效液相色谱仪、Thermo Scientific Q Exactive四极杆/轨道阱高分辨质谱仪、Xcalibur质谱 工作站、Hypersil GOLDTMVanquish色 谱 柱(100 mm×2.1 mm,1.9 μm)均购 于 美国Thermo Scientific公司;梅特勒电子天平(精确值:十万分之一,瑞士Mettler公司);HC-3018高速离心机(安徽中科中佳公司);XW-80A涡旋振荡器(海门市麒麟医用仪器厂)。
1.2 材料与试剂
AB-FUBICA、5F-ADBICA(N-(1-氨甲酰基-2,2-二甲基丙基)-1-(5-氟戊基)吲哚-3-甲酰胺)、ADB-BICA、ADB-FUBICA(N-(1-氨基-3,3-二甲基-1-氧代丁-2-基)-1-(4-氟苄基)-1H-吲哚-3-甲酰胺)、ADB-BINACA、ADB-BUTINACA(N-(1-氨基-3,3-二甲基-1-氧代丁-2-基)-1-丁基-1H-吲唑-3-甲酰胺)、4F-MDMB-BUTINACA(2-[1-(4-氟丁基)-1H-吲唑-3-甲酰氨基]-3,3-二甲基丁酸甲酯)、AMB-FUBINACA(3-甲基-2-[1-(4-氟苄基)吲唑-3-甲酰氨基]丁酸甲酯)、5F-ADB(3,3-二甲基-2-[1-(5-氟戊基)吲唑-3-甲酰氨基]丁酸甲酯)、MDMB-4en-PINACA(3,3-二甲基-2-[1-(4-戊烯-1-基)-1H-吲唑-3-甲酰氨基]丁酸甲酯)共10种合成大麻素对照品固体粉末(纯度>98%,美国GlpBio公司)。甲酸、甲醇、乙腈(色谱纯,美国Fisher Scientific公司),无水MgSO4、无水Na2SO4(分析纯,沈阳国药集团)。空白血(沈阳第四人民医院提供);雄性SD大鼠(中国医科大学动物实验中心提供);案例血液样本来自公安机关在涉毒案件中取样。
1.3 混合标准溶液的配制
精确称量各对照品固体粉末5 mg,置于10 mL容量瓶中,以甲醇溶解并定容,涡旋混匀10 s,配制成0.5 mg/mL的混合标准储备溶液。准确量取混合标准储备溶液适量,以甲醇逐级稀释,涡旋混匀,制备质量浓度分别为500.0、100.0、50.0、20.0、10.0、5.0、2.0、1.0、0.5、0.2、0.1 ng/mL的系列混合标准溶液备用,-20℃冷冻保存,临用时放至常温。
1.4 样本QuEChERS法处理
准确量取全血样本0.5 mL置于15 mL离心试管中,加入1.5 mL乙腈和350 mg无水MgSO4,涡旋振荡5 min,以10 000 r/min离心3 min,取上清液过0.22 μm有机微孔滤膜,装瓶后供分析。
1.5 动物实验
取雄性SD大鼠2只,单只重约230 g,采用腹腔注射5F-ADBICA与MDMB-4en-PINACA混合药物方式,给药剂量均为5 μg/kg,给药1 h后分别内眦取血各0.5 mL,按照“1.4”方法处理,待检测。
1.6 色谱-质谱条件
1.6.1 色谱条件Hypersil GOLDTMVanquish色谱柱(100 mm×2.1 mm,1.9 μm);流动相:0.1%甲酸水(A)和0.1%甲酸乙腈(B),流速为0.30 mL/min,柱温为40℃,进样量为10 μL。梯度洗脱程序:0~9 min,5%B;9~11 min,5%~100%B。
1.6.2 质谱条件离子源:采用加热电喷雾离子源正离子模式(HESI+),离子源温度:400℃;离子传输管温度:350℃;喷雾电压:3 500 V;辅助气:3 000 mL/min,鞘气:12 000 mL/min;扫描模式:采用全扫描(Full MS)/平行反应监测(PRM)模式,Full MS分辨率(R):70 000,质量扫描范围:m/z150~600;PRM分辨率:17 500,Orbitrap最大容量:2×105,最大注入时间:100 ms;阶梯碰撞能量:20、40、60 eV。
2 结果与讨论
2.1 实验条件的优化
2.1.1 色谱条件的选择采用10.0 ng/mL混合标准溶液进样,比较了甲醇-水、0.1%甲酸水-乙腈、0.1%甲酸水-0.1%甲酸乙腈3种不同流动相对各组分分离效果及色谱峰形的影响。实验表明,0.1%甲酸水-0.1%甲酸乙腈比其他两种流动相的洗脱分离效果更好,10种目标物出峰相对较快,色谱峰形较好。因目标物结构中均含有电负性基团,流动相中加入适量甲酸有利于形成[M+H]+分子离子峰,使得离子响应强度增加[15]。本实验设置流动相流速为0.30 mL/min,在保留时间(Rt)5.0~9.0 min范围内,10种合成大麻素离子峰的分离效果相对较好,其PRM色谱图如图1所示。

图1 10种合成大麻素的PRM色谱图(10.0 ng/mL)Fig.1 PRM chromatogram of 10 synthetic cannabinoids(10.0 ng/mL)the peak numbers of 1-10 denoted were the same as those in Table 1
2.1.2 质谱条件的选择按照“1.6”方法,取10.0 ng/mL混合标准溶液进样,分别在300、350、400、450、500℃下进行平行测定(n=6),考察离子源温度对10种合成大麻素峰面积响应值的影响。结果表明,随着温度的升高,各目标物的响应值均明显增强,并在400℃时达到峰值,离子源温度继续升高至500℃时,响应值无显著增加。综合考虑仪器保护及过高温度对目标物稳定性的影响,选择离子源温度为400℃。设置阶梯碰撞能量(Stepped CE):20、40、60 eV,对目标物的准分子离子进行碎裂,可获得不同能量碎裂离子的加合图谱,碎片离子信息更为丰富。10种合成大麻素的质谱信息见表1。
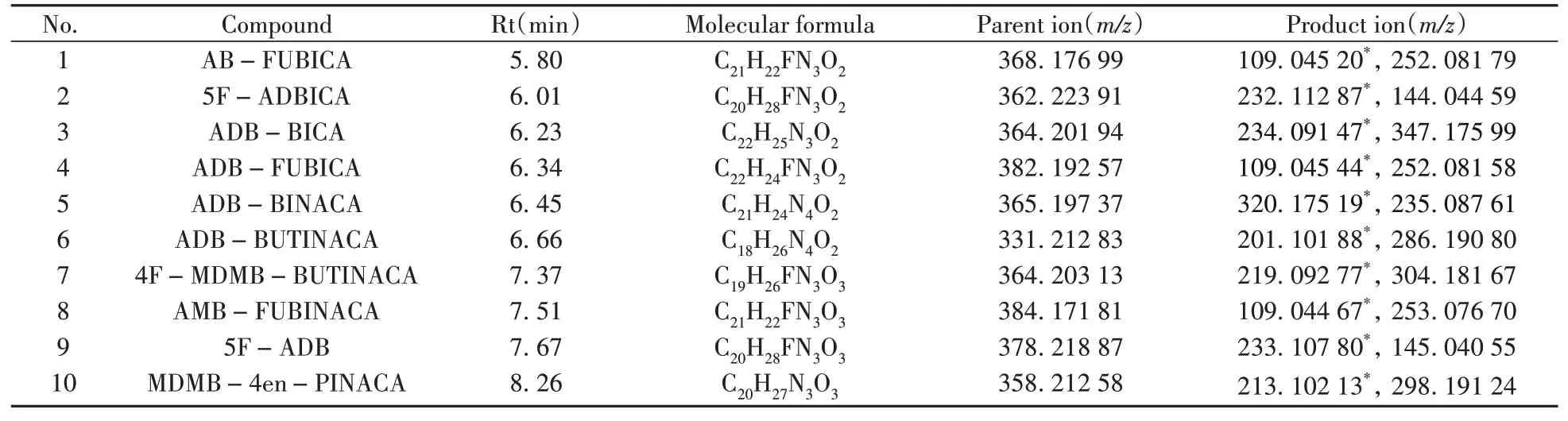
表1 10种合成大麻素的保留时间(Rt)、分子式及质谱信息Table 1 Retention times,formulas and mass spectrometry parameters of 10 synthetic cannabinoids
2.1.3 QuEChERS法的优化参考已有方法[17],本文QuEChERS法采用乙腈进行提取,以硫酸盐作为脱水剂和盐析剂,不仅可以脱掉全血中的水分,且能够增强水相的离子强度,从而增大全血中合成大麻素的分配系数,提高回收率。选择无水Na2SO4、无水MgSO4两种无机盐,以回收率为考察目标对相同浓度(10.0 ng/mL)的全血添加样本进行比较实验。结果显示,等量使用时无水MgSO4的回收率相对较高,且脱水过程中无结块现象。进一步考察了无水MgSO4用量(200、250、300、350、400、500 mg)对10种合成大麻素回收率的影响,结果显示,当用量超过350 mg后,目标物的回收率不再升高,因此确定无水MgSO4的用量为350 mg。
2.2 质谱碎裂分析
2.2.1 目标化合物分类按照化合物的母核结构,本文检测的10种合成大麻素可分为两大类:吲哚酰胺类,如AB-FUBICA、5F-ADBICA、ADB-FUBICA和ADB-BICA等;吲唑酰胺类,如ADBBINACA、ADB-BUTINACA、4F-MDMB-BUTINACA、AMB-FUBINACA、5F-ADB和MDMB-4en-PINACA等。其中吲唑酰胺类合成大麻素是传统JWH吲哚系列的升级替代产品[18],具有比吲哚类合成大麻素更强的精神活性[2]。
2.2.2 碎裂方式分析在HESI+/PRM模式下,10种目标物的二级质谱碎片离子碎裂方式呈以下特点:①分子结构中链接部酰胺的C—N键均可发生α断裂,形成带侧链的吲哚/吲唑酰阳离子;②相似结构化合物的碎裂方式相近,特征碎片离子一致;③母核(吲哚/吲唑核)碎片或母核N原子取代基的碎片离子峰特异性明显;④准分子离子峰[M+H]+的丰度值普遍较低。
AB-FUBICA、5F-ADBICA、ADB-FUBICA、ADB-BICA、ADB-BINACA和ADB-BUTINACA 6种化合物的结构相近,均为氨甲酰基吲哚/吲唑酰胺类合成大麻素,即顶部区域均含有氨甲酰基团,主要区别为前4种物质的母核为吲哚环结构,后2种物质的母核为吲唑环结构,母核中N原子的尾端取代基分别为氟苄基、5F-戊基、苄基和丁基等。6种化合物相近的碎裂方式为:分子结构中酰胺C—N键均发生α断裂,形成带侧链的吲哚/吲唑酰阳离子;当母核N原子上的取代基为苄基或氟苄基时,断裂产生丰度值最高的苄基或氟苄基阳离子;当母核N原子上的取代基为5F-戊基、丁基时,则发生杂环与烷烃N—C键断裂并伴随γH重排,形成吲哚/吲唑核酰阳离子m/z144或m/z145特征碎片,该碎片是区分吲哚与吲唑类合成大麻素的标志性碎片;6种化合物顶部区域均易发生酰胺C—N键断裂,产生准分子离子[M+H]+-NH3碎片离子,或氨甲酰基整体脱裂,产生准分子离子[M+H]+-CONH3碎片离子。具有代表性的3种物质的二级质谱碎裂方式分析如图2A~C所示。
4F-MDMB-BUTINACA、AMB-FUBINACA、5F-ADB和MDMB-4en-PINACA 4种化合物的结构相近,顶部区域酰胺键N原子上的链接组均为丁酸甲酯基团,母核均为吲唑环结构。主要区别在于母核N原子上的尾端取代基分别为4-氟丁基、氟苄基、5-氟丁基和1-戊-4-烯基,该类物质的主要碎裂方式与上述吲哚酰胺类物质相似。且4种物质的顶部区域均可发生酯基脱裂,形成准分子离子[M+H]+-COOCH3碎片离子。代表性物质的二级质谱碎裂方式分析如图2D所示。
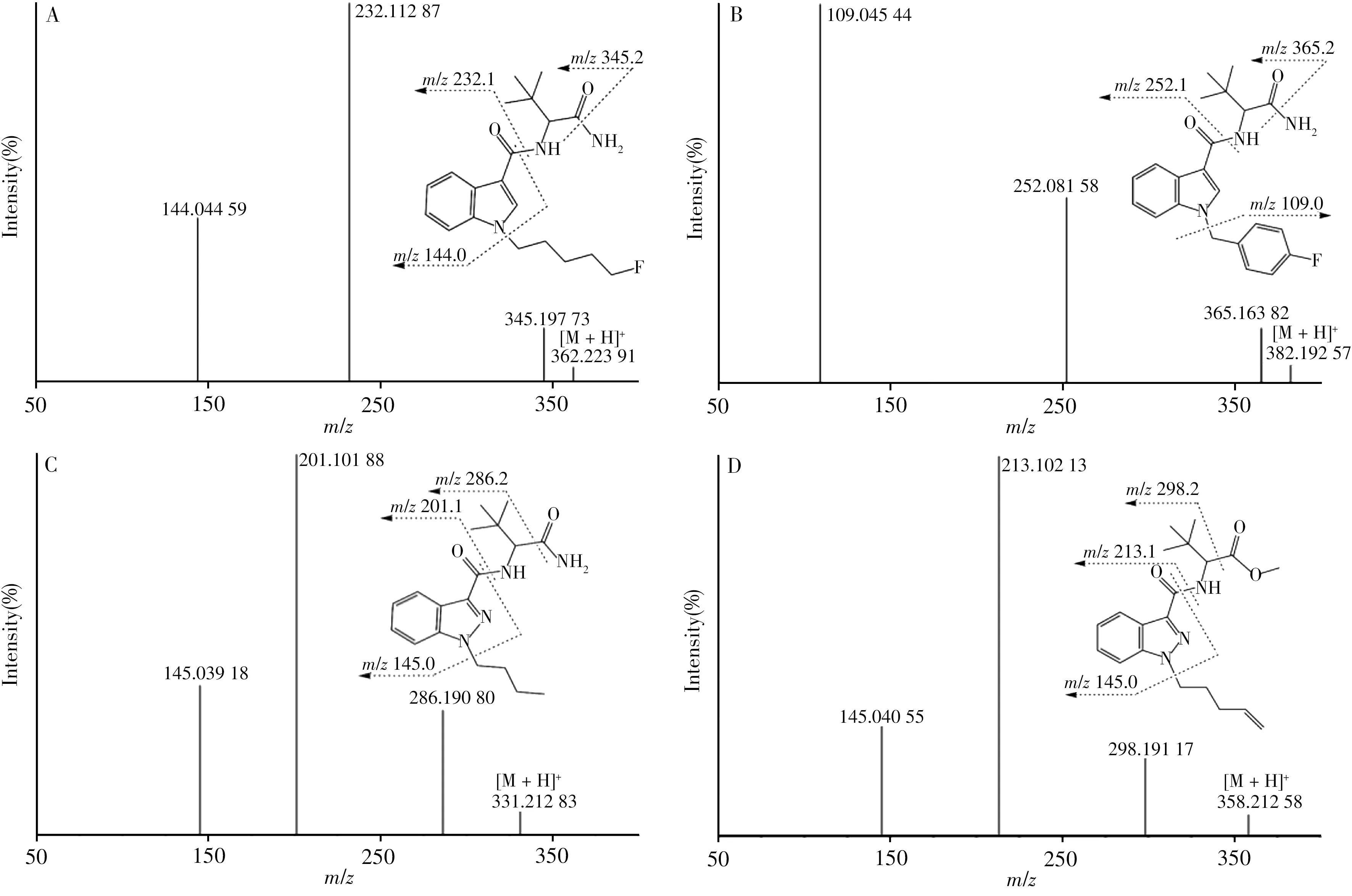
图2 4种代表性合成大麻素的MS2质谱图及碎裂方式分析Fig.2 MS2 spectra and fragmentation analysis of 4 typical synthetic cannabinoids
2.3 方法学建立
2.3.1 工作曲线、检出限及定量下限采用空白血液添加混合标准溶液方式,制备混标质量浓度分别为0.05、0.1、0.2、0.5、1.0、2.0、5.0、10.0、20.0、50.0、100.0 ng/mL的系列全血加标样本,按照“1.4”前处理方法和“1.6”仪器条件,由低到高浓度依次测定。以各目标物的质量浓度为横坐标(x,ng/mL),对应的定量离子响应值为纵坐标(y)进行线性回归。结果显示,10种合成大麻素在0.05~100.0 ng/mL或0.20~100.0 ng/mL范围内呈良好线性关系,相关系数(r2)均不小于0.999 0,检出限(LOD,S/N≥3)为0.01~0.05 ng/mL,定量下限(LOQ,S/N≥10)为0.05~0.20 ng/mL(见表2)。
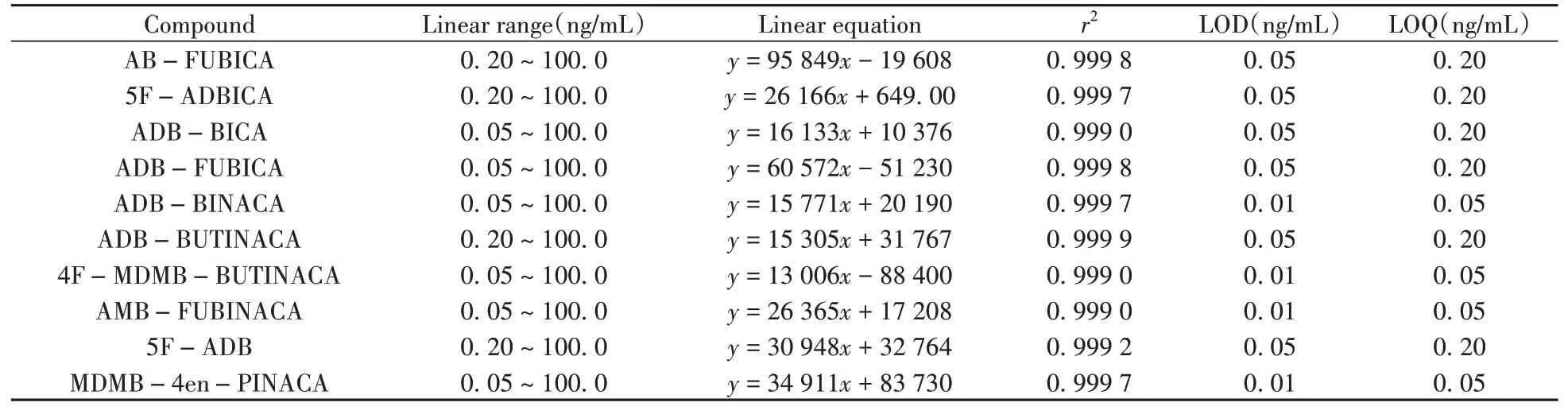
表2 10种合成大麻素的线性关系、检出限及定量下限Table 2 Linear relations,LODs and LOQs of 10 synthetic cannabinoids
2.3.2 加标回收率、基质效应及相对标准偏差采用空白基质添加混合标准溶液方式,分别制备10种合成大麻素质量浓度为0.2、5.0、50.0 ng/mL的空白血液加标样本,每个浓度平行制备3份。按照“1.4”前处理方法和“1.6”仪器条件进行测定,以加标样本中各目标物定量离子的峰面积为A;空白血液经QuEChERS法提取后加标样本中定量离子的峰面积为B;对应浓度混标溶液中各目标物定量离子的峰面积为C。参照Matuszewski[19]方法进行计算:加标回收率=A/C×100%,基质效应=B/C×100%。同一浓度全血加标样本当日重复测定6次,计算日内相对标准偏差(RSD),连续测定3 d,计算日间RSD。结果显示,10种目标物在3个加标水平下的回收率为92.1%~115%,基质效应为86.6%~115%;日内RSD均不大于8.5%,日间RSD均不大于10%(见表3)。
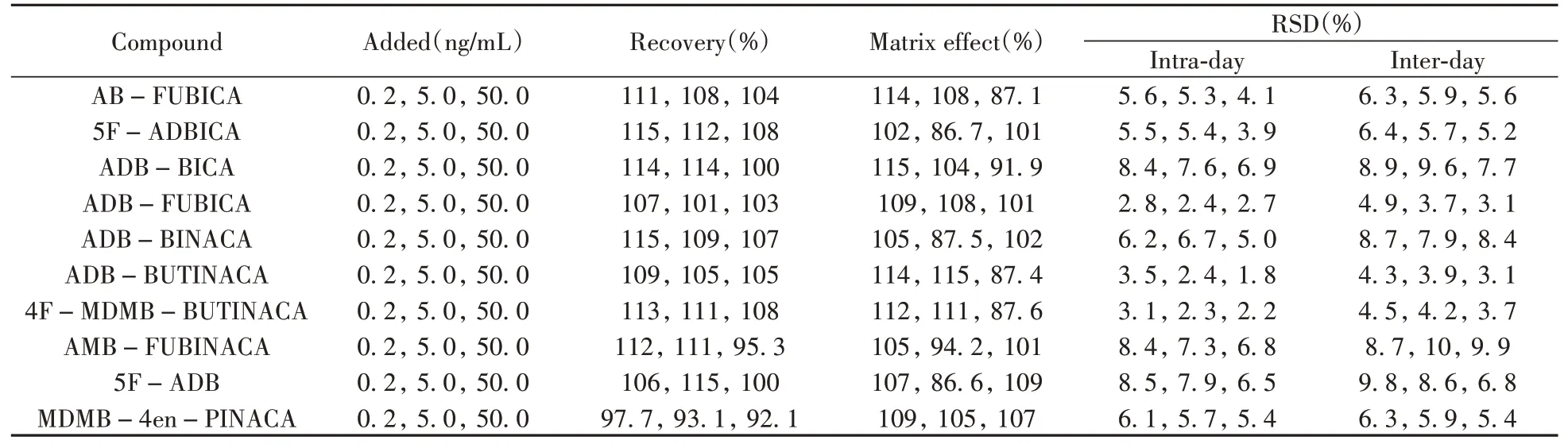
表3 10种合成大麻素的回收率、基质效应及相对标准偏差(n=6)Table 3 Recoveries,matrix effects and RSDs of 10 synthetic cannabinoids(n=6)
2.4 动物实验结果
应用本方法对注射混合药物的SD大鼠血液进行检测,结果显示,给药1 h后SD大鼠血液中均检出5F-ADBICA和MDMB-4en-PINACA,2只大鼠血液中5F-ADBICA的平均质量浓度为2.13 ng/mL,MDMB-4en-PINACA为1.76 ng/mL。表明所建方法适用于实际样品中合成大麻素物质的检验。
2.5 案例应用
应用本方法对一起因吸食合成大麻素导致伤害致死案件的嫌疑人血液样本进行检测,经与标准物质的色谱峰保留时间及质谱特征比较,确认该样本中检出MDMB-4en-PINACA。平行2个样本,每个样本测定6次,并结合工作曲线计算得到MDMB-4en-PINACA的平均质量浓度为3.72 ng/mL,测量值的RSD(n=6)均不大于5.4%。本方法稳定、检测结果可靠,检测结果为吸食合成大麻素行为认定提供了科学依据。
3 结论
本文通过对QuEChERS前处理方法、色谱流动相和质谱条件进行优化,建立了全血中10种新型合成大麻素的超高效液相色谱-四极杆/静电场轨道阱高分辨质谱检测方法,对10种目标物的质谱信息、碎片离子主要碎裂方式进行分析,并进行了方法学考察。本方法具有操作简便快捷、数据稳定、检测灵敏度及回收率高的特点,动物实验和真实案例的血液样本检测结果证明方法可靠,能够满足滥用合成大麻素案件检验鉴定的实际需要。

