不同β受体激动剂联合阿托伐他汀治疗COPD合并冠状动脉粥样硬化心脏病患者临床疗效的对比研究
叶 斌,叶 波
慢性阻塞性肺疾病(chronic obstructive pul‐monary Disease,COPD)在呼吸系统疾病中占据着较高的病发比例,其病发率和病死率高,患者病情恶化到一定程度还极易造成肺心病,从而对患者生活质量以及生命健康都构成严重威胁[1]。以往研究对COPD患者死亡后的尸体检查发现,其中合并冠状动脉粥样硬化心脏病患者比例高达77.7%,上述两种疾病在老年人群中有较高的发病率,是常见的慢性病之一,严重危害人类健康,影响患者生活质量。据推算,我国每年因冠心病去世的人数约有110万,给患者及其家属、国家带来了沉重的负担。该病发机制十分复杂,与肺功能、氧化应激水平之间都具有密切联系[2]。因此对患者的肺功能与氧化应激水平实施密切监测对于COPD患者的病情评估具有关键意义[3-4]。当COPD与心绞痛、心肌梗死、心力衰竭等疾病同时存在时,可以遵循心绞痛、心肌梗死、心力衰竭等疾病治疗指南,使COPD合并冠状动脉粥样硬化心脏病患者治疗更加规范化。目前临床上治疗COPD以药物治疗为主,其中β2受体激动剂的抗炎效果显著,可明显改善患者的血清炎性水平,减轻不良症状,从而改善患者的肺功能[5]。同时,阿托伐他汀治疗冠心病具有显著的效果,可有效改善血浆内皮素-1(endothelin-1,ET-1)与脑钠肽(brain natriuretic peptide,BNP)水平,并减轻患者炎症水平,改善氧化应激指标[6]。因此,本文旨在对比β受体激动剂硫酸特布他林雾化液和布地格福吸入雾化剂分别联合阿托伐他汀治疗COPD合并冠状动脉粥样硬化心脏病患者的疗效、肺功能和氧化应激水平,以及减少心血管事件的差异研究,旨在为COPD合并冠状动脉粥样硬化心脏病的临床治疗提供有效参考依据。
1 资料与方法
1.1 一般资料本次研究前瞻性选择2019年1月-2021年12月成都市第一人民医院收治的COPD合并冠状动脉粥样硬化心脏病患者104例。依据随机数表法将所有纳入患者分为治疗A组、治疗B组,每组各52例。其中,治疗A组年龄41~78岁,病程12~16 d;治疗B组年龄42~76岁,病程10~15 d。两组纳入患者的基础资料差异均无统计学意义(P>0.05),具有一定可比性,详见表1。本治疗方案获得本院伦理委员会的认可支持。
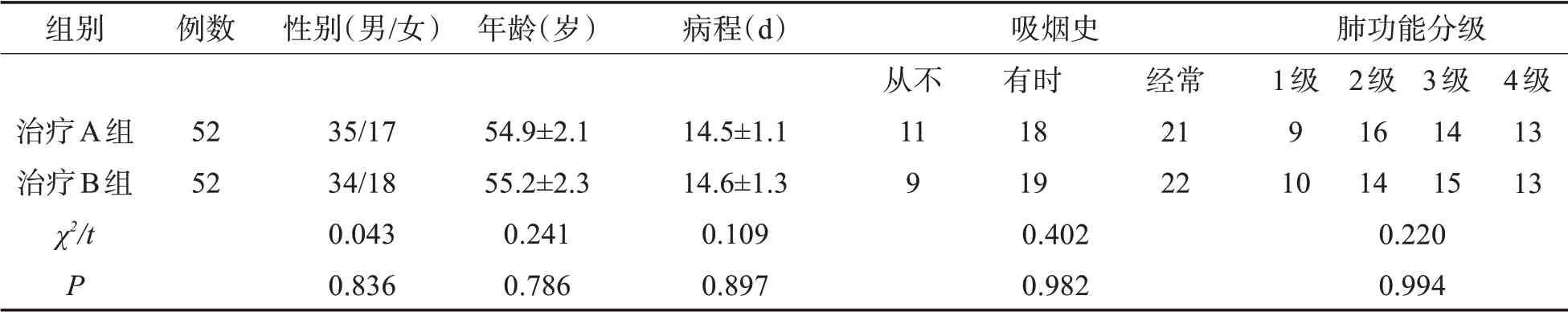
表1 两组患者的基础信息资料比较
1.2 纳排标准纳入标准:①确诊为COPD稳定期且合并冠状动脉粥样硬化心脏病的患者,依据《慢性阻塞性肺疾病基层诊疗指南(2018年)》[7]和《稳定性冠心病诊断与治疗指南》[8]中COPD稳定期和冠状动脉粥样硬化心脏病的诊断标准;②患者伴有呼吸困难、咳嗽等慢性阻塞性肺病临床症状[9];③患者在治疗前1个月内未接受过COPD治疗药物;④患者以及家属均知情同意本次研究,并签订研究知情同意书。排除标准:①患者伴有明显的阻滞剂禁忌证;②患者存在精神不正常或认知功能障碍等,不能独立配合完成研究;③患者具有肺部功能感染以及恶性肿瘤等症状;④患者属于支气管哮喘;⑤患者对本次治疗药物具有过敏史。⑥慢性阻塞性肺疾病急性加重期的患者
1.3 干预方法治疗A组:该组患者接受β2受体激动剂干预,给予患者硫酸特布他林雾化液(Astra‐Zeneca AB,注册证号H20140108,2 mL:5 mg*20支)进行雾化吸入干预,1次5 mg,1日2次及阿托伐他汀干预。治疗B组:该组患者予以阿托伐他汀干预,给予患者温水口服阿托伐他汀钙片(福建东瑞制药有限公司,国药准字H20193043,10 mg*28片),1次20 mg,1日1次,同时给予布地格福吸入雾化剂。两组患者均连续接受干预3个月。
1.4 观察指标
1.4.1 临床疗效评估显效:纳入患者的临床不良症状基本消失,肺功能指标监测改善,肺部感染症状也基本消失。有效:纳入患者的临床不良症状部分好转,肺功能指标有所改善;无效:纳入患者的临床不良症状、肺功能指标有所改善以及肺部感染症状均无好转。有效率=(显效+有效)/总例数×100%。
1.4.2 临床症状缓解时间评估仔细记录所有纳入患者在干预后的咳嗽缓解时长、喘息缓解时长以及肺啰音消失时长。
1.4.3 血清炎性水平检测所有患者在治疗一月后均于清晨空腹抽取静脉血5mL,4000 rpm/min,离心半径5.0cm,离心15 min后,取上层血清于-80℃冻存以备待检。通过酶联免疫吸附法对所有纳入患者的肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素8(Interleukin-8,IL-8)与白细胞介素6(in‐terleukin 6,IL-6)水平予以检测,试剂盒均购自中国上海联迈生物工程有限公司,具体操作按照说明书实施,控制批内差异保持<10%,批间差异保持<15%[10]。
1.4.4 肺功能评估通过肺功能仪(德国,耶格医疗器械有限公司)对所有纳入患者的第一秒用力呼气容积(Forced expiratory volume in one second,FEV1)、FEV1百分比(Forced expiratory volume in one second percentage,FEV1%)、第一秒用力呼气容积(Forced expiratory volume in one second,FEV1)/用力肺活量(Forced vital capacity,FVC)予以检测评估[9]。
1.4.5 血浆ET-1和BNP水平评估通过酶联免疫吸附法对所有纳入患者的血浆ET-1内皮-素1和BNP水平予以检测,试剂盒均购自中国上海西唐生物科技有限公司,具体操作按照说明书实施,控制批内差异保持<10%,批间差异保持<15%[10]。
1.4.6 氧化应激水平评估通过酶联免疫吸附法对所有纳入患者的活性氧(Reactive Oxygen Species,ROS)、丙二醛(Malonic dialdehyde,MDA)、谷胱甘肽过氧化物酶(Glutathione Peroxidase,GPX)、超氧化物歧化酶Orgotein(Superoxide Dismutase,SOD)水平予以检测,试剂盒均购自美国R&D公司,具体操作按照说明书实施,控制批内差异保持<10%,批间差异保持<15%[11]。
1.4.7 药物安全性评估仔细记录所有纳入患者在干预期间的转氨酶上升,皮肤过敏,腹部疼痛,排便困难等不良症状出现情况以此评估药物安全性。
1.4.8 主要心血管不良事件(major adverse cardio‐vascular events,MACE)发生率随访六个月,评估和记录新发心绞痛、急性心肌梗死、心力衰竭的发生率。
1.5 统计学处理本研究通过SPSS 26.0软件对本次所有研究数据进行分析。其中计量资料主要通过均数±标准差()予以描述,组间比较则通过t予以检验。计数资料通过百分数予以表示,组间比较则通过χ2予以检验。均以P<0.05表示差异具有统计学意义。
2 结果
2.1 临床疗效比较治疗B组接受联合干预方案后的临床治疗有效率为92.3%高于治疗A组69.2%(χ2=8.914,P<0.05)。见表2。

表2 两组COPD患者的临床疗效比较[n(%)]
2.2 临床症状缓解时间比较治疗B组接受联合干预方案后患者自觉咳嗽缓解时长、喘息缓解时长以及听诊肺啰音消失时长等指标均显著短于治疗A组(P<0.05)。见表3。
表3 对比2组COPD患者的临床症状缓解时间(±s)

表3 对比2组COPD患者的临床症状缓解时间(±s)
组别治疗A组治疗B组tP例数5252咳 嗽缓解时长(d)6.38 ±2.79 4.75 ±1.48 3.722< 0.001喘息缓解时长(d)4.96 ±1.62 3.22 ±1.06 6.481< 0.001肺啰音消失时长(d)6.56 ±2.85 3.24 ±2.18 6.672< 0.001
2.3 血清炎性水平比较干预前,两组患者TNFα、IL-8与IL-6水平差异无统计学意义(P>0.05);干预后,两组患者TNF-α、IL-8与IL-6水平均下降(P<0.05),且干预后治疗B组患者的TNF-α、IL-8与IL-6水平均显著低于治疗A组(P<0.05),说明B组患者炎症更轻,见图1。

图1 血清炎性水平比较a表示与同组干预前比较P<0.05;b表示与同组干预前比较P<0.05。
2.4 血浆ET-1和BNP水平比较干预前,两组患者血浆ET-1和水平差异无统计学意义(P>0.05);干预后,两组患者血浆ET-1和BNP水平均显著改善(P<0.05),且干预后治疗B组患者的血浆ET-1和BNP水平显著低于治疗A组(P<0.05),说明B组患者心脏负荷较低,见图2。

图2 血浆ET-1和BNP水平比较a表示与同组干预前比较P<0.05;b表示与同组干预前比较P<0.05。
2.5 肺功能比较干预前,两组患者的肺功能无明显差异(P>0.05),干预后,两组患者的肺功能有了明显改善(P<0.05),且干预后治疗B组患者的FEV1、FEV1%、FEV1/FVC水平则显著高于治疗A组(P<0.05),说明B组患者肺功能比A组患者好,见图3。

图3 肺功能比较a表示与同组干预前比较P<0.05;b表示与同组干预前比较P<0.05
2.6 氧化应激水平比较干预前,两组患者的ROS、MDA、GPX、SOD水平无明显差异(P>0.05),干预后,两组患者的ROS、MDA、GPX、SOD水平有了明显改善(P<0.05),且干预后治疗B组患者的ROS、MDA水平显著低于治疗A组,而GPX、SOD水平则显著高于治疗A组(P<0.05),说明B组氧化应激水平更低,见图4。

图4 氧化应激水平比较a表示与同组干预前比较P<0.05;b表示与同组干预前比较P<0.05
2.7 药物安全性比较两组COPD患者在干预过程中均未出现严重不良反应,药物干预方案安全性良好。治疗A组出现转氨酶上升4例,皮肤过敏2例,腹部疼痛2例,排便困难3例,不良症状出现率为21.2%(11/52);治疗B组出现转氨酶上升1例,皮肤过敏1例,腹部疼痛0例,排便困难1例,不良症状出现率为5.8%(3/52),暂停用药后两组患者不良症状均得到有效缓解,且治疗B组患者的不良症状出现率明显低于治疗A组(P<0.05)。
2.8 心血管事件比较随访6个月期间,治疗A组MACE 12例(23.1%),其中新发心绞痛6例(11.5%),急性心肌梗死2例(3.9%),心力衰竭4例(7.7%),治疗B组MACE 7例(13.5%),其中新发心绞痛3例(5.8%),急 性 心 肌 梗 死1例(1.9%),心 力 衰3例(5.8%),B组MACE低于A组(P<0.05)。
3 讨论
COPD作为临床上常见的气流受限性的呼吸系统疾病之一,其病发人群广,老年人群为主,且目前随着社会经济的不断发展,其病发几率也在逐年递增,进而为患者带来严重不良后果,降低其生活质量,严重者合并冠状动脉粥样硬化心脏病,从而对患者的生命健康构成严重威胁,已成为重要的社会公共问题。因此,对于COPD合并冠状动脉粥样硬化心脏病患者予以安全有效的治疗方案对缓解患者病情,改善其生活质量具有重要意义[12-13]。
β2受体激动剂作为一种支气管扩张剂,其具有抗炎效果,可以促使气道表面的β-受体保持兴奋,减弱微血管通透性,进而减轻气道不良症状。有研究表示,β2受体激动剂可作为治疗COPD患者的首选药物[14-15],但β2受体激动剂种类较多,不同药物的应用效果对比有待验证,因此本文就布地格福吸入雾化剂相比硫酸特布他林雾化液两种药物的疗效进行对比同时,也有研究表示阿托伐他汀对COPD患者具有一定治疗效果。其具有抗氧化效果,能有效减轻患者体内的自由基水平,以此阻碍肺纤维化的发生。同时,阿托伐他汀能有效抑制患者肺部多种炎性细胞的募集和趋化,抑制炎性细胞释放炎性细胞因子,从而起到抗炎效果。此外,阿托伐他汀还能改善患者的肺功能可改善COPD患者肺功能,降低病发率和病死率[16-17]。
目前临床有研究证实β2受体激动剂与阿托伐他汀均对COPD具有一定疗效[18]。本研究结果显示布地格福吸入雾化剂组患者在干预后的临床治疗有效率显著高于硫酸特布他林雾化液组(χ2=8.914,P<0.05),且布地格福吸入雾化剂组患者在干预后的咳嗽缓解时长、喘息缓解时长以及肺啰音消失时长等指标均显著短于硫酸特布他林雾化液组(P<0.05);同时,干预后两组患者TNF-α、IL-8与IL-6水平较干预前均显著下降(P<0.05),且干预后布地格福吸入雾化剂组患者的TNF-α、IL-8与IL-6水平均显著小于硫酸特布他林雾化液组(P<0.05);干预后两组患者血浆ET-1和BNP水平较干预前均显著改善(P<0.05),且干预后布地格福吸入雾化剂组患者的血浆ET-1和BNP水平显著低于硫酸特布他林雾化液组(P<0.05);干预后两组患者的肺功能较干预前有了明显改善(P<0.05),且干预后布地格福吸入雾化剂组患者的FEV1、FEV1%、FEV1/FVC水平则显著高于硫酸特布他林雾化液用药组(P<0.05);两组COPD患者在干预过程中均未出现严重不良反应,药物干预方案安全性良好,且布地格福吸入雾化剂组患者的不良症状出现率明显低于硫酸特布他林雾化液组(P<0.05),由此可以提示将β2受体激动剂布地格福吸入雾化剂与阿托伐他汀联合应用于COPD治疗的疗效显著,可加快临床症状缓解时间,有效改善患者肺功能、血浆ET-1与BNP水平,减轻血清炎性水平,且药物安全性良好。其原因分析如下:β2受体激动剂能有效减轻患者体内的炎性水平,抑制炎症反应的发生,从而促使患者肺部和气道的炎症均能获得有效控制。阿托伐他汀则能有效加快支气管内皮细胞因子生长,提高患者的通气功能,促使肺部血管得到扩张,进而改善其肺功能。因此两者联合应用,可有效进一步改善患者的肺功能,减轻其炎症水平以及不良症状。郭新跃研究证实,阿托伐他汀可显著改善患者的肺功能,并减轻其炎性因子水平,与本文研究结果相似[19]。
薛华等研究发现,COPD患者体内的气流受限不仅和患者自身机体的异常炎性水平有关,在疾病发生进展过程中,还和氧化应激水平的变化情况具有密切联系。氧化应激的出现可对患者的肺部组织造成损伤,还能使得炎性因子水平上升,进而加重患者病情。SOD作为人体内一种有效的自由基清除剂,对清除COPD患者体内过高的自由基发挥着重要作用,而在清除患者过高自由基时又需耗费大量SOD,所以COPD体内的患者SOD水平相较于正常人群而言较低。GPX作为人体内重要的抗氧化指标,能有效控制脂质过氧化,降低MDA的生成率,从而达到降低对患者造成的脂质氧化损伤[20]。因此,本文将重点监测患者的氧化应激水平,以此评估患者的病情变化情况。本研究中干预后两组患者的ROS、MDA、GPX、SOD水平较干预前有了明显改善(P<0.05),且干预后布地格福吸入雾化剂组患者的ROS、MDA水平显著低于硫酸特布他林雾化液组,而GPX、SOD水平则显著高于单纯用药组(P<0.05),提示β2受体激动剂联合阿托伐他汀能有效发挥抗炎和抗氧化应激的效果。Liu Y等研究文献表示,β2受体激动剂对改善氧化应激水平具有明显效果,还可改善患者的肺功能,与本文研究结果相似[21]。同时,本文发现随访6个月期间,治疗A组应用布地格福吸入雾化剂总心血管事件发生率明显降低,说明布地格福吸入雾化剂相比硫酸特布他林雾化液对患者心脏疾病预后有明显改善。
综上所述,将β2受体激动剂布地格福吸入雾化剂与阿托伐他汀联合应用于COPD治疗中,其临床疗效显著,可加快临床症状缓解时间,有效改善患者肺功能、血浆ET-1与BNP水平,减轻血清炎性水平,控制氧化应激水平,降低心血管事件,药物安全性良好,值得推广。由于研究的样本量受到一定的限制,所以其研究数据需进一步加大样本量进行研究证实。

