高血压合并心力衰竭患者血脂指标及比值与左心室重构的关系研究
刘玲玲,颜永进
高血压是常见的慢性心血管疾病,随机体血压的持续升高对心脏造成较大负荷,最终引发心力衰竭。相关研究显示,高血压常引发心室纤维化、心室腔内压力增加,出现心室扩大、心腔球形化趋势等代偿性重塑现象,心室重构是心力衰竭发生的病理基础,也是防治的重要内容[1]。近年来有研究显示,心周脂肪组织体积异常增加是发生心室重构的独立危险因素,提示心室重构与脂代谢异常有关[2]。还有研究发现,血脂水平及其比值与左心室构型明显相关,但该研究主要针对健康人群,在高血压、心力衰竭等心血管疾病患者中关系并不明确[3]。本次研究旨在分析高血压合并心力衰竭患者的血脂水平及比值变化,分析其与此类患者发生心室重构的相关性,以期为高血压患者心力衰竭防治提供参考。
1 资料与方法
1.1 一般资料选取2019年6月到2022年6月海安市人民医院收治的159例高血压患者作为研究对象,将全部研究对象分为训练集和测试集两大组:训练集患者80例,其中男性48例,女性32例;平均年龄(58.70±4.90)岁;体质量指数(body mass index,BMI)(24.09±1.24)kg/m2;其中51例高血压合并心力衰竭患者为研究组,男31例,女20例;年龄(58.74±4.92)岁;BMI为(24.08±1.23)kg/m2;纽约心脏病协会(New York Heart Association,NYHA)分级,Ⅱ级18例,Ⅲ级15例,Ⅳ级18例;29例高血压未合并心力衰竭患者为对照组,男17例,女12例;年龄(58.64±4.88)岁;BMI(24.11±1.25)kg/m2。测试集中患者79例,其中男性50例,女性29例;平均年龄(58.64±4.96)岁;BMI(24.06±1.19)kg/m2。
1.2 纳入标准①高血压诊断标准参考《中国老年高血压管理指南2019》[4],非同日测量三次血压值收缩压超过140 mmHg和(或)舒张压超过90 mmHg,且病程≥3年,心力衰竭诊断参考《中国心力衰竭诊断和治疗指南2018》[5];②临床资料完整;③年龄≥18岁;④患者知情并签署知情同意书。
1.3 排除标准①合并先天性心脏病、心包炎、肺心病等其他心脏病;②存在创伤、感染、免疫系统疾病、严重肝肾功能不全、恶性肿瘤或其他影响心功能的全身性疾病;③合并妊娠、内分泌疾病、贫血、慢性溶血等。
1.4 方法收集所有患者一般临床资料,包括性别、年龄、BMI、高血压病程、血压、血液生化指标、超声检查结果等。(1)血液生化指标检测:入院第一天抽取清晨空腹8 h以上静脉血,采用全自动生化仪(日立公司7600型)检测患者空腹血糖(fasting blood glucose,FBG)、尿素氮(blood urea nitrogen,BUN)、血肌酐(blood creatinine,Scr)、总胆固醇(total cholesterol,TC),甘油三酯(High density lipo‐protein,TG),高密度脂蛋白(high density lipopro‐tein,HDL-C),低密度脂蛋白(low density lipopro‐tein,LDL-C),并计算TC/HDL-C、TG/HDL-C、LDL-C/HDL-C比值。(2)超声检查:采用彩色多普勒超声(美国GE公司,LOGIQE9型)测定左心室心肌质量(left ventricular myocardial mass,LVM),软件自动获得左心室舒张末期容积(left ventricular end dia‐stolic volume,LVEDV)、左心室舒张末期内径(left ventricular end diastolic diameter,LVEDD)、左室射血分数(left ventricular ejection fraction,LVEF)及舒张末期左心室心肌质量(left ventricular mass,LVM)等参数,计算左心室重构指数(left ventricular re‐modeling index,LVRI)=LVM/LVEDV。
1.5 统计学处理SPSS 22.0软件包分析数据,符合正态分布计量资料以均数±标准差()表示,组间比较采用t检验;计数资料以百分率“%”表示,组间比较采用χ2检验;多因素Logistic回归分析影响高血压患者发生心力衰竭的危险因素,Pearson相关性分析LVRI与血脂指标及比值关系。记P<0.05为差异有统计学意义。
2 结果
2.1 训练集一般资料分布特征训练集中研究组患者高血压病程、FBG、TG、TC/HDL-C、TG/HDL-C、LDL-C/HDL-C、LVEDD高于对照组,HDL-C、LVEF、LVRI低于对照组(P<0.05)。见表1。
表1 训练集一般资料分布特征(±s)

表1 训练集一般资料分布特征(±s)
一般临床资料TC(mmol/L)LDL-C(mmol/L)高血压病程(年)FBG(mmol/L)TG(mmol/L)HDL-C(mmol/L)TC/HDL-C TG/HDL-C LDL-C/HDL-C LVEF(%)LVEDD(mm)LVRI(g/ml)研究组(n=51)5.02 ±0.81 3.12 ±0.83 14.76 ±4.02 6.48 ±1.50 1.76 ±0.48 1.18 ±0.36 4.25 ±0.72 1.49 ±0.41 2.64 ±0.51 49.06 ±4.10 54.76 ±8.45 1.14 ±0.21对照组(n=29)4.95 ±1.23 3.09 ±0.74 11.32 ±3.84 5.72 ±1.06 1.52 ±0.33 1.53 ±0.40 3.24 ±0.61 0.99 ±0.35 2.02 ±0.40 55.78 ±5.34 46.78 ±6.92 0.91 ±0.17 t值0.3070.1613.7392.4052.3884.0156.3625.5195.6306.3034.3245.031 P 值0.7600.8720.0030.0180.0190.001< 0.001<0.001<0.001<0.001<0.001<0.001
2.2 训练集和测试集一般资料分布特征训练集和测试集患者高血压病程、FBG、TG、TC/HDL-C、TG/HDL-C、LDL-C/HDL-C、LVEDD/HDL-C、LVEF、LVRI对比,差异不具有统计学意义组(P>0.05)。见表2。
表2 训练集和测试集一般资料分布特征(±s)

表2 训练集和测试集一般资料分布特征(±s)
一般临床资料TC(mmol/L)LDL-C(mmol/L)高血压病程(年)FBG(mmol/L)TG(mmol/L)HDL-C(mmol/L)TC/HDL-C TG/HDL-C LDL-C/HDL-C LVEF(%)LVEDD(mm)LVRI(g/ml)训练集(n=80)4.99 ±0.98 3.11 ±0.80 13.51 ±3.95 6.20 ±1.48 1.67 ±0.45 1.31 ±0.34 3.88 ±0.65 1.31 ±0.39 2.42 ±0.48 51.50 ±4.98 51.87 ±8.01 1.06 ±0.18测试集(n=79)4.99 ±0.98 3.20 ±0.83 13.68 ±3.77 6.33 ±1.37 1.60 ±0.42 1.40 ±0.45 3.79 ±0.59 1.28 ±0.42 2.34 ±0.57 52.38 ±5.12 50.68 ±7.80 1.10 ±0.20 t值0.7450.6960.2780.5751.0141.4240.9140.4670.9581.0990.9491.326 P 值0.4570.4870.7820.5660.3120.1560.3620.6410.3400.2740.3440.187
2.2 基于训练集患者分析不同NYHA分级高血压合并心力衰竭患者血脂指标、LVRI差异随NYHA分级增加,TG、TC/HDL-C、TG/HDL-C、LDL-C/HDL-C逐渐升高,HDL-C逐渐降低(P<0.05)。见图1。

图1 不同NYHA分级高血压合并心力衰竭患者血脂指标、LVRI差异
2.3 基于训练集患者的LVRI与血脂指标及比值的相关性分析Pearson相关性分析显示,LVRI与TG、TC/HDL-C、TG/HDL-C、LDL-C/HDL-C呈正相关,与HDL-C呈负相关(P<0.05)。见表3。

表3 LVRI与血脂指标及比值的相关性
2.4 基于训练集对影响高血压患者发生心力衰竭影响因素的回归模型建立将训练集一般资料中具有统计意义的指标纳入多因素Logistic回归分析如高血压病程,FBG,TG,HDL-C,TC/HDL-C,TG/HDL-C,LDL-C/HDL-C,LVEF,LVEDD,LVRI等指标。logistic回归方程为,Log(y)=-6.908+0.887*高血压病程+1.132*FBG+1.051*TC+0.827*TC/HDLC+0.991*TG/HDL-C+1.159*LDL-C/HDL-C+1.066*HDL-C+1.009*LVRI。见表4、图2。

表4 影响高血压患者发生心力衰竭的多因素Logistic回归分析
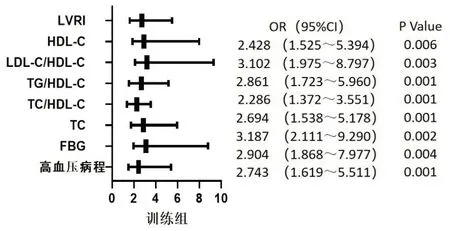
图2 基于训练集的危险因素示意图
3 讨论
心力衰竭是心血管疾病进展到终末阶段的表现,而高血压患者因长期心脏处于高负荷状态,心脏会出现左心室肥厚、形状变化等代偿性改变,引发心室重构[6-7]。心脏因长期病理变化最终引发心力衰竭,故心室重构是心力衰竭发生的基本病理机制[8]。心力衰竭治疗手段有限且病死率高,而早期识别并干预心室重构对降低心力衰竭发生具有重要意义。
高血压患者出现左室舒张功能下降时主要表现为心肌细胞肥大和心肌组织纤维化[9]。相关研究显示,原发性高血压患者若合并肥胖或血脂紊乱,左心室肥厚情况往往更加明显[10]。还有研究认为,血脂引发左心室重构可能与脂代谢异常、炎症因子大量释放引发心肌细胞纤维化加剧有关[11]。本次研究显示,与无心力衰竭患者比较,合并心力衰竭的高血压患者存在明显的TG、TC/HDL-C、TG/HDLC、LDL-C/HDL-C升高和HDL-C降低。TC、TG、HDL-C、LDL-C是临床常用的血脂代谢评价指标,其中TC、TG、LDL-C升高多提示血液粘稠度增加和动脉粥样硬化风险的升高[12]。相关研究显示,沉积在冠状动脉中的LDL-C能刺激巨噬细胞活化,分泌一系列炎症因子,加重心肌细胞损伤[13];而HDL-C能将周围游离的胆固醇逆向转运至肝脏,从而降低脂肪在心肌组织中的聚集[14]。本次研究发现,研究组TG高于对照组,HDL-C低于对照组,提示高血压患者发生心力衰竭与血脂水平异常有关。相关研究显示,TG的明显升高提示血脂超负荷,可增加血液粘稠度和心脏泵血负担,心肌细胞耗氧量增加,从而诱发心力衰竭[15]。血脂指标比值目前已经在糖尿病、冠心病等多种心血管疾病及其并发症评价中取得良好效果。相关研究认为,血脂比值能综合反映机体血脂的综合水平,相对于单项血脂指标具有更高的灵敏度和准确度[16]。还有研究发现,在多种心血管疾病的发病早期,各项血脂指标还未出现明显异常时,血脂指标已经开始发生变化[17]。
多因素Logistic回归分析显示,高血压病程长、高FBG、高TC、高TC/HDL-C、高TG/HDL-C、高LDLC/HDL-C、低HDL-C、低LVM是高血压患者发生心力衰竭的危险因素。高血压病程长和高FBG是高血压患者并发症的常见诱因,而本次研究发现,高TC、高TC/HDL-C、高TG/HDL-C、高LDL-C/HDL-C、低HDL-C也可预警高血压患者发生心力衰竭风险升高。有研究认为,机体中的甲羟戊酸途径能合成胆固醇和其他中间体,其中部分中间体能通过修饰细胞中的小分子G蛋白介导左心室重构过程,这也是胆固醇参与左室重构的重要原因[18]。此外,HDLC也因具有抗炎作用从而缓解血管内皮损伤,而血管内皮细胞损伤后期释放内皮素增加,反过来会促进血压的升高。还有学者发现,血脂代谢异常与胰岛素抵抗(insulin resistance,IR)、氧化应激密切相关,而后者也是引发心力衰竭的公认危险因素[19]。进一步分析血脂指标与LVRI关系发现,LVRI与TG、TC/HDL-C、TG/HDL-C、LDL-C/HDL-C呈正相关,与HDL-C呈负相关,提示以上血脂指标及比值可用于临床评估左心室重构程度。有学者发现,TG/HDL-C、LDL-C/HDL-C与IR高度相关,血脂代谢异常可能通过影响IR参与左心室重构。还有学者发现TC/HDL-C是影响脑梗死发病的独立因素,且脑梗死的发生是脂代谢异常引发的炎症反应和血管性病变、神经递质变化共同作用的结果[20]。因此血脂指标及比值可作为一类较易获得的血液指标用于评估左心室重构和预测心力衰竭的发生风险。
综上所述,高血压合并心力衰竭患者血脂水平及比值与左心室重构密切相关,临床需及早防控血脂异常,以降低心力衰竭的发生。但本次研究尚有不足之处,一是血脂指标及比值与LVRI的具体机制尚不明确;二是只分析了血脂与左心室结构变化关系,而对其与心室功能变化关系有待进一步研究。

