矿化法合成羟基磷灰石及其除氟性能
朱丹琛, 朱娟娟, 郑炳云
( 1. 莆田学院 环境与生物工程学院, 福建 莆田 351100;2. 福建省新型污染物生态毒理效应与控制重点实验室, 福建 莆田 351100;3. 福建省高校生态环境及其信息图谱重点实验室, 福建 莆田 351100 )
0 引言
由于人们生活的需要和社会生产的发展, 电镀、 冶炼、 半导体制造等行业得到大幅发展, 排放出大量的高浓度含氟废水, 如生产晶体硅太阳能电池板产生的氟化物废水浓度高达2 500 mg·L-1[1]。 而世界卫生组织(WHO)规定饮用水含氟量不超过1.5 mg·L-1。 饮用含有过量氟化物的水会损害人体健康, 如导致氟骨症、 甲状腺功能受损等, 严重的情况下还会引起膀胱癌、 骨肉瘤等癌症[2]。 目前采用的脱氟处理技术主要有混凝沉淀法、 膜处理、 吸附法和离子交换法[3]。 其中, 吸附法因具有处理效果好、 工艺流程简单等优点, 成为处理含氟废水的有效方法[4]。 羟基磷灰石(HA)具有较强的吸附性能以及良好的生物相容性, 是一种环境友好型的新型除氟剂[5-6]。
近年来不断有研究报道采用不同方法合成HA 及HA 复合材料, 并用于处理氟离子(F-);但所报道的合成方法中, 沉淀法合成的粉末容易团聚、 溶剂热法能耗较大, 影响了这两种方法的进一步使用。 矿化法是一种无机矿物相的缓慢结晶、 生长的方法, 具有易操作、 设备简单和成本低等优点。 然而较少报道采用矿化法合成HA 用于去除F-的文献。 本研究采用矿化法合成HA,通过改变合成时间探究合成HA 的最佳条件, 并探讨HA 的吸附时间、 投加量和溶液pH 值等对HA 除氟性能的影响。
1 实验部分
1.1 试剂与仪器
实验试剂: Ca(NO3)2·4H2O、 (NH4)3PO4·3H2O、 NaF、 浓氨水, 无水乙醇, 均为分析纯,国药集团化学试剂有限公司。 实验用水为超纯水。
实验仪器: DK-600S 三用恒温水箱(上海精宏实验设备有限公司); pHS-25 精密 pH 计(上海伟业仪器厂); SCS-24 温控培养摇床(上海市离心机械研究所有限公司); DZF-6050 真空干燥箱(上海精宏实验设备有限公司); X 射线衍射(XRD)仪, XRD-6100 型(岛津企业管理(中国)有限公司); 傅里叶变换红外光谱(FTIR)仪,TENSOR 27 型(德国 Bruker 公司); 扫描电子显微镜 (SEM), S4800 型 (日 本 日 立 公 司);ASAP2460 型比表面积及微孔物理吸附仪(美国麦克仪器公司); 离子色谱(IC)仪, 930 型(瑞士万通)。
1.2 HA 的合成
称取0.985 g Ca (NO3)2·4H2O 置于100 mL烧杯底部, 称取 0.507g (NH4)3PO4·3H2O 置于25 mL 烧杯底部, 保持[Ca]/[P]物质的量比为1.67。 将 25 mL 烧杯放置于 100 mL 烧杯中。 用恒压漏斗将100 mL 超纯水(用稀氨水调节pH =10.50)缓慢滴入上述大小烧杯中。 在三用恒温水箱中37℃下静置 3 ~15 d。 样品经抽滤后, 用超纯水、 无水乙醇分别清洗3 次, 50℃的真空干燥箱干燥24 h。
1.3 吸附实验
在50mL 不同浓度的含氟溶液中分别加入一定量的HA, 置于30℃温控培养摇床中振荡24 h, 采用离子色谱法测定除氟率。 除氟率(η) 和吸附量(Qe)计算方法如下:

式(1)、 式(2)中: C0为 HA 吸附前 F-的浓度,mg·L-1; Ce为 HA 吸附后 F-的浓度, mg·L-1。Qe为吸附量, mg·g-1; V 为含氟溶液的体积, L;m 为吸附剂(HA)的质量, g。
为检测共存阴离子的影响, 配置1 g·L-1的Na3PO4、 Na2SO4、 NaNO3、 Na2CO3和 NaCl 溶液,分别取一定量上述溶液加入5 mL 100 mg·L-1的F-溶液中, 定容至 50 mL, 得到含有 30~100 ppm的不同共存阴离子的10 mg·L-1的 F-溶液。 在50 mL 上述共存阴离子溶液中, 各加入0.020 g合成时间为5 d 的 HA, 在30℃下振荡6 h 后, 采用离子色谱测定除氟率。
1.4 表征分析
XRD: Kα 射线, Cu 靶, 管电流 30 mA, 管电压40kV, 扫描步长0.02°, 扫描范围20°~55°。
FTIR: 吸收精度0.07%T, 速度40 张光谱/秒, 波长范围 4 000 ~400 cm-1, 波数精度 0.005 cm-1。
SEM: 喷金处理, 电压 5 kV, 放大倍数 5 ~200 k。
比表面积: 77 K, 液氮为吸附质, BET 法计算比表面积。
IC: 取吸附后的上清液, 用 0.22 μm 过滤头过滤后进行测试。
2 结果与讨论
2.1 HA 结构分析
图1 是 HA 的 XRD 表征结果, 所有样品都在 2θ = 25.88°、 31.77°、 32.11°处出现 (002)(211)(112)晶面的衍射峰(PDF No.09-0432),并且没有其他杂峰, 说明合成的样品均为HA。其中合成时间为5 d 的样品主衍特征峰比较宽,说明其结晶度较低, 晶体的尺寸较小[7]。

图1 不同合成时间制备的HA 的XRD 图
图 2 是 HA 的 FTIR 图, 从中可看出, 在473、 566、 603、 963 和 1 024 cm-1处出现 PO3-4的特征峰, 在3 574 和 631 cm-1处出现 OH-的吸收峰, 873 cm-1处出现了 CO32-的吸收峰。 出现CO32-吸收峰可能是空气中的CO2溶入反应体系造成的[8]。 其中, 合成时间为 5 d 的样品, 特征峰比较弱和宽, 与XRD 结果相符。
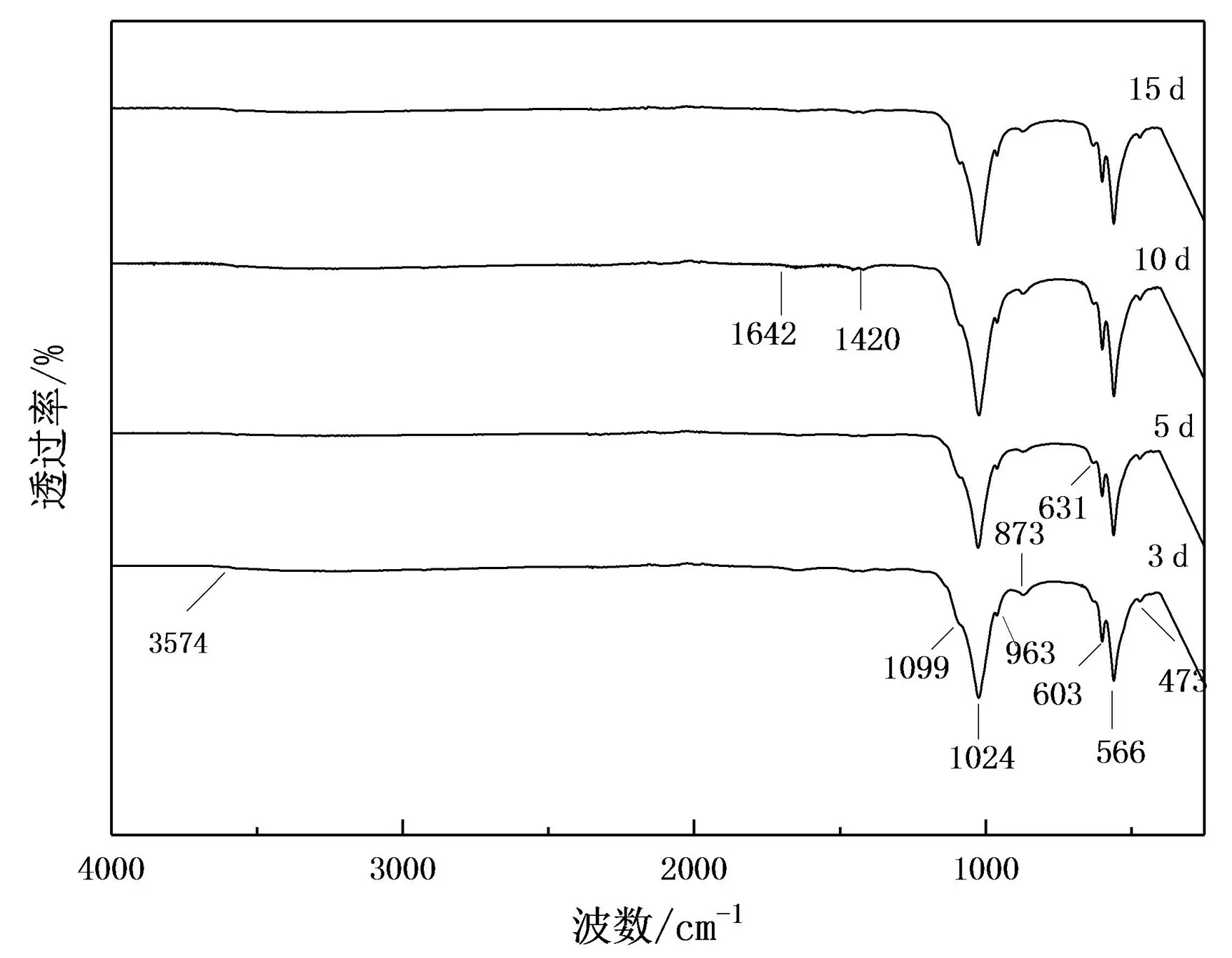
图2 不同合成时间制备的HA 的FTIR 图
图3 是不同合成时间制备的HA 的形貌图。样品均为粒状和棒状, 表面粗糙。 其中合成时间为 3 d 的 HA, 以棒状为主, 棒长 150 nm 左右,见图3(a); 合成时间为5d 的HA, 以粒状为主,粒径 20~50 nm, 表面最为粗糙, 见图 3(b); 合成时间为 10 和 15 d 的 HA, 以棒状为主, 棒长100~150 nm, 表面粗糙, 但棒之间的团聚较为严重, 见图 3(c)、 (d)。

图3 不同合成时间制备的HA 的SEM 图
不同合成时间制备的HA 的N2吸附-脱附曲线见图4。 由图4 可知, 所有样品的 N2吸附-脱附曲线都为II 型等温线, 具有无限制的单层-多层吸附特征; 且曲线均具有H3 型滞后环, 在高P/P0处未出现极限值, 说明样品具有平板状颗粒堆积而成的斜孔[9], 这与SEM 的结果相符。由图5 可知, 合成时间为5 d 的HA 由于样品晶粒较小, 表面较为粗糙, 所以比表面积最大, 为43.22 m2·g-1; 合成时间增加到 10、 15 d, HA的比表面积降低到 24.51、 19.60 m2·g-1。 这可能是由于合成时间为5 d 的样品晶粒较小, 表面较为粗糙, 所以比表面积比较大。

图4 不同合成时间制备的HA 的N2 吸附-脱附曲线

图5 HA 合成时间与比表面积的关系图
2.2 HA 除氟性能及机理
2.2.1 HA 合成时间对其除氟性能的影响
取不同合成时间制备的HA 各0.020 g, 分别置于50 mL 10 mg·L-1NaF 溶液中吸附6 h,HA 除氟率如图6 所示。 合成时间为5 d 的HA 除氟率最高, 为76.74 %。 除氟率随合成时间变化的趋势与比表面积的一致。

图6 HA 合成时/间对HA 除氟率的影响
2.2.2 除氟机理讨论
图7 为吸附前后样品(HA 合成时间为5 d)的XRD 图, 从中可以看出, 吸附前后样品都表现出磷灰石的特征衍射峰。 但吸附过程中F-进入HA 的晶格中, 形成了氟磷灰石(FHA, JCPDS 15-0876)。 由于氟替代羟基使得其晶胞参数a 值从0.9418nm 减小到 0.936 8 nm, c 值从 0.688 4 nm 增加到0.6885 nm。 a 值减小引起晶面间距d 减小,导致吸附后HA 的(211)(300)(202)等峰向右移动; c 值增大引起晶面间距d 增大, 导致吸附后HA 的(002)峰向左移动。 而且F-的进入使得特征峰明显变强变尖锐, 晶相更稳定[10]。 说明HA吸附F-过程中, 部分F-替换OH-的位置。 从吸附前后的 SEM 图(图8)也可以看出, 吸附前后, 粒子大小基本不变; 但是吸附后变得更为立体, 而且表面的葡萄状凸起更为细腻且明晰(图8(b)), 结晶度增加。 与吸附前后XRD 结果一样。

图7 吸附前后样品的XRD 图

图8 吸附前后样品的SEM 图
图9 和图10 为吸附前后样品的能谱图, 从中可以看出吸附后的样品中出现氟峰, F-均匀地分布在HA 中, 与XRD 结果相符。

图9 吸附前样品的能谱图

图10 吸附后样品的能谱图
2.3 除氟条件对HA 除氟性能的影响
2.3.1 吸附时间对HA 除氟性能的影响
在50 mL 10 mg·L-1的 NaF 溶液中加入0.020 g 的HA(合成时间5 d), 设置吸附时间为20 min~36 h, 除氟率如图 11 所示。 当吸附时间小于3 h 时, 除氟率随吸附时间的增长而急剧升高, 3 h 时达到 72.50%; 当吸附时间为 3 ~24 h时, 除氟率随吸附时间的增长而逐渐升高, 24 h时达到86.08%; 当吸附时间大于24 h 时, 除氟率趋于平稳。 推测是F-通过与OH-的交换作用,占据了HA 的表面活性中心位置, 24 h 时达到平衡, 之后除氟率基本稳定。

图11 吸附时间对HA 除氟率的影响
HA 吸附F-的准一级模型计算结果为: 溶液达到吸附平衡时吸附剂的吸附量Qe=7.899 5 mg·g-1, 准一级速率常数 K1= 0.001 8 min-1,方差R2=0.934 3; 准二级模型计算结果为: 平衡吸附量Qe=23.310 0 mg·g-1, 准二级速率常数[11]K2= 0.000 9 g·mg-1·min-1, 方差 R2=0.998 2。 其中, 准二级吸附动力学方程的R2>0.99, 能更好地拟合吸附过程。
准一级吸附动力学方程:

准二级吸附动力学方程:

式(3)、 式(4)中:Qt为t 时刻吸附剂的吸附量,mg·g-1。
2.3.2 投加量对HA 除氟性能的影响
称取0.005~0.050 g 合成时间为5 d 的 HA,分别投入50 mL 10 mg·L-1的 NaF 溶液中, 30℃振荡24 h, 测定除氟率。 从图 12 可以看出, 当HA 投加量小于0.020 g 时, 除氟率随投加量的增加而急剧升高; 当投加量为0.020 ~0.040 g时, 除氟率随投加量的增加而逐渐升高; 当投加量大于 0.040 g 时, 除氟率趋于平稳。 最优的HA 投加量为0.040 g, 除氟率可达99.26%。
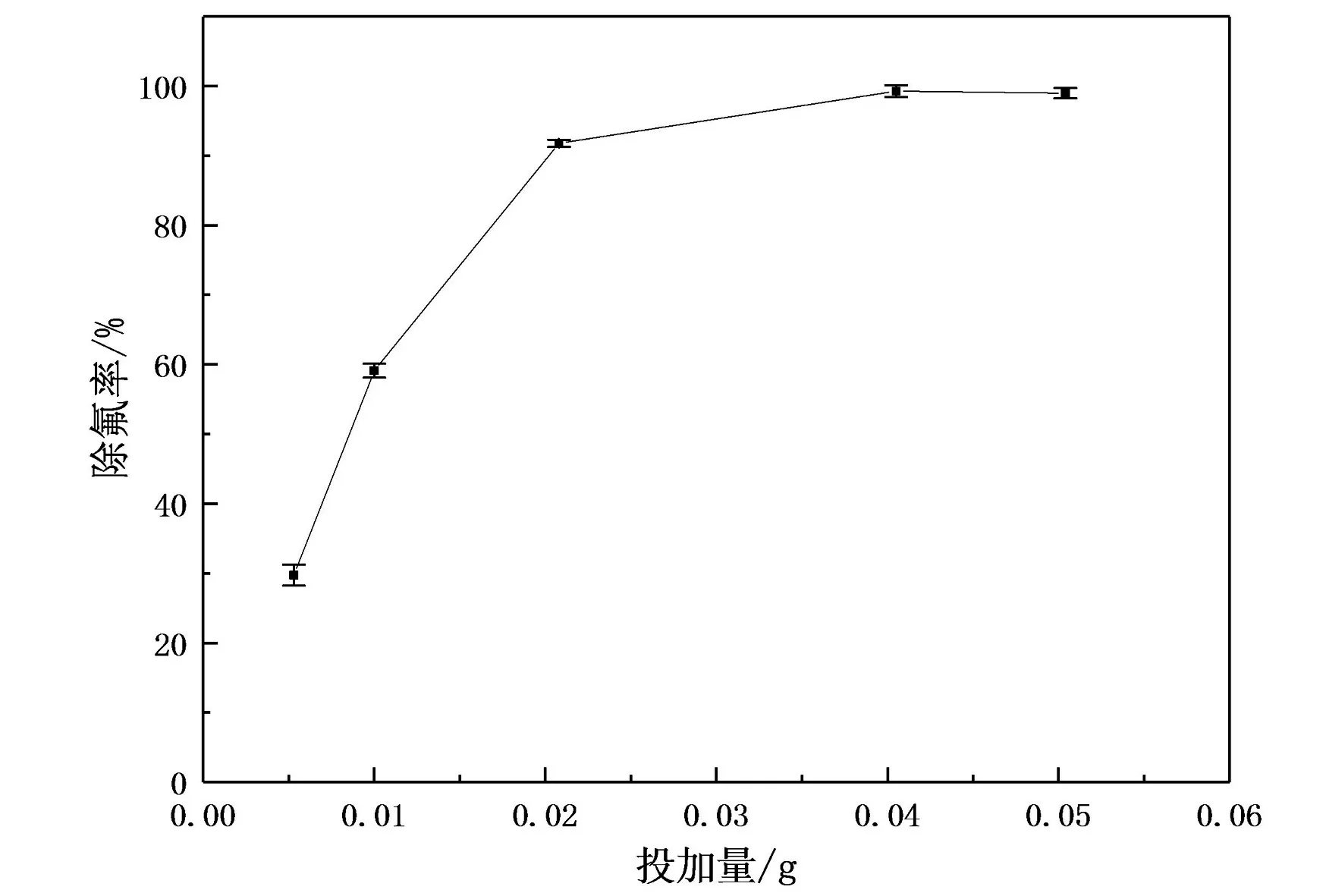
图12 HA 投加量对除氟率的影响
2.3.3 溶液pH 值对HA 除氟性能的影响
分别调节50 mL 10 mg·L-1NaF 溶液的pH值为 5、 6、 7、 8、 9、 10、 11, 各自投加 0.040 g的HA(合成时间为5 d), 30℃下振荡24 h, 测定除氟率, 结果见图13。 随着 pH 值的上升, 除氟率先上升后下降, 当 pH 值等 7 时, 除氟率最高, 达到99.26%。 在弱酸性条件下, H+的存在使HA 和F-之间的静电吸引力减弱, 使得除氟率变低; 而在弱碱性条件下, OH-会与F-竞争,

图13 溶液pH 值对HA 除氟率的影响
使得F-比较难进入HA 的表面活性中心位置[12],导致除氟率降低。
2.3.4 吸附等温线
分别配制 50 mL 10 ~ 300 mg·L-1的 NaF 溶液, 各自加入0.040 g 的HA(合成时间为5 d),30℃振荡 24 h, HA 吸附量如图 14 所示。 从图14 可以看出, 随着 F-浓度的上升, HA 吸附量先急剧升高后逐渐升高, 当 F-浓度达到 200 mg·L-1时, HA 达到了饱和吸附, 此时吸附量为 72.88 mg·g-1; 若 F-浓度继续升高, 吸附量基本保持不变。 对吸附曲线采用朗缪尔(Langmuir)和弗罗因德利希(Freundlich)吸附等温式进行拟合, 拟合曲线见图14。 Langmuir 吸附等温式拟合结果为 Qm= 71.667 1 mg·g-1, KL=0.117 6 L·m-1, R2= 0.8220; Freundlich 吸附等温式拟合结果为: KF= 21.466 4 L·g-1, 1/n =0.232 7, R2= 0.980 3。 对比吸附等温式的相关系数 R2, 显然 HA 吸附 F-的过程更符合Freundlich 吸附等温模型, 这表明吸附是多分子层吸附。 且1/n 值小于1, 说明样品易于吸附F-。

图14 F-浓度对HA 吸附量的影响
Langmuir 吸附等温式:
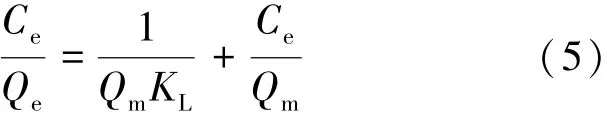
Freundlich 吸附等温式:

式(5)、 式(6)中: Ce为吸附平衡时溶质的浓度,mg·L-1; Qm为 HA 的饱和吸附量, mg·g-1; KL、KF为吸附常数; n 为描述吸附强度的常数。
2.3.5 共存阴离子的影响
含有 30、 50、 100 ppm 不同阴离子的 50 mL 10 mg·L-1NaF 溶液中, 分别加入 0.020 g 的 HA(合成时间为5 d), 30℃下振荡6 h, 测试共存阴离子对 HA 除氟性能的影响。 如图 15 所示,SO42-或NO3-的存在提高了HA 的除氟率, 这可能是因为这两种离子提高了溶液的离子强度, 而使除氟率升高; PO43-或CO32-的存在降低了HA存在竞争性吸附, 从而导致除氟率降低; 而Cl-对HA 除氟率几乎没有影响。

图15 共存阴离子对HA 除氟率的影响
2.4 不同方法合成HA 的除氟性能比较
将本文采用矿化法合成的HA(合成时间为5 d)与文献中采用其他合成方法制备的HA 的除氟率、 吸附量和饱和吸附量进行比较, 结果见表1。 从表1 可以看出, 与其他方法合成的 HA 相比, 本文方法合成的HA 除氟效果更好。 本文方法合成的HA 尺寸较小, 属于纳米级别, 但比表面积不算高, 其良好的除氟效果可能归功于吸附过程中的F-与OH-的离子交换。

表1 各种方法合成的HA 及其除氟率和吸附量
3 结论
(1)采用矿化法合成棒状和粒状的纳米HA。合成时间5d 得到的HA 比表面积达43.22 m2·g-1,除氟效果最佳。 吸附过程中F-进入HA 的晶格中, 形成氟磷灰石。
(2)通过单因素实验得出: 当HA 投加量0.040 g、 吸附时间 24 h、 pH = 7 时, HA 的除氟效率最好, 除氟率高达99.26%。 HA 的饱和吸附量可达72.88 mg·g-1。 与其他合成方法相比,矿化法合成HA 的除氟效果更好。
(3)HA 吸附F-过程符合准二级动力学方程和Freundlich 吸附等温模型。

