NbOx掺杂对Pt/TiO2催化燃烧氯乙烯的促进作用
高奕吟,付睿,王丽,郭耘
(华东理工大学化学与分子工程学院,工业 催化所,上海 200237)
引 言
含氯挥发性有机化合物(CVOCs)是常用于化工生产的原料之一,具有较高的化学稳定性[1]。氯乙烯(VC)作为CVOCs 的一种,是合成聚氯乙烯(PVC)的单体[2],它通常以工业废气的形式排放于自然界。由于其难降解性,会对环境造成持久性的污染,且部分物质还具有对生物的毒害作用,对人类的健康造成了威胁[3]。我国于2016年颁布的《烧碱、聚氯乙烯工业污染物排放标准》(GB 15581—2016)[4]中对氯乙烯(VC)严格规定了排放浓度限值,要求相关企业在大气中的排放量不可超过10 mg∕m3。
催化燃烧法是利用催化剂将CVOCs 氧化生成CO2、H2O 和HCl 的方法,具有能耗低、绿色环保等特点[5]。目前常用于CVOCs 氧化的催化剂有过渡金属氧化物催化剂和负载型贵金属催化剂[1]。Wang 等[6]研究发现Co(0.7)CeOx在225℃对于氯乙烯的氧化速率为1.52×10-5mol∕(g·s·m2),在281℃转化90%的氯乙烯时伴有16 μl∕L 二氯乙烷与55 μl∕L 三氯甲烷等多氯副产物。Hua 等[7]测得Sn0.6Mn0.4Ox的氯乙烯催化氧化的活化能降低至49.8 kJ∕mol,T90(转化率90%对应的温度)下生成38 μl∕L 三氯甲烷与6.8 μl∕L 四氯甲烷等含氯有机副产物。Wang 等[8]所制备的La0.5Sr0.5MnO-H 可在300℃将VC 完全氧化,但三氯甲烷、三氯乙烯等副产物在T90下的生成量约为50 μl∕L。
负载型贵金属催化剂,通常比过渡金属氧化物催化剂具有更高的反应活性[9]。目前关于氯乙烯氧化的贵金属基催化剂的研究主要有Ru 基与Pt 基催化剂。据报道Ru∕CoPO-MCF[10]实现了在高空速(48000 ml∕(g·h))、温度为313℃达到氯乙烯氧化的T90,但在该温度下产生以二氯甲烷与三氯甲烷为主的含氯副产物,并且浓度为33.7 μl∕L。对于负载Pt基催化剂,研究重点关注引入助剂或改变载体以提高催化剂的活性、减少尾气中有机多氯副产物的生成。方田等[11]所制备的Pt∕Mn0.7Zr0.3Ox在282℃转化90%的VC,并使含氯副产物的总浓度低于19.9 μl∕L。Zhang 等[12]在Pt∕CeO2催化剂上引入WOx,发现氯乙烯燃烧的活化能仅39.6 kJ∕mol,且顺-1,2-二氯乙烯与反-1,2-二氯乙烯在T90下总量减少至14 μl∕L。
NbOx是一种酸性氧化物,可作为催化剂载体。Nb2O5为载体时,可以促进活性组分在表面以高分散形式存在[13]。NbOx更多是作为助剂应用于不同催化剂体系和反应中。NbOx引入可使得催化剂的总酸量较未掺杂氧化物表面的酸量提高5.5 倍[14]。而对于负载贵金属体系而言,Nb2O5的引入可促进贵金属(Pt)与载体之间的相互作用从而实现在低温下还原[15],并提高贵金属分散度[15-16]。此外,Nb2O5还可提高催化剂的抗硫性能,如SO2仅导致Mn-Nb∕TiO2的反应性能下降8%,远低于其对Mn∕TiO2的影响(25%)[17]。
综上可知,NbOx的引入在提高催化剂酸性的同时有利于化学吸附氧的生成[14,17-19]。本文以Pt∕TiO2为研究对象,通过浸渍法引入NbOx制备了不同Nb∕Ti(摩尔比)的Pt∕Nbx∕TiO2催化剂,考察了NbOx的引入对氯乙烯催化燃烧性能的影响。采用X 射线衍射(XRD)、X 射线光电子能谱(XPS)、程序升温技术(NH3-TPD、H2-TPR)、吡啶红外(Py-FT-IR)等手段表征了NbOx的存在对于Pt∕TiO2物化性质的影响。此外,结合反应性能数据与催化剂表征结果,探讨了NbOx对Pt∕TiO2的VC催化燃烧促进机制。
1 实验部分
1.1 试剂
TiO2(P25,AR,德国赢创德固赛),铌酸铵草酸盐水合物(AR,麦克林生化科技有限公司),氯铂酸(AR,国药集团化学试剂有限公司)。
1.2 仪器
质谱仪(HPR-20,英国海德仪器有限公司),气相色谱仪(A61,常州磐诺仪器有限公司),氢气程序升温还原装置(天津市鹏翔科技有限公司),红外光谱仪(TENSOR 27,德国布鲁克仪器有限公司)。
1.3 催化剂的制备
称取一定量的TiO2与铌酸铵草酸盐水合物[Nb∕Ti(摩尔比)分别为0,0.015,0.03,0.09,0.18],溶于水后于55℃下旋蒸,110℃下干燥12 h,500℃焙烧3 h得到Nbx∕TiO2载体。称取一定量的氯铂酸溶液以等体积浸渍法负载于上述载体后,80℃干燥12 h,400℃焙烧4 h得到Pt∕Nbx∕TiO2。
1.4 催化剂的表征
1.4.1 X 射线衍射 采用Bruke D8Power X-ray Diffraction 型X 射线衍射仪获取样品的XRD 谱图。测试的条件为:以Cu Kα辐射作为入射光,以6(°)∕min在10°~80°进行扫描。
1.4.2 X 射线光电子能谱 采用ESCAL-AB 250Xi
型电子能谱仪检测催化剂表面元素组成与原子价态。其测试条件为:以单色Al Kα(E=1486.6 eV)作为激发光源,功率为150 W。以C 1s 结合能284.8 eV作为能量标准进行校正。
1.4.3 氢气程序升温还原 采用TP-5080 装置对样品进行氢气程序升温还原(H2-TPR)的测试。其测试条件为:称取100 mg 样品置于U 形石英反应管中,通入流速为40 ml∕min 的5% H2∕N2混合气,以10℃∕min 的升温速率由10℃升温至600℃,通过热导检测器(TCD)检测反应管出口处H2的浓度变化。
1.4.4 氨气程序升温脱附 采用与氢气程序升温还原装置相同的装置,将200 mg 样品在400℃Ar 气预处理后,降温至90℃,通入10.0%(体积分数)NH3∕Ar 混合气。吸附饱和后,在Ar 气氛中,以10℃∕min的升温速率升至400℃,采用热导检测器(TCD)记录反应管出口处NH3的浓度变化。
1.4.5 吡啶红外 采用BRUKER TENSOR 27 型红外光谱仪对样品进行吡啶红外(Py-FT-IR)测试。其测试条件为:称取100 mg 样品在400℃Ar 中预处理1 h,冷却至室温后,通入吡啶吸附饱和后抽真空以去除物理吸附的吡啶;然后在200℃采集红外信号。
1.4.6 Cl2选择性 配制一定浓度的NaOH 溶液吸收反应后的尾气,用N,N-二乙基对苯二胺(DPD)-硫酸亚铁铵(FAS)滴定法滴定副产物中Cl2的体积分数。
1.5 催化剂性能评价
采用固定床微型反应器评价催化剂活性并通过色谱在线检测含氯副产物体积分数。测试中氯乙烯含量为1000 μl∕L,空气作为平衡气,质量空速为30000 ml∕(g·h)。催化剂评价过程采用程序升温方式,以20℃∕min速率进行程序升温,达到设定温度后在该温度点保持40 min,催化剂稳定后进行取样分析。
2 结果与讨论
2.1 氯乙烯催化燃烧性能
2.1.1 NbOx掺杂对于Pt∕TiO2催化燃烧氯乙烯的影响 不同Nb∕Ti 摩尔比的Pt∕Nbx∕TiO2催化剂对氯乙烯的反应活性曲线如图1 所示。Pt∕TiO2催化剂对氯乙烯的氧化性能较差,在315℃可转化90%的氯乙烯。NbOx的引入显著提高了Pt∕TiO2催化剂的催化反应性能,氯乙烯的氧化活性随着NbOx的引入量呈现先增加后降低的趋势,其中Pt∕Nb0.09∕TiO2表现出最佳的反应活性,T90仅为246℃;与Pt∕TiO2的T90相比,向低温偏移了69℃。
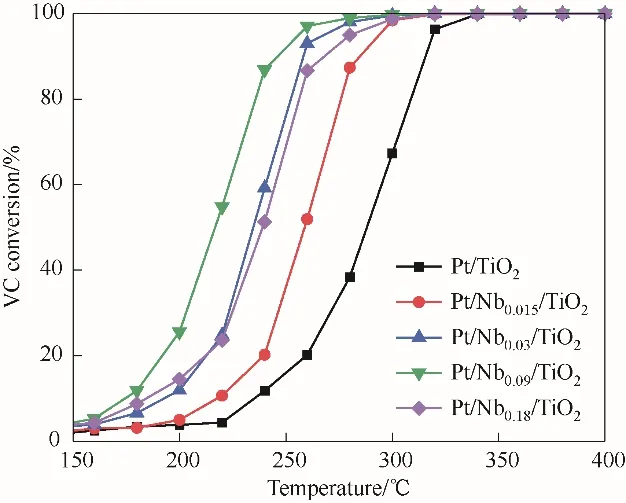
图1 Pt∕Nbx∕TiO2(x=0,0.015~0.18)对氯乙烯的催化燃烧活性Fig.1 The activity curves of Pt∕Nbx∕TiO2(x=0,0.015—0.18)for vinyl chloride catalytic combustion
2.1.2 副产物的分析 Pt∕Nbx∕TiO2催化燃烧过程中产生的含氯副产物种类及其含量如图2所示。不同催化剂在氧化氯乙烯的过程中生成的含氯有机副产物主要为顺-1,2-二氯乙烯和1,2-二氯乙烷。对于Pt∕TiO2而言,副产物主要以1,2-二氯乙烷为主;但是其不同含氯副产物在315℃(T90)下的总含量不高于0.3 μl∕L。方田等[11]所制备的Pt∕MnZrOx在相同转化率(90%)的温度下产生了总含量为19.9 μl∕L的多氯副产物。因此,Pt∕TiO2可有效抑制含氯副产物的生成。
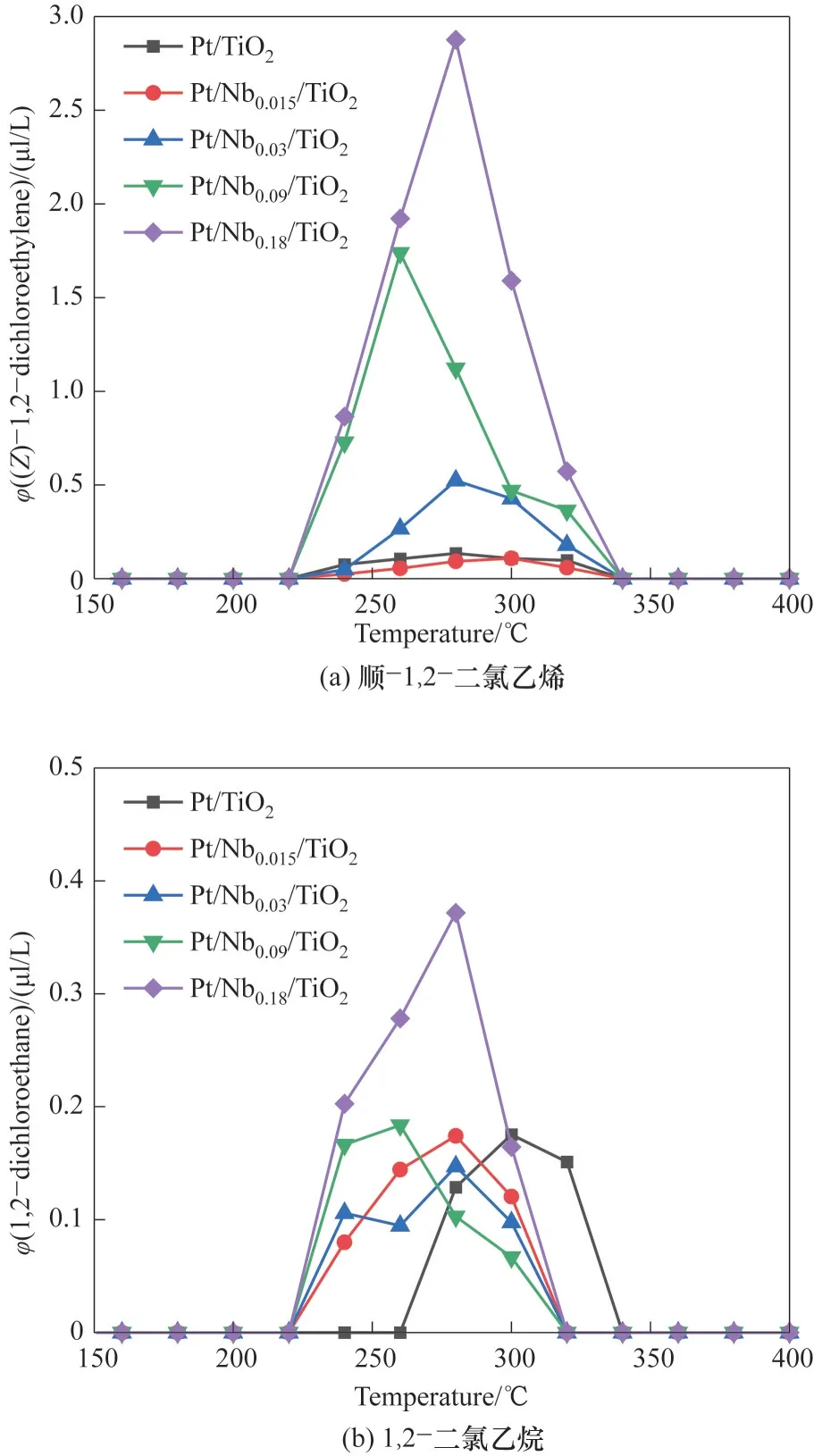
图2 Pt∕Nbx∕TiO2(x=0,0.015~0.18)含氯副产物含量与温度的关系Fig.2 The concentration profiles of chloric by-products over Pt∕Nbx∕TiO2(x=0,0.015—0.18)
由副产物的检测结果发现,NbOx的引入改变了含氯有机副产物的分布。当引入Nb∕Ti 低于0.09时,对于1,2-二氯乙烷生成浓度影响不显著;而Nb∕Ti 增加到0.18 则有利于1,2-二氯乙烷生成。相反,NbOx的引入会使得顺-1,2-二氯乙烯增加呈现线性相关的趋势。虽然Pt∕Nb0.18∕TiO2用于氯乙烯催化燃烧增加了副产物的浓度,但是T90下总含量低于3 μl∕L。含氯副产物的增多与催化剂的氧化还原能力相关。Wang 等[20]认为较高的氧化还原性能有利于氯自由基的产生,使氢原子更易被氯原子取代而产生多氯副产物。
2.1.3 Cl2的选择性 通过N,N-二乙基对苯二胺(DPD)-硫酸亚铁铵(FAS)滴定法对Pt∕Nbx∕TiO2催化燃烧氯乙烯的尾气中产生的Cl2进行标定[21],以确定催化剂组成对于Cl2生成的影响,结果如图3 所示。当反应温度超过320℃后,在催化剂上可以检测到Cl2的生成,且Cl2的生成量随着温度的升高而增加。通过对比Cl2的选择性发现,Pt∕TiO2对于Cl2的选择性较低,即使在400℃,对于Cl2的选择性仍然低于2%。值得关注的是,NbOx的引入会导致尾气中Cl2的选择性升高,且随着NbOx含量的增加呈现增加的趋势。其原因可解释为NbOx的引入虽然促进了氯乙烯的催化氧化,使其有利于转化为HCl,但同时在高温下也会促进Deacon 反应的发生,使部分HCl 氧化为Cl2[22]。
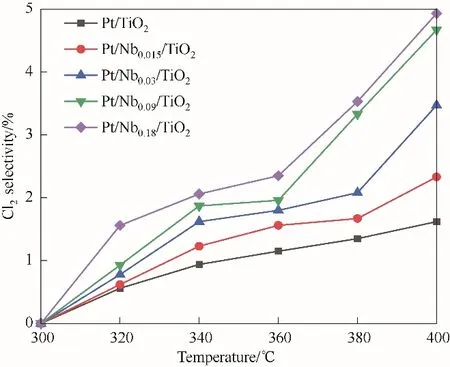
图3 Pt∕Nbx∕TiO2(x=0,0.015~0.18)催化剂的Cl2选择性Fig.3 The Cl2 selectivity of Pt∕Nbx∕TiO2(x=0,0.015—0.18)catalysts
2.1.4 稳定性测试 催化剂的稳定性是性能评价
的另一重要指标,因此对于Pt∕Nb0.09∕TiO2,分别在转化率达到90%和100%所对应的温度(T90与T100)下进行稳定性测试,其结果如图4 所示。无论是在T90(246℃)还是T100(292℃),Pt∕Nb0.09∕TiO2都可稳定运行70 h,表明该催化剂具有良好的稳定性。
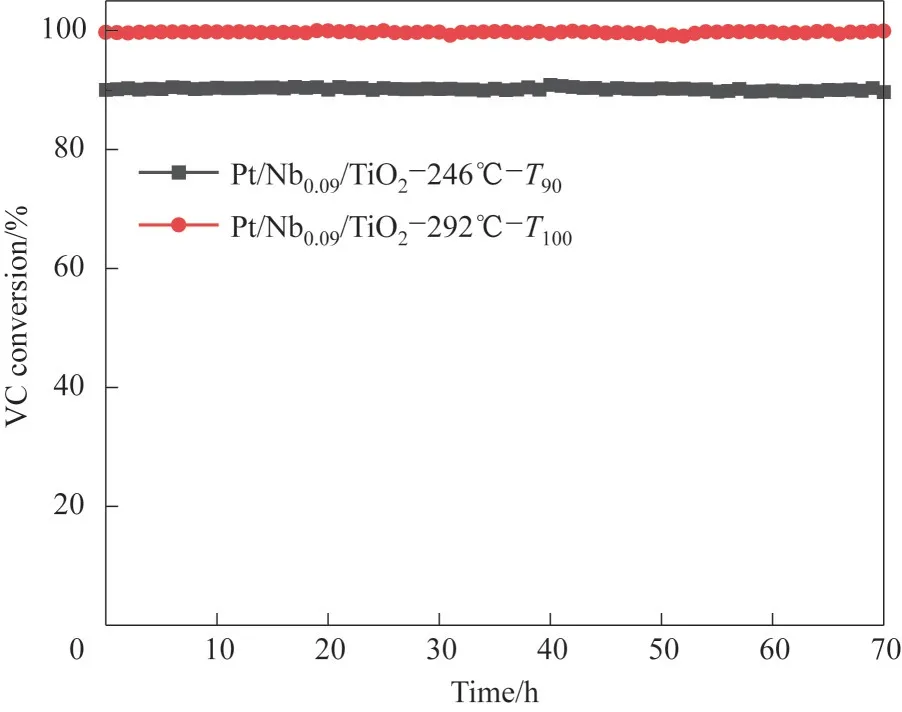
图4 Pt∕Nb0.09∕TiO2的稳定性Fig.4 The stability of Pt∕Nbx∕TiO2
2.2 催化剂表征
2.2.1 N2吸附-脱附和催化剂组成 负载型Pt 基催化剂的比表面积结果如表1 所示。Pt∕TiO2的比表面积为45 m2∕g;NbOx的引入对于催化剂的比表面积影响不显著。通过ICP-AES 测得的Pt 实际负载量在0.90%~0.98%,Nb的负载量与理论投料比相近。
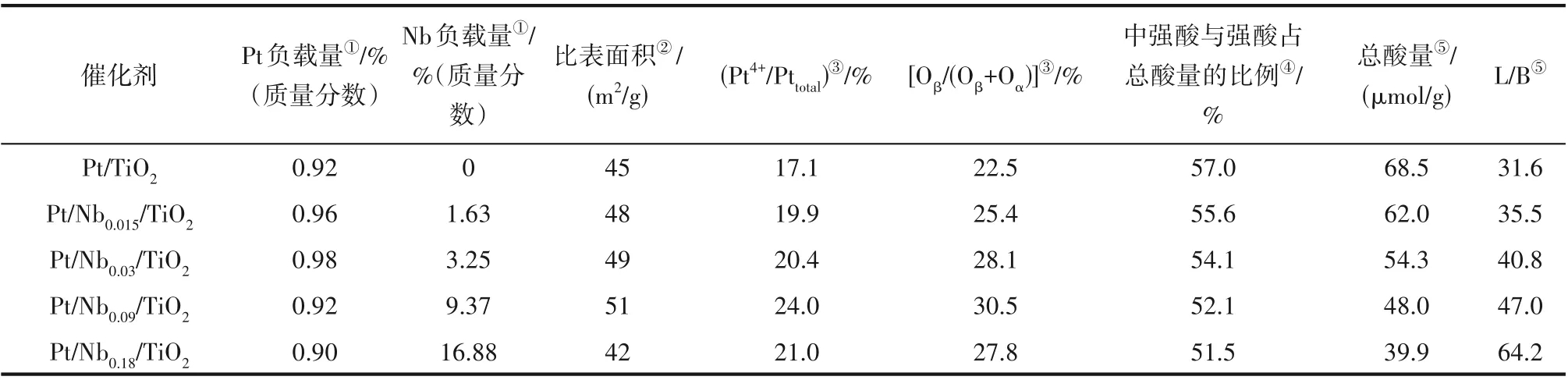
表1 Pt/Nbx/TiO2(x=0,0.015~0.18)的物理结构参数,XPS、NH3-TPD和吡啶红外吸附结果Table 1 The physical structure parameters,the data of XPS,NH3-TPD and Py-FT IR of Pt/Nbx/TiO2
2.2.2 XRD 表征 催化剂的XRD 谱图如图5 所示。其中25.3°、48.1°、62.7°(ICDD-PDF#21-1272)为TiO2锐钛矿相的特征衍射峰[23],而27.5°、41.3°、56.7°(ICDD-PDF# 21-1276)为TiO2金红石相的特征衍射峰[23]。当Nb∕Ti 为0.18,可在22.7°、28.6°处观察到Nb2O5的特征衍射峰[15]。这也表明引入NbOx的量低于9.36%,可高度分散在载体表面。此外,在催化剂表面未检测到与Pt 相关特征衍射峰,表明其在催化剂表面呈高度分散的状态或者低于XRD检测限。
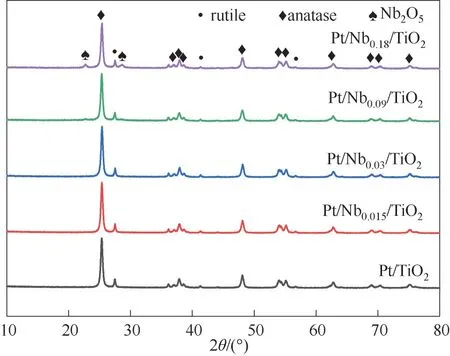
图5 Pt∕Nbx∕TiO2(x=0,0.015~0.18)的XRD谱图Fig.5 XRD patterns of Pt∕Nbx∕TiO2(x=0,0.015—0.18)
2.2.3 XPS 谱图 为进一步考察NbOx的引入对Pt∕TiO2表面组成以及元素价态的影响,对催化剂进行了XPS 表征,Pt∕Nbx∕TiO2的Pt 4f、Ti 2p、Nb 3d 与O 1s谱图如图6所示。
图6(a)为Pt 4f 的XPS 谱图,结合能位于74.5 与72.6 eV 的特征峰归属于Pt4+和Pt2+[24]。所有催化剂均未检测到金属态Pt0的存在,表明Pt 主要以Pt2+形式存在。图6(b)为Ti 2p 的XPS 谱图。TiO2的Ti4+特征峰位于458.4 eV[25]。Pt∕TiO2的Ti4+峰位于458.2 eV,较TiO2向低结合能偏移,这是由于Pt 与TiO2之间存在相互作用,即Pt 通过Pt—O—Ti 键向Ti 转移电子所致[26]。图6(c)为Nb 3d 的XPS 谱图。将结合能位于207.2 和210.0 eV 的特征峰归属于Nb5+物种,表明催化剂中的Nb物种主要是以Nb5+形式存在[14]。图6(d)为O 1s 的XPS 谱图。将结合能位于530.3 eV的特征峰归属于晶格氧,标记为Oα,将结合能位于531.4 eV 的特征峰归属于化学吸附氧,标记为Oβ[27]。通过积分峰面积可获得Oβ∕(Oβ+Oα),结果见表1。对于CVOCs 氧化反应,Oβ比Oα具有更高的反应活性[28]。随着Nb∕T(i摩尔比)增加至0.09,Oβ∕(Oβ+Oα)增加到30.5%,表明NbOx的引入会促进化学吸附氧的生成[14,17-19];但当Nb∕T(i摩尔比)进一步增加至0.18 后,Oβ∕(Oβ+Oα)反而减小,这与多聚态NbOx在催化剂表面的形成有关[19]。

图6 Pt∕Nbx∕TiO2(x=0,0.015~0.18)的XPS谱图Fig.6 XPS spectra of Pt∕Nbx∕TiO2(x=0,0.015—0.18)
2.2.4 H2-TPR 表征 为进一步考察NbOx的引入对催化剂氧化还原性能的影响,对样品进行H2-TPR表征,结果如图7所示。
将位于150℃以下低温还原峰归属于PtOx还原为金属Pt,将位于250~400℃的高温还原峰归属于以Pt-TiOx界面位点的形式与载体TiO2相互作用的Pt物种的还原[29]。计算耗氢量时发现Pt的实际耗氢量远低于其理论耗氢量。El Assal 等[30]的研究认为Pt∕TiO2中仅有2%的Pt可被还原,而Hwang等[31]则认为Pt前体中PtOxCly的存在会抑制Pt的还原。
由图7发现Pt∕Nbx∕TiO2两种耗氢峰均随着Nb∕Ti(摩尔比)的提高而逐渐变大,表明NbOx的引入可促进Pt 物种的还原。Yang 等[32]对于Pt∕Nb∕WOx的研究也发现NbOx的引入可促进Pt物种的还原。
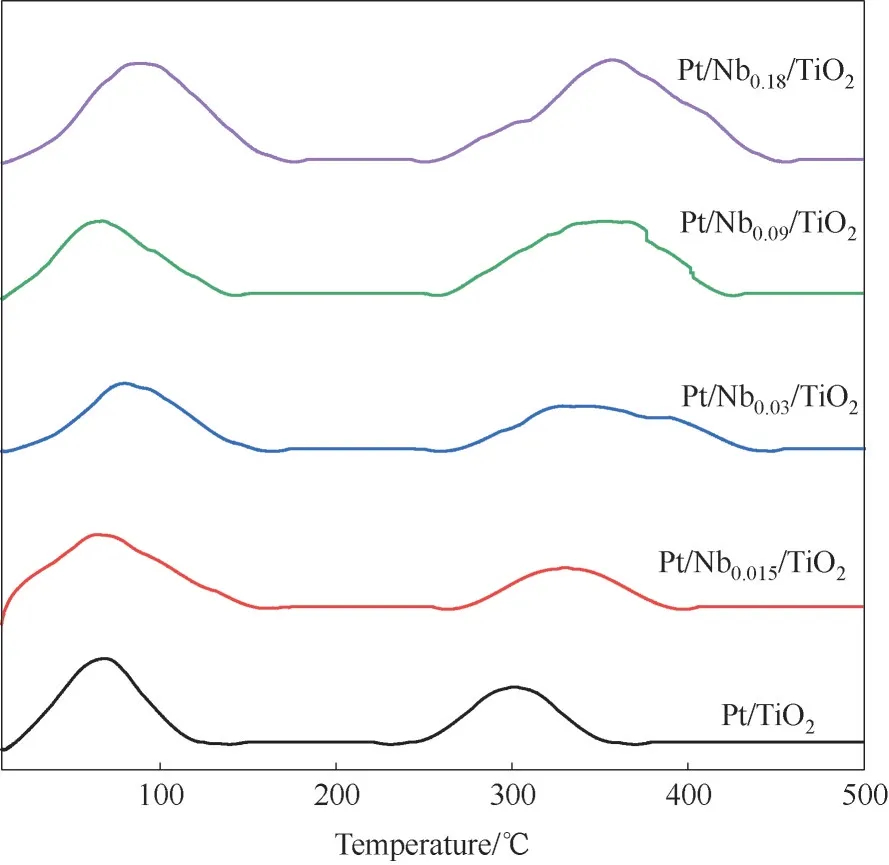
图7 Pt∕Nbx∕TiO2(x=0,0.015~0.18)的H2-TPR谱图Fig.7 H2-TPR profiles of Pt∕Nbx∕TiO2(x=0,0.015—0.18)
2.2.5 催化剂表面的酸量和酸分布 催化剂的酸性是影响催化燃烧氯乙烯性能的重要因素,具有较多酸量则有利于CVOCs 的吸附、活化与解离[33-34]。为探究NbOx的引入对Pt∕TiO2表面酸性的影响,对样品进行了NH3-TPD表征,结果如图8所示。
100~250℃、250~400℃、400~500℃的脱附峰分别归属于NH3在催化剂表面的弱酸、中强酸、强酸上的吸附[35]。由图8 可知,Pt∕TiO2表面具有丰富的酸中 心;而 进 一 步 对 比Pt∕Nbx∕TiO2和Pt∕TiO2的NH3-TPD 谱图,发现NbOx的引入并未减少催化剂表面酸中心的种类,但导致中强酸与强酸所占比例降低。通过吡啶红外结果获得催化剂表面的酸量,结果见表1。Pt∕TiO2催化剂表面的总酸量为68.5 μmol∕g,而NbOx的引入反而导致催化剂表面的总酸量降低。其中,Pt∕Nb0.18∕TiO2表面的总酸量降低到39.9 μmol∕g。Yang 等[36]的研究表明,TiO2的不同酸强度的酸量均高于Nb2O5,而Akizuki 等[37]对比商业TiO2与Nb2O5的NH3-TPD测试结果也得到相同的结论。
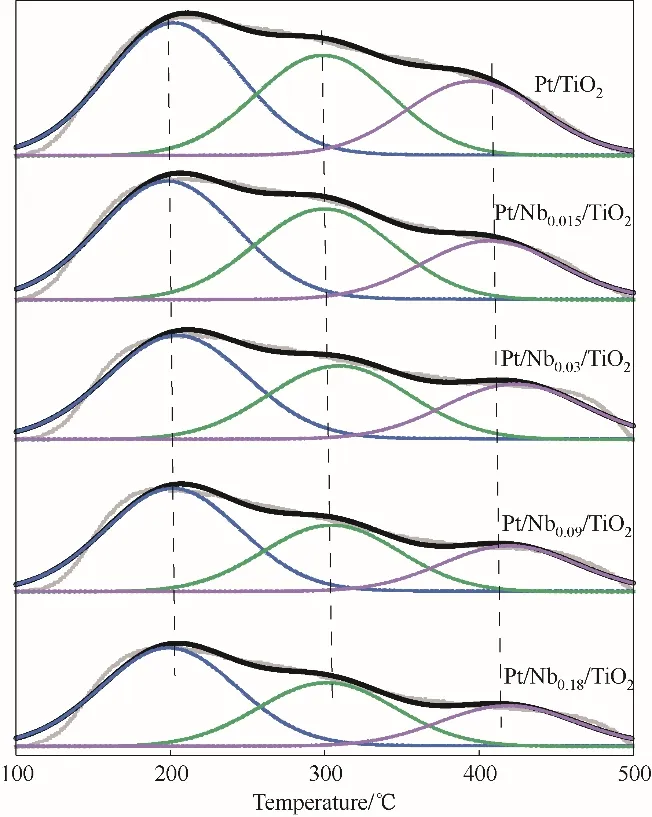
图8 Pt∕Nbx∕TiO2(x=0,0.015~0.18)的NH3-TPD谱图Fig.8 NH3-TPD profiles of Pt∕Nbx∕TiO2(x=0,0.015—0.18)
NbOx是一种常见的固体酸,其酸性与其含水量密切相关,因此高温焙烧会降低其含水量,从而显著 降 低NbOx的 酸 性。Morawa Eblagon 等[38]发 现600℃焙烧Nb2O5·nH2O 使得其酸量降低到20 μmol∕g。结合催化剂的焙烧温度(500℃)以及XRD 结果可知,弱酸性NbOx覆盖了具有较多酸中心(TiO2)而导致催化剂总酸量降低。
此外,吡啶红外表征(图9)亦可以获得NbOx的引入对催化剂表面Lewis(L)酸和Brönsted(B)酸分布的影响。1606、1445 cm-1处的峰归属于吡啶在L酸中心上的吸附,而1647、1543 cm-1处的峰归属于吡啶在B 酸中心上的吸附[39]。对峰面积进行积分可得到催化剂表面L 酸和B 酸量的比值(L∕B),结果见表1。
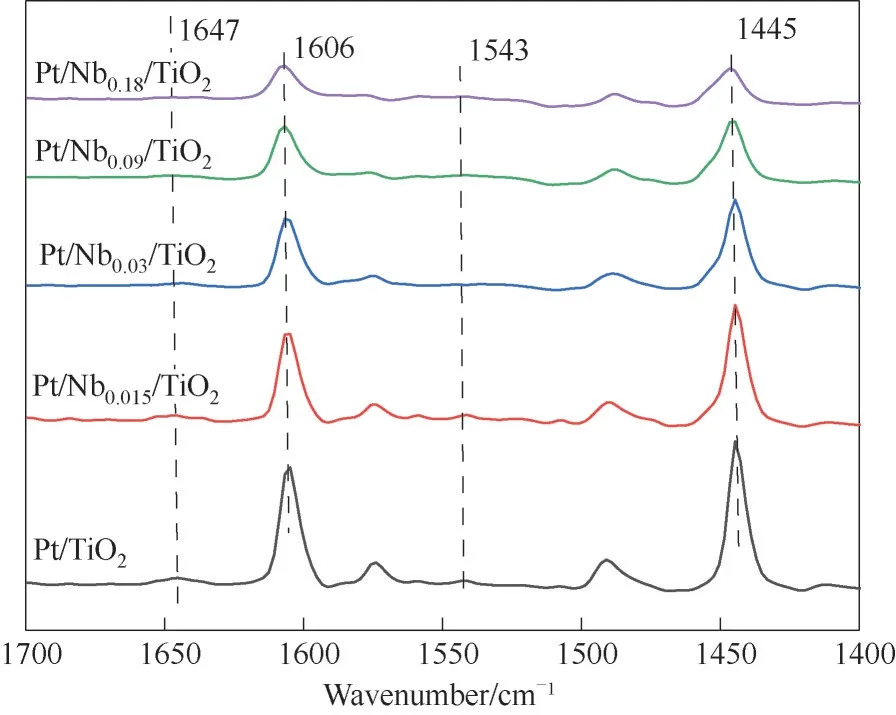
图9 Pt∕Nbx∕TiO2(x=0,0.015~0.18)的吡啶红外吸附谱图Fig.9 Py-FT-IR spectra of Pt∕Nbx∕TiO2(x=0,0.015—0.18)
由图9 可知,吡啶在Pt∕TiO2表面L 酸的吸附峰(1606、1445 cm-1)强度远高于其在B 酸(1647、1543 cm-1)吸附峰强度,表明Pt∕TiO2表面主要以L 酸为主。Pt∕TiO2表面L∕B 为31.6 的结果,进一步表明Pt∕TiO2表面主要以L 酸为主。NbOx的引入会降低催化剂表面的总酸量,从而减少了催化剂表面B 酸与L酸量。结合表1中催化剂表面L∕B 发现,表面L酸量受NbOx的影响尤为显著。Pt∕Nb0.18∕TiO2表面L 酸量较Pt∕TiO2减少了42%。
催化剂表面酸量增加有利于反应物分子(CVOCs)的吸附、活化与解离[33-34]。Pt∕TiO2表面具有丰富的酸中心,但是其T90反而高达315℃。虽然NbOx的引入不仅导致催化剂表面总酸量降低,并影响了表面L酸和B酸分布,但是使得T90向低温偏移,其中Pt∕Nb0.09∕TiO2的T90下降到246℃。这说明酸量和酸分布并不是决定催化剂反应性能的唯一因素。此外,分析NbOx引入对于催化剂的氧化还原性能以及Pt的化学状态的影响发现:NbOx引入促进了催化剂氧化还原性能提高以及高价Pt 的生成,这是由于NbOx增强了Pt 与TiO2之间的相互作用。结合上述分析可知:酸量和酸分布并不是决定催化剂反应性能的唯一因素;催化剂反应性能受催化剂酸量、氧化还原能力、Pt 的化学状态共同影响;提高催化剂的低温氧化还原性能则有利于提高催化剂对于氯乙烯的脱除性能。
3 结 论
(1)采用浸渍方法制备了负载不同NbOx含量的Pt∕Nbx∕TiO2催化剂,NbOx的引入使Pt∕TiO2对于氯乙烯催化燃烧性能提高,但其促进效果与NbOx的含量密切相关。Pt∕Nb0.09∕TiO2(Nb∕Ti 摩尔比为0.09)转化率为90%的温度为246℃。与Pt∕TiO2相比,达到相同转化率的温度降低69℃。
(2)NbOx增强了Pt 与载体(TiO2)之间的相互作用,从而使得表面高价态Pt 物种以及表面活性氧物种增加,并促进了催化剂的氧化还原能力提高。NbOx的引入改变了催化剂的表面总酸量以及表面酸分布。催化剂表面的总酸量随着Nb∕Ti 摩尔比的增加而降低,且对于L 酸的影响较B 酸显著。对于Pt∕Nbx∕TiO2的氯乙烯催化氧化反应,与催化剂表面的总酸量和酸分布相比,促进催化剂的低温氧化还原性更有利于反应性能的提高。

