液相色谱-质谱联用鉴定抗菌肽Cbf-14凝胶的有关物质
霍怡彤,徐柯卉,陆宇婷,马菱蔓,周长林,杭太俊,宋 敏*
(1中国药科大学药学院,南京 211198;2中国药科大学生命科学与技术学院,南京 211198)
随着抗生素的滥用,病原菌进化速度加快,多重耐药菌大量出现。近年来,抗菌肽(antimicrobial peptides,AMPs)被认为是现有抗生素最有潜力的替代品,与传统抗生素相比,AMPs 具有相对分子质量小、抗菌机制广、热稳定性好、毒性低等优点。由于其独特的抗菌机制和多样的生物活性,AMPs的研究和应用已成为生物制药领域的热点[1-2]。
Cbf-14 是一种由14 个氨基酸组成的阳离子抗菌肽,是根据天然抗菌肽cathelicidin-BF(BF-30)的序列利用生物信息学设计获得的多肽突变体[3-5]。其氨基酸序列为Arg-Leu-Leu-Arg-Lys-Phe-Phe-Arg-Lys-Leu-Lys-Lys-Ser-Val(RLLRKFFRKLKKSV),相对分子质量为1 819.33,等电点为12.31。Cbf-14具有抵抗耐药病原菌感染的作用,还可用于治疗真菌感染[5-6]。获得批准的专利制剂Cbf-14凝胶用于术后创面的护理及皮肤消毒处理,具有优异的杀菌活性,且无毒、无刺激。多肽药物的稳定性一直是备受关注的问题,其中的有关物质可能产生不良反应甚至毒性,因此Cbf-14 凝胶整个生产过程中的杂质谱研究至关重要[7-10]。
本研究采用液相色谱-高分辨率质谱(LCHRMS)联用技术,分离和鉴定Cbf-14 凝胶中的肽类有关物质,共鉴定出5个制剂生产工艺杂质和19个强制降解产物,以上24个杂质均未见文献报道。结合母离子及碎片离子的相对分子质量和元素组成分析,本研究阐明了以上杂质的来源和形成机制,为Cbf-14 凝胶中的有关物质检查和质量控制提供了参考依据。
1 材 料
1.1 药品与试剂
抗菌肽Cbf-14醋酸冻干粉(纯度≥99%,南京金斯瑞生物科技有限公司,批号:C660QFK300-1/20110501-DG01),甘油、甲基纤维素(上海阿拉丁试剂有限公司);甲酸铵、甲酸(AR 级,南京化学试剂有限公司);乙腈(HPLC 级,德国默克公司);去离子水(市售娃哈哈纯净水)。
1.2 仪 器
岛津LCMS-9030四极杆飞行时间质谱仪、Lab-Solutions 数据处理系统(日本岛津公司);BS21S 分析天平(德国Sartorius公司)。
2 方 法
2.1 液相色谱条件
Agilent Zorbax SB-Phenyl 色谱柱(150 mm ×4.6 mm,3.5 µm);流动相A 相为20 mmol/L 甲酸铵缓冲溶液(用甲酸调节pH至3.0),B相为乙腈,线性梯度洗脱(A∶B):0 min(95∶5)→30 min(80∶20)→50 min(40∶60)→52 min(95∶5)→60 min(95∶5),流速1.0 mL/min,柱温40 ℃,进样量20 µL。
2.2 质谱条件
高分辨Q-TOF/MS 测定,NaI 溶液(400 µg/mL)准确质量校正。电喷雾正离子化,喷雾电压4.0 kV,雾化气压力230 kPa,流量3 L/min,接口温度300 ℃,加热气流量10 L/min,干燥气流量10 L/min,氩气CID 碰撞能量5 ~ 50 eV,扫描范围m/z 50 ~2 000。
2.3 样品配制
Cbf-14 凝胶:将 Cbf-14 醋酸冻干粉 20 mg 和甘油100 mg 溶解于无菌纯净水860 mg 中,充分混匀并完全溶解。然后将甲基纤维素20 mg 搅拌加入上述溶液中,溶胀均匀后,离心除去气泡即得含量为2%的Cbf-14凝胶。
供试品溶液:取Cbf-14 凝胶适量(约相当于Cbf-14 10 mg),精密称定,置10 mL 量瓶中,加水适量,超声使Cbf-14 凝胶溶解,再以水稀释至刻度,摇匀,以0. 45µm 水系滤膜过滤,取续滤液即得质量浓度为1 mg/mL 的供试品溶液。精密量取上述溶液适量,加流动相定量稀释,配制0.5 %的自身对照溶液。
2.4 药物稳定性
查阅相关文献[11],本研究对 Cbf-14 凝胶进行了酸、碱、氧化、高温和光照加速破坏,考察Cbf-14凝胶潜在的降解杂质。强制降解实验操作如下:取 Cbf-14 凝胶适量(约相当于Cbf-14 10 mg),加1.0 mol/L 盐酸溶液 1 mL 并于 60 ℃水浴放置 2 h,或加1 mol/L 氢氧化钠溶液1 mL 并于室温放置2 h,或加3%过氧化氢溶液1 mL 并于60 ℃水浴放置2 h,或于40 ℃烘箱中放置1 h,或于强光照射(1.62 × 106lx·h,324 W·h/m2,25 ℃)下放置10 d分别处理。酸碱处理溶液放置室温后分别用同浓度的酸碱溶液中和,高温干燥样品和强光照射样品分别加水适量,振摇使溶解。以上强制降解溶液分别加水稀释至10 mL,以0.45µm 水系滤膜过滤,取续滤液作为Cbf-14 质量浓度约为1 mg/mL 的强制降解试验溶液。同时采用空白溶液进行平行对照试验。
3 结 果
3.1 有关物质检查结果
对于含有芳香族氨基酸的多肽类物质的分析,苯基柱是一种独特的选择,因为它具有疏水相互作用和π-π 电子相互作用的双重分离机制,使其显示出与烷基键合硅胶固定相不同的特性,可以替代ODS 和C4 分析多肽和蛋白质。参考各国药典中关于胰岛素、醋酸奥曲肽、鲑降钙素和醋酸亮丙瑞林有关物质的分析方法,离子对色谱法最为常用。但是,这种分离模式不适用于LC-MS 联用技术。本研究开发了一种使用挥发性流动相的液相色谱质谱联用方法,用于在线分离和鉴定Cbf-14 凝胶制剂中的有关物质,并采用多级液相梯度以减少分析时间。
本研究建立了适用于Cbf-14 有关物质分离检查和MS鉴定的反相HPLC 方法。供试品溶液及其强制降解试验溶液有关物质的HPLC 检查结果见图1。按保留时间由小到大顺序对含量大于0.5%的主要有关物质进行识别和编号,共分离并检出24 个主要有关物质,其中有关物质19~23 为制剂生产工艺杂质,有关物质1~18和24为降解产物。
强制降解试验结果表明,本品对强酸、强碱、氧化、高温条件、强光照射均不稳定。在酸破坏条件下产生13 个主要降解产物(有关物质1 ~ 11、15、18,图1-a);在碱破坏条件下产生4 个主要降解产物(有关物质12~14、16,图1-b);在氧化破坏条件下产生2个主要降解产物(有关物质17、24,图1-c),有关物质24 的含量较大;在高温条件下产生4个主要降解产物(有关物质12~14、16,图1-d);在光照条件下产生1 个主要降解产物(有关物质10,图1-e)。
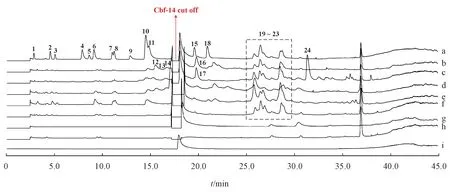
Figure 1 Total ion chromatograms of Cbf-14 gel and its stressed test solutionsa:Acid;b:Alkaline;C:Oxidation;D:Pyrolysis;e:Photolysis;f:Cbf-14 gel;g:Cbf-14 API;h:Blank gel;i:0.5%Reference
3.2 Cbf-14质谱裂解规律
使用HPLC-QTOF/MS 对Cbf-14 及其有关物质在ESI+模式下进行质谱分析,质谱数据汇总见表1。Cbf-14 的[M + 3H]3+离子的精确质量数为m/z 607.068 8,与离子式[C86H154N27O16]3+相应。Cbf-14的MS/MS二级质谱图见图2-a,Cbf-14的MS/MS主要特征碎片为 m/z 880.574 7、735.482 7、601.393 4、574.045 9、539.031 7 和 533.356 3。m/z 880.574 7([C85H148N24O16]2+)是由母离子中性丢失 1 分子胍(CH5N3)形成的;m/z 539.031 7([C78H138N25O12]3+)归因于母离子C 端的Ser-Val 残基的中性丢失,在此基础上脱去1 分子NH3形成m/z 533.356 3([C78H135N24O12]3+);m/z 574.045 9([C82H145N24O16]3+)是由母离子中性丢失1 分子C4H9N3,表明Cbf-14 分子中存在精氨酸残基。
3.3 Cbf-14凝胶中工艺杂质的结构鉴定
为了研究Cbf-14凝胶制剂的工艺相关杂质,对Cbf-14原料药和空白凝胶辅料进行对比分析,如图1 所示,原料药和空白辅料中均未检出含量大于0.5 %的杂质峰,Cbf-14 凝胶在 24.256 min 至31.507 min 处检出一系列含量在0.5 %左右的杂质峰,ESI(+)-QTOF-MS 共提取出 5 个不同的相对分子质量,编号为杂质19~23,推测以上杂质为工艺杂质。

Table 1 Related substances in Cbf-14 gel identified by LC-QTOF/MS

(Continued)

Figure 2 Product mass spectra of Cbf-14 gel and impurities 19-24A: Cbf-14 (m/z 607.068 8); B: Impurity 19 (m/z 611.067 4); C: Impurity 20 (m/z 615.739 4); D: Impurity 21 (m/z 621.071 0); E: Impurity 22 (m/z 625.743 0);F:Impurity 23(m/z 631.074 3);G:Impurity 24(m/z 606.723 6)
3.3.1 一级质谱数据解析 采用高分辨QTOF/MS 测定各有关物质的母离子及子离子的相对分子质量和元素组成,并与Cbf-14 的质谱特征进行对比分析,鉴定出各主要有关物质的结构。杂质19~23的一级质谱图见图3,质谱数据汇总见表1。分析一级质谱信息,共提取出10 种不同的加合物离子。其中,611.067 2、615.739 5、621.070 9、625.743 0、631.074 3为[M+3H]3+离子,916.100 8、923.109 2、931.106 4、938.114 5、946.111 4为相应的[M+2H]2+离子。
ESI(+)-QTOF-MS测得杂质19[M+3H]3+的m/z为611.067 2,与分子式C87H151N27O16相应,其相对分子质量为1 830.183 2,与Cbf-14 相比,其相对分子质量增加12,与Cbf-14 分子结构中引入一个亚甲基(CH2==)相应。

Figure 3 Mass spectrum of impurities 19-23 in Cbf-14 gel
ESI(+)-QTOF-MS测得杂质20[M+3H]3+的m/z为615.739 5,与分子式C88H153N27O16相应,其相对分子质量为1 844.198 9,与Cbf-14 相比,其相对分子质量增加26,与Cbf-14 分子结构中引入一个亚乙基(CH3CH==)相应。
ESI(+)-QTOF-MS测得杂质21[M+3H]3+的m/z为621.070 9,与分子式C88H153N27O17相应,其相对分子质量为1 860.193 8,与杂质20相比,其相对分子质量增加16,与杂质20 分子结构中引入一个氧(O)相应。
ESI(+)-QTOF-MS测得杂质22[M+3H]3+的m/z为625.743 0,与分子式C89H155N27O17相应,其相对分子质量为1 874.209 4,与杂质21相比,其相对分子质量增加14,与杂质21 分子结构中引入一个亚甲基(-CH2-)相应。
ESI(+)-QTOF-MS测得杂质23[M+3H]3+的m/z为631.074 3,与分子式C89H155N27O18相应,其相对分子质量为1 890.204 3,与杂质22相比,其相对分子质量增加16,与杂质22 分子结构中引入一个氧(O)相应。
Cbf-14 的分子结构中有8 个伯胺,其中有3 个来自精氨酸胍基、4 个来自赖氨酸氨基、1 个来自N端游离氨基酸。杂质19~23的MS/MS主要特征碎片有m/z 1 280.816 9、948.611 0和832.046 4,其中m/z 1 280.816 9([C62H106N17O12]+)为KFFRKLKKSV碎片离子,m/z 948.611 0([C48H78N13O7]+)为FFRKLKK碎片离子,m/z 832.046 4([C80H141N23O15]2+)为LLRKFFRKLKKSV 碎片离子。根据二级质谱分析,所得结果表明甘油与Cbf-14 发生反应的位点为Cbf-14 的N 端精氨酸。此外,胍基是共轭结构,电子云分布均匀,其反应活性远低于伯胺。综上所述,杂质19 ~ 23 是甘油与Cbf-14 的N 端游离伯胺缩合形成的N 端亚胺产物,分别为N2-亚甲基-Cbf-14、N2-亚乙基-Cbf-14、N2-(2-羟基亚丙基)-Cbf-14、N2-(3-羟基亚丙基)-Cbf-14 和 N2-(2,3-二羟基亚丙基)-Cbf-14。
3.3.2 二级碎片裂解途径归属 杂质19 ~ 23 的MS/MS 二级质谱图见图2-b~图2-f,其二级碎片裂解规律总结如下:由于Cbf-14 富含赖氨酸和精氨酸,杂质19~23 在二级裂解过程中易于丢失中性碎片氨[NH3]、胍[NH==C(NH2)2]和精氨酸残基[C4N3H8]。杂质 19 ~ 23 还易于丢失 C 端的 Val 残基和Ser-Val 残基。对于N2-(3-羟基亚丙基)-Cbf-14 和N2-(2,3-二羟基亚丙基)-Cbf-14,由于具有游离羟甲基结构,二者均可以失去1 分子的甲醛。此外,N2-(2,3-二羟基亚丙基)-Cbf-14 的N 端精氨酸胍基上的伯胺可攻击α-碳形成二氮杂䓬七元环,在此基础上失去1 分子3-氨基-1,2-丙二醇[CH2(OH)CH(OH)CH2NH2]产生特征碎片离子m/z 600.720 1([C60H149N26O16]3+),进一步失去 1 分子碳二亚胺[NH==C==NH]产生特征碎片离子m/z 586.712 8([C85H147N24O16]3+),N2-(3-羟基亚丙基)-Cbf-14具有上述相同的裂解规律。
3.4 Cbf-14凝胶中降解产物的结构鉴定
在Cbf-14 凝胶强制降解试验样品中还鉴定出了 19 个有关物质。其中杂质 1 ~ 11、15、17、18 为Cbf-14 水解产物,杂质 12 ~ 14、16 为 Cbf-14 异构体,杂质24为Cbf-14氧化产物,以上杂质的质谱数据汇总见表1。
杂质1~11、15、17、18是Cbf-14在酸或氧化条件下肽键水解所产生的。根据二级质谱分析,杂质 1 是 Cbf-14(1-5),杂质 2 是 Cbf-14(7-14),杂质 3是 Cbf-14(1-4),杂质 4 是 Cbf-14(4-14),杂质 5 是Cbf-14(1-3),杂质 6 是 Cbf-14(5-14),杂质 7 是 Cbf-14(1-6),杂质 8 是 Cbf-14(6-14),杂质 9 是 Cbf-14(3-14),杂质10 是Cbf-14(1-12),杂质11 是Cbf-14(1-13),杂质 15 是Cbf-14(1-8),杂质 17 是 Cbf-14(2-14),杂质18是Cbf-14(1-10)。
杂质12 ~ 14、16 是Cbf-14 的同分异构体。一般来说,多肽分子中存在许多手性中心,常见的消旋化机制主要有以下两种类型:直接烯醇化和唑酮(氮杂内酯)的形成,它们都是碱催化的消旋化机制。
杂质24(m/z 606.723 6,z = 3)被鉴定为[1-AIMAOPA]Cbf-14,是Cbf-14 的氧化产物。HO·是非常强的氧化剂,在过渡金属催化的Fenton 或Udenfriend 反应条件下在原位生成。原位产生的HO·氧化,要么发生在氨基的α-碳上,要么在胍基的α-碳上。所得到的α-羟基氨基酸残基很容易分解,分别产生谷氨酸半醛和氨基己二酸半醛[12-13]。由于杂质24与API相对分子质量相差1,结合其碎片信息和Cbf-14 结构特征,推测杂质24 为Cbf-14 N 端游离氨基的α-C 上发生氧化所得的α-羟基氨基酸脱去1 分子的游离氨,产生的2-氧代精氨酸。形成机制见图4。
杂质24 的MS/MS 二级质谱图见图2-g,其主要特征碎片为 m/z 600.720 5、586.713 3、573.701 0、538.686 6 和 533.012 0。[1-AIMAOPA]Cbf-14 的 N端精氨酸胍基上的伯胺可攻击α-碳形成二氮杂卓七元环,在此基础上失去1分子H2O产生特征碎片离子m/z 600.720 5([C60H149N26O16]3+),进一步失去1分子碳二亚胺[NH==C==NH]产生特征碎片离子m/z 586.713 3([C85H147N24O16]3+)。 m/z 573.701 0([C81H142N25O16]3+)是由母离子C端的Val残基丢失形成的;m/z 538.686 6([C78H135N24O13]3+)归因于母离子C 端的Ser-Val 残基的中性丢失,在此基础上脱去1分子NH3形成m/z 533.012 0([C78H132N23O13]3+)。

Figure 4 Formation mechanisms of aminoadipic semialdehyde,glutamate semialdehyde and 2-oxoarginine
4 讨 论
本研究建立了能够有效检测和分离Cbf-14 及其有关物质的挥发性流动相色谱条件,适用于Cbf-14 有关物质的色谱-质谱联用鉴定。在此条件下,共检测出24 个有关物质,其中5 个为制剂生产工艺有关物质,19 个为强制降解产物。对Cbf-14 有关物质结构及来源的推测对其生产工艺质量控制、评估药物稳定性及制定存储条件具有一定意义。
本研究建立的液相色谱-质谱联用法鉴定出Cbf-14 凝胶制剂生产工艺有关物质19~23 分别为N2-亚甲基-Cbf-14、N2-亚乙基-Cbf-14、N2-(2-羟基亚丙基)-Cbf-14、N2-(3-羟基亚丙基)-Cbf-14 和 N2-(2,3-二羟基亚丙基)-Cbf-14。以上杂质为凝胶辅料甘油与原料药Cbf-14 的N 端游离氨基缩合形成的N端亚胺产物,提示可能存在的原辅料相互作用。
强制降解试验表明,Cbf-14凝胶在酸性条件下易发生肽键水解产生特征有关物质1~11、15、18,在碱性条件或高温条件下易消旋异构产生特征有关物质12~14、16,在氧化条件下易产生水解产物17,并且易发生α-C 氧化形成脱氨氧代产物(有关物质24)。因此,Cbf-14 凝胶对酸、碱、氧化、高温及光照均比较敏感。Cbf-14 凝胶的储藏需密封避光,避酸避碱,尽量冷藏。

