检验指标及影像特征预测肝细胞癌微血管侵犯的初步研究
郭保亮 黄锡谊 陈家成 潘佳玲 胡秋根 杨少民
肝细胞癌(hepatocellular carcinoma,HCC)是一种形态异质性肿瘤,具有可变的结构生长模式和多种不同的组织学亚型,是常见的恶性肿瘤之一。据相关报道显示,全球范围内,男性HCC 的发病率在癌症中排名第五,女性排第九,男性HCC 的死亡率第二,女性第六,中国每年新增或致死的肝癌病例超过50%[1]。目前HCC 的治疗手段多样,其中肝切除和肝移植是当前最常用的治疗方式,但不同患者的预后各不相同[2]。微血管侵犯(microvascular invasion,MVI)与肝癌切除术后的预后有关,被认为是HCC 手术后早期复发的重要风险因子,但如何在术前进行有效的预测仍具有一定的难度[3]。以往的研究主要集中在评价不同的影像特征和图像组的表现上,在预测MVI 方面,相关血清指标和影像学指标之间的差异尚未得到较好的解释。本文将探讨检验指标及影像特征预测肝脏微血管侵犯的应用价值。
1 资料与方法
1.1 一般资料
2019年1月至2021年12月在南方医科大学顺德医院行肝脏切除术的119 例肝癌患者作为研究对象。其中男108 例,女11 例,年龄30~82 岁,平均年龄(55.62±7.34)岁。纳入标准:①符合《原发性肝癌诊疗规范(2017年版)》解读中HCC 的诊断标准[4];②经影像学和手术病理结果所证实;③术前1 个月内完成影像学检查;④所有患者及家属均知情且同意本次研究,并签署知情同意书。排除标准:①临床资料不齐全者;②影像图像质量影像观察病灶者;③以往接受过手术、化放疗、靶向治疗等相关治疗;④存在精神问题,无法配合检查者。本研究经医院伦理委员会批准同意。
1.2 方法
收集患者一般资料,包括性别、年龄,相关检验指标,包括谷草转氨酶(alanineaminotransferase,AST)、计算中性粒细胞/淋巴细胞比值(neutrophils to lymphocytes ratio,NLR)、凝血酶原时间(Prothrombin time,PT),相关影像指标,包括肿瘤累及的肝段、病灶的数量、形态、马赛克征、坏死、出血、扩散加权成像(diffusion-weighted images,DWI)表现、动脉期瘤周强化、瘤内动脉、冠状强化、肝胆期(hepatobiliary phase,HBP)瘤周低信号、表观扩散系数(Apparent diffusion coefficient,ADC),以及肿瘤直径。
1.2.1 分组方法
根据手术病理检查结果的MVI 况将其分为MVI 阳性组(49 例)和MVI 阴性组(70 例)。
1.2.2 检查方法
1.2.2.1 扫描方法 扫描采用德国西门子MAGNETOM Skyra 3.0T 磁共振仪,使用腹部相控阵线圈,利用腹带减少呼吸伪影的影响,扫描范围从膈顶到双肾下极。先行MRI 平扫,扫描序列为T1WI 3D VIBE(TR=4.28,TE=1.78)与T2WI TIRM(TR=4 000 ms,TE=104 ms),扫描参数:层厚4 mm,层间距1 mm,视野350 mm×350 mm,矩阵320×256。MRI 平扫完成后,采用单次激发平面回波成像技术行DWI 序列(TR=5 700 ms,TE=70 ms),扫描参数:层厚4 mm,层间距1 mm,视野350 mm×350 mm,矩阵320×256,扩散敏感系数为0、800 s/mm2。最后行MRI 增强扫描,对比剂经肘静脉团注0.2 mmol/kg。
1.2.2.2 图像后处理 扫描后DWI 数据传至Syngo.via 10 工作站,由2 名高年资影像科医师采用盲法阅片,意见不一时商讨达成一致。测量时尽量避开出血、坏死、囊变区,在ADC 图像勾画病灶实质部分的感兴趣区,面积≥50 mm2,测量表观扩散系数(apparent diffusion coefficient,ADC)值,取3 次均值。
1.2.3 相关血清指标检测
采取患者空腹静脉血3 mL,离心机以3 000 r/min 速度离心处理5 min,取上层血清,采用全自动生化分析仪及配套试剂盒以免疫放射法检测AST,采用酶联免疫法检测AKP、白蛋白、PT、中性粒细胞、淋巴细胞。
1.3 统计学方法
使用SPSS 20.0 统计学软件分析数据,单因素分析中,符合正态分布以()表示,行t检验,非正态分布采用Mann-Whitney 检验,计数资料以n(%)表示,采用卡方检验,采用Logistic 回归分析预测肝细胞癌MVI 的独立危险因素;受试者工作特征曲线(ROC)分析检验指标及影像特征预测MVI的诊断价值。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者各相关指标比较
两组患者NLR、PT、肿瘤累及的肝段、影像学形态、马赛克征、坏死、出血、DWI 表现、动脉期瘤周强化、瘤内动脉、冠状强化、HBP 瘤周低信号、肿瘤直径比较,差异有统计学意义(P<0.05)。见表1。
表1 两组患者各相关指标比较[n(%),(±s)]Table 1 Comparison of relevant indicators between the two groups of patients[n(%),(±s)]
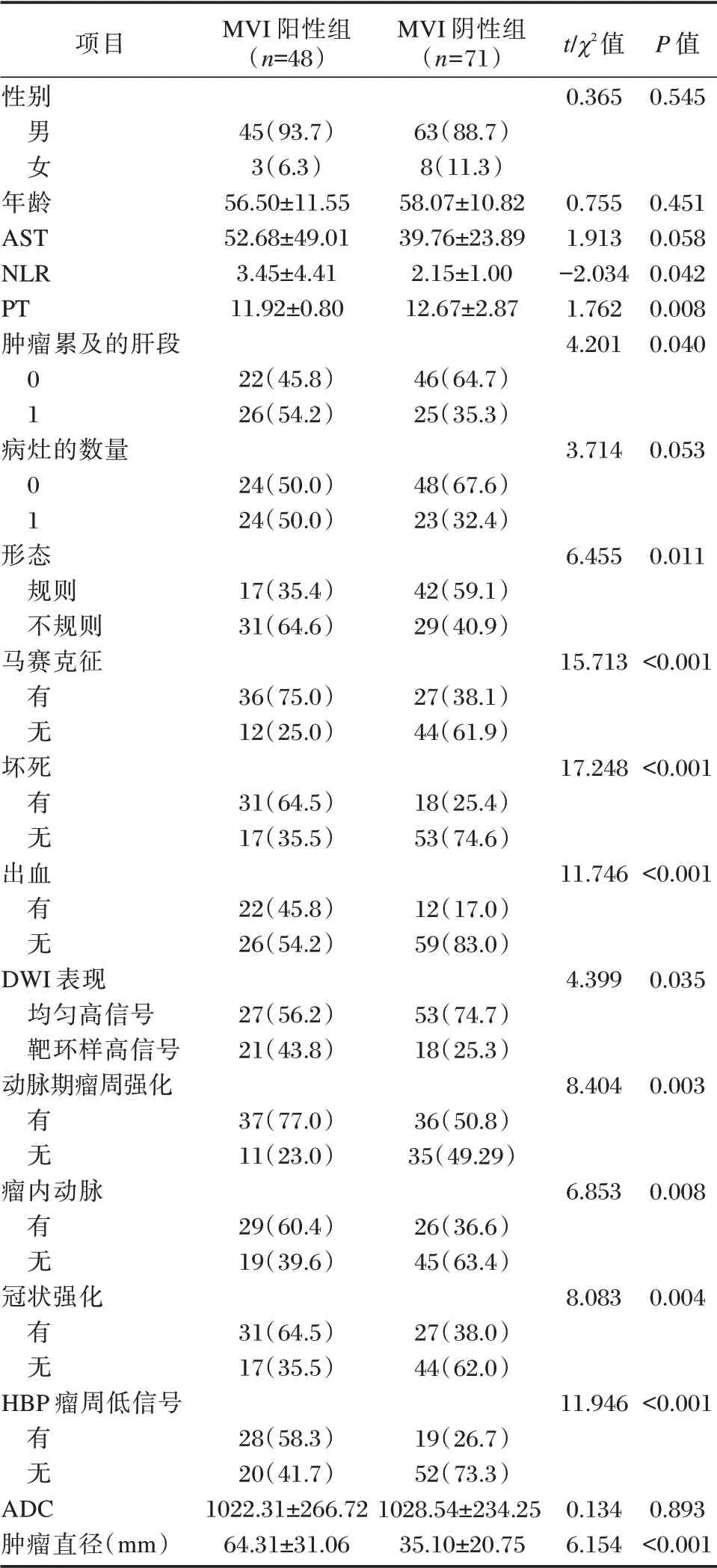
表1 两组患者各相关指标比较[n(%),(±s)]Table 1 Comparison of relevant indicators between the two groups of patients[n(%),(±s)]
项目性别MVI 阳性组(n=48)MVI 阴性组(n=71)t/χ2值0.365 P 值0.545男女年龄AST NLR PT肿瘤累及的肝段45(93.7)3(6.3)56.50±11.55 52.68±49.01 3.45±4.41 11.92±0.80 63(88.7)8(11.3)58.07±10.82 39.76±23.89 2.15±1.00 12.67±2.87 0.755 1.913-2.034 1.762 4.201 0.451 0.058 0.042 0.008 0.040 0 1 22(45.8)26(54.2)46(64.7)25(35.3)病灶的数量3.714 0.053 0 1 24(50.0)24(50.0)48(67.6)23(32.4)形态规则不规则马赛克征6.455 0.011 17(35.4)31(64.6)42(59.1)29(40.9)15.713<0.001有无36(75.0)12(25.0)27(38.1)44(61.9)坏死17.248<0.001有无31(64.5)17(35.5)18(25.4)53(74.6)出血11.746<0.001有无22(45.8)26(54.2)12(17.0)59(83.0)DWI 表现均匀高信号靶环样高信号动脉期瘤周强化4.399 0.035 27(56.2)21(43.8)53(74.7)18(25.3)8.404 0.003有无37(77.0)11(23.0)36(50.8)35(49.29)瘤内动脉6.853 0.008有无29(60.4)19(39.6)26(36.6)45(63.4)冠状强化8.083 0.004有无31(64.5)17(35.5)27(38.0)44(62.0)HBP 瘤周低信号11.946<0.001有无ADC肿瘤直径(mm)28(58.3)20(41.7)1022.31±266.72 64.31±31.06 19(26.7)52(73.3)1028.54±234.25 35.10±20.75 0.134 6.154 0.893<0.001
2.2 危险特征预测肝细胞癌MVI 的Logistic 回归分析
以MVI 阳性为因变量,赋予肿瘤累计的肝段(0=无,1=有)、形态规则(0=是,1=否)、马赛克征(0=无,1=有)、坏死(0=无,1=有)、出血(0=无,1=有)、DWI 表现均为高信号(0=是,1=否)、瘤内动脉(0=无,1=有)、冠状强化(0=无,1=有)、HBP 瘤周低信号(0=无,1=有),NLP、PT、肿瘤直径原值录入。Logistic 回归分析结果显示,NLR 水平升高、PT 低、有肿瘤累计的肝段、HBP 瘤周低信号、肿瘤直径长是影像预测肝细胞癌MVI 的独立危险因素(P值均<0.05)。见表2。

表2 影响预测肝细胞癌MVI 的Logistic 回归分析Table 2 Logistic regression analysis of influence prediction of liver MVI
2.3 检验指标及影像特征预测对预测肝细胞癌MVI 的诊断效能
绘制ROC 曲线图结果显示,检验指标及影像指标中的HBP 瘤周低信号预测肝细胞癌MVI 在截断值为0.50 时,敏感度为0.583,特异度为0.729,曲线下面积为0.809,对肝细胞癌MVI 诊断效能最大。见表3、图1。

图1 ROC 曲线分析Figure 1 ROC curve
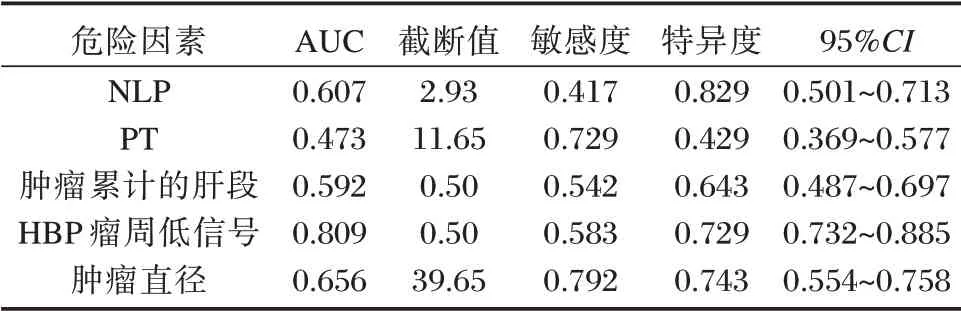
表3 检验指标及影像预测对预测肝细胞癌MVI 的诊断效能Table 3 Diagnostic efficacy of test indicators and image prediction in predicting liver MVI
3 讨论
近年来,我国HCC 的患病率和死亡率仍处于上升趋势。相关数据显示,2018年,全球每10 万人中肝癌发病率约为9.3,相应的死亡率为8.5[5]。病变部位虽可手术切除,但5年内复发的几率高达70%[6]。HCC 术后早期复发是影响预后较差的主要原因,减少HCC 的复发率是改善HCC 的总体临床效果的关键。MVI 是HCC 根治性手术后复发的独立危险因素之一,相关研究显示,存在MVI 的HCC 患者比无MVI 患者的复发率高4.4 倍[7]。手术病理检查是判断MVI 的金标准,但该检查属于有创操作,对患者伤害较大。因此,术前有效的检验指标和影像学指标对预测MVI 情况,延长患者生存期,降低复发率和提高生存质量具有重要意义。
研究结果显示,NLR、PT、影像学形态、马赛克征、坏死、出血、DWI 表现、动脉期瘤周强化、瘤内动脉、冠状强化、HBP 瘤周低信号、肿瘤直径与肝细胞癌MVI 阳性相关。Logistic 回归分析显示,NLR 水平升高、PT 低、有肿瘤累计的肝段、肿瘤直径长是影响预测肝细胞癌MVI 的独立危险因素。NLR 是常见的炎性指标,NLR 的增高通常是由于存在感染或严重的炎症反应,反映人体的炎症和免疫系统的总体状况,该指标可作为MVI 的预测因子[8]。卫泽源等[9]发现,HCC 手术前NLR 升高与MVI 发生有密切关系,而微血管侵犯则是肝癌肝内转移的重要标志,与本研究结果相符。PT 水平是反映肝功能损害的重要指标,PT 持续时间越长,说明肝功能越差,肝细胞损伤越重,提示肝内出血的风险增加[10]。PT 时间缩短可用于评价患者的血栓栓塞和心血管事件的危险,本研究MVI 阳性组PT 时间缩短,与提示机体处于高凝状态[11]。当HCC 患者存在MVI 时,机体多处于高凝状态,检测PT 对HCC 患者术前MVI 的诊断具有良好的临床应用价值。病理检查是MVI 的金标准,其标本取得是在肝段切除术后或肝移植术后,超过3 个肝脏部分的肝实质切除是影响围术期复发率和死亡率的重要因素,但该方法相对落后[12]。肿瘤直径对肿瘤预后有重要影响,肿瘤的直径越大,说明其进展的时间越长,而且临床上的肿瘤分期在相同时间内发展较快,病情越难控制,预后越差[13]。本研究MVI 阳性组肿瘤直径大于MVI 阴性组,提示肿瘤直径与MVI 密切相关,与刘连凤等[14]研究相符。原因考虑为,随着肿瘤的直径增大,周围的肝脏组织和微血管的数目增多,肿瘤细胞侵袭能力越强,MVI 的发生几率也随之增大[15]。ROC 曲线图显示,HBP 瘤周低信号预测肝细胞癌MVI 在截断值为0.50 时,敏感度为0.583,特异度为0.729,曲线下面积为0.809,对肝细胞癌MVI 诊断效能最大。
综上,可通过检验NLR、PT 水平、肿瘤累计的肝段、肿瘤直径大小来判断肝细胞癌患者是否存在MVI,其中HBP 瘤周低信号预测肝细胞癌MVI的诊断效能最大。

