低氧诱导因子调控肾透明细胞癌进程的分子机制研究进展
陈延萍 吴果 马孟丹 杨育宾 陈巍
最新癌症统计数据显示,全球范围内肾癌新增病例约43 万例,死亡人数达到17.9 万人[1],其中美国2021年男性及女性肾癌新增病例均位于全部癌种新增病例的前十,且分别占总新增病例数的5%、3%[2]。近年来我国肾癌发病率及死亡率逐年攀升[3],给我国医疗卫生事业带来了巨大挑战,肾癌逐渐成为我国泌尿肿瘤领域亟待解决的重要难题。肾透明细胞癌(Clear cell renal cell carcinoma,ccRCC)是肾细胞癌最常见的病理类型,约占所有肾细胞癌的80%[4]。ccRCC 微环境中普遍存在低氧现象[5],而低氧诱导因子(hypoxia inducible factor,HIF)则是这一现象的主要诱因,HIF 基因对ccRCC 的增殖、分化、血管生成、能量代谢以及肿瘤耐药发生、患者预后等具有调控作用[6-8]。因此综述HIF基因在ccRCC 中的作用具有重要的科学价值,或可为临床治疗提供理论基础。
1 ccRCC 的发展现状
ccRCC 常发生于双侧肾脏,伴有囊腔结构,影像学显示钙化阴影且胞浆透明,内含丰富的毛细血管网[9]。作为一种预后相对较差的肾恶性肿瘤,ccRCC 的预后受多因素影响,包括肿瘤大小、坏死程度以及TNM 分级等[10-11]。研究ccRCC 发病机理以及预后影响因素不仅有助于寻求更有效的方法提高ccRCC 患者的存活率,还可以建立并完善ccRCC 的预后分析系统,对临床治疗具有重要的指导意义。
因ccRCC 普遍具有转移性和异质性,临床上常用的根除性肾切除术、保留肾单位手术以及下腔静脉栓治疗等方案治疗效果不佳。HIF基因可作为治疗ccRCC 的有效靶点,目前靶向HIF基因的药物在临床应用中取得较好的治疗效果。因此,不断深入挖掘HIF相关调控基因及靶向药物并解析其作用机制对ccRCC 的临床诊疗意义重大。
2 HIF 基因
HIF 编码的蛋白包括HIF-1、HIF-2 及HIF-3,三者均含α 亚基和β 亚基构成的二聚体结构,α 亚基是依赖于细胞内氧气浓度水平的主要调节亚基,β 亚基则是组成性结构,在α 亚基未被泛素化的情况下与其结合形成二聚体并移入细胞核内发挥转录激活作用。
转录组学及蛋白质组学分析表明,HIF-1α 与HIF-2α 是ccRCC 肿瘤细胞适应低氧环境的重要作用因子,对ccRCC 的发生发展具有调控作用。转录后水平的研究数据表明,HIF-1α 主要调控糖酵解过程,而HIF-2α 调控脂蛋白代谢、核糖体发生以及相关基因的转录激活等[12]。部分研究者认为14 号染色体上(Von Hippel-Lindau,VHL)双等位基因失活时,HIF-1α 在ccRCC 中发挥抑癌功能,而HIF-2α 发挥促癌作用[6],但也有研究证明在原发性ccRCC 小鼠异种移植瘤模型中HIF-1α对肿瘤形成是必要的,因此HIF-1α 对ccRCC 的调控作用及机理有待进一步验证。关于HIF-3α 作用机制的研究较少,其在ccRCC 中的转录激活活性尚未被证实,HIF-3α 通过与HIF-1β 的竞争性结合调控HIF-1α 和HIF-2α 的功能,常被认作低氧诱导基因表达的负调节剂。
3 HIF 在ccRCC 中的具体调控机制
3.1 转录水平的调控
目前关于HIF基因转录水平的调控机制主要包括:HIFα-VHL 氧敏感信号通路、调控肿瘤新生血管生成的血管生长因子(vascular endothelial growth factor,VEGF)信号通路、转化诱导因子(transforming growth factor-β,TGF-β)信号通路以及丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信号通路和哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)信号通路。HIF基因通过以上信号通路参与调节ccRCC细胞增殖、血管形成、糖酵解等生物学行为。
3.1.1 HIFα-VHL 氧敏感信号通路
VHL基因功能丧失和低氧诱导因子HIF 不受抑制的激活是ccRCC 发生和发展的主要诱因,VHL基因的突变或失活作为ccRCC 发生的早期事件导致HIF 的积聚而激活下游基因的异常表达,进而促进ccRCC 的发生和发展。在细胞内不同氧水平下,HIF 参与细胞内信号通路的调控主要依赖其α 亚基与VHL基因编码产物(product of the VHL gene,pVHL)结合活性来实现,从而形成HIF-α-VHLPHD 轴来实现其对ccRCC 的调控作用。见图1。
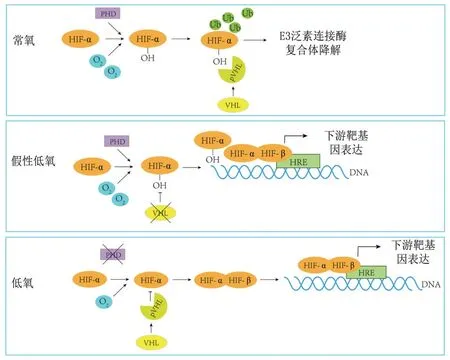
图1 不同氧水平下HIFα-VHL 氧敏感信号通路的调控机制Figure 1 The regulation mechanism of HIFα-VHL oxygen sensitive signaling pathways at different oxygen levels
常氧的条件下,pVHL 识别并结合脯氨酸羟基化酶(prolyl hydroxylase,PHD)作用后羟基化的HIF-α,并使其被进一步泛素化降解[13]。此外,与氧水平无关的VHL 双等位基因失活所介导的HIF-1α与HIF-2α 突变诱导的稳定作用使其能够与HIF-1β 结合并定位于核,从而使低氧反应途径的下游基因转录激活,出现“假性低氧”,这种假性低氧会促进诱导肿瘤细胞的增殖以及血管生成因子的表达以及代谢重编程等[14]。低氧时,PHD 失活导致HIF-α 的稳定,使其不被pVHL 识别降解而与HIF-β 结合形成二聚体转移到细胞核结合低氧反应元件,进而激活下游基因转录。HIF 结合位点的遗传变异可调节HIF-VHL 轴的致癌转录输出,在该轴中HIF-1α 和HIF-2α 调节下游基因的转录活性,从而介导肿瘤细胞对低氧水平的适应性[15]。
3.1.2 VEGF 信号通路
肿瘤组织内部高度血管化是ccRCC的显著特征,血管新生被认为是ccRCC发生、发展和临床治疗中的重大挑战。VEGF是刺激血管生成的重要细胞外信号转导蛋白,与非转移性肾癌相比,转移性ccRCC 中VEGF、VEGFR2 的mRNA 及蛋白表达水平均升高[16]。HIF的α、β亚基结合形成的二聚体可通过HRE定向作用于血管生长因子受体(vascular endothelial growth facto receptor,VEGFR)、血小板衍生生长因子(platelet derived growth factor,PDGF)、TGF-α 结合到其相应的下游受体上,进而调控血管生成[17]。
3.1.3 TGF-β 信号通路
TGF-β 信号通路相关蛋白表达水平与ccRCC的患者的临床病理参数以及预后紧密相关,而HIF-1α、HIF-2α 在经典以及非经典的TGF-β 信号通路中均发挥调控作用。具体概括为:在ccRCC早期低氧状态中,HIF-1α 的上调可激活TGF-β/Smad 通路致使低氧诱导的TGF-β 信号通路下游效应因子Smad3 上调,从而抑制肿瘤的发生发展进程、减缓肿瘤细胞氧敏感通路的低氧反应[18];常氧时,HIF-1α 以及HIF-2α 的上游驱动因子促进TGF-β 信号通路下游上皮间质转化基因(epithelial mesenchymal transition,EMT)相关靶基因的表达进而调控ccRCC 的发展进程。此外,在VHL基因失活的ccRCC 中,HIF-1α 异常激活并与间变型淋巴瘤激酶5(anaplastic lymphomakinase 5,ALK5)协同作用调控TGF-β 信号通路和低氧通路,进而介导ccRCC 的不良预后以及远端转移[19]。
3.1.4 MAPK 信号通路
HIF基因功能与MAPK 相关信号通路的磷酸化水平密切相关,MAPK 信号通路中的ERK1/2 及p38 能够在体外磷酸化HIF-1α 从而能够阻断其报告基因的活性;HIF-1α 通过与TRIB3 启动子结合调控其表达水平,进而影响MAPK 信号通路中p38蛋白、P44/42 以及SAPK/JNK 等的磷酸化水平[20]。ERK1/2 和ERK5 状态与ccRCC 预后高度相关,其中ERK5 过表达的ccRCC 患者预后较差[21]。
3.1.5 mTOR 信号通路
mTOR 是一种289 kDa 的丝氨酸、苏氨酸激酶,是肿瘤细胞生长和增殖的调节剂。有关报导表明PI3K-AKT-mTOR 信号通路参与了ccRCC 的启动和发展,如Nayak 等[22]发现p22 沉默子通过PI3KAKT-mTOR 信号通路降低了HIF-2α 依赖的靶基因的表达并抑制肿瘤的生长,认为P22 可成为靶向mTOR 通路有效治疗靶点;磷酸酶和张力蛋白同源物(phosphatase and tensin homologue deleted on chromosome ten,PTEN)是PI3K-AKT-mTOR 信号通路的关键级联抑制因子,其缺失会导致该信号通路下游激活,影响ccRCC 患者的整体生存率。
3.1.6 其他信号通路
HIF基因除了参与多个信号通路的调控影响ccRCC 表型外,还可以与多个癌基因互作间接发挥作用,见图2。丧失初级纤毛是ccRCC 的早期特征,HIF-1α 通过抑制β-catenin 转录活性降低极光激酶A(Aurora kinase A,AURKA)的表达水平,进而缩短肾脏成纤维细胞的纤毛长度[23];在低氧条件下,HIF-1α 可抑制原癌基因MYC 活性,促进ccRCC 肿瘤细胞在低氧条件下存活[24];在VHL突变失活依赖的ccRCC 中,HIF-1α 与p53 的表达水平存在负反馈调控机制,pVHL 的稳定性能够增强p53 的抑癌活性[25]。
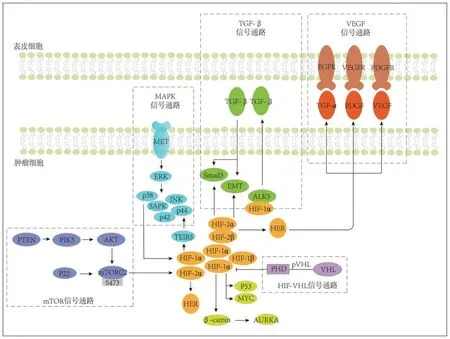
图2 HIF 基因转录水平调控信号通路Figure 2 HIF gene transcription level regulation signaling pathways
3.2 表观遗传学调控
表观遗传重编程是ccRCC 发生和发展过程中的重要事件,包含非编码RNA(long non-coding RNA,lncRNA)和微小RNA(micro RNAs,miRNAs)参与的基因表达调控、DNA 甲基化以及组蛋白修饰等。随着人类基因组计划的完成以及单细胞测序技术迅猛发展,更多的学者热衷于ccRCC的表观遗传的研究,以期找到ccRCC 的治疗新靶点。
3.2.1 长链非编码RNA
LncRNA 是一类碱基序列长度大于200 nt 且不编码蛋白质的RNA,能够在转录水平以及转录后水平参与基因表达调控、基因组印记、染色质修饰等多种生物学进程。
低氧条件下,lncRNA 通过调控氧感知受体以及激素受体的表达水平影响VHL基因失活对ccRCC 的调控作用。抑制雄激素受体的lncRNA(suppressing androgen receptor in renal cell carcinoma,lncRNA-SARCC)能够通过物理结合雄激素去稳定受体蛋白来抑制雄激素受体与HIF 基因共同信号转导途经调控细胞的低氧周期。一种新型的lncRNA,即人肾细胞相关转录本1(metastatic renal cell carcinoma-associated transcript 1,MRCCAT1)通过招募多梳抑制复合体2(polycomb repressive complex 2,PRC2)到利钠肽受体3(natriuretic peptide receptor 3,NPR3)启动子来抑制NPR3 的转录,进而激活p38-MAPK 信号转导途径促进ccRCC 的转移[26]。
3.2.2 微小RNA
miRNAs 是具有调节功能的内源性非编码单链RNA,能够靶向调节mRNA 的活性,近年来,miRNAs 的发现为癌症的新型诊断和治疗增添了新维度。报道显示,与癌旁组织相比,ccRCC 组织中miR-155 表达水平显著升高,且与HIFα-VHL基因表达水平呈正相关,认为miR-155 可能通过HIFα-VHL 通路调控ccRCC 的发生和发展[27];Neal等通过使用HIF-1α 和HIF-2α 特异性的siRNA 处理VHL基因缺失的细胞发现miR-155 表达水平明显降低,该现象表明miRNA 的诱导主要是通过HIF 所介导的[28],这可能为ccRCC 疾病的诊疗提供新的靶点。
3.2.3 DNA 甲基化
DNA 甲基化是肿瘤细胞中替代的互补机制,通过沉默抑癌基因表达诱导肿瘤发生和转移。ccRCC 中包括HIF基因在内的多个癌基因的转录因子结合位点存在高甲基化区域,甲基化程度显著影响HIF基因的转录活性。这类基因沉默会干扰ccRCC 中低氧相关的信号通路,例如依赖VHL的DNA 超甲基化通过影响HRE 中CpG 位点二核苷酸的甲基化调节HIF 与HRE 的结合,从而影响HIF下游基因表达水平[29]。氮端甲基腺嘌呤(N6-methyladenosine,m6A)RNA 去甲基化酶的转录修饰子FTO 作为VHL 的合成性致死伙伴,可选择性降低VHL 缺陷型、HIF 野生型以及HIF 缺陷型ccRCC 细胞存活率[30]。
4 结论与展望
低氧不仅影响由遗传因素引发的恶性肿瘤的发生发展,长期的低氧环境也会导致肾脏功能下降并诱发慢性肾脏疾病。总之,ccRCC 对低氧环境的适应主要受HIF基因调控,HIF基因的转录激活在血管新生、能量代谢以及缓解ccRCC 细胞低氧损伤等方面有重要调控作用。随着机体氧感知机制研究的不断深入,HIF基因的调控机制成为ccRCC 病理作用研究的热点,给ccRCC 的治疗开辟了新途径,还为进一步挖掘针对低氧所致的不同类型肿瘤的治疗提供借鉴。

