NaOH- NaNO3熔融盐法分离分银渣试验
房孟钊
(1.中国有色矿业集团刚果矿业有限责任公司, 北京 100000; 2.大冶有色金属有限责任公司, 湖北 黄石 435002)
0 前言
某冶炼厂稀贵车间通过回转窑半湿法工艺处理自产的铜阳极泥(图1),提取其中的Au、Ag、Pt、Pd、Sn、Te,尾渣为分银渣,但是分银渣中仍含有Au、Ag、Pb、Sn、Bi、Sb等多种富有经济价值的稀贵金属[1-8]。随着铜产量不断提高与再生铜处理量的加大,稀贵车间需要处理的铜阳极泥量不断增加。按照实际生产情况,处理1 t铜阳极泥会产生0.5~0.6 t分银渣,每年分银渣的产量非常大,由于没有成熟的工艺开发分银精矿,企业只能将分银渣返回铜冶炼系统中,与铜精矿混合一起进入铜冶炼奥斯麦特熔炼炉中。此方法不仅造成能源消耗和铜精矿处理的负荷加大,而且不能很好地提取其中的有价金属,造成资源损失浪费。因此,寻求经济有效的方法对分银渣加以综合回收,不仅可以实现资源的有效循环利用,也可创造新的利润增长点,适应当前我国节能减排的政策环境。

图1 铜阳极泥处理工艺流程
目前,分银渣的处理方法主要有湿法与火法,湿法又分为全湿法与半湿法。火法工艺因能耗大、设备复杂等缺点,应用较少;全湿法工艺避免了火法工艺的缺点,但是回收率低、波动大。江西铜业的孙文达[9]研究了火法熔炼和湿法浸出相结合的半湿法工艺流程来提取分银渣中的贵金属,避免了全湿法处理的缺点,但是也存在熔炼温度较高,能耗高,设备要求高等方面的不足。因此,低温碱性熔炼法在处理分银渣方面的优势得到了关注,中南大学田庆华教授[10]研究了NaOH、Na2S熔盐法处理分银渣,虽然效果较好,但实际生产过程中产生的二氧化硫对设备腐蚀严重。综上所述,本文选择NaOH、NaNO3熔融盐法分离分银渣。
1 试验
1.1 试验原料
目前,在实际生产中,每年分银渣的产出率很高,约2 000 t,其中的有价金属种类较多,如表1所示。除了少量贵金属金与银,分银渣中具有开发价值且含量较高的金属有铅、锡、铋、锑,其含量分别达到40.26%、3.859%、2.336%、11.1%。

表1 分银渣中主要金属品位
1.2 试验装置
选用的药剂NaOH、NaNO3为分析纯(国药集团化学试剂有限公司),熔融盐法分离分银渣的试验装置如图2与图3所示。首先在图2箱式电炉装置(生产公司:长沙市远东电炉厂)中完成熔融盐与分银渣的熔炼过程,得到熔炼渣;再在图3恒温磁力搅拌器装置(生产公司:巩义市予华仪器有限公司)内完成熔炼渣的浸出过程,得到浸出液与浸出渣。

1-箱式电炉; 2-温控仪; 3-电源; 4-导线图2 熔炼实验装置图
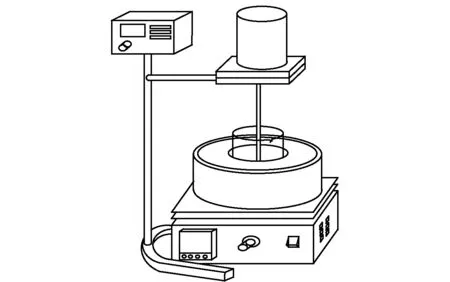
图3 浸出实验装置图
1.3 试验原理
分银渣的XRD物相图如图4所示。从图4可以看出,分银渣中的两性金属较多,因此在熔融盐熔炼条件下,NaOH易于与分银渣中的两性金属发生反应,即将分银渣中的Pb、Sn转化为易溶于水的钠盐;然后通过浸出,Pb、Sn以离子的形式进入溶液中。

图4 分银渣的XRD光谱
由于分银渣中少量的有价金属以低价态复盐形式存在,因此,以NaNO3为氧化剂,可以将低价态的Pb和Sn氧化为高价态,从而有利于分银渣中更多的Pb、Sn与NaOH反应,成为钠盐,最终进入浸出液中[11-14]。主要的化学反应式为:
PbSO4+4NaOH→Na2PbO2+Na2SO4+2H2O
(1)
PbO+2NaOH→Na2PbO2+H2O
(2)
2Sn+3NaOH+NaNO3→2Na2SnO3+NH3
(3)
SnO2+2NaOH→Na2SnO3+ H2O
(4)
2As+ 4NaOH+2NaNO3→2Na3AsO4+2H2O+N2
(5)
试验采用的工艺流程如图5所示。分银渣经过球磨、熔融盐熔炼、纯水浸出熔炼渣工艺的处理得到浸出液与浸出渣。后续针对浸出液的处理,考虑在浸出液中加入石灰,得到CaSn(OH)6与含铅溶液。CaSn(OH)6进行精制得到工业级氧化锡,在含铅溶液中加入硫化钠得到硫化铅。而对于浸出渣,将其进行低温熔炼分离Sb、Bi,通过加入双氧水精制生产工业级锑酸钠,最后将含铋渣与硫化铅进行低温碱性熔炼得到铅铋合金,从而有效富集贵金属。

图5 分银渣处理工艺流程图
1.4 试验方法
由于生产中产出的分银渣含水量高,因此需要提前将分银渣与药剂放在干燥箱中去除水分。为了保证分银渣中有价金属最大限度地参与反应,干燥后的分银渣需要在球磨机中进行球磨处理。分金渣球磨后粒径达到100目,然后继续放置干燥箱中,防止受潮。
称取定量的NaOH和NaNO3,与分银渣搅拌混匀,装入刚玉坩埚中。待马弗炉温度恒定后将刚玉坩埚放入其中,在预定温度下进行熔融盐熔炼并开始计时,到达反应时间后,取出刚玉坩埚在空气中自然冷却。利用浸出工艺分离熔炼渣中的Pb、Sn,滤渣送往鼓风干燥箱干燥,量取浸出液体积并取样分析。
2 试验结果与讨论
2.1 熔炼温度的影响
选取球磨后的分银渣10 g,在NaOH用量45 g,NaNO3用量20 g,熔炼时间2.5 h,浸出温度80 ℃,浸出时间40 min,液固比6∶1,搅拌速度为450 r/min的条件下进行试验,考察熔炼温度对金属回收率的影响,结果如图6所示。
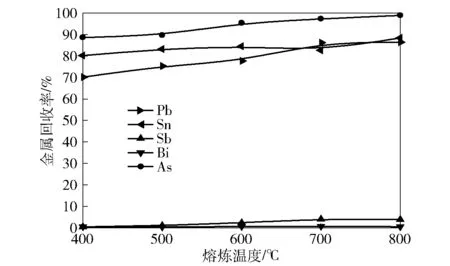
图6 熔炼温度对分银渣中金属回收率的影响
由图6可知,随熔炼温度的升高,Pb、As回收率逐渐增加,Sn回收率增长缓慢;在熔炼温度超过700 ℃后,Pb、As的回收率增长缓慢,Sn回收率变化不大;Sb与Bi的回收率始终很低且增长缓慢,说明Sb和Bi绝大部分富集到过滤渣里。产生此种现象的原因是:熔炼温度的提高可减少化学反应控制和外扩散过程对反应转化率的影响,从而提高Pb、Sn的回收率;分银渣中Sb和Bi的多金属复杂盐很少与碱反应生成可溶性盐,Sb和Bi的回收率均在4%以下。因此,选择700 ℃为最佳熔炼温度比较合适,此时Pb、 Sn的回收率分别达到86.21%、82.66%。
2.2 熔炼时间的影响
选取球磨后的分银渣10 g,在NaOH用量45 g,NaNO3用量20 g,熔炼温度700 ℃,浸出温度80 ℃,浸出时间40 min,液固比6∶1,搅拌速度为450 r/min的条件下进行试验,考察熔炼时间对金属回收率的影响,结果如图7所示。
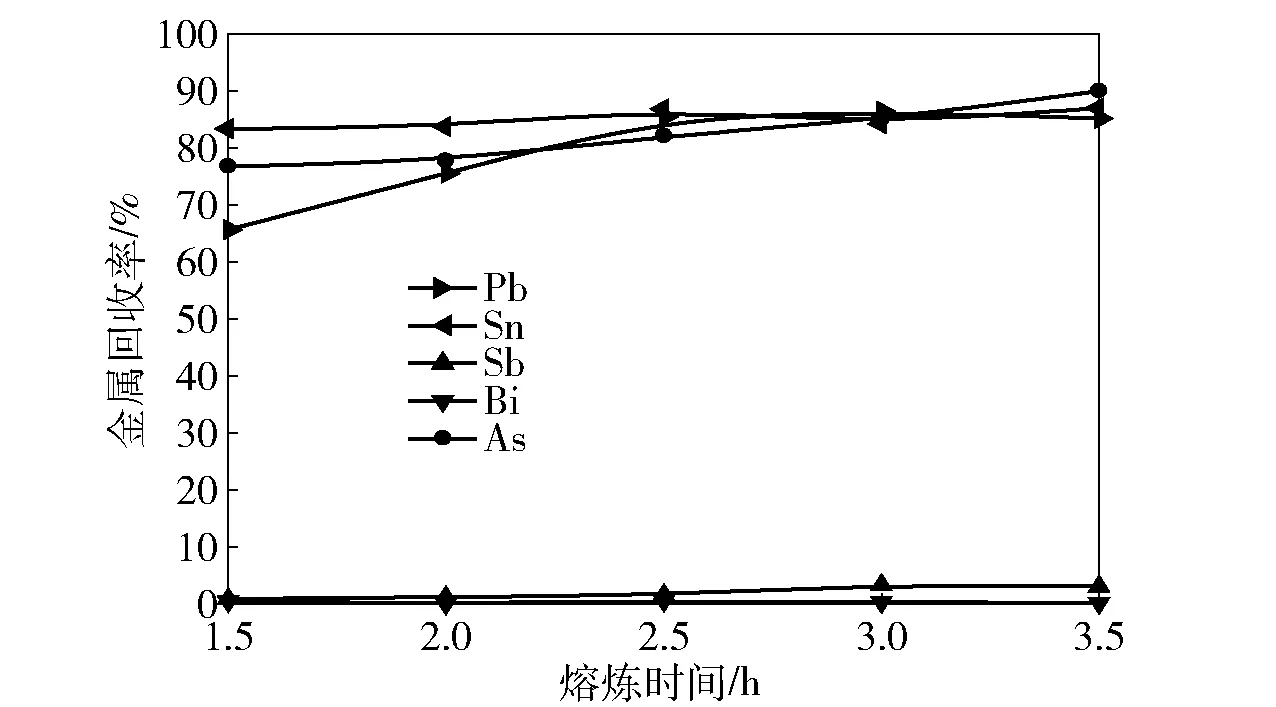
图7 熔炼时间对分银渣中金属回收率的影响
由图7可知,随着熔炼时间的增加,Pb、As的回收率逐渐升高,且相对于Sn的回收率曲线升高比较明显;Sb与Bi的回收率均在5%以下且增长缓慢,尤其是Bi的回收率几乎为0。熔炼时间超过2.5 h后,Pb、Sn的回收率基本不变,As的回收率缓慢增加。产生此种现象的原因是:刚开始反应处于扩散控制区,随时间的延长,反应过渡到化学反应控制区,再延长时间对回收率的影响不大。因此,选择熔炼时间2.5 h比较合适,此时的Pb、 Sn的回收率分别达到了85.54%、86.92%。
2.3 熔融盐用量的影响
2.3.1 NaOH用量的影响
选取球磨后的分银渣10 g,在NaNO3用量20 g,熔炼温度700 ℃,熔炼时间2.5 h,浸出温度80 ℃,浸出时间40 min,液固比6∶1,搅拌速度为450 r/min的条件下进行试验,考察NaOH用量对金属回收率的影响,结果如图8所示。

图8 NaOH用量对分银渣中金属回收率的影响
由图8可知,随NaOH用量的增加,Pb、As的回收率变化曲线上升很快,Sn的回收率有所下降,Sb与Bi的回收率基本不变且很低。NaOH用量超过40 g后,Pb的回收率增长缓慢,说明NaOH用量的增加对Pb的浸出有利,使更多的Pb参与反应进入溶液中,而随着Pb与碱反应的加强,Sn的浸出受到一定的抑制。综合考虑,选择NaOH用量45 g比较合适,此时的Pb、 Sn的回收率分别达到了86.16%、66.08%。
2.3.2 NaNO3用量的影响
选取球磨后的分银渣10 g,在NaOH用量45 g,熔炼温度700 ℃,熔炼时间2.5 h,浸出温度80 ℃,浸出时间40 min,液固比6∶1,搅拌速度为450 r/min的条件下进行试验,考察NaNO3用量对金属回收率的影响,结果如图9所示。
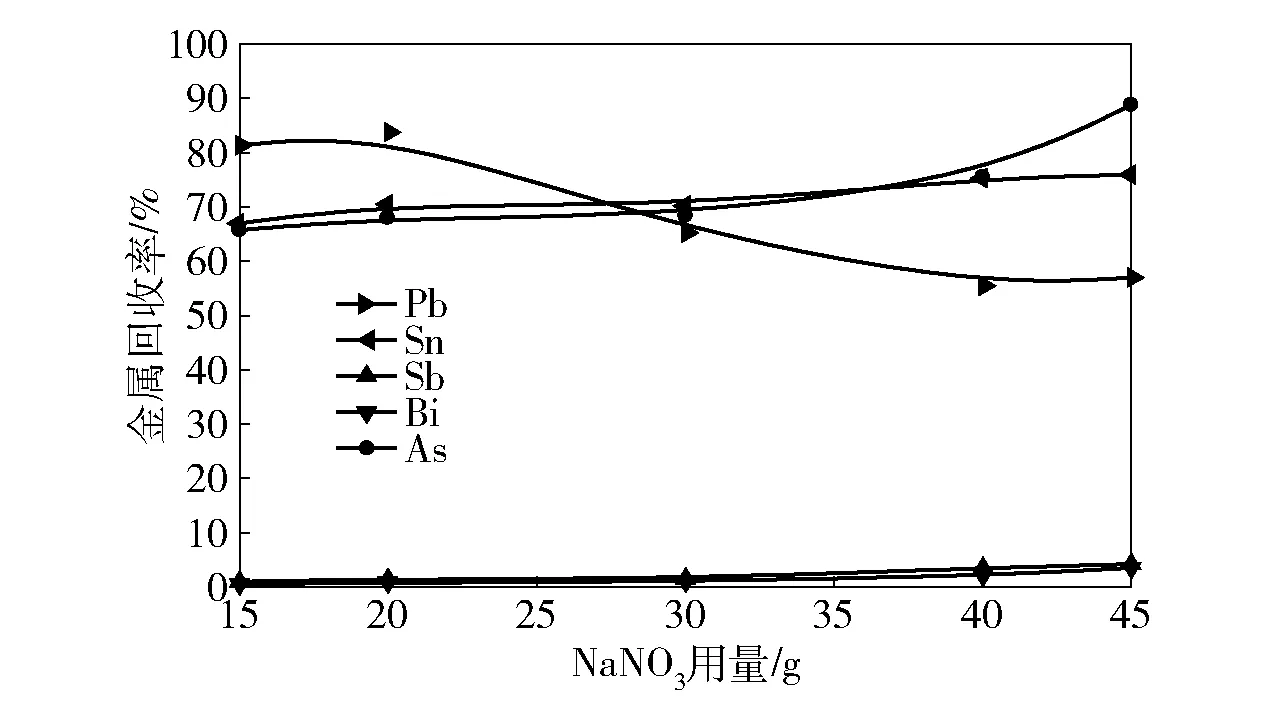
图9 NaNO3用量对分银渣中金属回收率的影响
由图9可知,随着NaNO3用量的增加,Pb的回收率曲线下降很快,Sn、As的回收率曲线逐渐上升;Sb与Bi的回收率仍然在5%以下且增长缓慢。这是因为在熔炼过程中随着NaNO3用量的不断增加,NaNO3与Pb生成了不溶于水的化合物,导致后续Pb的浸出受到抑制,但对Sn的浸出有利。综合考虑,NaNO3用量选择20 g为宜,即较优的熔融盐配比为NaOH∶NaNO3=45∶20,此时的Pb、Sn的回收率分别达到了83.77%、70.5%。
2.4 浸出温度的影响
选取球磨后的分银渣10 g,在NaOH用量45 g,NaNO3用量20 g,熔炼温度700 ℃,熔炼时间2.5 h,浸出时间40 min,液固比6∶1,搅拌速度为450 r/min的条件下进行试验,考察浸出温度对金属回收率的影响,结果如图10所示。

图10 浸出温度对分银渣中金属回收率的影响
由图10可知,随着浸出温度的增加,Pb、Sn、As、Sb、Bi的回收率均缓慢增加;当浸出温度从50 ℃上升到90 ℃时, Pb的回收率从60.32% 增加到78.66%,Sn的回收率从78.69% 增加到86.73%。产生此种现象的原因是:浸出温度的提高,可以强化浸出时的传质传热过程,使熔炼产物中易溶于水溶液的物相反应速度加快;而难溶于水溶液的含Pb物相反应速度较慢,需要更高的温度才能加速进行。 Sb和Bi的回收率仍然在5%以下。因此,选择80 ℃为最佳浸出温度。
2.5 浸出时间的影响
选取球磨后的分银渣10 g,在NaOH用量45 g,NaNO3用量20 g,熔炼温度700 ℃,熔炼时间2.5 h,浸出温度80 ℃,液固比6∶1,搅拌速度为450 r/min的条件下进行试验,考察浸出时间对金属回收取率的影响,结果如图11所示。
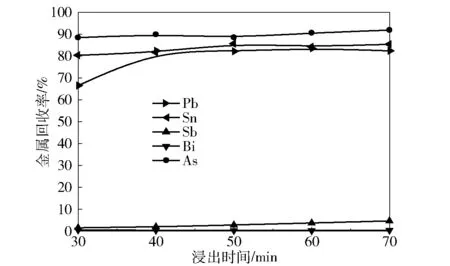
图11 浸出时间对分银渣中金属回收率的影响
由图11可知,随浸出时间的延长,除了Pb回收率有稍微的增加外,其他金属的回收率增加不明显; 当浸出时间从30 min延长到40 min时,Pb的回收率从66.52%增加到85.23%,Sn的回收率增加不明显,Sb和Bi的回收率仍然在5%以下。因此,选择40 min为最佳浸出时间,此时Pb、Sn的浸出率最大。
2.6 液固比的影响
选取球磨后的分银渣10 g,在NaOH用量45 g,NaNO3用量20 g,熔炼温度700 ℃,熔炼时间2.5 h,浸出温度80 ℃,浸出时间40 min,搅拌速度为450 r/min的条件下进行试验,考察液固比对金属回收率的影响,结果如图12所示。由于Bi的回收率为0,不再分析。
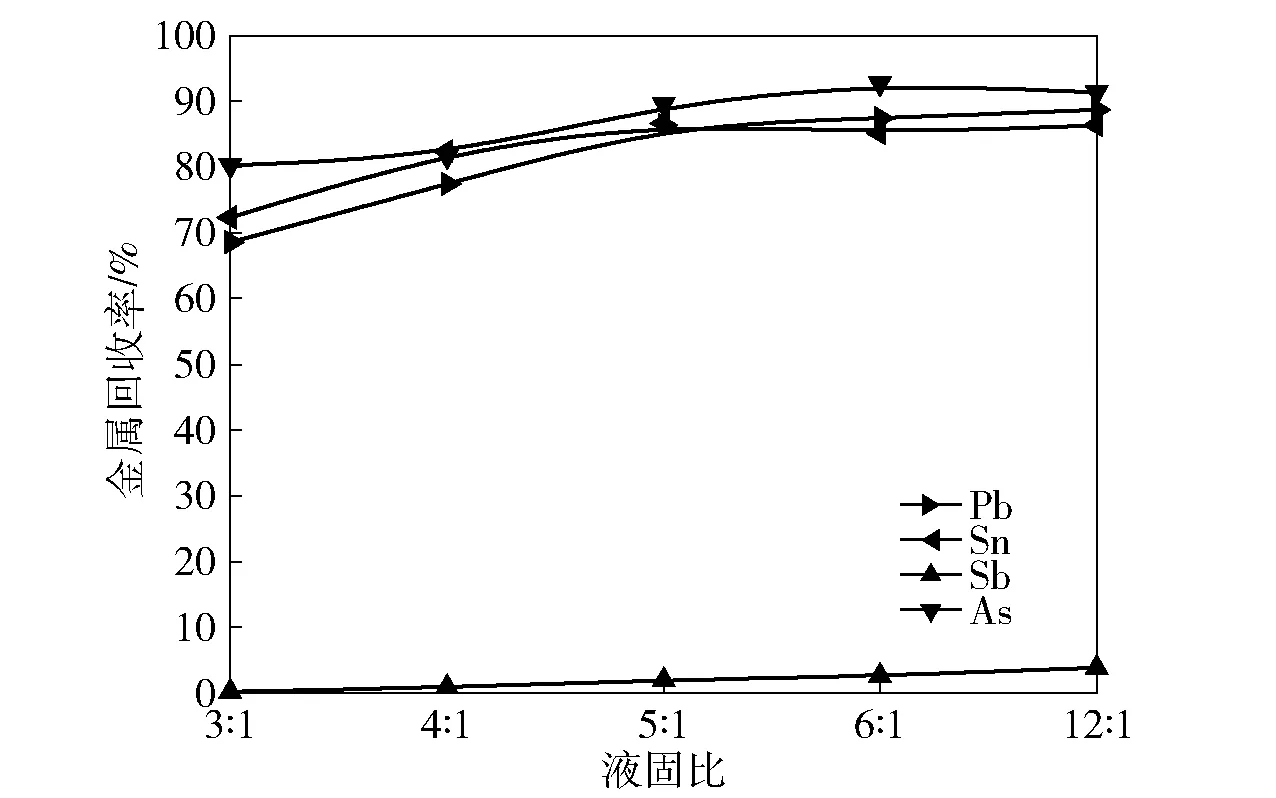
图12 液固比对分银渣金属回收率的影响
由图12可知,随着液固比的增加,Pb、Sn、As、Sb的回收率均有所增加;当液固比从3∶1增加到6∶1时,Pb、 Sn的回收率分别达到了88.73%、86.38%,但液固比大于6∶1时, Pb、Sn的浸出率不再增加,Sb的回收率仍然在5%以下。考虑到液固比太高,溶液中金属离子浓度会降低,因此,选择6∶1为最佳液固比。
2.7 优化试验的结果
在NaOH、NaNO3和分银渣的配比为45∶20∶10,熔炼温度700 ℃、熔炼时间2.5 h、浸出温度80 ℃、浸出时间40 min、液固比6∶1的最优条件下,采用NaOH- NaNO3熔融盐法对分银渣中Pb、Sn、Sb、Bi进行回收试验, Pb、 Sn的回收率分别达到83.77%、86.92%, 98%的Sb、99%的Bi进入过滤渣中。这说明在该优化工艺条件下,主体金属Pb、Sn的回收率比较稳定。
3 结论
采用NaOH- NaNO3熔融盐法分离分银渣,重点分析了分银渣中Pb、Sn和Sb、Bi的回收,确定了较优的工艺条件为NaOH、NaNO3和分银精矿的配比为45∶20∶10,熔炼温度700 ℃、熔炼时间2.5 h、浸出温度80 ℃、浸出时间40 min、液固比6∶1。
在上述条件下,分银精矿中Pb、Sn回收率分别达到了83.77%、86.92%,98%以上的Sb和Bi进入过滤渣里,为后续提取浸出液中Pb、Sn与浸出渣中Sb、Bi提供了有利条件。

