急性卒中患者住院期间感染的临床特征及危险因素分析
程实,李静,郭军平,胡爱香,于鑫玮,韩玮,梁瑛,张越巍,冀瑞俊
目的 探讨急性卒中患者住院期间感染的临床特征及危险因素,为制订感染预防策略提供思路。
方法 连续纳入2019年6月-2021年6月首都医科大学附属北京天坛医院神经内科收治的缺血性卒中(ischemic stroke,IS)、脑出血(intracerebral hemorrhage,ICH)及蛛网膜下腔出血(subarachnoid hemorrhage,SAH)患者,对其临床资料进行回顾性分析。根据患者住院期间是否发生感染分为感染组和非感染组,比较2组的临床特征、感染部位及时间分布,采用单因素及多因素logistic回归分析感染的危险因素。
结果 共纳入2884例急性卒中患者,男性2138例(74.1%),IS 2049例,ICH 531例,SAH 304例。426例患者住院期间出现感染,发生率为14.8%,感染发生的中位时间为卒中后4(1~7)d。IS、ICH及SAH患者的感染率分别为10.8%、21.3%和29.9%,呈逐渐升高趋势。肺脏为急性卒中后感染率最高且最早出现的感染部位。多因素分析显示,年龄增长(OR 1.038,95%CI 1.026~1.050,P<0.001)、合并心力衰竭(OR 2.339,95%CI 1.197~4.572,P=0.013)、慢性阻塞性肺疾病(OR 3.297,95%CI 1.676~6.486,P=0.001)、卒中类型为脑出血(OR 2.162,95%CI 1.548~3.021,P<0.001)或蛛网膜下腔出血(OR 8.271,95%CI 5.591~12.236,P<0.001)、入院NIHSS升高(OR 1.162,95%CI 1.132~1.193,P<0.001)及住院时间延长(OR 1.138,95%CI 1.109~1.168,P<0.001)为急性卒中患者住院期间发生感染的独立危险因素。
结论 感染是急性卒中患者常见的并发症之一,其中肺部感染发生率高且发病时间早。年龄升高、合并心力衰竭或慢性阻塞性肺疾病、神经功能损伤较重的患者感染发生率升高,与IS相比,ICH和SAH患者的感染发生率升高。
卒中具有高发病率、高死亡率、高致残率的特点,给患者家庭和社会造成沉重负担[1]。感染是急性卒中最主要的并发症之一,既往研究显示约30%的卒中患者合并不同程度的感染,对其生存和康复造成不利影响[2-3],因此积极预防和科学管理卒中后感染具有重要临床价值。然而既往文献中关于不同卒中类型感染特征及时间分布的研究并不充分,本研究回顾性分析急性卒中患者住院期间的临床资料,探讨感染的临床特征及其危险因素,为预防卒中后感染提供依据。
1 对象与方法
1.1 研究对象 回顾性连续纳入2019年6月-2021年6月在首都医科大学附属北京天坛医院神经内科住院治疗的急性卒中患者为研究对象。对纳入患者的临床资料和感染情况进行统计,并根据患者住院期间是否发生感染分为感染组和非感染组。
纳入标准:①年龄≥18岁;②卒中类型为缺血性卒中(ischemic stroke,IS)、脑出血(intracerebral hemorrhage,ICH)和蛛网膜下腔出血(subarachnoid hemorrhage,SAH),并经头颅CT和(或)MRI检查证实;③发病至入院时间≤7 d。排除标准:①其他卒中类型;②卒中发病前已存在感染;③病历资料不完整。
1.2 诊断标准 IS、ICH及SAH的诊断标准分别参照《中国急性缺血性脑卒中诊治指南2018》[4]、《中国脑出血诊治指南(2019)》[5]及《中国蛛网膜下腔出血诊治指南2019》[6]。目前尚无急性卒中后感染的统一诊断标准,本研究中各部位感染诊断标准参照卫生部2001版《医院感染诊断标准(试行)》[7],根据病历记录中的临床诊断报告(如有病原学诊断最佳)诊断,包括肺部感染、泌尿系统感染、中枢神经系统感染以及其他部位感染(如败血症、消化系统感染等)。
1.3 临床资料收集 收集患者临床资料,包括①人口学信息:年龄及性别;②卒中危险因素:吸烟、饮酒、高血压、糖尿病、脂代谢紊乱、心房颤动、冠心病及既往卒中;③合并疾病:心力衰竭、心脏瓣膜病、周围动脉疾病、慢性阻塞性肺疾病、肝功能不全、消化性溃疡、胃肠出血、肾功能不全、关节炎、恶性肿瘤、免疫性疾病等;④脑血管病特征信息:卒中类型、此次发病前mRS评分、入院时NIHSS及GCS;⑤住院时间;⑥住院期间感染部位:肺部感染、泌尿系统感染、中枢神经系统感染、其他部位感染,以及感染时间。
1.4 统计学方法 采用SPSS 25.0软件对数据进行统计分析。计数资料用例数和率(%)表示,采用χ2检验或Fisher精确检验进行组间比较;服从正态分布的计量资料用表示,采用独立样本t检验比较组间差异;偏态分布的计量资料用M(P25~P75)表示,采用Mann-WhitneyU检验比较组间差异。以是否发生感染为因变量,将单因素分析中P<0.05的变量作为自变量纳入多因素logistic回归方程,采用后退法,分析感染的独立危险因素。另外,分别按卒中类型和感染部位分层,计算感染率及感染发生时间,采用χ2检验比较组间感染率,采用Kruskal-Wallis非参数检验比较感染发生时间,对差异有统计学意义的变量采用Bonferroni法进行两两比较。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 本研究共纳入2884例急性卒中患者,年龄19~94岁,平均59.0±12.8岁,男性2138例(74.1%),女性746例(25.9%)。IS 2049例(71.1%),ICH 531例(18.4%),SAH 304例(10.5%)。426例患者住院期间出现感染,2458例患者住院期间未发生感染。
感染组平均年龄,合并心房颤动、冠心病、心力衰竭、慢性阻塞性肺疾病、肝功能不全、消化性溃疡、肾功能不全、关节炎的比例,卒中类型中脑出血和蛛网膜下腔出血的比例,卒中前mRS≥3分的比例,入院NIHSS以及住院天数等指标均高于非感染组;男性比例,卒中类型中缺血性卒中的比例及入院时GCS分值低于非感染组,差异有统计学意义。其余变量在2组间的差异无统计学意义(表1)。
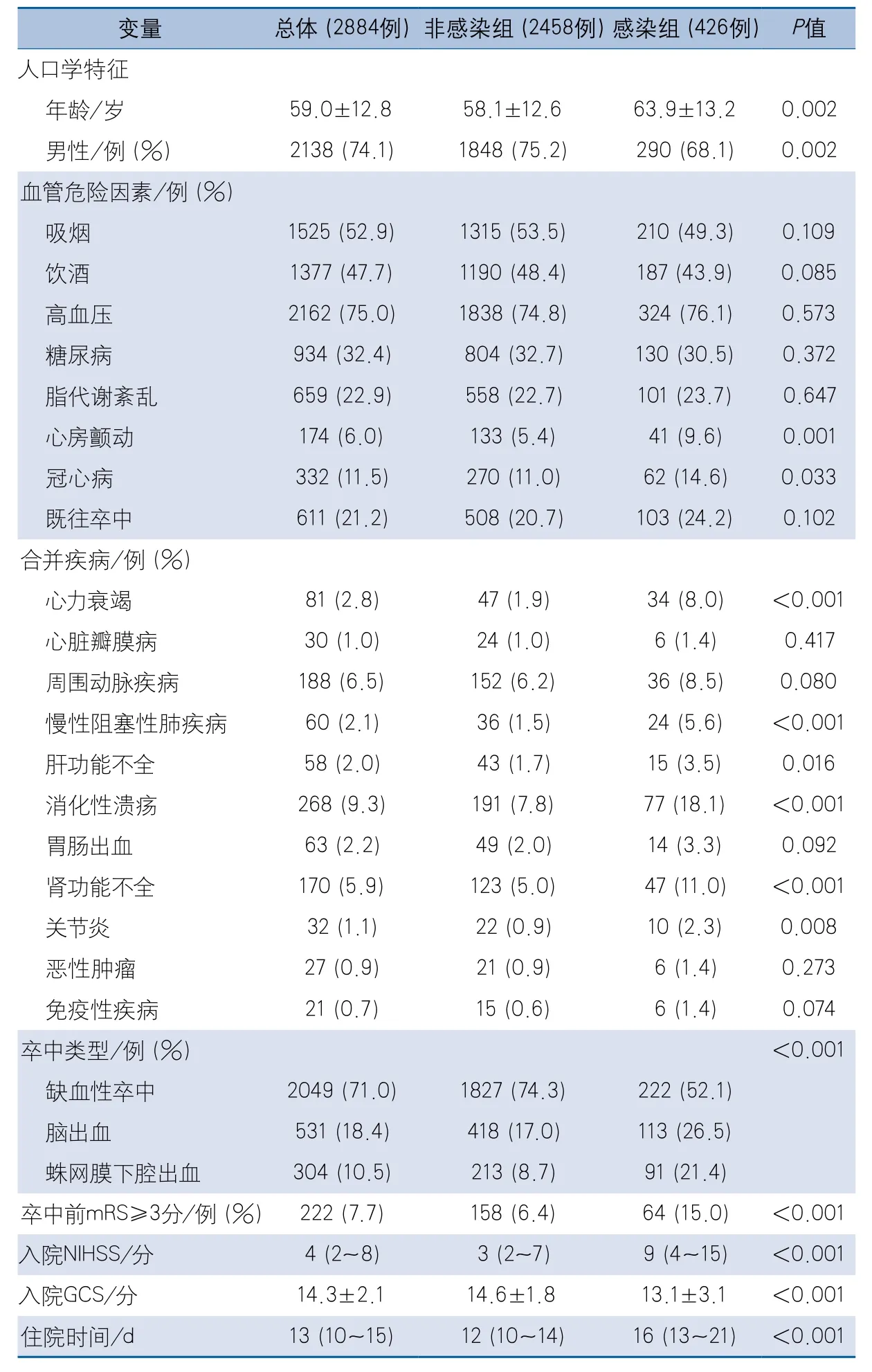
表1 感染组和非感染组临床资料比较
2.2 住院期间发生感染的多因素分析 多因素logistic回归分析结果显示,年龄增长、合并心力衰竭、慢性阻塞性肺疾病、卒中类型为脑出血或蛛网膜下腔出血、入院NIHSS增加及住院时间延长为急性卒中患者住院期间发生感染的独立危险因素(表2)。
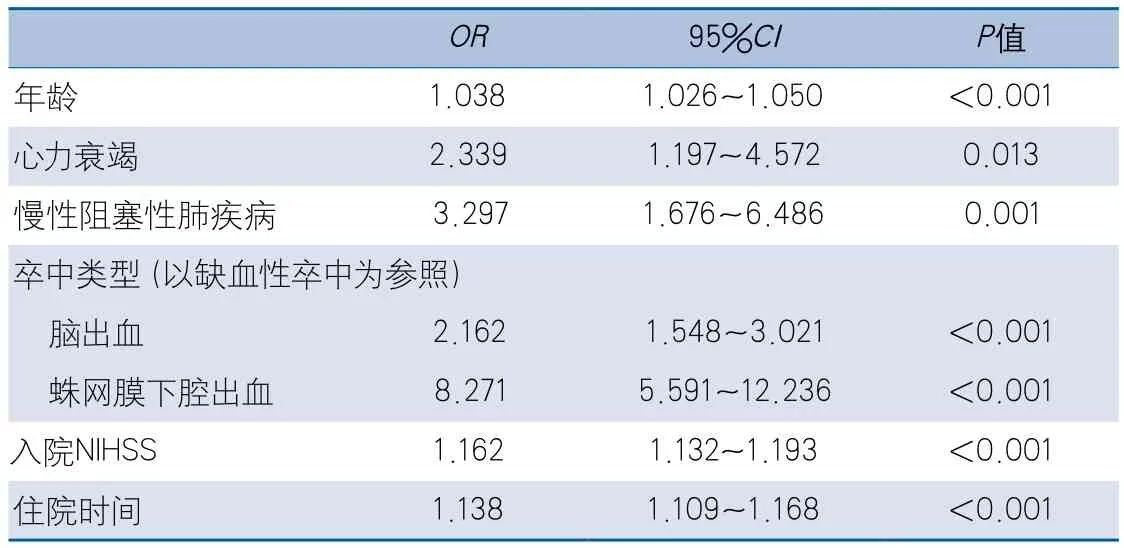
表2 急性卒中患者住院期间发生感染的多因素logistic回归分析
2.3 不同分层的感染率及感染发生时间 本研究中426例急性卒中患者住院期间发生1个或多个部位感染,总体感染率为14.8%,卒中发病至首次出现感染的中位时间为4(1~7)d。
按卒中类型分层,IS、ICH和SAH患者的总体感染率、肺部感染率、中枢神经系统感染率和其他部位感染率呈逐渐升高趋势,差异有统计学意义。两两比较显示。ICH的总体感染率、肺部感染率、中枢神经系统感染率及其他部位感染率高于IS组,SAH的总体感染率、中枢神经系统感染率高于IS和ICH,肺部感染率高于IS。IS、ICH和SAH患者首次感染发生时间和肺部感染发生时间的差异也具有统计学意义,两两比较显示,ICH的首次感染时间及肺部感染发生时间均早于IS组,差异有统计学意义(表3)。
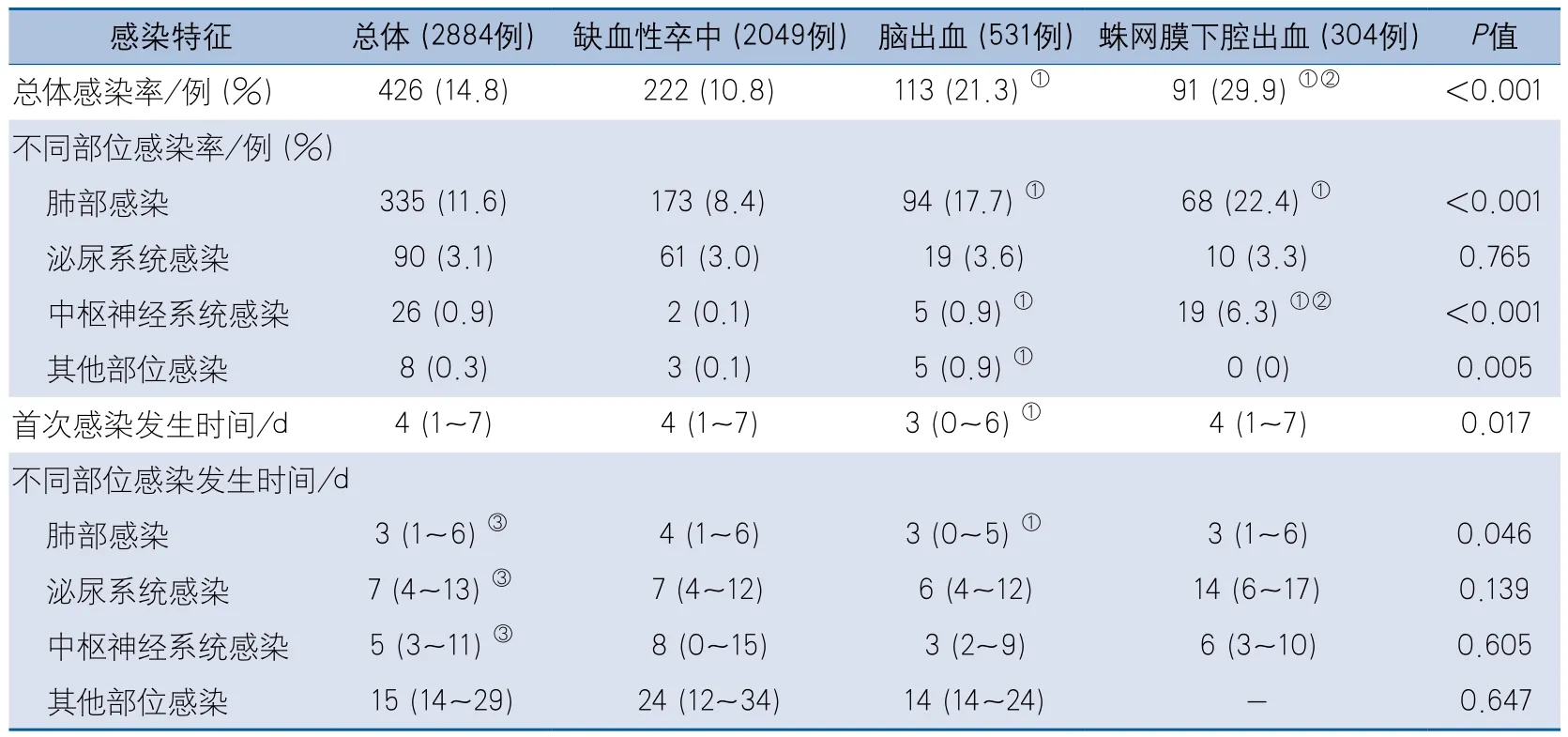
表3 不同分层的感染率及感染发生时间分析
按感染部位分层,感染率由高到低的部位依次为肺部、泌尿系统、中枢神经系统和其他部位。肺部感染出现时间最早,且肺部感染、泌尿系统及中枢神经系统感染发生均早于其他部位感染,差异有统计学意义(表3)。
3 讨论
感染是急性卒中最主要的并发症之一,与患者的不良预后密切相关。本研究结果显示,急性卒中患者住院期间的感染发生率为14.8%,对不同卒中类型分别进行统计后发现,IS、ICH及SAH患者卒中后感染的发生率分别为10.8%、21.3%和29.9%,呈逐渐升高趋势,与《中国卒中报告2019(中文版)》的数据趋势一致[8]。结果提示出血性卒中虽在卒中类型中的比例不高,但住院期间更易出现感染并发症。对不同类型卒中患者进行早期感染危险因素评估,进而根据患者所处的不同风险等级,针对性地制订诊疗和护理方案,具有重要的临床意义。
本研究结果显示,肺部感染为急性卒中患者住院期间最主要的感染,其次为泌尿系统感染,少数患者出现2个及以上部位感染,与既往文献结果类似[9]。有证据表明,急性卒中引起的卒中诱导的免疫抑制综合征(stroke-induced immunosuppression syndrome,SIDS)可抑制细胞免疫功能,使机体防御能力下降,感染风险增加[10]。此外,急性卒中患者发病后通常伴有不同程度的意识障碍、吞咽障碍及肢体功能障碍,均可增加误吸风险,引起肺部感染的发生[11]。卒中患者早期出现的尿储留或尿失禁可能是引发尿路感染的重要原因[12]。另一方面,导尿管留置等侵入性操作及导尿管本身导致的污染,可直接诱发尿路感染,且导尿管留置时间越长,发生尿路感染的风险越高[13]。
本研究中,SAH患者的总体感染率及中枢神经系统感染率显著高于其他2种卒中类型。手术干预是目前治疗SAH的有效手段,但同时也面临感染、脑血管痉挛、再出血、脑积水等术后并发症的风险。开颅手术使颅内开放与外界相通,可能导致致病菌直接进入颅内,手术时间长、有创操作多等因素都可能增加患者术后感染的风险[14]。另外,全身其他部位的炎症也可能通过循环系统蔓延至颅内。何双英等[15]的研究显示,意识障碍和术后入住重症监护病房是SAH患者医院感染的独立危险因素。
既往关于卒中患者感染发生时间的报道较少。孙悦等[16]的研究发现,在IS患者中,卒中发病至肺炎确诊的中位时间为4 d,结合卒中相关性肺炎入院时血白细胞计数已呈明显升高趋势,提示卒中相关性肺炎高发于IS发病4 d内。本研究中总体感染发生的中位时间为卒中后4(1~7)d,此外,本研究还对不同卒中类型及不同部位的感染时间分布进行了分层研究,发现肺部感染为卒中后最早出现的感染,ICH患者出现肺部感染的时间显著早于IS患者。肺部感染发生率高且发病时间早,是不同卒中类型患者在院期间诊疗和康复的共同挑战,因此早期肺部感染危险因素评估及早期干预尤为关键。
本研究多因素分析显示,年龄增长、合并心力衰竭、慢性阻塞性肺疾病、卒中类型为脑出血或蛛网膜下腔出血、入院NIHSS增加及住院时间延长为急性卒中患者住院期间发生感染的独立危险因素。老年卒中患者脏器功能及机体防御能力下降,营养状况欠佳,且多伴有各种基础疾病,因此面临更高的感染风险。心力衰竭可导致不同程度的肺淤血和肺水肿,肺毛细血管通透性增加,使肺脏的清除能力和抗感染能力降低[17],而肺部感染可进一步加重或诱发心力衰竭,形成恶性循环,因此积极控制心力衰竭和预防感染这两方面均尤为关键。慢性阻塞性肺疾病患者的气道长期处于慢性炎症状态,肺功能下降,痰液积聚在肺里不易排出,极易发生肺部感染。Szylińska等[18]的研究发现,急性缺血性卒中合并慢性阻塞性肺疾病患者出现肺部感染、心力衰竭、心房颤动等心肺并发症的风险显著高于没有合并慢性阻塞性肺疾病的患者。NIHSS是评估卒中患者神经功能缺损严重程度的重要指标,有研究显示,入院时NIHSS升高与卒中后感染风险升高相关[19],本研究结果也显示NIHSS升高是卒中患者住院期间感染的独立危险因素。
本研究连续纳入住院患者的临床数据进行分析,样本量较大,因此结果具有一定代表性,此外,本研究综合分析了IS、ICH及SAH 3种不同卒中类型人群的感染特征及时间分布规律,为临床实际工作和预防策略制订提供了参考依据及思路。本研究尚存在一定不足。首先,本研究未对患者进行长时间随访以探究感染并发症对卒中患者长期预后的影响;其次,由于败血症、消化系统感染等其他部位感染例数较少,未做深入分析;再次,本研究为单中心研究,可能存在选择偏倚。后续可进行前瞻性的多中心登记研究来弥补研究中回顾性数据、无随访数据、代表性不足及样本量有限的问题,以期为临床提供更有力的数据支持,降低卒中后感染的发生率,改善患者预后。

