壳聚糖引发对盐胁迫下水稻种子萌发及幼苗生长的影响
何 昊,李丹丹,潘非凡,吴 泽,杨书运*
(1.安徽农业大学 资源与环境学院,安徽 合肥 230036;2.农业部合肥农业环境科学观测实验站,安徽 合肥 230036)
【研究意义】土壤盐渍化是限制作物生长及产量的重要逆境胁迫之一,全世界约20%的耕地和33%的灌溉农田受到盐胁迫的影响,预计到2050年,50%以上的耕地面积将出现盐碱化[1-3]。中国盐碱地面积约9 913 万hm2,是土地盐碱化最为严重的国家之一[4]。水稻是三大主要粮食作物之一,而水稻属于中度盐敏感作物,易受盐胁迫造成作物减产及品质下降,且苗期是最易受胁迫的时期之一[5-6]。在土壤盐渍化风险增加的大趋势下,深入开展水稻耐盐性的研究,充分保障盐碱地水稻种植,对于保障粮食安全具有重要意义。【前人研究进展】种子引发(Seed priming)是一项广泛应用的播种前处理技术,通常做法是采用引发剂处理种子,控制种子缓慢吸收水分并停留在吸涨的第二阶段,同时防止胚根伸出[7]。研究表明,引发可有效打破种子的休眠,促进细胞膜的修复,增加种子活力,提高干旱、重金属、高温和盐害等胁迫下的幼苗抗逆性[7-9]。引发技术在水稻上已有所应用,孙园园等[10]研究表明,水分胁迫下,利用聚乙二醇(PEG)引发可提高水稻幼苗形态指标及抗氧化酶活性,促进相关糖代谢;Ali 等[11]利用硝酸钾(2.5%和5%)及二氧化硅(2.5%和5%)溶液引发,显著提高水稻种子萌发指标、幼苗活力、可溶性蛋白以及蔗糖含量,增强水稻抗旱性。引发显著提高水稻抗胁迫能力,机理为引发增加了逆境防御类、能量代谢类等蛋白合成含量和丰度,使种子获得“逆境记忆(stressful memory)”进而提高抗逆性[12]。利用抗坏血酸、氯化钙及β-氨基丁酸作为引发剂可提高苗期水稻幼苗活性氧(ROS)的清除能力,保护细胞蛋白质以提高种子的萌发率和幼苗活力,提高水稻的耐盐性[13-14]。因此,选取适当的引发剂对于提高水稻幼苗的耐盐性有着广泛的应用前景。【本研究切入点】壳聚糖(chitosan,CTS)是甲壳素脱乙酰化后得到的一种聚氨基葡萄糖,作为具有潜力的非生物胁迫抗性诱导剂,在农业方面广泛应用[15-16]。干旱胁迫下,利用CTS处理显著提高了向日葵叶片叶绿素、可溶性蛋白和游离氨基酸含量,激发抗氧化防御系统[17];水分胁迫下,叶面喷施CTS 可有效提高辣椒谷胱甘肽(GSH)及抗坏血酸(AsA)的含量,降低MDA 的含量,因此CTS 可通过调节能量合成来达到缓解逆境胁迫[18];利用0.5 g/L 壳聚糖包衣能有效提高油菜种子及幼苗的耐盐性[19]。且有研究得出,盐胁迫下外源施加壳聚糖可提高玉米、小麦作物的抗氧化酶活性,激活其防御机制,更好地抵御盐胁迫[20-21]。然而,利用CTS 引发对盐胁迫下水稻种子萌发及幼苗生长缺乏系统性的研究,有必要探索最适宜质量浓度的CTS 来缓解盐胁迫。【拟解决的关键问题】,本研究以皖稻16 为材料,采用不同质量浓度CTS溶液进行引发,对其盐胁迫下水稻种子萌发及幼苗生长进行分析,为应对盐胁迫制约水稻种植提供理论依据和技术参考。
1 材料与方法
1.1 试验地点以及供试材料
本试验于2021年在安徽农业大学资源与环境学院土壤学实验室进行。供试水稻品种为皖稻16,该品种穗大且成穗率高,生育期约150 d。供试壳聚糖药剂为生物技术级,利用2%的醋酸溶解,然后再分别稀释成所需质量浓度,调节各质量浓度pH值至6.5左右。
1.2 试验设计
1.2.1 种子引发处理选取均匀饱满的水稻种子,使用0.2%HgCl2消毒10 min,之后用蒸馏水反复冲洗干净。未经引发且无盐胁迫处理记为CK,未引发但有盐胁迫处理记为S-CK;设置6个引发处理,即用纯水及50,100,150,200,250 mg/L CTS溶液(分别以S-0,S-50、S-100、S-150、S-200、S-250表示)对水稻种子进行引发,种子质量(g)与溶液体积(mL)比约为1∶3,在25 ℃的发芽箱内引发培养24 h,引发结束后将种子纯水冲洗干净,使用吸水纸吸干表面水分,置于28 ℃的鼓风干燥箱中干燥至原含水量(约为13.3%)。
1.2.2 发芽试验将各处理水稻种子置于平铺有蛭石的标准发芽皿中(规格为12 cm×12 cm×5 cm),分别加入80 mL 的100 mmol/L 的NaCl 溶液,保证蛭石被溶液淹没;各处理重复3 次,每个重复播种30 粒种子,按5行6列均匀摆置。发芽皿放置在28 ℃的光照培养箱中培养,待种子出土后,设定光照4 000 lx,每天光照时长12 h,昼夜温度分别为28 ℃与20 ℃。
1.2.3 测定项目与方法(1)发芽指标。播种后第1天开始,计算以下参数:发芽势=(3天内供试种子发芽总数/供试种子数)×100;发芽率=(7 天内供试种子发芽总数/供试种子数)×100%;发芽指数=∑Gt/Dt(Gt为第t天的发芽数,Dt为相应发芽的天数)。(2)幼苗形态指标。播种后第12天,选取长势一致的水稻幼苗,测量相关的水稻根苗形态指标。将水稻分为地下部分与地上部分,利用天平测量鲜重;并且利用游标卡尺测量水稻的根长、苗长与根直径;利用描形数格法测定水稻单株叶面积。(3)丙二醛以及相关抗氧化酶活性含量。参照王学奎[22]的方法,采用硝基氮蓝四唑(NBT)法测定幼苗叶片超氧化物歧化酶(SOD)活性;愈创木酚法测定过氧化物酶(POD)活性;紫外分光光度计法测定过氧化氢酶(CAT)活性;硫代巴比妥酸(TBA)染色法测定丙二醛(MDA)含量。(4)可溶性糖含量、蔗糖磷酸合成酶(SPS)、蔗糖合成酶(SS)活性的测定参照刘丽杰[23]的方法。
1.3 数据处理与分析
利用Excel 2016软件进行数据处理,采用SPSS 22.0软件进行方差分析。
2 结果与分析
2.1 壳聚糖引发对盐胁迫下水稻种子萌发的影响
由图1和表1可知,盐胁迫明显降低了水稻种子萌发速率,且均显著降低种子发芽率、发芽势和发芽指数(P<0.05),降幅依次分别为12.36%、52.18%和36.99%;利用纯水引发可有效缓解盐胁迫对水稻种子发芽的抑制,而加入各质量浓度CTS溶液引发可进一步缓解盐胁迫,表现为随CTS溶液质量浓度的增加,各项发芽指标呈先升高后下降的趋势。与S-CK相比,各引发处理下水稻发芽指标均达到显著水平(P<0.05)。综合来看,以S-100与S-150处理表现较优,与S-CK相比,发芽率、发芽势和发芽指数分别显著提高12.10%、90.94%和33.57%(S-100)及10.48%、87.29%和37.01%(S-150),且2个处理间无显著差异。

表1 壳聚糖引发对盐胁迫下水稻种子萌发指标的影响Tab.1 Effects of CTS priming on rice seeds germination under salt stress
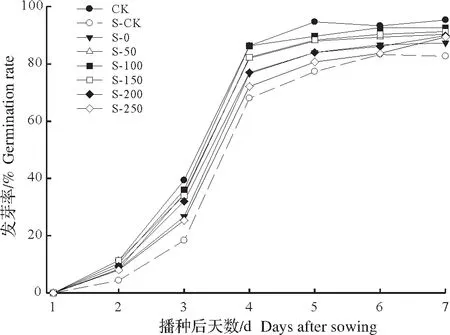
图1 壳聚糖引发对盐胁迫下水稻种子萌发率的影响Fig.1 The effects of CTS priming on the germination rate of rice seeds under salt stress
2.2 壳聚糖引发对盐胁迫下水稻根苗生长的影响
由图2可得,盐胁迫显著降低了水稻幼苗鲜重(35.33%)、苗长(22.14%)和单株叶面积(22.51%)。利用水和各质量浓度CTS 溶液引发可有效缓解盐胁迫对水稻幼苗的抑制作用,且整体表现为随溶液质量浓度的提高先升后降。各处理中以S-100处理缓解幼苗盐胁迫最佳,与S-CK 相比,幼苗鲜重、苗长和单株叶面积分别增加52.32%、20.64%和22.51%,且均与CK 无显著差异(P>0.05);其次为S-150 处理,各幼苗生长指标与S-100 无显著差异,与CK 相比,幼苗鲜重无显著差异,而苗长与单株叶面积则差异显著。
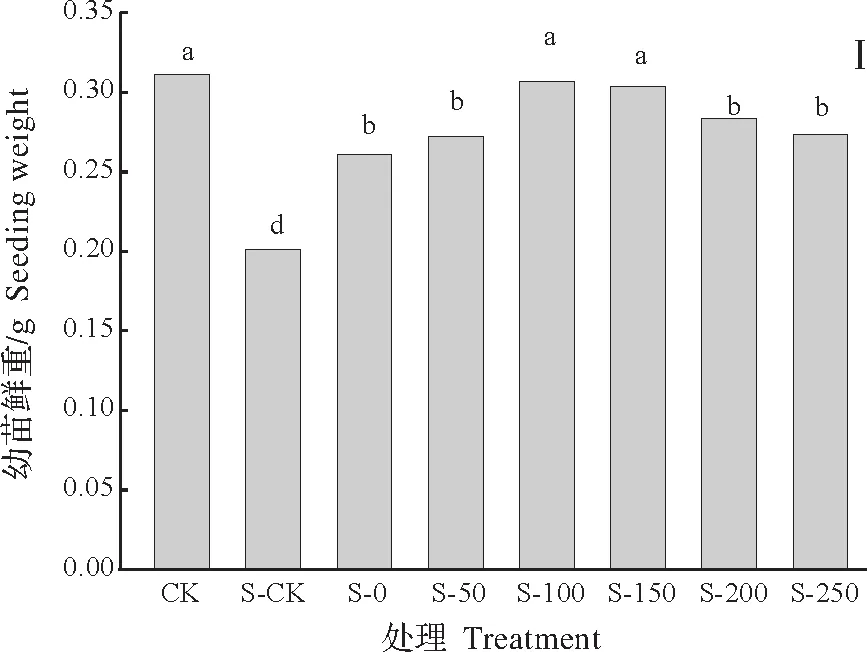

图2 壳聚糖引发对盐胁迫下水稻幼苗生长的影响Fig.2 Effects of CTS priming on the seeding growth of rice under salt stress
由表2 可得,与CK 相比,盐胁迫(S-CK)显著降低了水稻幼苗根系的生长,根直径、根数、根长和根系鲜重分别降低了22.90%、19.36%、39.94%和32.54%。利用纯水以及各质量浓度CTS溶液引发均能不同程度促进水稻根系的生长,其中,根系各项指标以S-100处理表现最优,与S-CK 相比,根直径、根数、根长和根系鲜重分别提高了23.65%、10.72%、38.31%和29.52%,且根系直径与CK 无显著差异,其次为S-150处理。而过高质量浓度的CTS溶液引发对于缓解盐胁迫效果相对较低,且随质量浓度增加存在下降的趋势。

表2 壳聚糖引发对盐胁迫下水稻根系生长的影响Tab.2 Effect of CTS priming on the growth of rice roots under salt stress
2.3 壳聚糖引发对盐胁迫下水稻幼苗MDA含量以及抗氧化酶活性的影响
由表3可得,与CK相比,盐胁迫(S-CK)导致水稻幼苗叶片MDA含量显著增加了67.41%;与S-CK相比,利用纯水以及各质量浓度CTS 溶液引发均显著降低了水稻叶片中MDA 含量,降低幅度为15.53%~28.79%,其中以S-100、S-150与CK相比差异最小,但仍显著(P<0.05)。
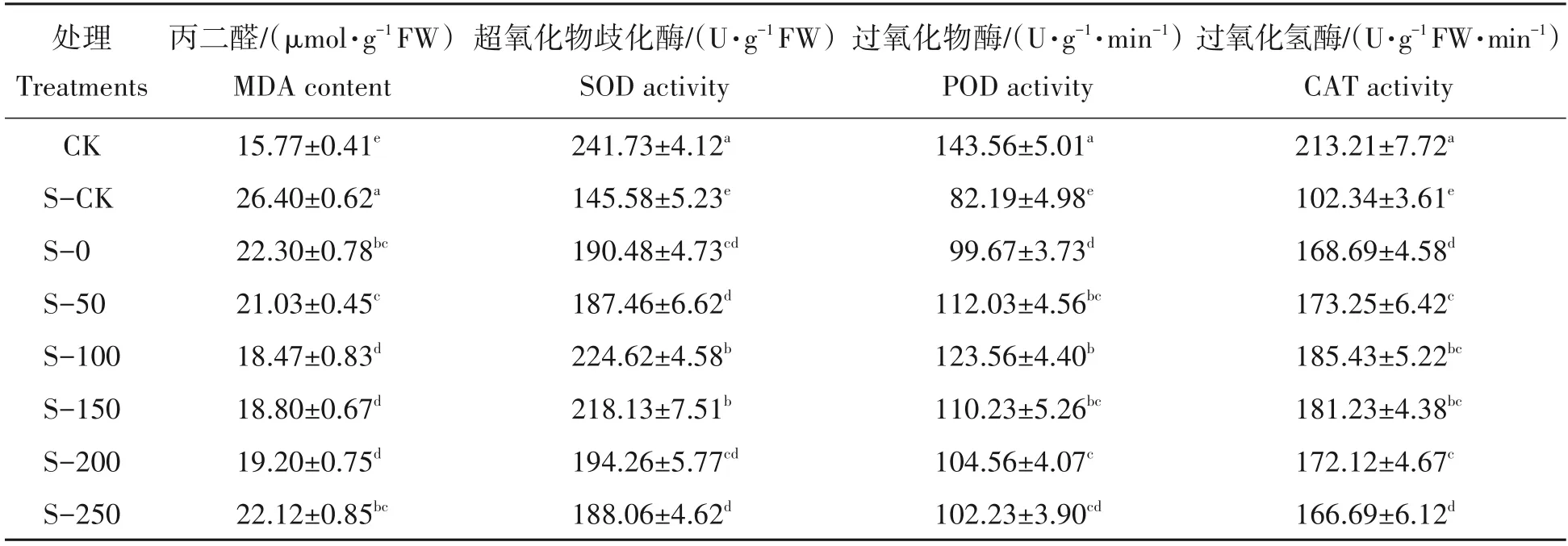
表3 壳聚糖引发对盐胁迫下水稻叶片MDA含量及抗氧化酶活性的影响Tab.3 Effects of CTS priming on MDA content and antioxidant enzyme activities of rice seedling leaves under Nacl stress
与MDA 表现趋势相反,水稻幼苗叶片SOD、POD 和CAT 活性在盐胁迫下均显著降低,分别为39.74%、42.75%与52.00%。与S-CK相比,随着CTS引发质量浓度的增加,叶片中3种抗氧化酶活性均大致呈先升高后降低趋势,SOD、POD 和CAT 活性增加幅度分别为28.89%~53.99%、21.27%~50.33%以及62.88%~81.19%。综合来看,以S-100 最佳,与S-CK 相比,SOD、POD 和CAT 活性分别提高53.99%、50.33%与81.19%,其次为S-150 处理,3 种抗氧化酶活性依次提高50.17%、34.12%与77.09%,但各处理的抗氧化酶活性与CK相比仍差异显著。
2.4 壳聚糖引发对盐胁迫下水稻幼苗可溶性糖含量及相关蔗糖酶活性的影响
由图3 可得,与CK 相比,盐胁迫(S-CK)显著提高水稻幼苗叶片的可溶性糖含量(38.47%);与S-CK相比,利用纯水以及各质量浓度CTS引发处理会进一步增加可溶性糖含量,增加幅度为61.74%~94.55%;其中以S-100 增幅最大,为94.55%,其次为S-150与S-50,增幅分别为87.95%与87.00%,3 组处理之间无显著差异。

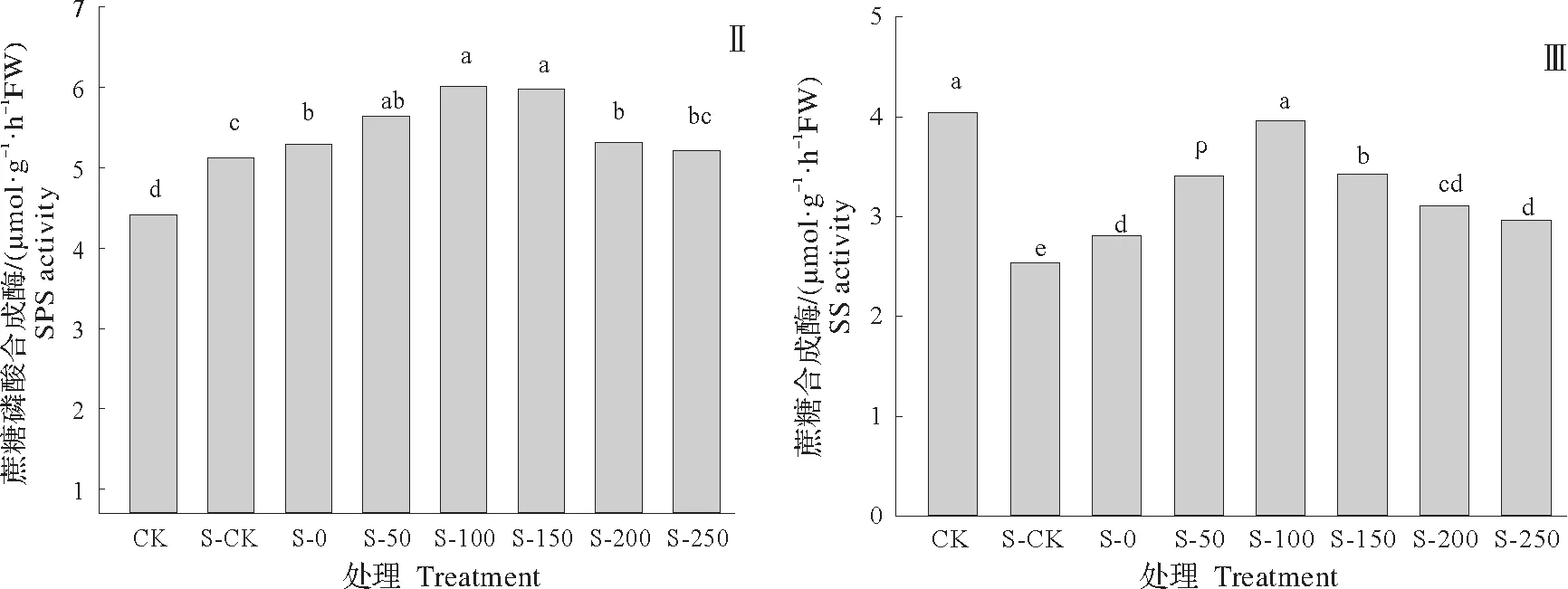
图3 壳聚糖引发对盐胁迫下水稻幼苗叶片可溶性糖和蔗糖代谢酶活性的影响Fig.3 Effects of CTS priming on soluble sugar content,SS and SPS activity of rice seedling leaves under NaCl stress
盐胁迫(S-CK)显著增加水稻幼苗蔗糖磷酸合成酶(SPS)活性,增幅为15.84%,而蔗糖合成酶(SS)活性则显著下降,降幅为37.19%。与S-CK 相比,各引发处理提高了水稻幼苗SPS 与SS 活性,增加幅度分别为1.76%~17.38%与10.54%~55.74%。其中,S-100 与S-150 处理提升SPS 活性最大,分别为17.38%与16.80%,且2 个处理之间无显著差异;以S-100 提升SS 活性最高,为55.74%,且与CK 相比无显著差异。
3 讨论与结论
根系是作物吸收水分以及矿质的重要器官,盐胁迫导致水稻根系生长指标显著下降,表明盐离子通过根系吸收进入到植株体内,存在于细胞液泡中,阻碍水稻的地上部分的生长[24-25],利用一定质量浓度CTS 溶液对于提高根系直径、根数、根长和根系鲜重等关键根系形态指标效果明显,表明CTS 可进入植株体内与盐离子发生螯合作用,以缓解盐胁迫[20]。本研究中,盐胁迫(S-CK)显著降低水稻种子的萌发指标,利用纯水引发可有效缓解盐胁迫对水稻种子发芽的抑制,并且加入各质量浓度CTS 溶液会进一步缓解盐胁迫,促进根苗的生长,其中以100 mg/L CTS 溶液引发效果更佳。表明利用纯水以及CTS溶液引发可有效提高种子发芽率,缓解逆境胁迫,这与相关学者利用CTS 提高绿豆、花生以及玉米的抗逆性研究结果一致[16,20,26]。
植株体内MDA 含量是评估细胞膜受逆境胁迫损伤程度的重要指标,MDA 含量越高,表明植物细胞膜质过氧化程度高,细胞膜受到的伤害越加严重;盐胁迫导致水稻幼苗积累大量ROS,植株体通过增加SOD、POD 以及CAT 等酶活性,参与到ROS 的清除[27-29]。本研究表明,盐胁迫显著增加水稻幼苗叶片MDA 含量,降低SOD、POD 及CAT 活性,这可能是植物应对逆境胁迫的应激反应[30],利用CTS 引发可提高幼苗抗氧化酶活性,表明CTS 作为一类常见的抗氧化剂,可参与到植株体ROS 的清除,降低胁迫对水稻幼苗叶片氧化损伤,保持细胞膜的完整。曲丹阳等[31]研究表明,利用100 mg/L 壳聚糖处理提高了玉米幼苗AsA-GSH 循环速率,显著提高可溶性蛋白含量以及根苗抗氧化酶活性,更好抵御镉胁迫,这与本研究结果相似。此外,与POD 活性相比,CTS 引发提高SOD 与CAT 酶活性效果更佳,可能是由于CTS 引发主要调控SOD 与POD 酶活性基因的表达,以达到抗逆境的目的,这与王聪等[15]对大豆幼苗的研究结果相似。然而随着引发质量浓度的升高,根苗生长、抗氧化酶活性呈下降趋势,因此利用CTS 引发存在一定的质量浓度效应,在今后的研究中针对不同作物,有必要探究最适引发质量浓度以达到植株抗逆效果。
可溶性糖含量与植株体抗逆性呈正相关关系,含量越高,逆境胁迫下失水可能性越低,细胞膜稳定性越强,蔗糖磷酸合成酶(SPS)和蔗糖合成酶(SS)活性与植株体蔗糖合成能力息息相关[32-33]。研究表明,盐胁迫下新麦草、黄芪幼苗可溶性糖含量会明显增加[34-35];外源施加壳聚糖可有效提高小麦幼苗叶片可溶性糖含量,促进生长发育[36],均与本试验结果相似。盐胁迫下,水稻幼苗叶片可溶性糖含量、SPS 活性均显著提高,表明植株体在应对盐胁迫时会产生应激抵御机制,而SS活性则有所降低,是由于盐胁迫阻碍了幼苗正常的呼吸作用,阻碍了正常的糖代谢进程[36]。本研究证实,引发促进可溶性糖含量、SPS与SS活性提高,缓解细胞渗透压,促进蔗糖的合成速率,维持正常的生理活动,提高水稻幼苗抗盐能力。
盐胁迫显著降低水稻种子萌发指标,抑制根苗的生长,影响相关抗氧化酶活性,并阻碍了正常的糖代谢进程。引发剂壳聚糖可提高盐胁迫下水稻种子发芽指标及发芽速率,促进水稻幼苗叶片相关蔗糖酶、抗氧化酶活性,进而提高水稻种子萌发过程中的抗盐胁迫能力,以100 mg/L CTS 溶液引发效果为佳。

