葡萄蒸馏酒香气成分顶空固相微萃取条件优化
孙丽君,刘建学,2,3*,韩四海,2,3,李佩艳,2,3,郭金英,2,3,罗登林,2,3
1(河南科技大学 食品与生物工程学院,河南 洛阳,471023)2(河南省食品原料工程技术研究中心,河南 洛阳,471023) 3(食品加工与安全国家级实验教学示范中心,河南 洛阳,471023)
葡萄蒸馏酒是在20世纪末21世纪初新兴的一种饮料酒[1],是以葡萄为主要原料,经发酵、蒸馏、勾兑而成的,它与世界六大蒸馏酒之一的白兰地的区别在于没有经过橡木桶的贮藏陈酿,大大缩短了生产处理周期,最大程度的保留了酿造葡萄原有的香气特点[2],且价格适中,近年来深受消费者喜爱。
香气是反映葡萄蒸馏酒品质的重要指标[3],也是影响人们选择购买的主要因素。香气成分的分析主要包括香气成分的提取浓缩和分离检测。GC-MS以其可以准确、快速的定性、定量分析的特性已经成为分析酒精饮料挥发性物质最常见的方法[4]。无论使用多么先进的分析方法,将香气物质浓缩富集提取出来是获得理想分析结果的前提[5],固相微萃取技术是一种无溶剂萃取技术[6],与液-液萃取等传统技术相比,快速简便,低成本,自动化且与多种分析系统兼容[7]。顶空固相微萃取(headspace solid-phase microextraction,HS-SPME)作为固相微萃取的一种,在挥发性成分提取中更具有明显的优势[8],此外,通过将最少量、不需要的分子引入分析系统,可以使色谱柱获得更长的寿命[9-10]。本文采取HS-SPME与GC-MS结合对葡萄蒸馏酒中的香气成分进行提取与分析,为了能获得更好的萃取效果,对影响HS-SPME萃取效果的各因素进行优化。
近年来,对葡萄蒸馏酒的相关研究多集中在其发酵过程控制[11-12]、生产工艺优化[13]和不同葡萄品种蒸馏酒香气成分分析[14-15],而对于香气成分萃取条件优化的研究较少,为更好地分析葡萄蒸馏酒中的挥发性香气成分,本文对影响HS-SPME萃取效果的条件进行优化,确定了葡萄蒸馏酒香气成分萃取的较优条件,以期为葡萄蒸馏酒的挥发性香气成分研究提供有益参考。
1 材料与方法
1.1 实验材料
1.1.1 实验材料
酒样(52°),九朝雅宴葡萄蒸馏酒;2-辛醇(色谱纯),上海麦克林生化科技有限公司;NaCl(分析纯),天津化学试剂一厂;顶空瓶(20 mL),北京博赛德科技有限公司。
1.1.2 仪器与设备
TSQ9000气相色谱-三重四级杆串联质谱仪,赛默飞世尔科技公司;萃取手柄、50/30 μm DVB/CAR/PDMS萃取纤维(1 cm),美国Supelco公司;ZNCL-TS磁力搅拌器,巩义市予华仪器有限责任公司。
1.2 实验方法
1.2.1 气相色谱及质谱条件
色谱柱:AT.LZP-930白酒分析专用柱(30 m×0.32 mm,1 μm);进样口温度:250 ℃;升温程序:35 ℃ 保持5 min,然后以3 ℃/min升至60 ℃,再以2 ℃/min 升至135 ℃,最后以4 ℃/min升至220 ℃;载气(He)流速2.0 mL/min,压力30 kPa;不分流。
EI离子源;电子能量70 eV;传输线温度230 ℃;离子源温度240 ℃;采用全扫描模式,扫描的质荷比范围是35~600。
1.2.2 顶空固相微萃取条件
首先,由于三相纤维包含了不同性质的萃取涂层,对酯类、醇类等多种化合物(C3~C20)具有足够的提取能力[16],所以选定萃取纤维为50/30 μm DVB/CAR/PDMS;在20 mL的钳口瓶中加入稀释到一定浓度的葡萄蒸馏酒8 mL、NaCl和磁力转子,密封小瓶,在转速为400 r/min下预热平衡一段时间,插入萃取纤维进行顶空吸附一定时间,最后将其插入GC进样口解析。
1.2.3 单因素试验
以组分分离所得的色谱峰的总峰面积和峰个数为参考指标,选取萃取温度(20、30、40、50、60 ℃)、解析时间(2、4、6、8、10 min)、平衡时间(0、5、10、15、20 min)、萃取时间(10、20、30、40、50 min)、NaCl添加量(0、0.1、0.2、0.3、0.4 g/mL)、乙醇体积分数(5%、10%、15%、20%、25%)进行单因素试验。
1.2.4 响应面优化试验
根据单因素试验结果并考虑到萃取纤维的使用寿命及前处理时间,确定解析和平衡时间,在此基础上以各组分色谱图的总峰面积(Y1)和峰个数(Y2)为响应值,对萃取温度(A)、萃取时间(B)、NaCl添加量(C)、乙醇体积分数(D) 4个单因素进行响应面优化试验。
1.2.5 定性与定量分析
定性分析方法:将样品的质谱图与赛默飞mainlib谱库中的标准谱图进行对比定性,保留匹配度>800的化合物。保留指数(retention index, RI)采用一系列正构烷烃C7~C40计算,具体计算方法[17]如公式(1)所示:
(1)
式中:RIx,待分析化合物的保留指数;n,正构烷烃碳原子数;tx,待分析化合物的保留时间,min;tn,碳数为n的正构烷烃的保留时间,min;tn+1,碳数为n+1的正构烷烃的保留时间,min。
定量分析方法:选用内标半定量法,通过内标物的峰面积与样品中各组分的峰面积比值,计算各化合物的相对浓度,浓度计算如公式(2)所示:
(2)
式中:C1,待测化合物的质量浓度,μg/mL;f,相对校正因子,f=1;A1,待测化合物的峰面积;A0,内标(2-辛醇)的峰面积;C0,加入内标(2-辛醇)的质量浓度,μg/mL;V0,加入内标(2-辛醇)的体积,mL;V1,萃取的8 mL稀释酒样的体积,mL。
1.3 数据分析
按照上述的试验方法进行试验,每个试验重复3次,计算峰个数和总峰面积,用Excel 2016、SPSS 25进行数据分析、Origin 2019作图。
2 结果与分析
2.1 单因素试验优化结果
2.1.1 萃取温度的选择
样品瓶中加入8 mL稀释至乙醇体积分数为15%的葡萄蒸馏酒、1.6 g NaCl进行磁力搅拌,在400 r/min下平衡10 min后插入萃取纤维,顶空萃取30 min,然后解析6 min,在此条件基础上考察不同萃取温度(20、30、40、50、60 ℃)对萃取效果的影响;由图1可知,总峰面积和峰个数达到峰值时萃取温度为30 ℃。加热会加快样品分子热运动,使得挥发性香气成分更好地释放,从而增加其在顶空部位的浓度,但温度的升高,会降低在涂层纤维上的分配系数,使得挥发性成分的吸附减少,且温度过高时会使分子质量大的难挥发性成分吸附,分子质量小的易挥发性成分从萃取纤维上解析下来[18]。因此选择30 ℃进行后续优化试验。

图1 萃取温度对萃取效果的影响Fig.1 Effect of extraction temperature on extraction efficiency
2.1.2 解析时间的选择
吸附到萃取纤维上的香气成分能否更好地解析到气相色谱中进行分析取决于解析时间,时间太短不仅会解析不充分,还会造成萃取纤维上较多残留;时间过长可能会减少萃取纤维的使用次数,所以要确定合适的解析时间。由图2可知,解析时间为2~6 min时,总峰面积和峰个数呈现出快速增加的趋势,当解析时间为6 min时,2个响应值均达到峰值。随着解析时间增加,萃取到的挥发性香气成分不断解析下来,但当解析时间>6 min时,总峰面积和峰个数呈现出小幅下降的趋势。因此,综合分析,确定解析时间为6 min。

图2 解析时间对萃取效果的影响Fig.2 Effect of desorption time on extraction efficiency
2.1.3 平衡时间的选择
在萃取纤维进行吸附之前,样品瓶中液相在30 ℃磁力搅拌条件下平衡一段时间,挥发性成分会在顶空和样品之间达到平衡[19],此时萃取效果较优。由图3可以看出,平衡时间为10 min时,响应值达到极大值,萃取效果较好,两者之间达到了平衡。因此,确定平衡时间为10 min。

图3 平衡时间对萃取效果的影响Fig.3 Effect of equilibrium time on extraction efficiency
2.1.4 萃取时间的选择
挥发性成分在萃取纤维上的吸附也是一个动态平衡的过程,是样品、顶空部分和萃取纤维三者之间的平衡[20],只有三者达到动态平衡时才有最大吸附量。由图4可知,萃取时间为30 min时,总峰面积和峰个数达到极大值。相对分子质量较低的物质很容易被萃取吸附到萃取纤维上,反之,相对分子质量较大的就很难被萃取,如果萃取时间过长,大分子物质竞争性吸附增加会造成小分子物质解析。萃取时间为30 min时,三相之间达到平衡,所以选择萃取时间为30 min进行后续优化试验。
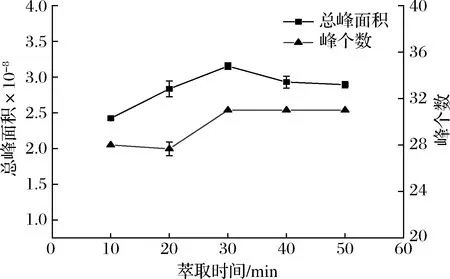
图4 萃取时间对萃取效果的影响Fig.4 Effect of extraction time on extraction efficiency
2.1.5 NaCl添加量的选择
由图5可知,当NaCl添加量为0.2 g/mL时,挥发性成分总峰面积和峰个数达到极大值。加入NaCl会降低香气物质在液相中的溶解度,更易萃取;并且通过实验发现,当NaCl添加量为0.2 g/mL时,溶液并未达到饱和状态,可见并不是NaCl添加量越多越好,当继续添加NaCl至饱和或过饱和时,在增加挥发性成分气-液分配比的同时也将影响基质黏度,降低其扩散速度[21]。因此选择NaCl添加量0.2 g/mL进行后续条件的优化。

图5 NaCl添加量对萃取效果的影响Fig.5 Effect of NaCl addition on extraction efficiency
2.1.6 乙醇体积分数的选择
由图6可知,随着乙醇体积分数增加,挥发性成分的总峰面积和峰个数先增加后减少,乙醇体积分数为10%时,挥发性成分总峰面积和峰个数达到极大值。乙醇是酒的主体成分且沸点较低,若不稀释直接萃取,萃取纤维会吸附较多的乙醇,对酒中其他挥发性成分的吸附降低;并且在谱图分析中,大乙醇峰会使其他化合物峰后移[4],影响香气物质的分析。将酒样进行不同浓度的稀释后,会缩小提取过程中乙醇与其他香气成分之间的竞争性吸附差异,但稀释浓度过大,乙醇与其他香气成分浓度过低,使总体萃取效果降低,由图6可知,乙醇体积分数为10%时,萃取效果较好。

图6 乙醇体积分数对萃取效果的影响Fig.6 Effect of ethanol volume fraction on extraction efficiency
2.2 响应面试验优化结果
利用Design-Expert.V8.0进行Box-Behnken试验设计,试验结果如表1所示。

表1 响应面试验设计及结果Table 1 Experimental design and results for response surface analysis
通过对表1结果进行二元多次回归统计分析,建立回归模型,此模型得出葡萄蒸馏酒中香气成分的总峰面积(Y1)、峰个数(Y2)与各变量因素之间的拟合方程为:
Y1=3.449×108+2.897×106A+7.730×106B+2.510×106C+4.828×106D-1.178×106AB-3.242×107AC-2.481×107AD+1.011×105BC+6.771×106BD+6.734×106CD-3.362×107A2-2.737×107B2-4.262×107C2-6.598×107D2
Y2=33.40+0.75A+0.58B+1.25C-0.42D-0.75AB-AC-AD-0.5BD-1.25CD-3.33A2-1.33B2-2.07C2-2.07D2。
为了检验方程的有效性,对结果进行方差分析(表2)。由表2可知,对于总峰面积和峰个数两个响应值,模型的P值均<0.000 1,说明模型极显著;模型失拟误差P值均>0.05,说明模型失拟项不显著,试验误差较小。对模型进行可信度分析可知,模型响应值总峰面积和峰个数的决定系数R2分别为0.989 8、0.926 7,校正后R2分别为0.979 6、0.853 4,表明模型拟合度高;模型的变异系数均<10%,说明模型对响应值的置信度良好,可以较好地反映真实的实验结果。综上所述,该回归模型对2个响应值的拟合度较高,能够较好的反应响应值与自变量的关系。
Design-Expert.V8.0软件对试验的优化结果为萃取温度30.02 ℃、萃取时间31.76 min、NaCl添加量0.21 g/mL、乙醇体积分数10.81%。采用优化后的参数进行验证试验,为方便操作将优化后的条件适当调整为萃取温度30 ℃、萃取时间30 min、NaCl添加量0.20 g/mL、乙醇体积分数10%,平行试验3次取平均值,测得总峰面积为3.494×108,与模型3.513×108无明显差异,峰个数为34,与模型33相近,说明优化后的萃取条件存在可行性。
2.3 葡萄蒸馏酒香气成分分析结果
在8 mL稀释的酒样中添加50 μL、400 μg/mL的2-辛醇(内标),使用优化后的萃取条件对葡萄蒸馏酒中的香气成分进行检测,并计算其保留指数,具体香气成分见表3。
3 结论
本实验通过HS-SPME与GC-MS结合测葡萄蒸馏酒挥发性成分,对影响萃取效果的因素进行了单因素试验和响应面试验优化,得到了顶空固相微萃取的较优萃取条件:萃取温度30 ℃、解析时间6 min、平衡时间10 min、萃取时间30 min、NaCl添加量0.20 g/mL、乙醇体积分数10%。对优化后的条件进行验证,该条件下进行萃取得到总峰面积为3.494×108,峰个数为34,表明该萃取条件试验效果好,具有一定的通用性。在优化条件下从葡萄蒸馏酒中鉴定出酯类物质16种,醇类6种,醛类1种、酚类1种。本研究优化的测定方法简单、快速,在葡萄蒸馏酒及其他酒类香气成分分析中具有较好的应用前景。

