氧化石墨烯吸附模拟废水中重金属的研究*
张 琳,严熠博,汤文飞
(西北工业大学,陕西 西安 710129)
引 言
随着全球工业化生产规模的扩大,环境污染问题日趋严重。据统计,当前已发现的化学品达7000万之多并且逐年增加。一些废弃的化学品通过排水、掩埋、焚烧等多种途径进入自然环境中,尤其是水体环境[1~2]。其中,重金属离子极易溶于水中,不易降解,并且能在食物链中发生富集,最终进入人体,危害人类的健康,一直都是人们关注的问题[3]。
目前对于重金属废水的处理方法有很多,如化学试剂法,直接吸附法,滤膜交换法等[4]。其中吸附法操作性强、成本低、附加污染小,分为化学吸附、物理吸附[5]。此外,大部分吸附过程可逆,因此吸附剂可以重复利用进而节约成本。常见的吸附剂有活性炭、活性氧化铝、黏土等[6]。为了提高吸附剂的吸附效率,纳米技术被应用到吸附剂的研发中[7]。石墨烯是一种极其特殊的纳米材料,它的所有原子都处于同一表面,以二维片层结构为基础形成了三维立体结构。独特的结构让其拥有无可比拟的吸附面积。因此,石墨烯是良好的吸附材料。做为纳米材料的代表,石墨烯被大量应用于废水中重金属的吸附。
在石墨烯的开发利用过程中,人们发现了比石墨烯吸附效率更高的化合物-氧化石墨烯(GO),利用Hummers法[8]制得的氧化石墨烯片层中衍生出含氧官能团,能提供大量的物理吸附和化学反应结合位点,极大地提高了实际处理效率。本文旨在探究在不同模拟液浓度、不同吸附时间、不同模拟液pH值、不同模拟液温度下,氧化石墨烯对铜、铅、锌、镉四种重金属吸附效率的变化规律,以确定氧化石墨烯吸附模拟废水重金属的最佳条件。
1 实验部分
1.1 仪器与试剂
原子吸收分光光度计(ZEENit 700P),德国耶拿公司;电子分析天平(XS205),瑞士梅特勒公司;油浴锅(SC-25),宁波新芝公司;水浴锅(DK-98),天津泰斯特公司;电热鼓风干燥箱(101-2AB),天津泰斯特公司;离心机(JC-TDZ5),青岛聚创公司;超纯水仪(A10)美国密理博公司。
天然石墨粉(分析纯),国药有限公司;高锰酸钾、硝酸钠、硝酸、硫酸、过氧化氢(优级纯),天津科密欧公司;铜、铅、锌、镉金属标准溶液(浓度均为1000mg/L),环保部标样所。
1.2 氧化石墨烯的制备
(1)粗称3.4g石墨粉、1.7g硝酸钠,混匀后加入到4℃80mL浓硫酸中,搅拌5min。
(2)少量多次加入10g高锰酸钾,控制体系温度<10℃,搅拌5min,随后升温至35℃,搅拌30min。
(3)将上述溶液缓慢加入到170mL去离子水中,控制体系温度(60±2)℃搅拌。
(4)控制体系温度(90±2)℃反应15min,而后升温至98℃,搅拌加入70℃去离子水280mL,最后加入30%双氧水4mL。
玫瑰茄,采自湖南高产奇和医药合富农业有限公司,去核后冻干备用;AB-8型大孔树脂,天津波鸿树脂科技有限公司;乙酸钠、氯化钾、无水乙醇、盐酸和氢氧化钠等均为分析纯。
(5)离心后用去离子水反复洗涤沉淀,至上清液呈中性,将沉淀物低温(<80℃)烘干后研磨,即得氧化石墨烯粉末。
1.3 模拟液的配制
将四种标准溶液分别稀释,每种元素分别配制10.0、20.0、50.0、100、200mg/L浓度梯度。
1.4 吸附实验
1.4.1 不同模拟液浓度
在一系列100mL的锥形瓶中加入10mg氧化石墨烯,再依次量取10.0、20.0、50.0、100、200mg/L模拟液各50mL至锥形瓶中,另外用加了等质量石墨烯的去离子水做空白参比。在恒温25℃磁力搅拌水浴锅中搅拌30min后离心取上清液,测得重金属离子的浓度,计算吸附率。
1.4.2 不同吸附时间
在一系列100mL的锥形瓶中加入10mg氧化石墨烯,在锥形瓶上做好时长标记,量取50mL浓度为10.0mg/L的一种重金属元素水溶液至每个锥形瓶中,在恒温25℃磁力搅拌水浴锅中搅拌,分别于5、10、20、30、40、50、60min时离心取上清液,测得重金属离子的浓度,计算吸附率。重复另外三种元素实验。
1.4.3 不同吸附温度
在一系列100mL的锥形瓶中加入10mg氧化石墨烯,量取50mL浓度为200mg/L的一种重金属元素水溶液至每个锥形瓶中。将锥形瓶分别置于15、25、35、45及55℃恒温磁力搅拌水浴锅中,恒温搅拌30min。后离心取上清液,测得重金属离子的浓度,计算吸附率。重复另外三种元素实验。
在一系列100mL的锥形瓶中加入10mg氧化石墨烯,量取50mL浓度为10.0mg/L的一种重金属元素水溶液至每个锥形瓶中,调节溶液pH值至1、2、4、6、7(由于金属离子在碱性溶液中会发生沉降反应,因此不考虑pH值大于7情况)。在恒温25℃磁力搅拌水浴锅中搅拌30min后离心取上清液,测得重金属离子的浓度,计算吸附率。重复另外三种元素实验。
1.5 仪器条件
优化仪器操作条件,使待测元素的灵敏度等指标达到分析要求。各元素测定条件见表1。

表1 石墨炉原子吸收光谱仪工作参数Table 1 Parameters of graphite furnace atomic absorption spectrometer
2 结果与讨论
2.1 模拟液浓度对吸附结果的影响
结果显示,当模拟液中金属离子浓度变大后,氧化石墨烯对四种离子的吸附率呈下降趋势;由图1可以看出,在相同梯度离子浓度的模拟液中,氧化石墨烯对四种重金属离子的吸附率也是有差别的,对Pb离子的吸附率始终大于另外三种离子,Cd离子吸附率稍高于Zn离子,而Cu离子吸附率最小。
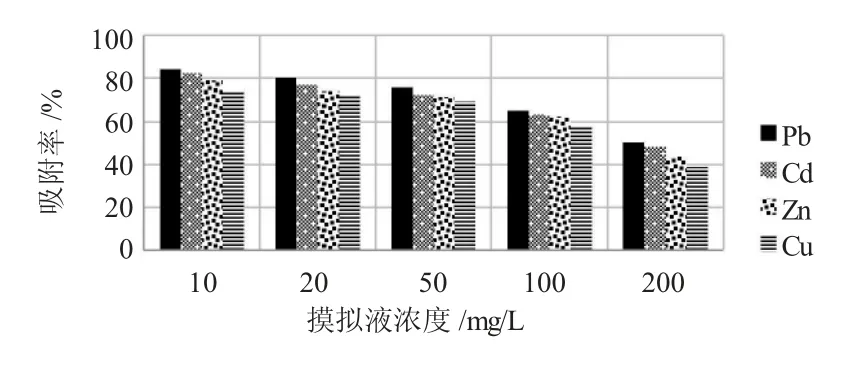
图1 不同模拟液浓度下各重金属离子的吸附率Fig.1 The adsorption rates of heavy metal ions at different simulated liquid concentration
氧化石墨烯的比表面积大,可大量吸附模拟液中的重金属离子。当模拟液中重金属离子浓度升高,离子密度变大,吸附过程快速达到平衡,此时模拟液浓度继续增大,但氧化石墨烯已不能继续发挥吸附效能,因此,吸附率随之下降。从结果上看,四种离子吸附率变化趋势是相同的,氧化石墨烯吸附Zn离子易受模拟液浓度的变化影响,吸附率下降幅度最大。总体上看,随着模拟液浓度从10.0mg/L增加到200mg/L,四种金属离子吸附率下降将近50%。
2.2 吸附时间对吸附结果的影响
结果显示,当改变吸附时间时,四种重金属离子的吸附率在5min就已经达到峰值,且随着时间的推移,吸附率不再增加或不再有明显变化,说明吸附过程在5min内就已经完成。从曲线可以看出氧化石墨烯对这四种金属离子吸附迅速,吸附过程十分高效。
由图2可以看出,氧化石墨烯对金属离子的吸附达到峰值后,随着时间的增加四种离子吸附率稍有变化呈上下浮动状态,说明氧化石墨烯对金属离子的吸附和释放达到了动态平衡。

图2 不同吸附时间各重金属离子的吸附率Fig.2 The adsorption rates of heavy metal ions in different adsorption time
2.3 温度对吸附结果的影响
结果显示,当吸附温度升高时,四种离子的吸附率都呈上升趋势。吸附温度从15℃增加到55℃,Pb离子吸附率增幅为20.6%,Cd为19.8%,Cu为19.6%,Zn为21.7%。
由图3可以看出,随着温度的升高,四种离子吸附率都有所上升,一般来说温度升高会促进化学反应的进行。而金属离子的吸附过程大多数为物理过程而非化学反应。氧化石墨烯对金属离子的吸附率也会随温度升高而变大,说明此过程中既有物理吸附过程,也有化学反应参与。石墨烯发生氧化反应后会在C-C键上加入环氧基团以及OH等官能团,这些官能团的加入间接增大了与金属离子接触的面积,因此氧化石墨烯对金属离子的吸附效果要强于普通石墨烯。
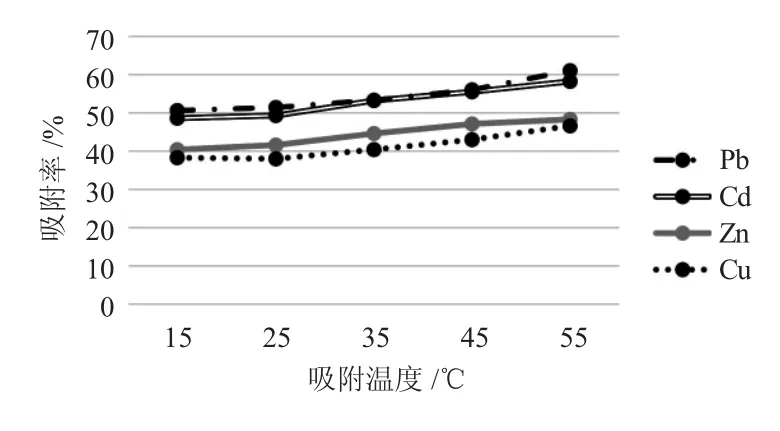
图3 不同吸附温度各重金属离子的吸附率Fig.3 The adsorption rates of heavy metal ions at different adsorption temperature
2.4 pH值对吸附结果的影响
当pH值为近中性7或6时,氧化石墨烯对四种重金属离子的吸附率为峰值,且变化不大;当pH值降为4时,四种离子吸附率都大幅下降;当pH值等于2时,四种离子吸附率都降至30%以下;当pH值等于1时,Zn和Cu离子吸附率甚至在20%以下。当模拟液浓度偏碱性时,金属离子会发生沉淀反应,无法计算吸附效率,因此此处只讨论pH值呈酸性范畴。

图4 不同模拟液pH值各重金属离子的吸附率Fig.4 The adsorption rates of heavy metal ions at different pH values of simulated solution
氧化石墨烯的表面会有大量环氧基官能团,在强酸条件下,会开环吸附大量氢离子而不是金属离子,导致氧化石墨烯表面带有正电荷并进一步降低吸附效率。而随着pH值的升高,氧化石墨烯表面的羧基官能团逐渐失去氢离子,使得氧化石墨烯表面带有大量负电荷,因此可以吸引金属离子形成络合物,促进吸附过程完成。
3 结论
本文探究了氧化石墨烯对Cu、Pb、Cd、Zn四种重金属离子在模拟废水中的吸附作用。着重探究了不同模拟液浓度、不同吸附温度、不同吸附时间以及不同模拟液pH值对氧化石墨烯吸附重金属离子过程的影响。实验表明:模拟液中金属离子浓度越大,氧化石墨烯对金属离子的吸附率越低;氧化石墨烯对金属离子的吸附十分迅速,延长吸附时间对吸附率影响不大;吸附温度升高,氧化石墨烯对金属离子的吸附率也随之升高;若模拟液pH值降低,氧化石墨烯对金属离子的吸附率会大幅下降。本次探究为氧化石墨烯的应用以及氧化石墨烯复合材料的开发利用提供了宝贵的实验依据,为石墨烯产品的研发提供了新的思路,为石墨烯在废水处理行业的开发利用奠定了基础。

