地表水中悬浮物含量和粒径对磷测定的影响
韩超南,孙宁宁,戴 岩,秦延文
1.南京林业大学土木工程学院,江苏 南京 210037 2.中国环境科学研究院,北京 100012
磷含量水平高低直接影响着水体的营养状态。与氮不同,水体中的磷容易被泥沙颗粒吸附,水体悬浮物含量对水体磷形态分布有一定影响。YAO等[1]研究表明,黄河水体悬浮物含量越高,水体总磷(TP)、颗粒态磷(TPP)含量越高,但单位质量泥沙颗粒吸附磷(PP)含量越小。我国水系众多,各流域水体悬浮物含量和颗粒性质差异较大,且丰水期、枯水期流域水体悬浮物含量变化明显,使得各水体TP含量变化大[2-3]。陈铭等[4]研究表明,黄河上游河段悬浮物含量低,TP含量随悬浮物含量沿程上升;中游河段悬浮物含量升高,TP含量波动变化;下游河段悬浮物含量最高,TP含量却随悬浮物含量沿程下降。连心桥等[5]研究表明,强降雨对太湖入湖河道水体磷形态影响明显,其中以TPP含量的响应最快,强降雨当天就出现峰值。由此可见,各流域水体磷含量与悬浮物含量、颗粒组分物化性质的关系密切,但并非单一的同步的相关关系。

1 材料与方法
1.1 颗粒物样品采集
采集长江上游干流沉积物样品(巫山站)作为颗粒物材料,自然风干后经150 μm孔径的筛网过筛,干燥保存备用。取部分150 μm颗粒,采用干筛法进行0~30 、30~50、50~150 μm粒径分级,干燥保存备用。
为了查明不同悬浮物含量对水体TP含量测定的影响,后续补充采集长江下游干流岸边土壤样品(南京站),自然风干后经150 μm孔径的筛网过筛,干燥保存备用。
1.2 颗粒物磷形态测定
采用改进的SEDEX化学提取法[12-13]提取颗粒物中6种磷形态:先用氯化镁溶液提取弱吸附态磷(Exc-P),再用十二烷基硫酸钠溶液提取可提取态有机磷(Exo-P),用柠檬酸钠-碳酸氢钠溶液提取铁锰结合态磷(Fe-P),用醋酸缓冲液提取自生磷灰石磷(Ca-P),用盐酸溶液提取碎屑磷(Det-P),最后高温煅烧-盐酸溶液提取非活性磷(Res-P)。6种磷形态含量之和作为单位质量颗粒总磷含量,即PP质量分数,单位为mg/g。
1.3 等温吸附磷实验

采用潘刚等[14]修正的Freundlich交叉型吸附等温方程对3种粒径颗粒的等温吸附磷行为进行拟合,见式(1)。
(1)
式中:Q为颗粒物对磷的吸附容量,mg/g;KF为吸附系数,L/g,Ceq为水体平衡磷质量浓度,mg/L,EPC0为颗粒物吸附-解吸磷平衡质量浓度,mg/L,n和β为常数。为简化分析,Cp-n中的n取值为0[14]。
1.4 水体总磷含量测定的多种预处理设计
以南京站采集颗粒物为溶质,以超纯水为溶剂,配制悬浮物质量浓度为10、50、100、300、600、1 000 mg/L的泥水混合液,25 ℃恒温振荡50 h。基于GB 11893—1989水体 TP含量测定的钼酸铵分光光度法[7],考虑水体悬浮物的测定干扰,设计“静沉30 min-消解”“混匀-消解-浊度补偿”“混匀-消解-过滤”3种预处理方式,对上述泥水混合液TP含量进行测定。
1)“静沉30 min-消解”:GB 11893—1989标准方法,水样混匀后静沉30 min,取上清液经过硫酸钾消解和钼锑抗显色测定TP含量;
2)“混匀-消解-浊度补偿”:水样混匀后加入过硫酸钾进行消解,之后一份加入钼锑抗显色剂正常显色,另一份加入浊度补偿液(硫酸、钼酸盐溶液),通过两者吸光度差值计算得到TP含量;
3)“混匀-消解-过滤”:水样混匀后加入过硫酸钾进行消解,之后经过0.45 μm滤膜过滤,过滤液加入钼锑抗显色剂显色测定TP含量。
为保证实验质量,每组处理设置3个平行。
1.5 数据处理
采用单因素ANOVA分析各颗粒样品中赋存的磷形态含量差异(P<0.05),采用成对样本t检验分析两两预处理组TP含量的测定差异(Sig.<0.05),实验数据和图形用Excel 2019、SPSS 22.0、Origin 8.0进行处理绘制。
2 结果与讨论
2.1 不同粒径颗粒中磷形态含量特征
3种粒径颗粒中磷赋存形态的含量分布如图1所示。

图1 3种粒径颗粒中磷形态的组成与含量特征Fig.1 Concentrations of phosphoruscomponents of three size particles
从图1可见,粒径50~150、30~50、<30 μm的单位质量颗粒所含PP质量浓度分别为0.92、0.92、1.01 mg/g。在水体搅动、氧化还原环境变化等条件下,Exc-P、Exo-P、Fe-P比较容易从颗粒上解吸而释放入水体,所以三者之和通常被认为是生物有效态磷(Bio-P)[15]。从图1可以看出,3种粒径颗粒所赋存的磷形态均以Fe-P形态为主,Bio-P含量分别占PP含量的62%、61%和66%。粒径<30 μm颗粒所含PP、Bio-P含量明显高于粒径50~150 μm、30~50 μm颗粒(ANOVA分析,P<0.05),说明同等单位质量条件下,粒径小于30 μm颗粒所吸附的PP、Bio-P、Fe-P含量相比粒径50~150、30~50 μm颗粒较多,这与黄河干流[16]、长江干流[17-18]的实际调研结果一致。

2.2 不同粒径颗粒对磷的解吸-吸附特性
在水体初始磷质量浓度0~1.2 mg/L范围内,对3种粒径颗粒的磷解吸-吸附特性进行了分析(图2)。在水体初始磷质量浓度为0 mg/L条件下,粒径50~150、30~50、<30 μm颗粒经过50 h振荡,其单位质量颗粒物释放磷量分别为0.11、0.11、0.14 mg/g。可见,在水空白环境中,粒径<30 μm颗粒的磷释放量高于粒径50~150、30~50 μm颗粒,此现象与小粒径颗粒所赋存PP尤其是Bio-P含量较高有关。
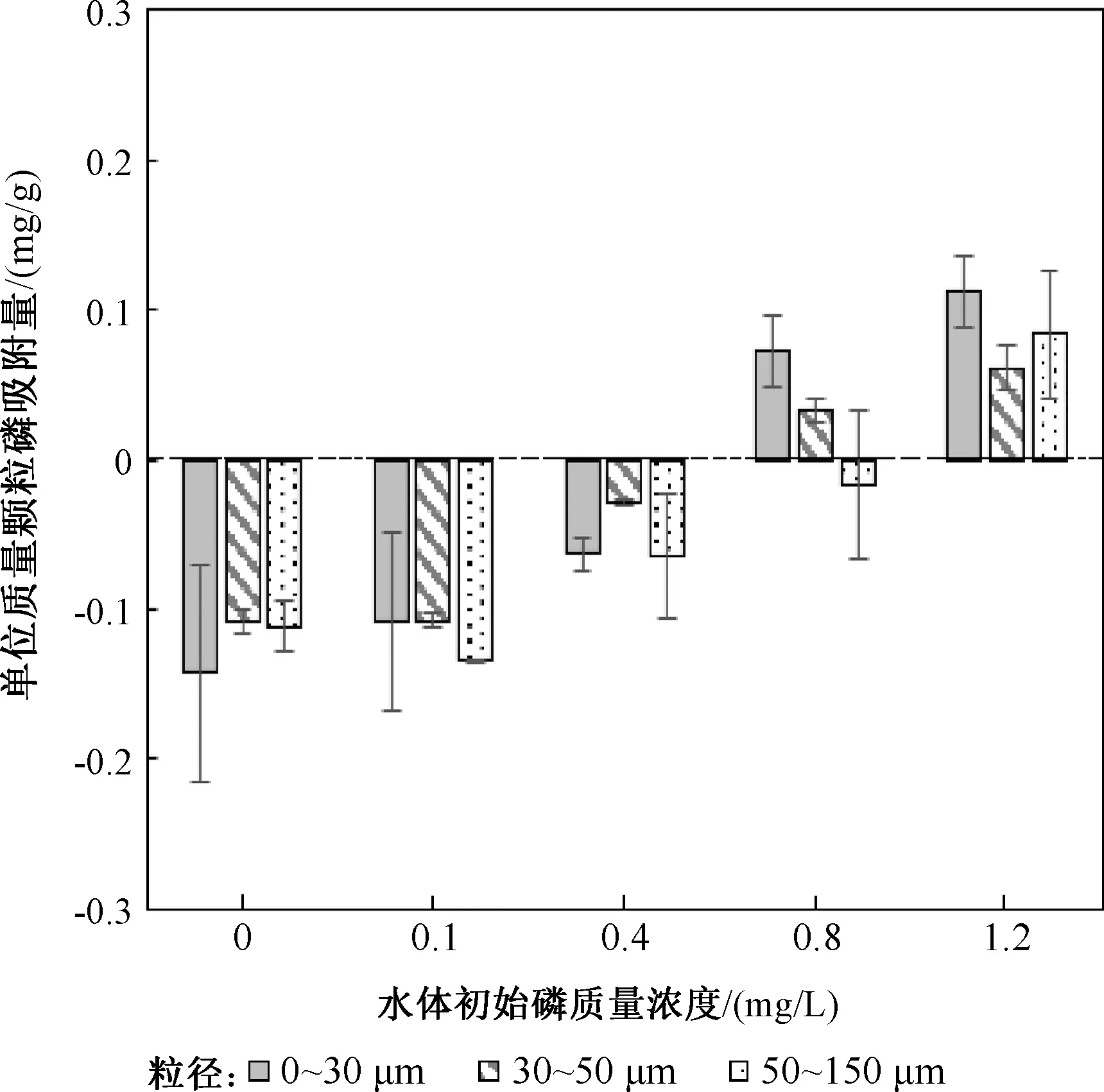
图2 3种粒径颗粒的磷解吸-吸附特性Fig.2 Characteristics of phosphorus desorption-adsorption capacities of three size particles

在25 ℃和水体初始磷质量浓度0~1.2 mg/L条件下,选用Freundlich交叉型吸附曲线[11]对3种粒径颗粒物的等温吸附磷能力进行拟合,等温吸附磷拟合曲线如图3所示,拟合方程分别见式(2)~式(4)。

图3 3种粒径颗粒的等温吸附磷拟合曲线Fig.3 Isothermal phosphorus adsorptioncurves of three size particles
粒径50~150 μm颗粒:
Q= 0.17×(Ceq1.80- 0.841.80)r=0.934
(2)
粒径30~50 μm颗粒:
Q= 0.26×(Ceq0.48- 0.630.48)r= 0.933
(3)
粒径<30 μm颗粒:
Q= 0.34×(Ceq0.68- 0.580.68)r= 0.910
(4)
从以上等温吸附方程可以看出,粒径50~150、30~50、<30 μm颗粒样品的磷吸附系数(KF)分别为0.17、0.26、0.34 L/g,这也说明小粒径颗粒物具有相对较高的磷吸附能力。此外,粒径50~150、30~50、<30 μm颗粒样品的磷吸附解吸平衡质量浓度(EPC0)分别为0.84、0.63、0.58 mg/L。《地表水环境质量标准》(GB 3838—2002)Ⅰ~Ⅴ类水体TP含量限值均不高于0.4 mg/L[6],而上述3种粒径颗粒的EPC0含量均高于0.4 mg/L,表明在大多地表水体中3种粒径颗粒均会呈释放磷的状态。
因此,相比粒径50~150、30~50 μm颗粒,粒径<30 μm颗粒所赋存的磷含量最高,释放磷量最多,更易达到解吸-吸附平衡状态。这也间接说明,同等条件下粒径<30 μm颗粒相比粒径50~150、30~50 μm颗粒对水体中磷具有更高的缓冲能力。
2.3 不同悬浮物含量对水体总磷含量测定的影响
我国不同地区地表水体悬浮物含量的空间差异大,且各地悬浮物的粒径组成各有不同。据《中国泥沙公报》统计[17],长江干流、黄河干流和淮河流域的多年平均悬浮物质量浓度分别为392~1440、589~27500、125~932 mg/L。众所周知,地表水体中悬浮物的存在,影响使用“静沉30 min-消解”测定水体TP含量的准确性。为规范地表水体TP监测技术要求,中国环境监测总站于2019年12月制定了《地表水总磷现场前处理技术规定(试行)》[25]:针对地表一般水体,根据原水浊度为≤200 NTU、200~500 NTU、>500 NTU,前处理方式分别采用自然沉降、自然沉降、离心。
然而,上述实验结果说明:小粒径颗粒(尤其是粒径≤30 μm)相比大粒径颗粒赋存更多的PP含量,并且在水体中具有更强的释放-吸附磷的缓冲能力。因此,该规定即使对原水浊度≤500 NTU的地表一般水体均使用自然沉降的预处理方式,留下的上清液中仍会保留各地区不统一的小粒径颗粒物或胶体物质,从而仍对水体TP含量测定造成干扰。针对水体悬浮物的测定干扰,设计“静沉30 min-消解”“混匀-消解-浊度补偿”“混匀-消解-过滤”3种前处理方法,对比采用它们处理水体后测定TP含量的结果,如图4所示。

图4 不同悬浮物质量浓度条件下水体总磷质量浓度特征Fig.4 Total phosphorus contents in water bodieswith different suspended solid contents
当悬浮物质量浓度不高于600 mg/L时,3种处理方式中以“静沉30 min-消解”测定TP含量最高,其显著高于“混匀-消解-过滤”“混匀-消解-过滤”测定结果(成对样本t检验,Sig.=0.033),主要由静沉30 min后留在上清液中的小粒径颗粒或胶体也能产生吸光度所引起。所以,国标法“静沉30 min-消解”前处理方法无法保证统一的沉降效果,对于低浊度、低悬浮物含量的水样测定TP含量结果会偏高。
当悬浮物质量浓度达到1 000 mg/L时,“静沉30 min-消解”测定的TP含量最低,相比“混匀-消解-浊度补偿”“混匀-消解-过滤”的TP测定结果低约23%、18%。此TP测定损耗是由“悬浮物质量浓度1 000 mg/L”水样在静沉30 min过程中沉淀了大部分携带颗粒磷的大粒径泥沙所致。所以,对于高浊度、高悬浮物含量的水样,“静沉30 min-消解”测定TP含量会偏低,即存在高损耗率的问题。
“混匀-消解-过滤”方法是在水体TDP和TPP均被过硫酸钾消解之后且显色剂加入之前,对水体粒径>0.45 μm颗粒物进行了过滤去除处理,从而在保留有颗粒物携带磷信息的同时又有效减轻了粒径>0.45 μm颗粒在700 nm的吸光度影响,理论上是属于比较准确且易于统一标准化实施的方法。“混匀-消解-浊度补偿”增加了对颗粒本身产生的吸光度测定环节,能够一定程度消除悬浮物含量差异对TP测定的影响,但存在测定水样用量和工作量均加倍的问题[26]。由此,在使用国标法“静沉30 min-消解”前处理测定地表一般水体TP含量时,建议增加“混匀-消解-过滤”前处理方法测定TP含量作为参考。
3 结论
1)粒径<30 μm颗粒所赋存PP、Bio-P含量明显高于粒径50~150、30~50 μm颗粒,水空白环境中粒径<30 μm颗粒的磷释放量也高于粒径50~150、30~50 μm颗粒。
2)粒径<30 μm颗粒相比粒径50~150、30~50 μm颗粒具有更高的磷吸附能力,但其EPC0质量浓度为三者最低(0.58 mg/L),说明其在地表Ⅰ~Ⅴ类水体(TP≤0.4 mg/L)中更易达到磷解吸-吸附平衡状态。
3)地表水体悬浮物含量和粒径组成的空间分异大,国标法“静沉30 min-消解”前处理方法无法保证统一的沉降效果,测定水体TP含量可能偏低或偏高。针对地表一般水体,建议同时增加“混匀-消解-过滤”前处理方法测定水体TP含量作为参考。

