肾肿瘤靶血管定位法在零缺血腹腔镜下肾部分切除术中的应用
宋 鑫,顾寅珺,蒋 晨,刘东明,薛 蔚,黄翼然
(上海交通大学医学院附属仁济医院泌尿外科,上海 200001)
肾肿瘤是泌尿系最常见的恶性肿瘤之一,约占全身恶性肿瘤的3%,发病率每年以3%~4%的速度上升,且呈年轻化趋势,严重威胁人体健康[1-2]。传统的肾部分切除手术过程中,需临时阻断肾动脉主干,以期达到一个相对无血的操作环境,保证肿瘤完整切除,但热缺血时间过长势必会影响其他正常肾单位的功能[3]。
三维重建技术是通过计算机辅助设计软件,将连续的二维图像叠加形成完全的三维图像[4]。国内有学者报道将三维重建技术应用于肾部分切除手术中,能很好地显示肿瘤与肾脏的关系,便于手术规划及术前沟通[5],但其在肾脏肿瘤外科治疗中的应用价值还远未得到充分发掘。本研究旨在探索建立并完善肾肿瘤靶血管三维重建定位法,并将其应用于腹腔镜下零缺血保留肾单位手术中,以期优化零缺血保留肾单位手术,切实保护患者利益。
1 资料与方法
1.1 临床资料回顾性分析2019年1月-2020年9月上海交通大学医学院附属仁济医院泌尿外科收治的80例早期肾癌患者的资料,根据手术方式及肿瘤位置进行分组,其中30例患者行肾肿瘤靶血管定位零缺血后腹腔镜肾部分切除术为零缺血组,50例患者接受血管阻断下后腹腔镜肾部分切除术为传统手术组,零缺血组的患者根据其肿瘤位置分为肾门部肿瘤组与其他部位肿瘤组,收集所有患者相关资料包括患者性别、年龄、肿瘤直径及位置、手术时间、术中出血量、住院时间,以及术前、术后3个月及12个月的患肾肾小球滤过率(glomerular filtration rate,GFR)和血肌酐水平等进行统计分析。
零缺血组入组标准:①患者术前肾计算机断层扫描血管街影(computed tomography angiogra-phy,CTA)诊断为肾肿瘤,且呈外生性生长;②R.E.N.A.L评分小于12分,PADUA评分小于14分,肿瘤直径2~7 cm;③既往未进行任何抗肿瘤治疗;④无明显肺脏、肝脏、骨骼等远处转移;⑤既往无腹部及腰背部手术史。排除标准:①有明显解剖学异常者;②术区手术史及其他系统严重疾病者;③术后失访或术后未能检查GFR者。所有患者术前均被告知手术风险并签署知情同意书。
1.2 方法所有患者术前行肾CTA检查,确认肿瘤供应血管及肿瘤情况(图1A、B)。基于患者CTA的DICOM数据,计算机软件分析处理为三维图像,由影像科医生、泌尿外科医生及软件工程师共同沟通修正,重建出符合后续工作的三维重建图像(图1C、D)。所有手术均由同一术者完成。
患者全身麻醉后健侧卧位,经腹膜后采用3通道法,根据术中情况增加腋中线肋缘下通道。两组患者均常规沿腰大肌、肾周脂肪囊之间游离肾动脉或肾动脉分支,游离肾肿瘤。两组患者均采用“球冠状”肾部分切除术[6]。传统手术组患者阻断肾动脉后,在肾实质与肾肿瘤交界约3 mm处锐性切开肾包膜,楔形切入肾实质,寻找肾实质与肿瘤假包膜之间的过渡带。锐性切割和钝性分离相结合,将肾肿瘤完整切除,然后缝合关闭创面。
零缺血组患者手术操作依据肿瘤三维重建模型,应用肾肿瘤靶血管定位法选择合适的手术切入点,行肾脏肿瘤“球冠状”切除[6-7],肿瘤切除顺序依据肿瘤大小、位置,遵循从易到难的操作原则,使用腹腔镜剪刀在肿瘤周围约3 mm处分离肿瘤,必要时打辅助孔置入吸引器,将肾脏创面的出血充分吸走,保持视野清晰并帮助调整瘤体方向。根据肾肿瘤三维重建模型,初步确定靶血管大概方位,分离至肿瘤靶血管时,应用剪刀和吸引器相结合,沿着肿瘤包膜钝性结合锐性分离,完全暴露肿瘤靶血管,予以百克钳或者Hem-O-lok夹闭离断(图1E、F)。完全切除肿瘤后检查创面,用2-0倒刺可吸收线缝合肾脏表面创面,如果存在出血点应用3-0倒刺可吸收线缝合止血。检查肾脏创面无明显渗血后留置后腹腔引流管,将肾肿瘤标本置入标本袋并取出,依次逐层缝合关闭。
2 结 果
2.1 零缺血组与传统手术组患者一般资料的比较本研究共纳入80例患者,其中男性46例,女性34例;年龄(52.6±7.4)岁,肿瘤直径(42.1±11.4)mm,两组患者性别、年龄、肿瘤直径差异均无统计学意义(P>0.05,表1)。
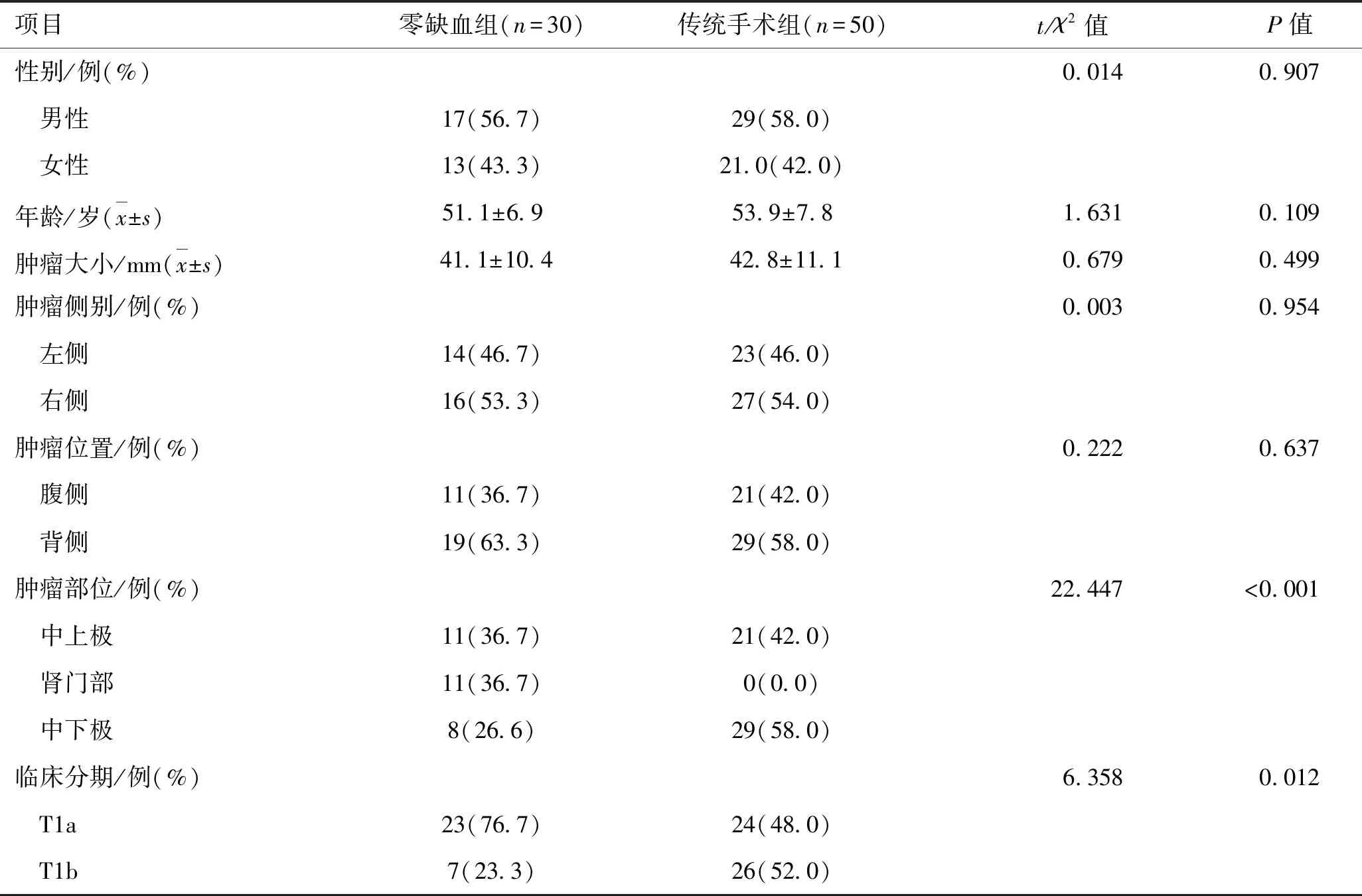
表1 两组肾癌患者一般临床资料比较
2.2 零缺血组中肾门部肿瘤组与其他部位肿瘤患者临床资料的比较两组患者性别、年龄、肿瘤直径差异无统计学意义(P>0.05)。肾门部肿瘤组靶血管数量绝大多数为单靶点,1例为双靶点,其他部位肿瘤组单靶点患者10例,多靶点患者9例,差异无统计学意义(P<0.05,表2、图2)。
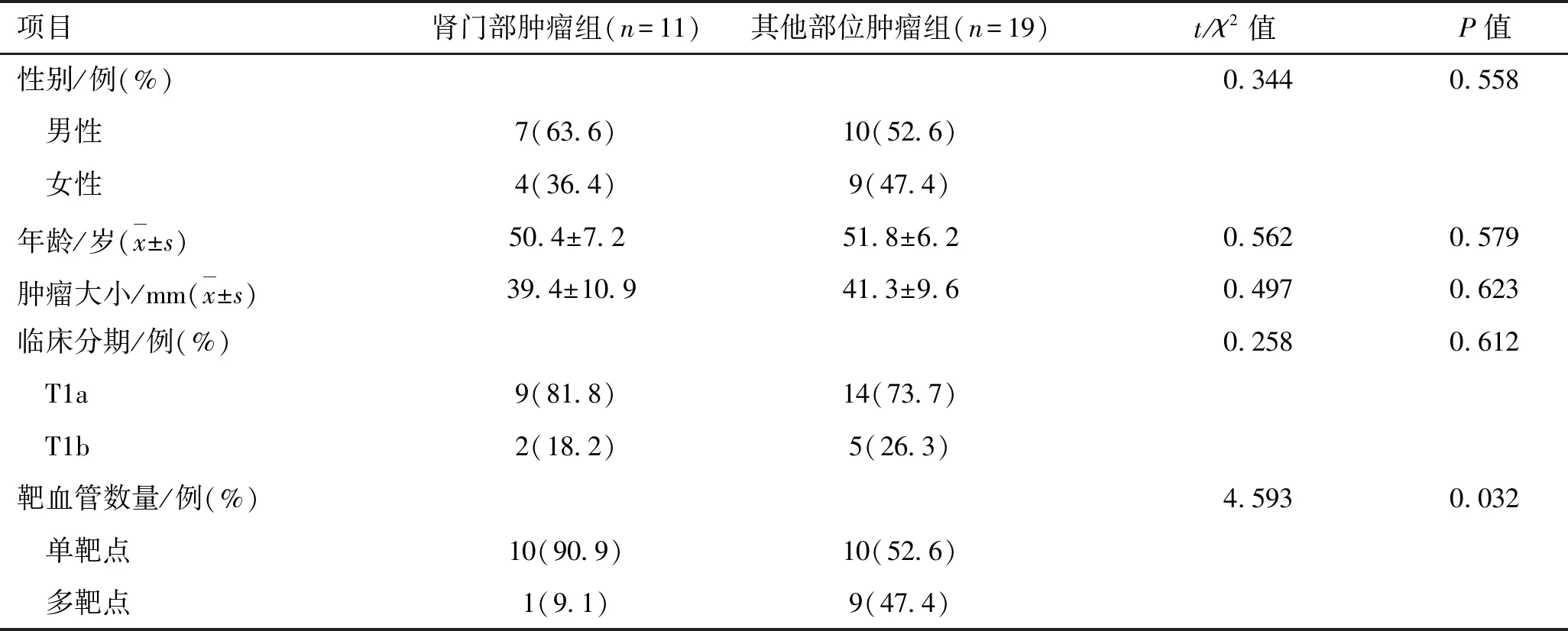
表2 零缺血组肾门部与其他部位肿瘤组患者临床资料比较
2.3 零缺血组与传统手术组手术情况比较传统手术组患者手术均顺利完成,无中转开放。零缺血组患者中有4例中途阻断肾动脉后行保留肾单位手术(纳入传统手术组),其余26例患者均完成零缺血保留肾单位手术,术中无中转开放或根治性肾全切术。零缺血组较传统手术组的手术时间[(92.5±9.8)minvs.(71.6±9.9)min,P<0.001]、术中出血量[(150±22)mLvs.(80±19)mL,P<0.001 ]有所增加,住院时间[(7.2±0.4)dvs.(7.1±0.9)d,P>0.05]差异无统计学意义。肾门部肿瘤患者与其他部位患者相比,手术时间有所延长[(109.3±10.2)minvs.87.3±9.5)min,P<0.001 ],术中出血量[(154±25)mLvs.(148±21)mL,P>0.05]及住院时间[(7.3±0.5)dvs.(7.2±0.9)d,P>0.05]差异均无统计学意义。
2.4 两组患者术后随访情况比较两组患者术前患肾GFR及血清肌酐比较差异无统计学意义(P>0.05)。术后随访1个月,两组患者无出血、尿漏、感染等相关并发症发生。术后随访12个月,两组患者未见肿瘤复发及转移。两组患者术后3个月及12个月的血清肌酐比较,差异无统计学意义(P>0.05)。术后3个月患肾GFR两组比较差异有统计学意义(P<0.001),零缺血组患者的患肾GFR恢复较快,差异有统计学意义(P<0.05);而术后12个月的患肾GFR差异无统计学意义(P>0.05,表3)。
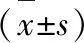
表3 两组肾癌患者肾功能的比较
3 讨 论
保留肾单位手术因其具有与根治性肾切除手术一样的治疗效果,并且能降低术后慢性肾病的发生率,减少由于慢性肾病引起的心脑血管并发症和死亡风险,早已成为治疗早期肾癌的标准术式[2,8]。
传统的肾部分切除术需临时阻断肾动脉主干,以期达到一个相对无血的操作环境,保证肿瘤完整切除,但热缺血时间过长势必会影响其他正常肾单位的功能[9-10]。因此国内外学者提出了诸多缩短热缺血时间的方法。BAUMERT等[3]在传统腹腔镜肾部分切除术基础上,采用早期松开血管阻断钳技术,即在肿瘤切除后缝合基底创面完毕便松开血管阻断钳,再采用止血纱布填塞创面可吸收线连续贯穿缝合肾实质及包膜,将热缺血时间缩短了近50%。SHAO等[11]通过节段性阻断肾动脉分支血管,可造成肿瘤部位及周围少部分正常组织热缺血,而在其余肾脏组织血液灌流正常的情况下完成保留肾单位的手术,术后肾功能的恢复效果优于主干阻断者。GILL等[12]分离阻断供应肿瘤的肾动脉分支,配合术中超声明确肿瘤血供是否完全阻断,同时在切割肿瘤最深处时降低动脉血压至60 mmHg,来完成腹腔镜下或机器人辅助肾部分切除术,术前、术后的肌酐及GFR水平无差别。以上的这些技术手段在保证肿瘤完整切除的同时都能一定程度上有效保护肾功能,但是这些手术路径是从肾门往肾窦方向解剖,容易造成静脉、肾盂集合系统等周围解剖结构的损伤,仅限于技艺精湛的外科医生应用。
三维重建技术是通过计算机辅助设计软件,将连续的二维图像叠加形成完全的三维图像,最早出现于上世纪80~90年代,最初应用于工业领域,而后逐步拓展至医学领域[13]。随后以其独特的优势在医学领域得到广泛应用,但该技术在肾肿瘤领域的应用尚处于初步探索阶段。2014年美国杜兰大学的SIBERSTEIN等[13]成功打印了世界上首个带瘤肾脏模型,这个模型与患者患肾尺寸一致,带有肾脏主要的血管结构、肾盂和近端输尿管,肿瘤以区别于肾实质的其他颜色标识。随后南加州大学的BERNHARD等[4]为7例肾部分切除术前患者打印了量身定制的带瘤肾脏模型,结果显示患者看过自身模型之后,对肾脏生理的理解程度提高了16.7%,对肾脏解剖的理解提高了50%,对肿瘤特点的认识提高了39.3%,而对手术方式的理解程度和接受度提高了44.6%,由此可见三维重建技术为患者的教育和医患沟通提供了良好的工具,能显著提高患者对治疗的满意度和依从性。国内也有诸多学者报道将三维重建技术应用于传统肾部分切除手术中,能很好地显示肿瘤与肾脏的关系,易于术前肿瘤的定位,便于手术规划及术前沟通[14]。上述应用仅是较为初步的,在肾脏肿瘤外科治疗中的应用价值还远未得到充分发掘。
我们基于三维肾肿瘤血管重建技术,在术前详细评估肾肿瘤血管,定位肾肿瘤靶血管,优化手术治疗方案,指导术中操作,更能精确地处理肿瘤靶血管,真正实现了腹腔镜下零缺血保留肾单位手术。本研究中有4例肾下极T1b期肾癌,术前三维肾肿瘤血管重建技术评估其肿瘤血管为多靶点,拟行无肾蒂阻断LPN,结果术中出血明显,中途阻断肾动脉后行保留肾单位手术,随后入组到肾蒂阻断LPN传统手术组中。其余26例患者均顺利完成零缺血腹腔镜下肾部分切除术,围手术期未发生尿漏以及出血等并发症,术后随访结果显示无切缘阳性及术后局部复发的病例。传统手术组患者均顺利完成肾部分切除术,无中转开放手术或根治性肾全切术。两组患者术后3个月及12个月的血清肌酐水平比较,差异无统计学意义,术后3个月患肾GFR比较差异显著,表明应用肾肿瘤靶血管定位法实施零缺血后腹腔镜下肾部分切除术的患者肾功能恢复较快。术后随访12个月,两组患者未见肿瘤复发或转移。两组患者手术时间和术中出血量差异有统计学意义,但是其住院时间及术后并发症发生率差异并无统计学意义,表明应用肾肿瘤靶血管定位法实施零缺血后腹腔镜下肾部分切除术与后腹腔镜下肾动脉全阻断保留肾单位手术相比并未增加围手术期风险,肾肿瘤靶血管定位法实施零缺血后腹腔镜下肾部分切除术是安全有效的。
根据以往临床经验,多数医生认为肾门部肿瘤手术难度大,不适合采用零缺血手术,所以本研究对零缺血组患者的肿瘤靶血管进行了分析,发现有4例患者因为术中出血多而中途进行了肾动脉阻断,这4例患者肿瘤均位于下极且直径超过4 cm,其肿瘤血管靶点较多。而相较于肾两极肿瘤的靶点血管,肾门部肿瘤靶点血管多为单支,且肾门部肿瘤靶点血管较粗,手术过程中更容易寻找完成阻断,表明肾肿瘤靶血管定位法尤为适用于肾门部单发早期肾癌患者。
我们应用三维肾肿瘤血管重建技术更好地实现了腹腔镜下零缺血保留肾单位手术,体现精准医学的临床价值,在完整切除肾肿瘤的同时,最大限度地保护了残余肾单位的肾功能,降低患者术后肾功能不全
的可能性,进而避免肾脏替代治疗,节约社会资源。但是并不是所有的肾肿瘤病例都适合此项技术,临床中实施肾肿瘤靶血管定位法零缺血后腹腔镜下肾部分切除术时应注意以下几点:①选择外生型肿瘤患者,建议外生瘤体部分比例>50%,肿瘤直径在2~5 cm最佳;②肿瘤单发、肾门部肿瘤推荐使用此方法;③为了避免术中出血太多无法控制,建议术中常规预先分离并处理好肾蒂血管备用。
综上所述,对于部分早期肾癌患者,应用三维肾肿瘤血管重建技术能够更好地实现腹腔镜下零缺血保留肾单位手术,有利于患者肾功能的保护。肾门部单发早期肾癌其靶血管较易寻找,更适用于三维肾肿瘤血管重建技术实施腹腔镜下零缺血保留肾单位手术。

