影响先天性甲状腺功能减低症不同转归的早期因素
刘小瑜 廖燕霞 林 芬
梅州市妇幼保健计划生育服务中心儿童保健科(梅州 514021)
先天性甲状腺功能减低症(congenital hypothyroidism,CH)主要影响儿童的体格和智能发育,是儿科常见的内分泌疾病。根据疾病转归分为持续性甲状腺功能减低症(permanent congenital hypothyroidism,PCH)与暂时性甲状腺功能减低症(transient congenital hypothyroidism,TCH)。随着国内新生儿筛查工作的广泛推开,筛查检测方法不断改进,灵敏度持续增加,CH检出率明显提高,其中多为受各种因素影响引起的促甲状腺素(thyroid stimulating hormone,TSH)升高[1]。本研究旨在寻求早期区别PCH与TCH的因子,为探索更完善的诊治、随访方案提供依据。
1 资料与方法
1.1 一般资料
按照《新生儿疾病筛查技术规范(2010版)》的要求,对2013年12月—2017年3月在本市出生的新生儿进行筛查。根据《先天性甲状腺功能减低症诊疗共识》的要求,TSH升高,血清游离甲状腺素(free thyroxine,FT4)降低,确诊为CH,共126例。CH患儿予左甲状腺素钠片 (levothyroxine sodium,LT4)口服替代治疗,个性化用药,定期随访至3岁,试停药失败者诊断为PCH。CH患儿随访满2~3年后停药,并继续随访满1年无复发者诊断为TCH。126例CH患儿因各种原因转诊或失访,最终获得有效病例80例,其中PCH 29例, TCH 51例。PCH与TCH患儿中各有1 例早产儿。
1.2 方法
1.2.1 筛查方法:按《新生儿疾病筛查技术规范2010》的筛查要求,对2013年12月—至2017年3月在本市出生后72小时~7天的新生儿采集干血片,用酶联免疫荧光分析法测TSH值 。若TSH≥9.5 mIU/L 为筛查阳性。召回采用电化学发光法测定静脉血TSH和游离甲状腺素FT4的水平进行确诊。
1.2.2 诊断、随访方法:按《先天性甲状腺功能减低症诊疗共识》的要求,TSH升高,FT4降低,确诊为CH的患儿立即予左甲状腺素钠片口服。同时查甲状腺彩超,了解甲状腺发育情况。凡彩超显示甲状腺缺如、发育不全视为异常。根据患儿血清TSH和 FT4水平逐步调整药量。首次治疗后2周复查甲功,每次调整剂量后1个月复查。若患儿甲功正常,1岁以内每2~3个月复查1次,1~3岁每3~4月复查1次,3岁以上每6个月复查1次。维持患儿TSH在正常范围,FT4在平均值至正常上限范围之内。每次复查时均进行体格检查,每年查1次甲状腺彩超。定期进行发育评估。
1.2.3 停药方法与判定标准:按《先天性甲状腺功能减低症诊疗共识》的治疗规则,在正规治疗2~3年后试停药1个月,若TSH 及 FT4正常,继续停药随访1年以上甲功均维持在正常范围者为TCH,否则为PCH。如LT4剂量较大,可先减至原剂量一半,1个月后复查甲功正常者,再停药继续随访甲功,了解其转归。
1.3 统计学方法

2 结 果
2.1 2组临床情况比较
本研究共入选CH患儿80例,经2~3年随访后有51例患儿确诊为TCH,29例为PCH。2组患儿在初筛TSH值、TSH恢复正常所需剂量、试停药时LT4的剂量、早期甲状腺发育方面差异有统计学意义(P<0.05)。在性别、孕周、初次FT4值方面差异无统计学意义,见表1。
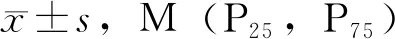
表1 PCH与TCH患儿临床基本情况比较
2.2 2组患儿早期预测因素ROC曲线
初筛TSH值对区分PCH与TCH的有效性见图一。通过ROC曲线分析可知,预测2组患儿转归的最佳初筛TSH临界值为37.825 mIU/L(AUC=0.745;灵敏度0.897;特异度0.490)。为验证该数据是否可准确判断患儿转归,对所有入选的CH病例初筛TSH 值进行评估,预测准确率为63.75%[(26+25)/80],见表2。

表2 区分PCH与TCH最佳初筛TSH值验证[n(%)]
根据患儿临床情况比较结果,为进一步寻求早期预测转归的临床因素,本研究对2组患儿出生后不同月龄LT4用药剂量进行分析。以出生后第一个月每公斤体质量每天用药剂量μg/(kg·d)为第1个月剂量,出生后第二个月每公斤质量每天用药剂量为第2个月剂量,由此类推。从图2、图3可见,ROC曲线下面积与月龄成正比。提示2组间的区别随月龄的增大而增大。由表3可见出生第4月龄开始 PCH 与 TCH的LT4用药剂量的ROC曲线分析结果有诊断意义,根据约登指数,找出第4~24月龄的用药临界值并验证其准确率,分析得第8月龄LT4剂量3.38 μg/(kg·d),预测准确率为75%[(17+43)/80],可早期预测CH的转归。

表3 区分 PCH 与 TCH的LT4用药剂量的ROC曲线分析结果及验证
3 讨 论
随着新生儿疾病筛查技术的不断完善,灵敏度增加,CH检出率提高,发病率也有所上升。根据《先天性甲状腺功能减低症诊疗共识》规定CH按疾病转归可分为PCH和TCH。PCH因甲状腺激素持续缺乏,患儿需要终身替代治疗;TCH因其甲状腺功能可恢复正常,替代治疗2~3年后可停药[2]。为避免过度治疗,探索个性化治疗方案,本研究尝试寻找可影响CH疾病转归的早期因素。
3.1 2组患儿基本临床情况进行对比、分析
本研究发现PCH与TCH 2组患儿在初筛TSH值、TSH恢复正常所需剂量、早期甲状腺超声结果方面的差异有统计学意义。而在性别、孕周、初次FT4值方面的差异无统计学意义。提示初筛TSH值、TSH恢复正常所需剂量、早期甲状腺超声结果对CH的疾病转归存在一定关联。本研究对2组患儿的初筛TSH值进行ROC曲线分析,发现初筛TSH值在37.825 mIU/L(AUC=0.745; 灵敏度0.897;特异度0.490)时,预测准确率63.75%[(26+25)/80]。该临界值与Kang MJ等[3]发现的区分TCH和PCH的显著预测因素初筛TSH临界值31 mIU/L相近。另外,有文献报道[4],早期甲状腺超声检查可以预测PCH和TCH,与本研究结论一致。主要是通过超声检查明确甲状腺形态是否正常。Habib A等[5]、Oron T等[6]研究发现确诊时首次的静脉血TSH值对预测PCH和TCH也有统计学意义,因本研究病例确诊TSH值在≥100 μIU/mL时,无明确标出具体数据,可比性不强,故未纳入研究范围。
3.2 从2组随访治疗方案进行分析
本研究在2组患儿随访治疗过程中发现PCH与TCH 2组患儿用药剂量也不同。首先,2组治疗后TSH恢复正常所需剂量对比有统计学意义,TSH恢复正常所需剂量PCH明显大于TCH(P<0.05)。其次,通过2组出生后每月龄每天所需LT4剂量的ROC曲线可知第8个月龄的LT4用药剂量临界值3.38 μg/(kg·d)(AUC =0.759,灵敏度 0.586,特异度 0.843)可早期区分PCH与TCH。经验证后显示该临界值预测准确率为75%[(17+43)/80]。从表3可见,第4个月龄开始AUC>0.7,说明临界值有一定准确性,从第4~7个月龄临界值预测的准确率有波动。而第8个月开始每个月龄的临界值预测准确率逐渐上升,表明取该月用药临界值有助于早期识别PCH与TCH。关于通过治疗剂量区分PCH与TCH,国外文献报道较多。Oron T等[6]通过随访142例CH患儿发现确诊时的 TSH 和治疗中的 L-T4 剂量可以更好的区分PCH和TCH。ITONAGA T等[7]随访99例CH患儿发现,1岁时LT4剂量在4.7 μg/(kg·d)以上和1.8 μg/(kg·d)以下可能有助于分别预测PCH和TCH。Saba C等[8]研究92例CH 患儿发现6 个月龄时 LT4 剂量需求的截止值为 3.2 μg/(kg·d),低于此阈值的患儿可预测是TCH。Asena M等[9]发现无论病因如何,对于区分永久性患者和暂时性患者,6 个月时 LT4 剂量的最佳临界值为2 μg/(kg·d)。本研究发现出生后第8个月用药剂量临界值3.38 μg/(kg·d)可早期区分PCH和TCH,与上述作者的最佳剂量临界值不尽相同,考虑与各地CH相关基因有关,未来有必要使用和CH相关基因的二代测序进行前瞻性研究,以确定更准确的 CH 病程和结果预测特征[6]。
本研究有10个TCH患儿在随访过程中出现TSH正常,伴FT4升高,予及时减量,提前停药,随访甲功1~2年均正常。TCH组试停药时LT4剂量为(1.55±0.45)μg/(kg·d),对比PCH组试停药时的LT4剂量(3.29±1.06)μg/(kg·d)在统计学上有显著差异(P<0.05)。与Kara C等[10]研究发现的早期停止治疗的唯一指征是低剂量的L-甲状腺素,停药时剂量为(1.25±0.27)μg/(kg·d)相似。提示TCH患儿在随访过程中应注意剂量的调整,避免过度治疗。
综上所述,结合初筛TSH值、出生后LT4用药剂量及早期甲状腺超声检查结果,可早期预测CH患儿的临床转归。对探索更完善的诊治、随访方案,减少过度治疗有重要意义。本研究样本数尚少,未进行CH相关基因检测,结论具有区域性特点,还有待进行全国多中心选取大样本数据进一步研究。

