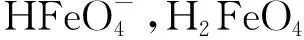高铁酸钾去除饮用水中亚硝基二苯胺的研究
丁春生,邹兆政,周丽君,李元丰
(浙江工业大学 土木工程学院,浙江 杭州 310023)
在给水处理的消毒环节中,会形成不同种类的消毒副产物(DBPs)[1-3]。据统计,当前已发现的DBPs有700多种[4-5],在众多的DBPs中,含氮消毒副产物(N-DBPs)的毒性较强且检出频率较高[6]。NDPhA是N-DBPs的一种,研究表明:NDPhA在多种遗传毒性测试中呈阳性,会导致染色体畸变和DNA损伤[7],并且国际癌症研究署(IARC)已将NDPhA收录到Ⅲ类致癌物清单中[8],因此,对NDPhA开展研究具有重要意义。
高铁酸钾(K2FeO4)有较强的氧化性,其电极电位达到了2.20 V,能够有效地降解有机物,且K2FeO4中的Fe(Ⅵ)会还原成Fe(Ⅲ),进而形成具有良好絮凝效果的Fe(OH)3胶体,促进有机物的去除[9-10]。此外,K2FeO4还具有杀菌除臭的作用[11],因此高铁酸钾在水处理领域得到了广泛的应用[12-16]。Waite等[17]发现K2FeO4可有效地氧化降解苯酚及其他水中残留有机物;杨卫华等[18]研究表明用K2FeO4可有效地去除水中十六烷基三甲基溴化铵;丁春生等[19]发现K2FeO4能较好地去除饮用水中的2,6-二氯-1,4-苯醌。笔者探究在不同反应时间、温度和pH值等条件下,K2FeO4对NDPhA去除效果的影响。
1 试验材料与方法
1.1 试验试剂和仪器
NDPhA标准品,单标,纯度>98%(GC);甲醇,色谱级;高铁酸钾,AR;硫代硫酸钠,AR;磷酸氢二钠,AR;磷酸二氢钾,AR。
高效液相色谱仪(LC 20A,岛津);恒温往复式摇床(IKS KS 130 basic,IKS公司);恒温振荡器(SHA-B);台式pH计(LAPH10KIT型,HACH公司)。
1.2 试验方法
1.2.1 反应时间的影响
配制150 μg/L的NDPhA溶液,取100 mL加入250 mL锥形瓶中,投加质量浓度为1.2 g/L的高铁酸钾,在温度25 ℃、pH=7的条件下,每隔5 min取样,检测目标污染物的剩余质量浓度,考察不同的反应时间对去除率的影响。
1.2.2 投加量的影响
配制150 μg/L的NDPhA溶液,取100 mL加入250 mL锥形瓶中,分别投入0.5,0.8,1.2,1.5,2.0 g/L的高铁酸钾,在温度25 ℃、pH=7的条件下,每隔5 min取样,检测目标污染物的剩余质量浓度,考察高铁酸钾的质量浓度变化对去除率的影响。
1.2.3 pH值的影响
配制150 μg/L的NDPhA溶液,取100 mL加入250 mL锥形瓶中,投加质量浓度为1.2 g/L的高铁酸钾,pH值分别为5,6,7,8,9,反应时长为30 min,温度为25 ℃,每隔5 min取样,检测目标污染物的剩余质量浓度,考察不同pH值对去除率的影响。
1.2.4 温度的影响
“呃……这位……道爷?”胖子想了半天挤出个这么样的称呼,“我只是来散散心。”一边说着,胖子一边打量起地摊上的玉器。
配制150 μg/L的NDPhA溶液,取100 mL加入250 mL锥形瓶中,投加质量浓度为1.2 g/L的高铁酸钾,分别在15,25,35 ℃的温度下反应30 min,并在pH=7的条件下,每隔5 min取样,检测目标污染物的剩余质量浓度,考察温度变化对去除率的影响。
1.3 分析方法
试验测定NDPhA的方法为高效液相色谱法。色谱柱型号为安捷伦C18柱(5 μm,4.6×150 mm)。流动相为V(甲醇)∶V(水)=75∶25,检测波长为245 nm,流速为1 mL/min,柱温为25 ℃。每次样品进样体积为20 μL,单个样品的采样时长为5 min。用甲醇配制成10 mg/L的NDPhA储备液。每次试验前,使用去离子水将NDPhA标准储备液(10 mg/L)稀释成所需质量浓度的标准溶液,将不同目标物质量浓度和出峰面积分别设为横、纵坐标,绘制线性回归标准曲线(R2=0.999 2)。
2 结果与讨论
2.1 反应时间对NDPhA的去除影响
向150 μg/L的NDPhA溶液中投加1.2 g/L的K2FeO4,设置温度为25 ℃,pH值为7,反应结果如图1所示。

图1 反应时间与去除效果的关系Fig.1 Relationship between reaction time and removal effect
由图1可知:反应前5 min,去除率增长较快,5~30 min,去除率增长渐缓,反应30 min后,去除率基本不再增加。主要原因:反应前5 min,参与反应的K2FeO4的量较多,K2FeO4能够发挥强氧化性快速去除NDPhA。在高铁酸根酸性、碱性条件下,当标准电极电位E0分别为2.20,0.72 V时,其反应式为
(1)
[O]+H2O→2·OH
(2)
当·OH的E0=2.80 V时,氧化能力比高铁酸根更强,同时·OH的氧化和高铁酸根的直接氧化共同氧化NDPhA。另外,K2FeO4中的Fe(Ⅵ)还会还原成Fe(Ⅲ),并产生正价态水解产物,这些水解产物具有较高的正电荷和较大的网状结构[20-21],能够使得Fe(Ⅲ)快速形成具有絮凝作用的Fe(OH)3胶体[22],进一步促进NDPhA的去除,其反应式为
(3)
(4)
随着反应的进行,参与反应的K2FeO4的量减少,导致高铁酸根离子与NDPhA发生有效碰撞的概率减少,溶液中的氧化去除及絮凝作用不断减弱,所以去除效果逐渐减弱。
将上述数据进行线性拟合,结果如图2所示。由图2可知:R2为0.948 6,表明拟合的方程线性较好,符合一级动力学规律。
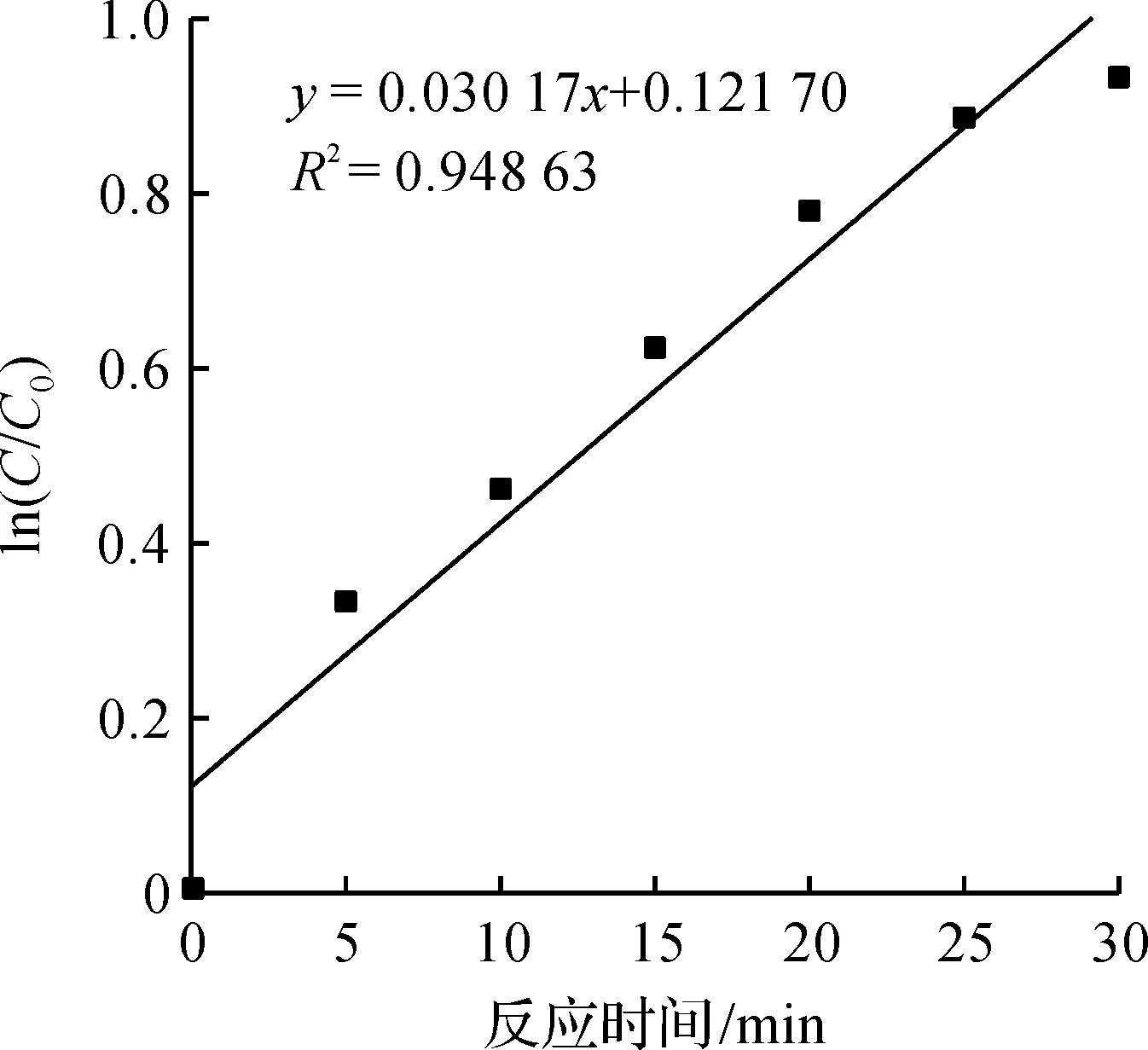
图2 ln(C/C0)与反应时间t的关系Fig.2 Relationship between ln(C/C0) and time
2.2 高铁酸钾投加量对NDPhA的去除影响
在25 ℃,pH值为7的条件下,将不同质量的K2FeO4投加到150 μg/L的NDPhA溶液中,去除结果如图3所示。
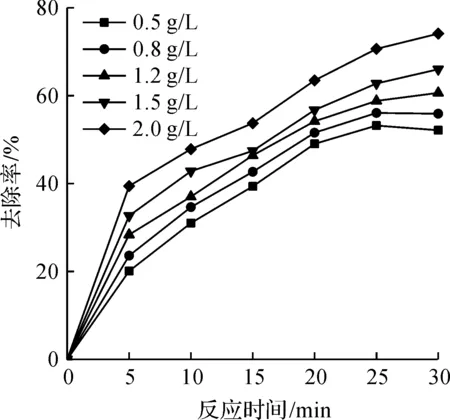
图3 投加量与去除效果的关系Fig.3 Relationship between dosage and removal effect
由图3可知:反应30 min,不同K2FeO4投加量对应的NDPhA去除率分别为52.14%,55.88%,60.65%,66.01%,74.12%,随着K2FeO4投加量的增加,NDPhA的去除率不断上升。主要原因:K2FeO4投加量的增加使得具有强氧化性的高铁酸根离子质量浓度增多,高铁酸根离子与NDPhA发生有效碰撞的几率不断增加[23],所以NDPhA的去除率不断上升。同时,随着K2FeO4投加量的增加,水解生成的Fe(OH)3胶体的量不断增加,溶液中的絮凝作用显著增强,进一步提高了NDPhA的去除率。
将上述数据进行拟合,结果如表1和图4所示。由表1和图4可知:R2均大于0.915,表明数据线性拟合较好,符合一级反应动力学规律。
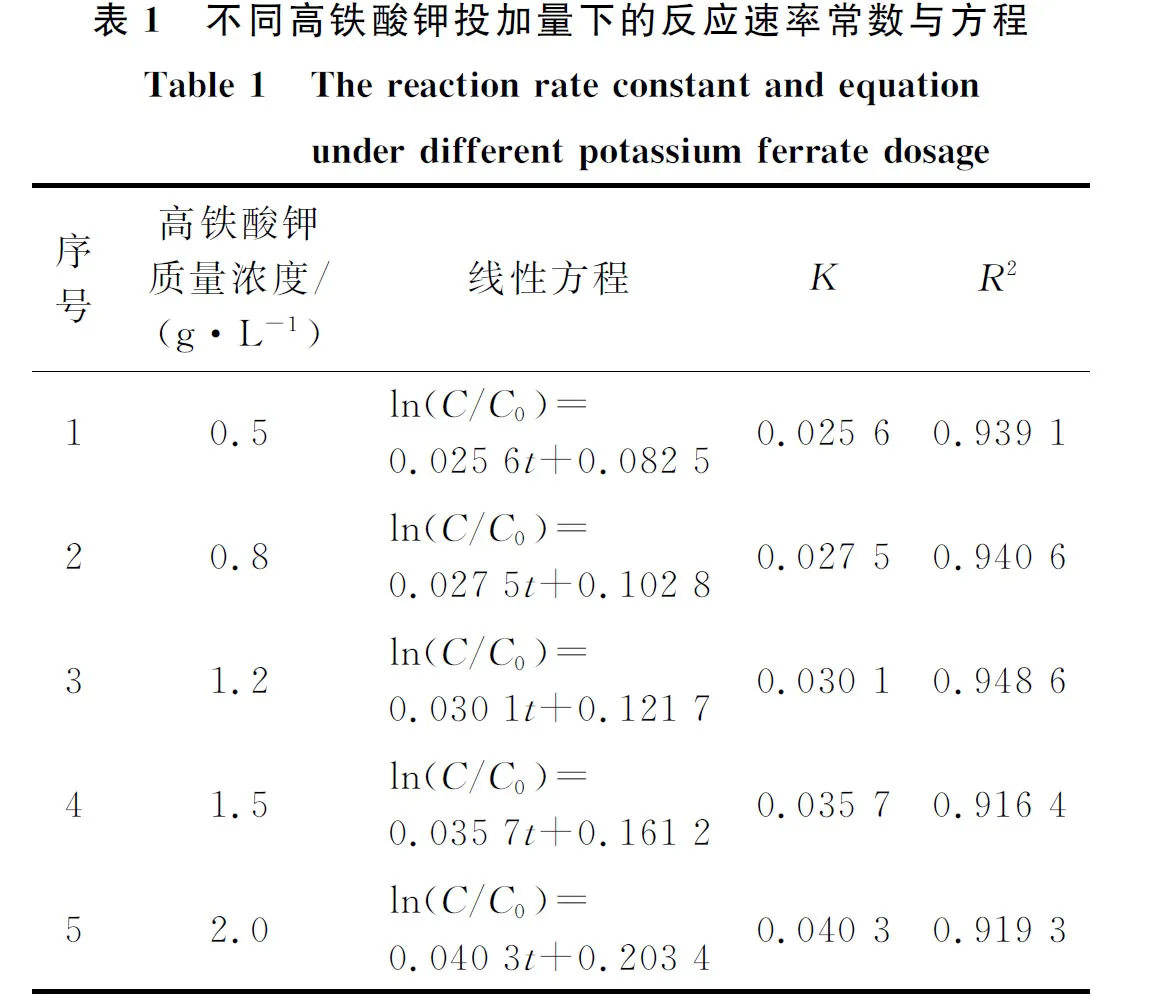
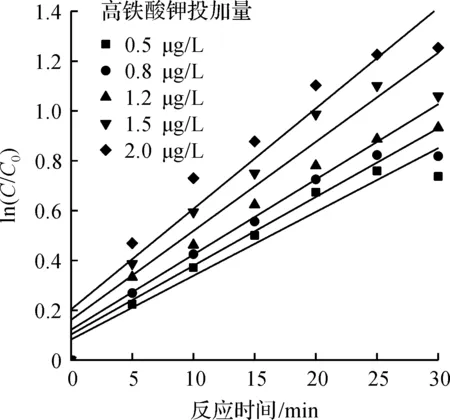
图4 不同高铁酸钾投加量下ln(C/C0)与时间t的关系Fig.4 Relationship between ln(C/C0) and timeunder different potassium ferrate dosages
2.3 pH值对NDPhA的去除影响
向150 μg/L的NDPhA溶液中投加1.2 g/L的K2FeO4,设置温度为25 ℃,pH值分别为5,6,7,8,9,反应结果如图5所示。

图5 pH与去除效果的关系Fig.5 Relationship between pH and removal effect

(5)
(6)
式中pKa(a=1,2)为解离常数。pKa能给予分子的酸性或碱性以定量的量度,pKa越小酸性越强,pKa越大碱性越强。
2.4 温度对NDPhA的去除影响
向质量浓度为150 μg/L的NDPhA溶液中投加1.2 g/L的K2FeO4,设置温度分别为15,25,35 ℃,pH值为7,反应结果如图6所示。
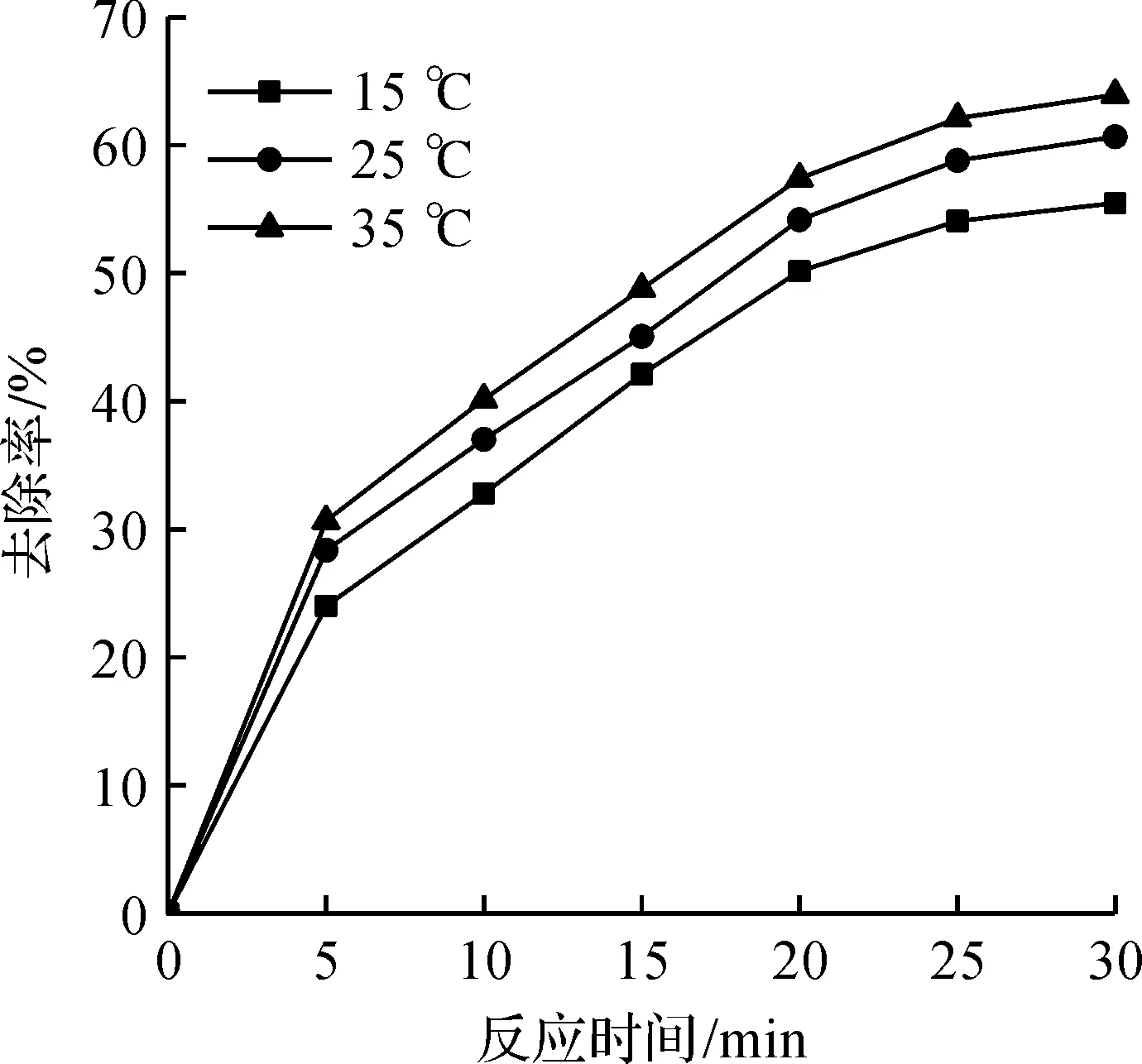
图6 温度与去除效果的关系Fig.6 Relationship between temperatureand removal effect
由图6可知:随着温度的升高,NDPhA的去除率也随之上升,但去除效果不明显,当反应30 min时,35 ℃对应的去除率为63.95%,比15 ℃时高8.47%。主要原因:温度上升会使分子动能升高,加快了运动速度,使得K2FeO4与NDPhA接触的概率增大,进而提高去除效果。温度上升,会降低K2FeO4的稳定性[26-27],导致K2FeO4更容易发生分解,使得NDPhA的去除效果减弱。
将上述数据进行线性拟合,结果如表2和图7所示。由表2和图7可知:R2均大于0.948,表明数据线性拟合较好,符合一级反应动力学规律。

表2 不同温度下的反应速率常数与方程
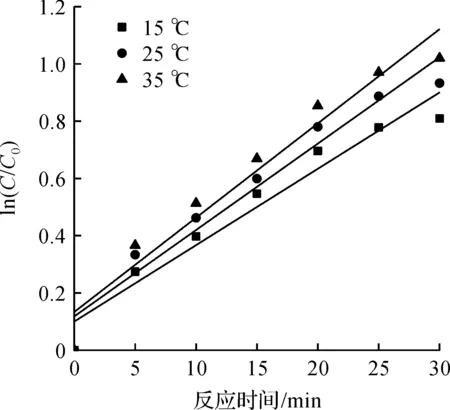
图7 不同温度下ln(C/C0)与时间t的关系Fig.7 Relationship between ln(C/C0) and timeat different temperatures
3 结 论