高校科研项目伦理管理现状及其对策研究
肖世华,苏锦云
(福建医科大学 科学技术处,福建 福州 350122)
随着生物医药科学研究的广泛开展,国家意识到伦理审查工作的重要性,通过多种渠道强化生物医学科研伦理管理工作的力度和深度。国家卫健委2016年对《涉及人的生物医学研究伦理审查办法》[1]进行修订,将伦理审查上升为行政法规,补充伦理审查原则、规程、标准和跟踪审查的相关内容,但未将高校纳入管理范畴。2019年10月,科技部、中央宣传部等多部委联合发文《科研诚信案件调查处理规则(试行)》[2]中将违反科研伦理规范行为列入科研失信行为。国家自然科学基金委自2019年起,在《项目申请指南》[3]中将科研伦理审查列入申请规定的总则要求,要求依托单位对涉及医学伦理的研究项目需提供所在单位机构伦理委员会的审查证明材料。高校是开展医学科学研究活动的重要阵地,在国家创新体系中占据重要的地位,其医学伦理状况直接影响科学研究的价值方向。高校积极成立医学伦理委员会推进伦理审查工作,在伦理审查、伦理决策和维护研究参与者权益等方面发挥了重要作用。但随着科技的不断发展,例如基因编辑等技术的出现,基础研究的伦理风险不断增加,加上高校科研项目的医学伦理审查与医疗机构存在较大差异,使《涉及人的生物医学研究伦理审查办法》无法直接应用于高校,迫使伦理审查委员会积极探索符合其自身实际的伦理审查制度规定(standard operating procedure,SOP)。因此,笔者通过梳理高校医学伦理委员会现状,探讨存在的问题并提出加强委员会建设的新思路。
一、科研项目伦理管理中的常见问题
高校医学伦理委员会建立时间较短或前期建设未得到重视,导致科研项目的伦理审查工作仍存在诸多问题。
(一)项目申报前伦理审查衔接不畅
伦理审查是高校伦理审查委员会对科研项目开展监督的重要手段之一,涉及伦理的科研项目需经伦理审查委员会审查通过后方可申报,但在实际工作中总有些项目未进行伦理审查。一方面,项目主管单位对伦理审查的重视程度会影响提交审查的积极性。以福建省X高校为例,对2017—2021年提出伦理审查的项目类型进行比较,发现提交伦理审查的国家自然科学基金(221项)比省科技厅项目(74项)多近2倍,分析原因可以发现,国家自然科学基金项目指南[3]中生命学部和医学部均要求提交所在单位或上级主管单位机构伦理委员会的审核证明,未提供相应证明的项目将无法通过形式审查,这促使科研人员申报这类科研项目前注意伦理审查申请,而省科技厅项目申报[4]通知对伦理审查无相应要求,提交伦理审查申请的项目明显较少。另一方面,大量自筹项目、自选项目或大学生创新项目等游离在审查体系之外,项目实施前未提交审查申请,立项后甚至投稿后才提交伦理审查申请[5-7]。从福建省X高校2017—2021年的自筹项目伦理审查申请情况来看,随着项目负责人伦理意识提高,自筹项目实施前提交伦理审查的数量不断增加,但申请量占总项目数的比例仍较低(图1)。
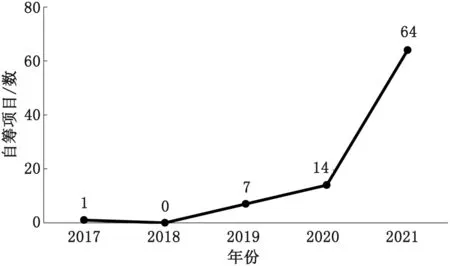
图1 福建省X高校2017—2021年自筹项目提交伦理审查情况
(二)项目执行过程中缺少监督环节
跟踪审查是伦理委员会以保护受试者权益为出发点,根据审查办法对通过审查并开始实施的项目进行监督和评价。目前伦理委员会在跟踪审查方面做的还不到位,原因包括两个方面,一是从机构设置看,机构伦理委员会大多挂靠某个行政部门,缺乏独立的办事人员、经费和场地。委员会大多由行政领导和学科带头人组成,委员基本为兼职,各类繁忙的事务使其职责履行程度大打折扣。二是从操作层面看,随着各单位科研体量的增长,涉及科研伦理的项目越来越多,监管难度不断加大。从福建省X高校2017—2021年提交伦理审查的项目数量来看,2021年比2017年增长了一倍多,年均增长21.3%(图2)。此外,随着审查科研项目内容的学科跨度越来越大、专业要求越来越高,伦理跟踪审查的难度逐渐增加。
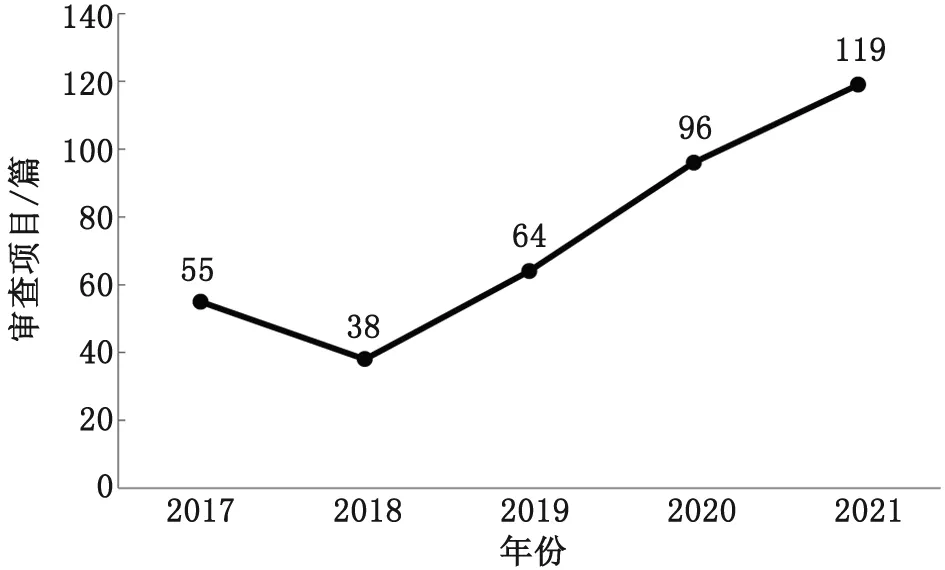
图2 福建省X高校2017—2021年伦理审查项目数量情况
(三)伦理档案管理不规范
随着涉及人的科研伦理的项目数量迅速增加,伦理档案数量也随之增加。高校从研究人员到管理人员对伦理档案管理的意识不强,伦理档案信息化还相对薄弱,档案多以纸质形式保存,导致伦理档案管理不规范。一是存在部分项目丢失知情同意书的情况,这与研究人员对知情同意书的保管意识不强密不可分,且没有相关文件规定知情同意书保存的时间期限,有些历史项目的知情同意书已经遗失。二是伦理审查的档案材料缺乏相关制度和规范,导致档案材料管理是否规范与管理人员的个人素质和责任心相关,影响归档材料的有序性和完整性,从而严重影响档案的质量,使其无法查阅,降低使用价值。
(四)伦理宣传教育力度不足
张莉莉[8]等人在国家自然科学基金资助下对我国从事基础研究的人员进行伦理认知方面的调查,发现科研人员的伦理意识强但知识和能力不足,有近半的科研人员没有接受过伦理知识的相关培训。这提示,一方面,我国医学科研伦理宣传已初见成效,绝大多数科研人员已具备伦理意识。另一方面,伦理教育培训工作还有待提高,应避免科研人员凭借个人直觉或者科学道德来判断伦理。鉴于伦理教育是一个系统工程,除了伦理委员会,还需科研管理部门、研究生院、教务处及各教学单位等多部门协同,共同参与到伦理教育培训工作中。
二、进一步完善高校科研项目伦理管理的政策建议
《关于加强科技伦理治理的指导意见》指出,科技伦理是科技活动中必须遵守的价值准则,根据增进人类福祉、尊重生命权利、公平公正、合理控制风险和保持公开透明的原则,健全多方参与、协同共治的治理体制机制,塑造科技向善的文化理念和保障机制[9]。作为伦理监督的一线,高校伦理委员会应结合涉及人的生命科学和医学研究的实际,充分落实和发挥委员会的职责和功能,尝试从以下几个方面进行改进。
(一)联合校内相关管理部门构建伦理审查保障机制
科研项目的生物医学伦理管理主体是高校伦理审查委员会,同时也需要相关职能部门(如科研管理部门)进行合作,将伦理审查工作嵌入到行政管理的流程当中。根据《涉及人的生物医学研究伦理审查办法》,伦理委员会不仅需要审查项目是否符合伦理要求,还需对研究者的资格、研究方案的科学性与先进性和风险性等进行审查。此外,科研项目申报的时限性对伦理委员会的审查效率提出了很高的要求。因此,第一,将项目申报资格和研究方案的审查纳入行政部门的管理流程中,由科研管理部门组织学术委员会及相关领域专家对项目进行低质量初筛,形成意见建议。通过审查的项目再提交给伦理委员会。这种联动方式审查有助于提高申报项目的质量,也可以从伦理角度进行约束,保障项目伦理审查的质量。第二,涉及伦理的在研项目可联合科研管理部门在项目中检、结题等节点进行跟踪审查,由项目组报送跟踪审查报告和结题报告,委员会根据不同伦理风险级别采取抽查或现场检查的方式进行检查,减轻项目负责人额外报送材料负担的同时提高审查效率。第三,与相关职能部门制定配套政策,形成“组合拳”让伦理委员会监督检查有抓手和着力点。将伦理审查作为项目申报必备的前置条件,并与经费下达、项目管理和科研诚信等内容挂钩,纳入项目绩效考核的指标体系。
(二)重视伦理委员会建设
为保障委员会高效运作,第一,应加强伦理委员会队伍建设。首先,应努力建立一支专业经验丰富、敢于担当的多学科专家队伍,能不受干扰地对科研项目进行审查,并且能提供专业培训和伦理咨询服务。其次,伦理委员会秘书应具备伦理审查基本知识和经验,以及一定的专业识别和处理问题的能力;可以初步审查申请材料,递交高质量的伦理审查材料供委员会审查。第二,建立高质、高效的伦理审查制度。审查制度是伦理委员会开展工作重要保障和准绳,不仅决定了伦理审查的质量,而且会影响审查的效率。根据伦理风险等级采取相应的伦理审查方式,如对已批准研究项目进行小修改且不影响研究风险收益比的项目可以开展快速审查,并以抽查方式进行跟踪审查。涉及人体生物样本或临床研究项目可由合作医院提供伦理说明后召开会议审查,并进行定期跟踪审查。针对特殊人群(如儿童、孕妇)开展的高伦理风险项目进行会议审查并进行全过程跟踪审查。第三,规范、健全科研项目审查材料的格式和内容。伦理审查相关表格有审查申请表、研究方案、知情同意书和进展报告等,统一规范的审查材料可大大减少伦理委员会的工作量,提高审查效率,且便于档案整理和存档。
(三)加强伦理教育和培训
医学伦理教育需伦理委员会成员、科研人员和受试者三方共同参与。第一,应加强对伦理委员会成员的培训。伦理委员会成员的知识储备和审查水平是保证审查质量的重要保障之一[7],定期培训和学习有助于提高委员审查水平。针对委员会新成员需重点开展包括科研项目的管理流程、伦理基本要求和必备信息的获取,研究方案和知情同意的要素要求,跟踪审查类别与目的等内容的培训,并帮助新成员知晓科研项目伦理审查申请过程的重点关注内容。此外,委员会全体成员应加强对外交流,通过积极参加生物医学伦理科技团体及其主办的会议或培训,增加同行交流,学习最新案例和先进经验。第二,加强科研人员伦理知识的储备。一方面,继续引导科研人员树立“受试者的权益、安全和健康必须高于对科学和社会利益的考虑”“生物医学研究必须通过伦理审查后方能开展”等伦理意识,形成科研人员主动提交伦理审查的自觉性,变“被动”伦理审查为“主动”。另一方面,要加强科研人员的伦理知识宣讲和技能培训,加强伦理相关法律法规和规章制度宣传,介绍伦理审查申请的流程及注意事项,针对研究方案、知情同意书的撰写等内容进行培训。第三,积极开展伦理教育与普及。高校伦理知识普及嵌入本科生和研究生教育,培养方案中设置医学伦理学课程,目前多数高校已开设医学伦理学课程,让学生入职前建立伦理概念、提升伦理意识。同时高校可以组织制作伦理知识科普宣传材料,向公众普及伦理知识[10]。伦理认知水平的提高有助于公众提升自我保护能力及强化监督伦理开展的意识,同时有助于消除公众参加科学研究的抵触情绪。
(四)建立健全伦理档案保存规范和流程
医学伦理档案是记录科研项目伦理审查全过程的原始记录,能够真实反映科研项目伦理审查经过、监督和指导的全过程,做好医学伦理档案规范化
管理有助于提升伦理审查质量。因此,第一,应建立健全相关档案管理制度。高校可以参照《档案法》《药物临床试验伦理审查工作指导原则》等相关规定,制定合理的存档和查档工作流程。此外,伦理档案记录科学研究全过程,可能涉及参与试验对象的个人信息等隐私,因此,还需完善档案保密制度。第二,推动伦理审查信息化。随着信息技术的不断发展,伦理档案的信息化管理越来越重要,实现无纸化办公,建立高效的会议流程,不仅能节约人力和物力,而且能减少档案材料存储的难度。

