复合透水材料在处理微污染水中的应用
周晓锋,黄 莉,张静娅
(1.河海大学理学院,江苏 南京 210000;2.南通市水利勘测设计研究院有限公司,江苏 南通 226006)
透水材料是利用材料自身的大孔隙率让雨水能下渗到基层土壤的建筑材料,在当前生态保护和城市建设中发挥着积极作用。海绵城市和水美乡村这两大环保理念的提出为系统治理我国水体污染、改善生态环境提供了绿色发展的方案,促进了我国社会和生态和谐发展、城镇和乡村协同发展。在微污染水体中,常见的水体危害有氮化物、磷化物和有机物,污水处理厂一些常见的治污手段在微污染水质治理中不经济、低效率,很难推广。因此本文提出从材料学和物理治理的角度来研究解决城乡微污染水。
1 复合透水材料的功能性原料
本文制备的透水材料是在保持传统透水材料的特性下,遵从绿色化、消耗农业废弃物的环保原则。复合透水材料原料有:煤粉、矸石末、锅炉渣、干化铝基污泥、复合农业固废弃物和活性炭。各原料的质量分数为40%煤粉、15%矸石末、20%锅炉渣、10%干化铝基污泥、10%复合农业固废材料、5%活性炭。
复合透水材料制备原料中的煤粉、矸石末、锅炉渣具有良好的透水能力;干化铝基污泥和复合农业固废弃物(花生壳、秸秆等)为废物利用,环保性强;活性炭粉能够进一步增强复合透水材料的吸附能力。
其中,干化污泥具有氮磷吸附作用;复合农业固废弃物由沸石、花生壳和秸秆等组成。这些固体废弃物能够大幅度增大材料比表面积,实现高效吸附,消耗植物废弃物,降低成本,变废为宝,是资源绿色化的有效途径。研究证实花生壳中含有65.7%~79.3%纤维素,可被酸水解为单糖,具有脱除重金属离子及螯合重金属离子的作用,可吸附废水中的重金属污染物铬(Cr)、铜(Cu)、铅(Pb)以及镉(Cd)等[1]。近年来许多研究者开展了秸秆吸附水中废弃物的研究[2],秸秆吸附的水中废弃物主要分为以下两种:一是有机物,如残留农药、印染废水中残留染料等;二是无机金属离子,如铁离子、铜离子等。
2 复合透水材料的制备方法及功能复合
2.1 透水材料的制备
(1)干化铝基污泥的制备。使用氯代十六烷基吡啶对铝污泥粉末进行改性,将铝污泥粉末造粒得到颗粒状的铝污泥基质,然后将铝污泥基质与粉煤灰以73∶27的质量比混合均匀;在1 000~1 020℃条件下煅烧获得干化铝基污泥。
(2)复合农业固废弃物的制备。按等质量比称取废石、矿渣、花生壳、梧桐叶和秸秆,混合后获得复合农业固废弃物。
(3)透水材料的制备。用天平按比例称取煤粉∶矸石末∶锅炉渣=40∶15∶20,加水放在容器内用搅拌器搅拌均匀作为基体材料;按10∶10∶5的质量比称取干化铝基污泥、复合农业固废弃物和活性炭粉,用蒸馏水和HPMA(水解聚马来酸酐)作为分散剂进行溶解和超声分散40 min,获得功能填料;将基体材料和功能填料混合,用搅拌器搅拌30 min;接着将混合浆体放入模具中,使用液压器在30 MPa下压制成立方体,放入烤箱在100℃下干燥;最后在高温炉中1 000℃烧炼30 min,得到成品。
2.2 复合光催化层
污水中的有机物、亚硝酸盐、硫化物等污染物需要氧化处理,化学需氧量(COD)可以间接地反映出水体中有机污染物的浓度和水体受污染的严重程度。为了增强材料微污水质处理能力,在前面制备透水材料的基础上对制备出来的吸污功能的透水材料进行表面喷涂修饰,本文中选用二氧化钛制备光催化层。复合透水材料光催化(去COD)层的制备步骤如下:
(1)将制备的透水材料进行表面湿润,用超声喷雾装置对透水材料表面进行水雾化喷淋,表面水润的目的是为了解决在后续喷涂层容易出现的粉化问题[3]。
(2)将5%二氧化钛水溶液溶解到醇酯十二成膜助剂中,用磁力加热搅拌的方式在磁力搅拌器中搅拌30 min。
(3)在湿润后的复合透水材料上二次使用二甲基亚砜进行超声喷雾再次湿润,将制备好的二氧化钛/醇酯十二成膜助剂均匀涂刷于浮床的表面,30 min后表面干燥成膜,进行二次涂刷。
(4)成品喷涂好二氧化钛/醇酯十二成膜助剂后,静置4 h,即得成品光催化涂层浮床。
光催化层位于透水材料表面之上,主要功能是在太阳光照射下进行光催化反应,降低水体中COD质量浓度。
2.4 复合除氮层、脱磷层
在3层结构复合透水材料(光催化层、除氮层、脱磷层)中,第一层使用的喷涂二氧化钛实现光催化功能,对于除氮、脱磷的功效主要由添加了花生壳、秸秆的透水材料的填充层实现,在制备阶段有针对性地加入沸石[4]和磷酸铵镁粉体(MAP)[5],利用这两类材料的固有特性结合多孔吸附的植物类材料,实现人工吸附透水材料的除氮、脱磷功效。
透水材料中除氮层、脱磷层的制备过程:
(1)将沸石粉体(1 000目)在水溶液中进行有效分散,分散时间为超声分散2 h,磁力搅拌0.5 h,配置的水溶液中沸石的含量为15%。
(2)将含量为15%的沸石溶液与其他固体废物一起在原料搅拌中添加。
(3)将磷酸铵镁粉体(1 000目)配制成水溶液,在2.1节透水材料的搅拌过程中进行添加,参与后续的压制过程,制备出包含磷酸铵镁粉体的复合透水材料。
3 复合透水材料的测试效果研究
3.1 天然沸石吸附氮磷实验
用天平称取2.0712 g NH4Cl和0.2637 g KH2PO4溶液倒入烧杯中,加入蒸馏水制作成1 L的模拟污水样品。得到污水中的磷元素的质量浓度为60 mg/L,氮元素的质量浓度为542.0 mg/L,磷氮比例为20∶1。在25℃环境下使用搅拌器转速为200 r/min,搅拌各组的实验溶液。
第一组实验:选用6 g粒径为180~200目的沸石加入装有模拟污水的烧杯中,使用磁力搅拌器分别搅拌20、40、60、80、100、120 min后过滤掉沸石。测定出不同沸石处理时间后水中氮磷量,获得沸石最佳的处理时间。
第二组实验:分别将粒径为130、150、170、190、210目的沸石倒入5个盛有模拟废水的烧杯中,机械搅拌(搅拌时长选取第一组实验中测出的最佳处理时间),过滤沸石测定氮磷质量浓度,得到沸石的最优粒径。
第三组实验:使用第一、第二组实验得到的处理时间和沸石粒径的最优参数,分别向盛有模拟污水的5个烧杯中加入6、8、10、12、14 g沸石,测定经过搅拌吸附后的氮磷质量浓度,得到最佳沸石使用量。
沸石吸附去除氮磷的实验结果:
(1)反应时间对氮磷去除的影响。
在图1氮磷去除率随时间变化,因为刚开始时污水中氮磷浓度高,新投放的沸石吸附效果也最强,所以氨氮的去除在反应最开始的时候比较迅速。沸石在10 min内完成对污染物的吸附,沸石吸附过程不超过15 min[6]。

图1 反应时间对氮磷去除的影响
在吸附过程进行一段时间后,沸石的吸附孔隙被污染物占据堵塞,吸附能力下降,同时,污水中的氮磷浓度减低,随着时间的推移,去污率的增长速率变缓。最终在15 min后,去污率的曲线趋向平缓不变。在实验中还能明显发现沸石对氮的去效果远超对磷的吸附效果。在沸石去污时间中推荐将沸石去污时间控制在80 min左右。
(2)沸石粒径对氮磷去除效果的影响。
沸石颗粒越细,它的比表面积就越大,相同量沸石颗粒和污水的接触面积就越大,沸石中的孔隙利用率就越高,吸附量就更多、吸附速率就更快。因此细颗粒沸石的净化污水效果越好。但当沸石颗粒的粒径小于120 μm(细度在200目以上)时,沸石的表面效应已经充分发挥,比表面积不再是影响吸附效果的主要因素。
虽然沸石粒径越小,比表面积就越大,单位质量沸石可交换活性点就越多,因而吸附去除率就越高。考虑到沸石的收集和成本,推荐使用170~200目细度的沸石。

表1 沸石粒径、用量和去污时间实验
(3)沸石用量对氮磷去除效率的影响。
沸石用量的增加可以提高对污水中氮磷的吸附量和吸附速率。随着对沸石使用量的增加,对污水中氮磷的去除率变缓,接近对数曲线,沸石用量达到饱和后,继续增加用量,沸石对氮磷的去除率也不会有明显的增加。当沸石用量控制在12 g/100 mL时,除污效果和成本综合效益最大。
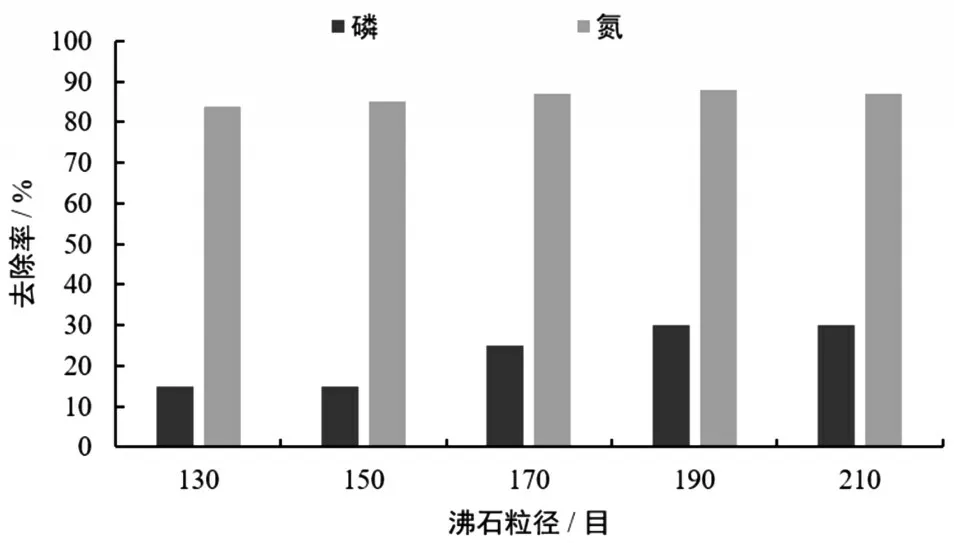
图2 沸石粒径对氮磷去除的对比

图3 沸石用量对氮磷去除的对比
3.2 MAP法与沸石吸附组合工艺去除氮磷实验(除氮层、脱磷层)
重复3.1节中模拟污水的制备步骤制备实验污水,按照镁磷质量比为1.5∶1计算出向模拟废水添加0.3274 g硫酸镁(MgSO4)药剂,再用烧碱溶液将污水调节成pH=10碱性环境。将配置好的溶液不断搅拌15 min后,静止沉淀,过滤后,测定氮磷浓度。氨氮的测定用钠氏试剂分光光度法;正磷酸盐的测定采用钼锑抗分光光度法。
组合MAP沉淀法和沸石吸附法共同去污,将MAP沉淀过滤后的溶液在沸石去污最佳时间、用量、粒径的条件下再次开始沸石氮磷实验,测算最后溶液中的氮磷量。
变化MAP沉淀后的溶液中pH值并通过添加镁盐改变Mg2+浓度,探究H+和Mg2+沸石效果的影响,寻找MAP和沸石组合去污的规律。
污水原始的氮磷质量浓度分别为542.0 mg/L、60.0 mg/L,通过单纯的MAP沉淀法以及MAP-沸石组合工艺处理的效果如表2所示。
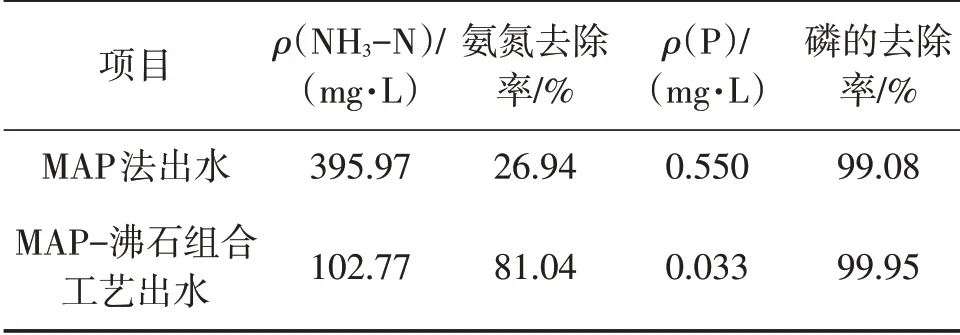
表2 组合工艺的除氮脱磷效果
通过结合具有高效去磷的MAP沉淀法和对氨氮高效去除率的沸石吸附法,可以实现对氮磷污染物的同时去除且效果非常可观。两种方法的机理分别为:MAP法通过增加反应物Mg2+的浓度、减小生成物H+的浓度促进化学反应向正向进行,高效脱磷;在碱性环境中NH4+易于形成氨气被沸石所吸附,高效除氮。
3.3 TiO2光催化层去除COD实验
污水样品取自河海大学莲池污水,检测得到COD的初始质量浓度为21 540 g/ml。
实验仪器有:天平、紫外灯光源和烧杯若干。
实验步骤:将光源垂直悬挂在实验台15 cm上方,将污水样品放置在光源正下方的磁力搅拌器上。向每组烧杯中添加定量二氧化钛粉末,开启紫外光和搅拌器进行实验,一段时间后关闭仪器,过滤溶液,测定COD的浓度。
(1)光照时间对COD去除率的影响。
在TiO2用量不变的条件下,分别控制每次光催化时间的长短,研究光照时间对COD去除效果的影响。
本次实验选取的时间参量分别是:0、4、8、12、16、20 h。实验结果如表3所示。

表3 光照时间对COD去除率的影响
(2)TiO2用量对去除COD的影响。
本次实验通过改变添加进污水中的TiO2用量来研究光催化剂用量对去除COD的影响。实验控制TiO2用量参数分别是0、2、4、6、8 g/L。实验结果如表4所示。

表4 TiO2用量对COD去除率的影响
通过以上实验分析可得,光催化刚开始的时候COD去除速率最快,随着氧化反应的进行,化学反应中的反应物COD浓度降低,生成浓度升高,氧化反应的速率减小。最终化学反应的正向速率和反向速率达到相等,即化学平衡状态,溶液中的各物质的浓度不再变化。从图4知TiO2催化COD反应,室温条件下15 h达到平衡,去除率在26%左右。要提高去除率可以通过沉淀生成物浓度,改变反应条件来实现。

图4 COD去除率随光照时间的变化
如图5所示在TiO2用量对COD影响实验中,起初TiO2质量浓度过低,催化剂对氧化过程的影响较小,当TiO2质量浓度增加到4 g/L后,催化剂对氧化反应的影响增强,当催化剂的质量浓度增加到6 g/L后,催化剂用量达到饱和,反应物质量浓度和其他条件因素成为制约COD去除率的主要因素。

图5 TiO2用量对COD去除率的影响
3.4 水质实测实验
实验用水釆用人工配水和实际取样相结合的方式,在河海大学莲池取样污水滴加NH4Cl和KH2PO4混合溶液使其与微污水成分基本相似。使用复合透水材料进行水质净化的效果如表5所示。

表5 水体污染物净化效果对比
(1)水中的NO3-N浓度从经过硝化反应后累积到的52.7 mg/L下降为29.2 mg/L,NO3-N的转化率为52.15%。
(2)水中的总磷去除率约为90.58%,水中悬浮物的去除率约为98.18%。
综合分析得到,复合透水材料对水中的总氮、总磷、COD都有较好的处理效果,满足初始设计的原理要求,达到了设计时的处理微污染水目标。
4 结论
(1)复合透水材料整体分为3个功能层,分别为光催化层、除氮吸附层、脱磷吸附层。
(2)光催化层在水面之上,主要功能是在太阳光照射下进行光催化反应,降低水体中COD质量浓度。通过添加的秸秆、花生壳类等农业固废弃物的大比表面积增大吸附量,同时大幅提高二氧化钛的光催化去除COD效率。
(3)除氮层,直接接触微污染水体,利用沸石、花生壳、秸秆等材料复合,大幅增大比表面积,高效去除水体中的氮含量。
(4)脱磷层,直接接触微污染水体,利用沸石、MAP、秸秆等,大幅增大比表面积,同时利用功能填料的阳离子交换能力和磷复合形成磷固体液,被强化吸附层吸收,高效去除水体中的磷含量。
(5)通过整体透水的植物纤维和多孔特点,粗纤维素所含的羟基上的氢原子物化性质非常活泼,可以螯合重金属离子使其在污水中脱除。还有秸秆花生壳的高表面比,在重金属离子的物理吸附方面能发挥很好的效果,对磁性絮状物(水处理残留)进行直接吸附,对非磁性污染物、杂质金属离子等进行磁化,提高微污染水的生物水净化进程及降解效率。

