油田采出水模拟溶液中咪唑啉类缓蚀剂残余浓度检测技术
周祥,逄建鑫,叶正荣,武冬明,伊然,崔晓东,刘翔,孙建波,孙冲
油田采出水模拟溶液中咪唑啉类缓蚀剂残余浓度检测技术
周祥1,逄建鑫2,叶正荣1,武冬明2,伊然1,崔晓东1,刘翔1,孙建波2,孙冲2
(1.中国石油勘探开发研究院,北京 100083;2.中国石油大学(华东) 材料科学与工程学院,山东 青岛 266580)

咪唑啉类缓蚀剂;残余浓度检测;紫外–可见分光光度法;矿化度;pH;Fe3+
在油气开采过程中,油气管材往往面临严重的CO2/H2S腐蚀问题[1-3]。在众多腐蚀防护措施中,缓蚀剂具有成本低、操作简单、不影响金属材料的机械性能、使用灵活等优点,被认为是抑制碳钢腐蚀最为经济有效的方法[4-6]。咪唑啉及其衍生物是高效的有机缓蚀剂,尤其是在酸性介质(CO2或H2S环境)中具有优良的缓蚀性能。因此,在国内外油田使用的有机缓蚀剂中咪唑啉的用量最大[7-10]。但是,咪唑啉类缓蚀剂在高温条件下易发生水解开环反应,生成酰胺类物质,进而导致缓蚀剂失效[11]。随着缓蚀剂在油田环境中服役时间的延长,其有效质量浓度将会降低,进而影响其防腐效果[12]。因此,需要对油田采出水中缓蚀剂的残余浓度进行检测,以便制定更合理有效的加药周期,确定最为经济的加药量,从而确保缓蚀剂的防护效果[13-14]。
目前,有关缓蚀剂浓度的检测方法已有众多研究报道,包括交流阻抗法、液相色谱法、荧光光谱法、两相滴定法、萃取显色法、红外分光光谱法、紫外–可见分光光度法等[15-24]。交流阻抗法适合测定的缓蚀剂范围广,但测试结果受采出水中氧含量、油含量等因素影响较大,测定不准确[15-16]。液相色谱法测灵敏度高,但其只适合痕量分析,且对油田采出水的预处理要求高,一般也不具备实现油田现场缓蚀剂浓度快速检测的仪器条件[15,17]。荧光光谱法操作简便,但是荧光剂的加入量不同对试验结果有很大的影响[18-19]。两相滴定法对测试人员的化学试验技能要求较高[20-21]。而萃取显色法则需要添加特殊显色剂[18,22-24],对水溶液预处理要求较高。红外分光光谱法[16]测定速度较快,试样的用量较少,但是咪唑啉类缓蚀剂在红外光区无明显吸收峰,因此红外分光光谱法并不能用于检测咪唑啉类缓蚀剂浓度。这也一定程度上限制了这些方法在油田用缓蚀剂浓度检测中的应用。紫外–可见分光光度法具有谱图简单、灵敏度高、检出限低、操作简便快速等优点。相比上述几种方法,其能够满足油田采出水中缓蚀剂浓度准确快速检测的需求,被普遍认为是适用于油田用咪唑啉类缓蚀剂浓度检测的有效方法之一[15-16,20-21]。然而,紫外–可见分光光度法的检测精度受到众多因素的影响。相关研究表明,油田采出水中常见的Na+、K+、Mg2+、Cl‒、SO42‒等离子,pH值的变化以及管材腐蚀产生的Fe2+或Fe3+等均会影响咪唑啉类缓蚀剂的吸光度值,进而影响缓蚀剂浓度的检测精度[15,20,25]。
本文采用紫外–可见分光光度法研究了油田采出水矿化度、pH值及Fe3+等对咪唑啉类缓蚀剂吸光度的影响,探究了不同因素影响下咪唑啉类缓蚀剂的浓度与其吸光度之间的相关性。基于试验结果,消除了各种因素对缓蚀剂浓度检测的干扰,提出了适用于咪唑啉类缓蚀剂浓度检测的技术方法,为油田采出水中缓蚀剂残余浓度检测提供了一种潜在的策略。
1 试验
1.1 试验原理及方法
有机化合物的吸收峰是由于分子中某些基团的存在而产生的,每一种基团都具有特征的吸收峰。咪唑啉分子结构中含有2个N原子的五元杂环,其中C==N双键在紫外区200~300 nm波段有较强的特征吸收峰[21]。在特征吸收峰值处的物质对光的吸收值与物质的浓度相关。根据朗伯–比尔定律,溶液的吸光度与溶液浓度和液层厚度的乘积成正比,见式(1)。即在特定的溶液层厚度下,缓蚀剂浓度与吸光度呈线性关系。基于上述原理,采用紫外–可见分光光度法测定咪唑啉类缓蚀剂残余浓度的基本方法为:(1)测量缓蚀剂溶液的紫外吸收光谱,根据图谱确定缓蚀剂特征吸收峰的波长;(2)在特征吸收峰波长处测量不同浓度缓蚀剂溶液的吸光度值,基于线性关系式(1),对不同缓蚀剂浓度下的吸光度测量数据进行线性拟合,得到吸光度与缓蚀剂浓度的线性方程;(3)在特征吸收峰波长处测定未知缓蚀剂浓度样品溶液的吸光度,代入(2)中所得线性方程,计算样品的缓蚀剂浓度。
=(1)
式中:为吸光度,无因次量;为吸光物质在特征波长、溶剂和温度条件下的特征常数,L/(mol·cm);为液层厚度,cm;为咪唑啉类缓蚀剂浓度,mol/L。
1.2 缓蚀剂吸光度测量
本文采用的缓蚀剂为国内某油田应用的KTY– A1型和KTY–X2型咪唑啉类缓蚀剂。采用去离子水配制不同浓度缓蚀剂溶液,即标准溶液。采用岛津– UV1800型紫外–可见分光光度计测定标准溶液的紫外吸收光谱,扫描波长范围为200~600 nm。测量不同浓度缓蚀剂的吸光度,研究标准溶液中缓蚀剂浓度与其吸光度的相关性,缓蚀剂质量浓度范围为0~ 300 mg/L。
采用去离子水和分析纯试剂分别配制不同浓度的缓蚀剂溶液,即非标准溶液。模拟国内某油田地层采出水组成,配制不同矿化度的水溶液,其化学组成如表1所示。采用NaOH、HCl、K2HPO4∙3H2O、NaH2PO4∙2H2O及去离子水配制不同pH的水溶液,pH值范围为2.5~11。采用FeCl3∙6H2O和去离子水配制不同Fe3+浓度的水溶液,Fe3+质量浓度范围为0~ 280 mg/L。采用紫外–可见分光光度计测定上述非标准溶液的紫外吸收光谱和吸光度,研究采出水矿化度、pH及Fe3+等因素对缓蚀剂浓度检测的影响。
表1 国内某油田地层采出水的模拟水溶液化学组成

Tab.1 Chemical composition of the simulated formation water extracted from a carbonate oilfield in China mg/L
2 结果与分析
2.1 标准溶液中缓蚀剂浓度与吸光度的相关性
图1为标准溶液中KTY–A1型缓蚀剂的紫外吸收光谱。不含缓蚀剂的标准溶液的紫外吸收光谱在测试波长范围内无特征峰出现。当添加不同浓度KTY– A1型缓蚀剂后,在234 nm波长处出现1个特征峰,即为KTY–A1型缓蚀剂的特征吸收峰。特征吸收峰的位置不随缓蚀剂浓度变化,但其峰值(即吸光度)受缓蚀剂浓度影响显著。因此,需在234 nm波长处测定KTY–A1型缓蚀剂的吸光度。图2示出了在234 nm波长处不同浓度KTY–A1缓蚀剂的吸光度测量值。显然,KTY–A1缓蚀剂浓度与吸光度之间存在良好的线性关系。根据朗伯–比尔定律,拟合测量数据得:
s1=0.003 35c1(2)
式中:1为KTY–A1型缓蚀剂浓度,mg/L;S1为标准溶液中KTY–A1型缓蚀剂的吸光度,无因次量。上述经验公式为标准状态下KTY–A1型缓蚀剂浓度与其吸光度的关系式。后文中不同影响因素试验的测量数据均以标准态数据作为参考标准,从而确定不同因素对缓蚀剂浓度检测的影响。

图1 在标准溶液中不同浓度KTY–A1型缓蚀剂的紫外吸收光谱
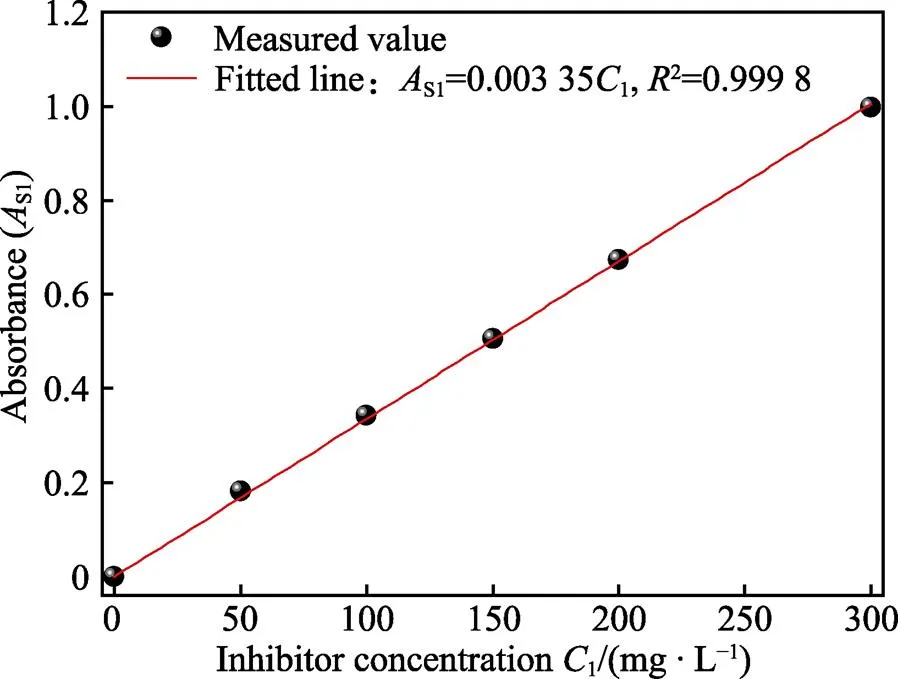
图2 在标准溶液中KTY–A1型缓蚀剂浓度与吸光度的关系
2.2 不同因素对缓蚀剂浓度检测的影响
2.2.1 介质矿化度的影响
图3为不同矿化度溶液中100 mg/L KTY–A1型缓蚀剂的紫外吸收光谱。可见,介质矿化度变化及各种离子的存在不会改变KTY–A1型缓蚀剂的特征峰波长。图4是不同矿化度溶液中不同KTY–A1型缓蚀剂浓度对应的吸光度。与标准溶液(矿化度0 mg/L)相比,在209 154 mg/L矿化度溶液中Na+、K+、Ca2+、Mg2+、Cl‒和SO42‒的存在几乎不改变吸光度的大小以及缓蚀剂浓度与吸光度的线性关系,说明其对缓蚀剂浓度检测的影响不大。在123 473 mg/L矿化度水环境中,各种离子的存在不改变缓蚀剂浓度与吸光度的线性关系,且线性变化斜率基本与标准溶液相同,但是该介质环境的吸光度显著增加。
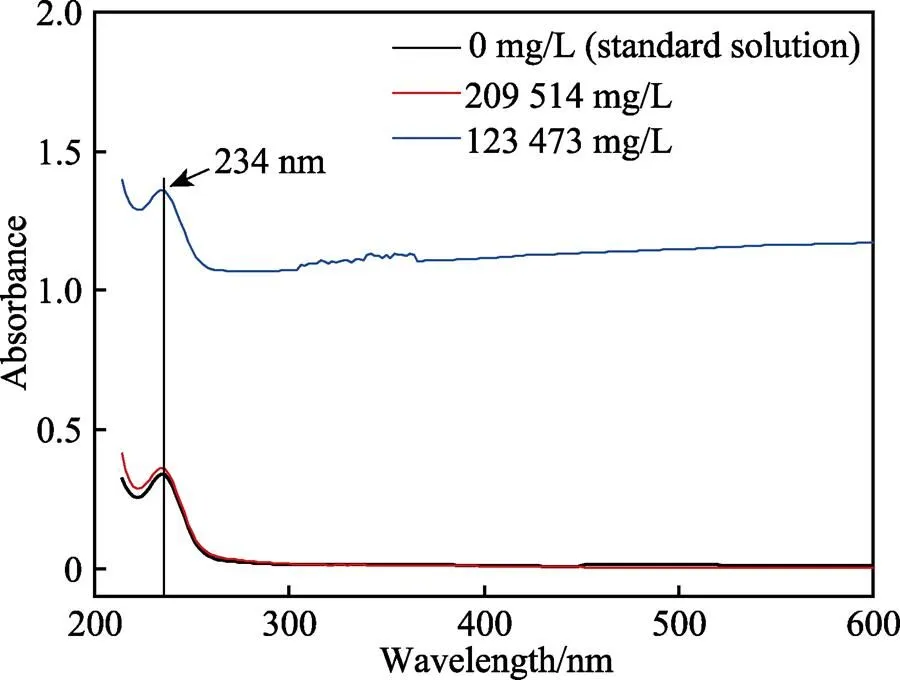
图3 不同矿化度溶液中100 mg/L KTY–A1型缓蚀剂的紫外吸收光谱
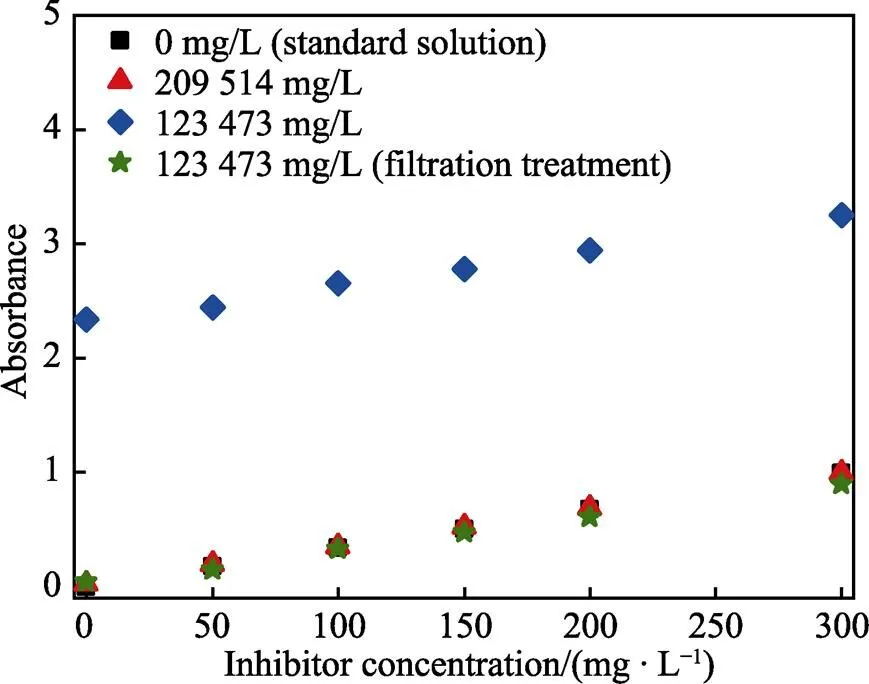
图4 在不同矿化度溶液中KTY–A1型缓蚀剂浓度与吸光度的关系
与209 154 mg/L矿化度溶液相比,123 473 mg/L矿化度溶液中不含K+,含有HCO3‒,且SO42‒浓度有所增加,而主要离子Na+、Ca2+、Mg2+和Cl‒的浓度大大降低(表1)。上述差异不足以说明吸光度的变化与离子种类及浓度的差异有关。值得注意的是,室内配制的209 154 mg/L矿化度溶液是清澈透明的,而123 473 mg/L矿化度溶液为悬浊液,这可能影响紫外光的透过性,进而干扰缓蚀剂的吸光度的检测。为了证实该推测,对123 473 mg/L矿化度溶液进行过滤处理,并测量过滤后溶液的吸光度,如图4所示。显然,过滤后溶液的吸光度显著降低,这证实混浊介质对于缓蚀剂吸光度的测试结果具有显著影响。不同缓蚀剂浓度条件下过滤后溶液的吸光度与标准溶液及209 154 mg/L矿化度溶液的吸光度近似相同,这表明Na+、K+、Ca2+、Mg2+、Cl‒、SO42‒、HCO3‒等离子的存在以及其浓度的变化不改变KTY–A1型缓蚀剂的吸光度,即对缓蚀剂浓度检测的干扰程度低。
上述结果表明,在采用紫外–可见分光光度法对采出水进行缓蚀剂浓度检测之前,需要对采出水进行过滤处理,去除水中悬浮固体颗粒、浮油等影响吸光度测定的干扰物质。
2.2.2 pH的影响
图5示出了在含150 mg/L KTY–A1型缓蚀剂溶液中pH值对缓蚀剂吸光度的影响。在碱性环境中pH值的变化(7~11)对KTY–A1型缓蚀剂吸光度基本无影响。当溶液由中性转变为弱酸性时,吸光度值发生变化。例如,在pH=6.15(采出水pH=6.13~6.18)时,缓蚀剂的吸光度相对于标准溶液降低约0.03。随着pH进一步降低,吸光度呈近似线性增加。根据线性变化规律,大约在pH=3.5左右,缓蚀剂的吸光度回归到中性或碱性条件下的水平(即标准溶液条件下的水平)。总体上看,酸性介质pH的变化对缓蚀剂吸光度会产生一定影响。在pH=2.5~7的测试范围内,缓蚀剂的吸光度在–0.02~0.02内波动。基于标准状态下缓蚀剂浓度与吸光度关系经验公式(2),计算可得上述波动造成的检测误差约为±5 mg/L。相比测试条件下150 mg/L的缓蚀剂浓度,上述误差非常小。
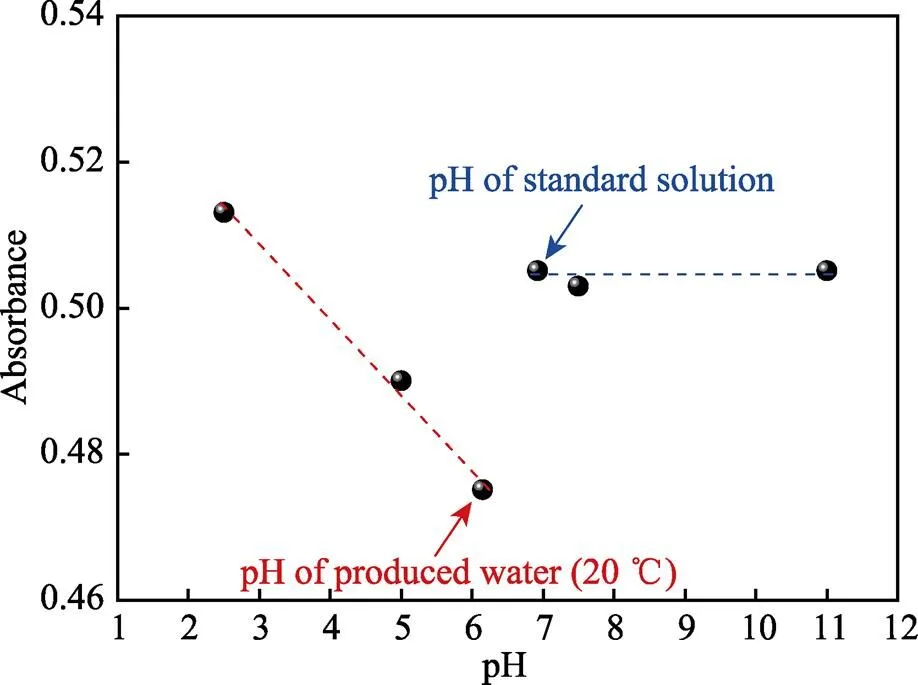
图5 在含150 mg/L KTY–A1型缓蚀剂溶液中pH值对吸光度的影响
鉴于pH=6.15的弱酸性环境对吸光度的影响相对较大,进一步测量了该环境条件下含不同浓度缓蚀剂溶液的吸光度,并与标准溶液(pH=6.93)作比较,如图6所示。尽管在较高缓蚀剂浓度下弱酸性环境对缓蚀剂吸光度的影响较大,但是随着缓蚀剂浓度的降低,其与标准溶液的吸光度偏差越来越小。总体上看,介质pH对于缓蚀剂浓度检测的影响较小。
2.2.3 铁离子的影响
含不同浓度的Fe3+溶液中100 mg/L KTY–A1型缓蚀剂的紫外吸收光谱,如图7所示。当Fe3+浓度较低时,仍可在234 nm波长处检测到KTY–A1型缓蚀剂的特征吸收峰。随着Fe3+浓度的增加,紫外吸收光谱发生明显变化,在较广的波长范围内紫外吸收光谱强度显著增加。当Fe3+质量浓度的增加到56 mg/L时,KTY–A1型缓蚀剂的特征吸收峰被Fe3+产生的高强度紫外吸收光谱掩盖。当溶液中Fe3+增加至280 mg/L时,在缓蚀剂特征吸收峰周围一定波长范围内,光谱强度超过了紫外–可见分光光度法的最大检测极限(吸光度极限值为4)。上述结果证实Fe3+会对缓蚀剂浓度检测产生严重干扰。因此,在缓蚀剂浓度检测过程中需要去除Fe3+的影响。
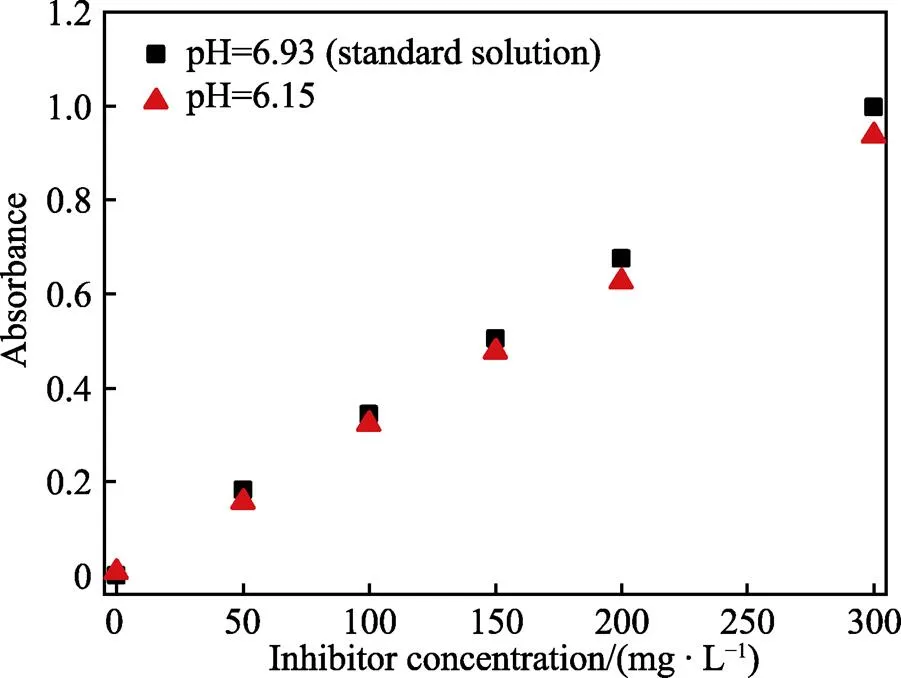
图6 在不同pH环境中KTY–A1型缓蚀剂浓度与吸光度的关系

图7 在含不同浓度Fe3+溶液中100 mg/L KTY–A1型缓蚀剂的紫外吸收光谱
图8示出了Fe3+浓度对KTY–A1型缓蚀剂吸光度的影响。Fe3+浓度与缓蚀剂吸光度存在良好的线性相关性,缓蚀剂浓度变化不改变两者的线性变化斜率。此外,在KTY–A1型缓蚀剂质量浓度为200 mg/L和Fe3+质量浓度为56 mg/L时,吸光度达到了极限值,其处于两者线性关系曲线上,说明进一步提高Fe3+浓度将无法测量缓蚀剂溶液的吸光度。结合图7,可以认为采用紫外–可见分光光度法检测KTY–A1型缓蚀剂残余浓度的临界Fe3+质量浓度为56 mg/L。
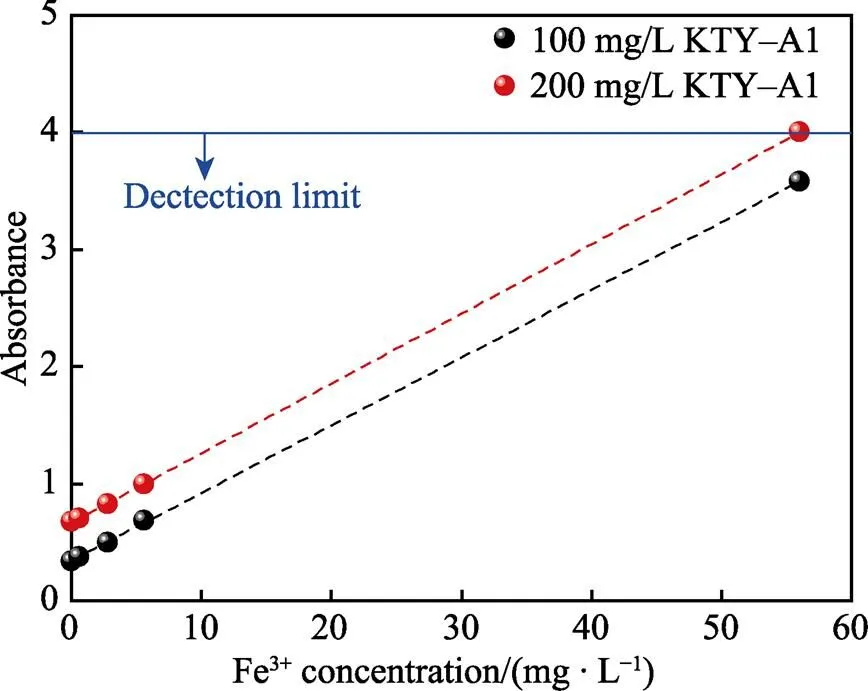
图8 Fe3+浓度对KTY–A1型缓蚀剂吸光度的影响
含不同浓度Fe3+环境中缓蚀剂浓度与吸光度的关系曲线,如图9所示。可见,Fe3+不改变缓蚀剂浓度与吸光度的线性关系。在不同Fe3+浓度下,缓蚀剂浓度与吸光度的线性变化斜率基本与不含Fe3+的标准溶液相同。显然,在某一固定Fe3+浓度下Fe3+导致吸光度的增量(即Fe3+的吸光度)为定值,与缓蚀剂的浓度变化无关。根据图8中Fe3+浓度与吸光度的线性关系,可以确定Fe3+的吸光度与其浓度之间存在线性相关性。为了证实上述推论,从图9中测量的含Fe3+的缓蚀剂溶液的吸光度(Fe3+和缓蚀剂的吸光度之和)中将通过标准溶液测得的缓蚀剂吸光度去除,即可获得不同浓度Fe3+的吸光度,如图10所示。可见,Fe3+浓度与其吸光度存在良好的线性相关性。对测量数据进行线性拟合可得:
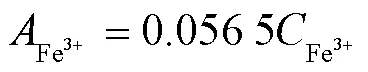
式中:为Fe3+质量浓度,mg/L;为Fe3+的吸光度。在特定缓蚀剂类型下,不受缓蚀剂浓度的影响,仅与Fe3+有关。

图10 Fe3+浓度与其吸光度的关系
2.3 非标准溶液中缓蚀剂浓度与吸光度的相关性
前文研究结果显示,介质矿化度(或介质中各种离子及浓度变化)和pH对于缓蚀剂吸光度的影响轻微,其对缓蚀剂浓度检测的影响可以忽略。因此,可以采用标准溶液中KTY–A1型缓蚀剂浓度与吸光度的关系式(2)计算确定缓蚀剂的残余浓度。为了进一步证实上述推论,通过对不同矿化度和pH条件下测量的数据进行线性拟合(图11),得到式(4)。
ns1=0.003 41(4)
式中:1为KTY–A1型缓蚀剂质量浓度,mg/L;NS1为不含Fe3+非标准溶液中KTY–A1型缓蚀剂浓度的吸光度。在不含Fe3+的情况下,NS1与水质组成及pH无关,仅与缓蚀剂浓度有关。对比式(2)和式(4)可见前者的斜率(0.003 35)近似等于后者的斜率(0.003 4),即标准溶液与非标准溶液(不含Fe3+)中缓蚀剂浓度与其吸光度的关系式相同。这证明在对采出水中缓蚀剂浓度检测时可以忽略采出水成分(Fe3+除外)及pH等因素的影响。
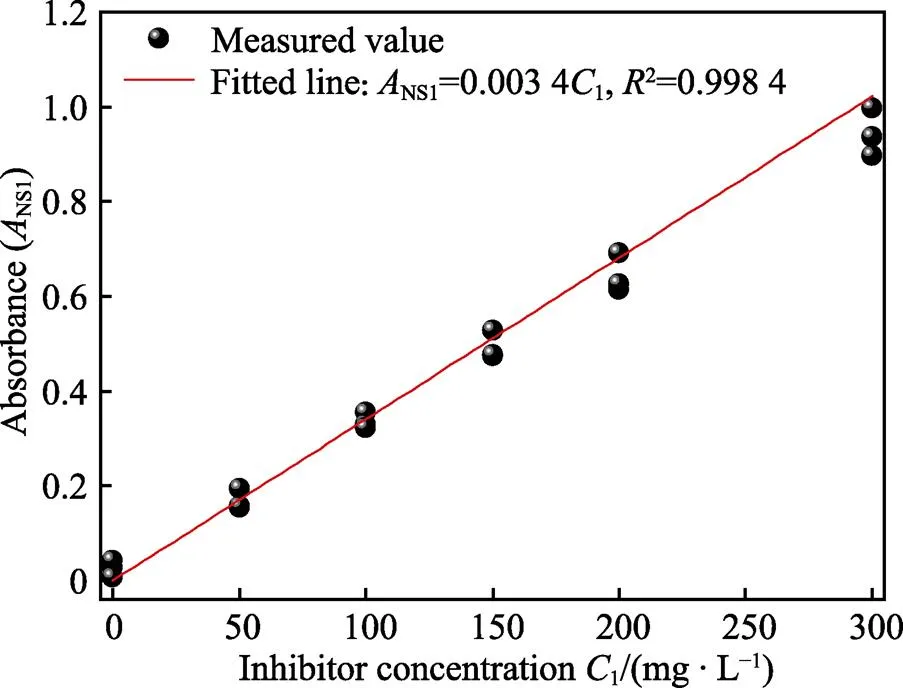
图11 在不含Fe3+的非标准水溶液中KTY–A1型缓蚀剂浓度与吸光度的关系
根据上述研究结果,当采出水样中不含Fe3+时,可以直接采用式(2)计算KTY–A1型缓蚀剂的残余浓度R1,将在234 nm波长处测得含KTY–A1型缓蚀剂水样的吸光度M1代入式(2)中,可得:
r1=294.12m1(5)
当采出水中含有Fe3+时,则要考虑Fe3+的影响,需将其产生的吸光度从测得的水样吸光度M1中去除,即:

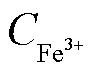

2.4 缓蚀剂残余浓度检测方法的适用性
由于缓蚀剂的特征吸收峰位置(波长)以及缓蚀剂与吸光度的相关系数随缓蚀剂类型的变化而改变。因此,基于KTY–A1型缓蚀剂提出的缓蚀剂残余浓度具体计算公式(5)和公式(7)不适用于其他咪唑啉类缓蚀剂的残余浓度检测。基于前文研究结果,当缓蚀剂类型改变后,首先需要确定该缓蚀剂的特征吸收峰波长以及缓蚀剂浓度与吸光度的经验公式。基于KTY–A1型缓蚀剂浓度与吸光度的线性相关性(图2和图11),至少需要测量2个未知缓蚀剂浓度的吸光度,即可得到未知缓蚀剂浓度与吸光度的关系式,进而计算在不含Fe3+溶液中缓蚀剂的浓度。当溶液中含有Fe3+时,将式(7)与式(3)联立,即可计算得到在含有Fe3+溶液中缓蚀剂的浓度。
为了验证上述方法的可行性,测量了另一种KTY–X2型咪唑啉缓蚀剂的紫外吸收光谱,确定其特征吸收峰波长为207 nm。在207 nm波长处测得不同浓度缓蚀剂的吸光度,如图12所示。通过线性拟合,获得KTY–X2型缓蚀剂与吸光度的关系式,如图12所示。通过测量未知KTY–X2型缓蚀剂浓度水样(不含Fe3+)的吸光度,利用式(5)则可确定缓蚀剂的浓度。为了验证式(5)的计算精确性,测量了含300 mg/L KTY–X2型缓蚀剂标准溶液(不含Fe3+)的吸光度,计算的缓蚀剂质量浓度为300.5 mg/L。由此可见,在不含Fe3+的标准溶液中KTY–X2型缓蚀剂的检测浓度与真实浓度之间误差很小。进一步测量了含Fe3+的模拟地层水溶液中150 mg/L KTY–X2型缓蚀剂的吸光度,并计算得到缓蚀剂的检测浓度,如表3所示。可见,在含2.24 mg/L和22.4 mg/L Fe3+的地层水溶液中KTY–X2型缓蚀剂的检测质量浓度分别为148.1 mg/L和158.5 mg/L,检测值与缓蚀剂的真实质量浓度150 mg/L之间的误差低于10 mg/L。显然,采用上述方法确定未知缓蚀剂样品浓度与吸光度的关系式是可行性。
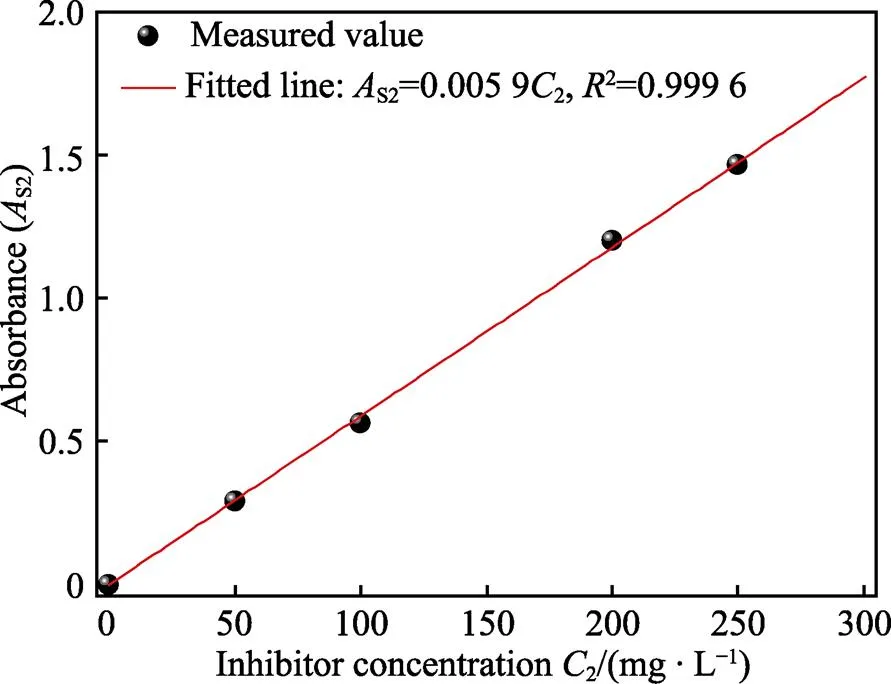
图12 在不含Fe3+的标准溶液中KTY–X2型缓蚀剂浓度与吸光度的关系
2.5 咪唑啉类缓蚀剂残余浓度检测技术
综合考虑前文研究结果,提出了一种咪唑啉类缓蚀剂残余浓度检测的方法及流程,具体技术方案如下。
1)取缓蚀剂样品,配制至少2种不同浓度的缓蚀剂溶液,采用紫外–可见分光光度计测量缓蚀剂溶液的紫外吸收光谱。确定特征吸收峰波长,并在波长处测定至少2个缓蚀剂浓度对应的吸光度。绘制缓蚀剂浓度与吸光度标准曲线,拟合确定二者线性关系式,即确定相关系数值:
=(8)
2)提取含未知浓度缓蚀剂的采出水样品,对水样进行过滤处理,去除水样中的悬浮颗粒等影响吸光度测定的干扰性物质。提取过滤后的水样2 mL,采用便携式紫外–可见分光光度计在波长处测量水样的吸光度。
表2 在含Fe3+的模拟地层水溶液中KTY–X2型缓蚀剂检测浓度

Tab.2 Detected concentration of KTY-X2 corrosion inhibitor in simulated formation water with Fe3+
4)缓蚀剂残余浓度计算。根据(3)中检测结果,通过步骤(5)或步骤(6)中方法计算缓蚀剂残余浓度。
5)当采出水样中不含Fe3+时,将测得的水样吸光度代入式(8),即可获得现场缓蚀剂残余浓度R:
r=/(9)
6)当采出水中含有Fe3+时,需将其Fe3+产生的吸光度从测得的水样吸光度中去除,并联立式(3),即可获得缓蚀剂残余浓度R:

上述缓蚀剂残余浓度检测技术方案,在本文测试的缓蚀剂浓度范围内(0~300 mg/L),缓蚀剂残余浓度检测误差低于10 mg/L,而且采出水样中缓蚀剂的残余浓度越低,检测结果的误差越小。此外,当Fe3+质量浓度高于56 mg/L时,受限于紫外–可见分光光度法的吸光度范围(吸光度极限值为4),将无法采用该方法对缓蚀剂浓度进行检测。本文的研究结果可为油田现场咪唑啉类缓蚀剂残余浓度检测提供一种潜在的方法。但是,上述缓蚀剂残余浓度检测方法是基于模拟地层水试验结果提出的,而油田现场采出水通常比模拟地层水更加复杂。因此,仍需要通过进一步的研究确定其在油田实际采出水环境中的适用性和可靠性。
3 结论
1)油田采出水矿化度(或Na+、K+、Ca2+、Mg2+、Cl‒、SO42‒、HCO3‒等离子及其浓度变化)和pH值对咪唑啉类缓蚀剂的吸光度影响轻微,可以忽略其对缓蚀剂残余浓度检测的影响。
2)采出水中可能存在的悬浮物(浮油、固体颗粒等)及Fe3+对咪唑啉类缓蚀剂吸光度的测量影响很大,在缓蚀剂残余浓度检测过程中需要对采出水进行过滤处理,并去除Fe3+的干扰。
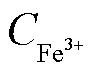
[1] ZHANG Chen, ZAHEDI ASL V, LU Yuan, et al. Investigation of the Corrosion Inhibition Performances of Various Inhibitors for Carbon Steel in CO2and CO2/H2S Environments[J]. Corrosion Engineering, Science and Technology, 2020, 55(7): 531-538.
[2] TIU B D B, ADVINCULA R C. Polymeric Corrosion Inhibitors for the Oil and Gas Industry: Design Principles and Mechanism[J]. Reactive and Functional Polymers, 2015, 95: 25-45.
[3] ZHENG You-gui, NING Jing, BROWN B, et al. Electrochemical Model of Mild Steel Corrosion in a Mixed H2S/CO2Aqueous Environment in the Absence of Protective Corrosion Product Layers[J]. Corrosion, 2015, 71(3): 316-325.
[4] 任铁钢, 苏慧双, 刘月, 等. 金属缓蚀剂的研究进展[J]. 化学研究, 2018, 29(4): 331-342.
REN Tie-gang, SU Hui-shuang, LIU Yue, et al. Research Progress of Metal Corrosion Inhibitors[J]. Chemical Research, 2018, 29(4): 331-342.
[5] VERMA D K, FANTAZI A A, VERMA C, et al. Experimental and Computational Studies on Hydroxamic Acids as Environmental Friendly Chelating Corrosion Inhibitors for Mild Steel in Aqueous Acidic Medium[J]. Journal of Molecular Liquids, 2020, 314: 4896.
[6] GUTIÉRREZ E, RODRÍGUEZ J A, CRUZ-BORBOLLA J, et al. Development of a Predictive Model for Corrosion Inhibition of Carbon Steel by Imidazole and Benzimidazole Derivatives[J]. Corrosion Science, 2016, 108: 23-35.
[7] 张明, 程刚, 方勇, 等. 缓蚀剂的研究现状及发展趋势[J]. 化工技术与开发, 2020, 49(4): 43-45.
ZHANG Ming, CHENG Gang, FANG Yong, et al. Research Status and Development Trend of Inhibitors[J]. Technology & Development of Chemical Industry, 2020, 49(4): 43-45.
[8] 郭文姝, 程丽华, 丛玉凤, 等. 磷酸酯基咪唑啉化合物的合成及其在HCl水溶液中的腐蚀抑制机理[J]. 表面技术, 2018, 47(5): 188-194.
GUO Wen-shu, CHENG Li-hua, CONG Yu-feng, et al. Synthesis of Phosphate-Based Imidazoline Compound and Its Corrosion Inhibition Mechanism in HCl Aqueous Solution[J]. Surface Technology, 2018, 47(5): 188-194.
[9] 陆原, 张国欣, 刘保山, 等. 丙炔醇改性硫脲基咪唑啉在CO2/H2S共存体系中对X65钢的腐蚀抑制作用[J]. 表面技术, 2021, 50(7): 345-350.
LU Yuan, ZHANG Guo-xin, LIU Bao-shan, et al. The Corrosion Inhibition Effect of Proparynol-Modified Midazolin on X65 Steel in CO2/H2S Co-Existence System[J]. Surface Technology, 2021, 50(7): 345-350.
[10] 刘然克, 王立贤, 刘智勇, 等. 咪唑啉类缓蚀剂对P110钢在CO2注入井环空环境中应力腐蚀行为的影响[J]. 表面技术, 2015, 44(3): 25-30.
LIU Ran-ke, WANG Li-xian, LIU Zhi-yong, et al. Effect of Imidazoline Corrosion Inhibitor on Stress Corrosion Cracking Behavior of P110 Steel in Simulated Annulus Environment in CO2Injection Wells[J]. Surface Technology, 2015, 44(3): 25-30.
[11] 王宁, 杜敏, 张静. 紫外分光光度法测定较高温度下咪唑啉类缓蚀剂开环程度[J]. 理化检验-化学分册, 2009, 45(8): 987-990.
WANG Ning, DU Min, ZHANG Jing. Determination of Degree of Opening of the Heterocyclic Ring of Imidazolinium Inhibitors at Elevated Temperatures by UV-Spectrophotometry[J]. Physical Testing and Chemical Analysis (Part B: Chemical Analysis), 2009, 45(8): 987-990.
[12] 潘若生. CO2驱采油井腐蚀监测技术研究[D]. 大庆: 东北石油大学, 2015.
PAN Ruo-sheng. Corrosion Monitoring Wells CO2Flooding Technology[D]. Daqing: Northeast Petroleum University, 2015.
[13] 张成果. CO2驱油集输管线缓蚀剂性能评价及现场加注工艺研究[D]. 大庆: 东北石油大学, 2013.
ZHANG Cheng-guo. Performance Evaluation and Research on Implantation Technique of Corrosion Inhibitor for Gathering Pipeline of CO2-EOR[D]. Daqing: Northeast Petroleum University, 2013.
[14] HEYDARI M, JAVIDI M. Corrosion Inhibition and Adsorption Behaviour of an Amido-Imidazoline Derivative on API 5L X52 Steel in CO2-Saturated Solution and Synergistic Effect of Iodide Ions[J]. Corrosion Science, 2012, 61: 148-155.
[15] 张云善, 徐晓峰, 周兴付, 等. 紫外分光光度法测定须家河组气井产出液中缓蚀剂的含量[J]. 石油与天然气化工, 2011, 40(3): 298-302, 308, 221.
ZHANG Yun-shan, XU Xiao-feng, ZHOU Xing-fu, et al. Determination of Corrosion Inhibitor Content in Prodduced Fluid from Xojiahe Gas Well by UV Speetrophotometry[J]. Chemical Engineering of Oil & Gas, 2011, 40(3): 298-302, 308, 221.
[16] 刘元清, 贾丽, 李志远, 等. 油田污水中咪唑啉缓蚀剂浓度检测技术研究[J]. 石油化工腐蚀与防护, 2002, 19(4): 57-59, 64.
LIU Yuan-qing, JIA Li, LI Zhi-yuan, et al. Study on Technique for Testing Imidazoline Inhibitor Concentration in Oil Field Waste Water[J]. Petrochemical Corrosion and Protection, 2002, 19(4): 57-59, 64.
[17] 郭学辉, 赵远鹏, 石明杰, 等. 反相高效液相色谱法分析油溶性咪唑啉缓蚀剂的主要成分[J]. 石油与天然气化工, 2010, 39(1): 70-74, 99.
GUO Xue-hui, ZHAO Yuan-peng, SHI Ming-jie, et al. Analysis of Principal Component of Oil-Soluble Imidazoline Corrosion Inhibitor via Reverse-Phase High Performance Liquid Chromatography[J]. Chemical Engineering of Oil & Gas, 2010, 39(1): 70-74, 99.
[18] 熊新民, 南楠, 石鑫, 等. 应用显色萃取法测定塔里木油田采出液中残余缓蚀剂的浓度[J]. 油气田地面工程, 2019, 38(2): 12-14, 21.
XIONG Xin-min, NAN Nan, SHI Xin, et al. Determination of the Residual Corrosion Inhibitor Concentration in the Produced Liquid of Tarim Oilfield by the Development-Extraction Method[J]. Oil-Gas Field Surface Engineering, 2019, 38(2): 12-14, 21.
[19] 郭贤贤. 油田采出水介质中咪唑啉缓蚀剂残余浓度的检测[D]. 武汉: 华中科技大学, 2012.
GUO Xian-xian. Detection of the Residual Concentration of Imidazoline Inhibitors in Oilfield Production Water[D]. Wuhan: Huazhong University of Science and Technology, 2012.
[20] 焦其正, 付朝阳, 王丽荣, 等. 油气田用咪唑啉类缓蚀剂浓度的检测方法[J]. 天然气工业, 2006, 26(6): 131- 133, 172.
JIAO Qi-zheng, FU Chao-yang, WANG Li-rong, et al. Concentration Measurement of Imidazoline Inhibitor Applied in Oil and Gas Field[J]. Natural Gas Industry, 2006, 26(6): 131-133, 172.
[21] 刘建国, 李言涛, 郑凤. 紫外分光光度法咪唑啉残余质量浓度分析[J]. 装备环境工程, 2012, 9(3): 115-117, 124.
LIU Jian-guo, LI Yan-tao, ZHENG Feng. Residual Mass Concentration Analysis of Imidazoline by Ultraviolet Spectrophotometry[J]. Equipment Environmental Engineering, 2012, 9(3): 115-117, 124.
[22] 于剑祥, 王林海, 魏强. 显色反应法的改进——海上油田高硬污水缓蚀剂浓度检测[J]. 中国海上油气, 2009, 21(4): 264-266.
YU Jian-xiang, WANG Lin-hai, WEI Qiang. Improvement of Color Reaction Method: The Concentration Test for Water-Soluble Corrosion Inhibitor in Highly Mineralized Industrial Wastewater on Offshore Oilfields[J]. China Offshore Oil and Gas, 2009, 21(4): 264-266.
[23] 谢娟, 王虎, 段明, 等. 显色反应法检测双子季铵盐缓蚀剂残余浓度[J]. 油田化学, 2014, 31(4): 615-619.
XIE Juan, WANG Hu, DUAN Ming, et al. Detecting Residual Concentration of Gemini Quaternary Ammonium Salt Corrosion Inhibitors by Color Reaction Method[J]. Oilfield Chemistry, 2014, 31(4): 615-619.
[24] 高秋英, 渠蒲, 贺海洲, 等. 西北油田水处理系统缓蚀剂浓度检测技术研究与应用[J]. 油气田地面工程, 2021, 40(12): 16-20.
GAO Qiu-ying, QU Pu, HE Hai-zhou, et al. Research and Application of Corrosion Inhibitor Concentration Detection Technology in Water Treatment System of Northwest Oilfield[J]. Oil-Gas Field Surface Engineering, 2021, 40(12): 16-20.
[25] MALIK H. Effect of pH on the Corrosion Inhibition of Mild Steel in CO2Saturated Brine Solution[J]. Anti-Corrosion Methods and Materials, 2000, 47(2): 88-93.
Residual Concentration Detection of Imidazoline Corrosion Inhibitor in Simulated Formation Water of Oilfield
1,2,1,2,1,1,1,2,2
(1. Research Institute of Petroleum Exploration and Development, PetroChina, Beijing 100083, China; 2. School of Materials Science and Engineering, China University of Petroleum (East China), Shandong Qingdao 266580, China)
The corrosion inhibitor has been widely used to mitigate the corrosion of carbon steel in oil and gas industry. The effective concentration of corrosion inhibitor inevitably decreases with the prolongation of its service time in oilfield environment, thereby affecting its anti-corrosion effect. It, thus, puts forwards an urgent demand for the residual concentration detection technology of corrosion inhibitor in oilfield. The primary objective of this study is to determine a feasible method used for the residual concentration detection of imidazoline corrosion inhibitor in oilfield. In this regard, the ultraviolet absorption spectrum and absorbance of imidazoline corrosion inhibitor were measured by ultraviolet-visible spectrophotometry in the solution with various salinity, pH and Fe3+concentration. The effects of the salinity of the simulated formation water, pH and Fe3+on the absorbance of corrosion inhibitor were investigated and meanwhile, how the above factors affecting the relationship between inhibitor concentration and absorbance were analyzed.
The results show that the variation of the salinity of produced water as well as the presence of ions such as Na+, K+, Ca2+, Mg2+, Cl‒, SO42‒and HCO3‒rarely affects the absorbance of corrosion inhibitor, which does not disturb the detection on the inhibitor concentration. However, the potential suspended substance in produced water has significant influence on the absorbance measurement of corrosion inhibitor. Therefore, the produced water needs to be filtered prior to the detection on inhibitor concentration. The change of pH in the range of 7 to 11 has no obvious effect on the absorbance of corrosion inhibitor while that in the range of 2.5 to 6 results in the fluctuation of absorbance within –0.02-0.02, which can cause the small detection error of about ±5 mg/L for the corrosion inhibitor. The influence of the possible Fe3+in produced water on the absorbance measurement of corrosion inhibitor is very huge. It is necessary to eliminate the interference of Fe3+on the absorbance measurement of corrosion inhibitor when conducting the inhibitor concentration detection on the produced water containing Fe3+.
A feasible method to implement the residual concentration detection of imidazoline corrosion inhibitor in the formation water of oilfield is proposed as follows: taking the corrosion inhibitor sample to prepare at least two solution with different inhibitor concentrations, measuring the wavelength () of characteristic absorption peak and the absorbance () to determine the relationship between inhibitor concentration and absorbance (); taking the produced water sample with unknown concentration of corrosion inhibitor; filtering the water sample; measuring theof water sample atby means of ultraviolet-visible spectrophotometry; detecting Fe3+and measuring its concentration (Fe3+); calculating the residual concentration of corrosion inhibitor (R) according to the formula ofr=/in produced water without Fe3+or determiningRaccording to the formula ofR=(–0.056 5Fe3+)/in produced water with Fe3+. The detection error of the proposed method is less than 10 mg/L in the inhibitor concentration range of 0-300 mg/L, especially the lower the residual concentration of corrosion inhibitor in the produced water, the smaller the errors of the detected results. This work provides a potential strategy for the residual concentration detection of corrosion inhibitor in the formation water of oilfield.
imidazoline corrosion inhibitor; residual concentration detection; ultraviolet-visible spectrophotometry; salinity; pH; Fe3+
2021-08-17;
2022-04-15
ZHOU Xiang (1987-), Male, Doctor, Engineer, Research focus: oil and gas production engineering.
孙冲(1988—),男,博士,教授,主要研究方向为材料的腐蚀与防护。
SUN Chong (1988-), Male, Doctor, Professor, Research focus: corrosion and protection of materials.
周祥, 逄建鑫, 叶正荣, 等. 油田采出水模拟溶液中咪唑啉类缓蚀剂残余浓度检测技术[J]. 表面技术, 2022, 51(9): 188-196.
TG174
A
1001-3660(2022)09-0188-09
10.16490/j.cnki.issn.1001-3660.2022.09.000
2021–08–17;
2022–04–15
国家科技重大专项(2016ZX05016–004);中央高校基本科研业务费专项资金项目(20CX06075A)
Fund:The National Science and Technology Major Project of China (2016ZX05016-004); the Fundamental Research Funds for the Central Universities (20CX06075A)
周祥(1987—),男,博士,工程师,主要研究方向为采油采气工程。
ZHOU Xiang, PANG Jian-xin, YE Zheng-rong, et al. Residual Concentration Detection of Imidazoline Corrosion Inhibitor in Simulated Formation Water of Oilfield[J]. Surface Technology, 2022, 51(9): 188-196.
责任编辑:万长清

