含铬电镀废水处理技术研究进展
韩明君,孙伟,岳彤,余恒,李赛,张晨阳
(中南大学资源加工与生物工程学院,湖南长沙,410083)
电镀行业被认为是当今全球三大污染工业之一,其中含铬电镀废水是危害最严重的重金属废水之一[1]。随着电子电镀行业的发展,涉及的表面镀铬工艺不断增多,导致含铬废水排放量增大,含铬废水的污染防治问题日益突出。现阶段含铬电镀废水处理主要面临工艺流程长、过程效率低、药剂消耗量大、处置成本高、铬资源浪费、水资源循环利用率低等问题[2−3]。当前电镀行业清洁生产标准和电镀污染物排放标准分别从电镀生产和废水治理的角度对电镀废水防治提出了基本要求[4−5]。根据文献[6],2021—2025年将不断提高再生水利用率,2025—2035年将形成系统、安全、环保、经济的污水资源化利用格局。可以预见,以含铬电镀废水为代表的重金属废水资源化处理技术的发展将成为重点研究方向之一。
本文在总结现有含铬电镀废水主要处理技术的基础上,对相关方法的基本原理和优缺点进行阐述,同时,结合实例讨论含铬电镀废水主要处理技术的应用效果,并根据目前处理过程中存在的问题对今后电镀废水防治技术的发展前景进行展望,以期对电镀行业的清洁生产、重金属废水污染防治和资源化处理提供借鉴与指导。
1 电镀含铬废水的产生及特性
1.1 产生过程
电镀含铬废水主要产生于镀槽和镀件等清洗用水、老化报废的电镀液、镀槽废液、车间冲洗水、通风设备冷凝水、镀槽渗水、泄露或操作不当造成“跑、冒、滴、漏”的各种槽液及排出废水等[3,7−8]。其中,镀件清洗水占车间废水排放总量的80%以上,主要含有Cr(III),Cr(VI),Zn(II),Cu(II),H2SO4和HNO3,还有少量的Fe(II)和Fe(III)等。在生产过程中,不同镀件、不同电镀工艺和清洗方式对废水日排放量及浓度影响较大。
1.2 铬离子的赋存状态
铬(Cr)是地壳中含量较高的金属之一[9]。自然界中Cr有+2,+3和+6价,工业废水环境中多以Cr(III)和Cr(VI)的形式存在,铬离子的主要存在形态及转化过程如图1所示。
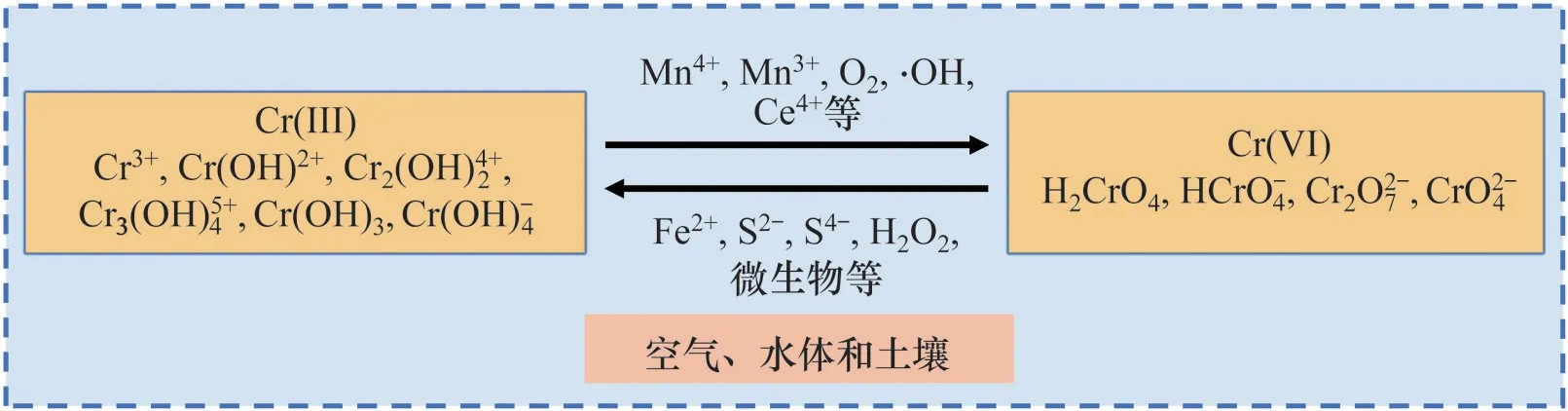
图1 废水中重金属铬的主要存在形态及转化过程Fig.1 Main forms and conversion processes of heavy metal chromium in wastewater
Cr 的存在形态随pH 的变化会发生很大变化,不同pH 下Cr-H2O 体系中金属离子赋存状态见图2[10]。从图2(a)可见:Cr(III)-H2O 体系中主要有Cr(OH)+2,Cr(OH)3(aq),Cr(OH)-4和Cr3+等几种存在形式;当pH 较低时,Cr(III)可溶解;随着pH 增加,Cr3+转化为Cr(OH)2+,Cr2(OH)4+2和Cr(OH)+2;当pH 为4.5 左右时,Cr(OH)2+,Cr2(OH)4+2,Cr(OH)+2和Cr3(OH)5+4的存在形态最多,然后转化为Cr(OH)3(am)和Cr(OH)-4;Cr(OH)3(am)在pH 为5~13时稳定存在,Cr(OH)-4随着溶液中碱性增加而产生。从图2(b)可见:Cr(VI)主要以H2CrO4,HCrO-4,Cr2O2-7和CrO2-4的形式存在,pH和总铬浓度是影响Cr(VI)以何种复杂化合物形式存在的关键因素;当pH=1.0时,Cr(VI)以H2CrO4的形式存在;当pH 为1~6 时,Cr(VI)主要以Cr2O27-和HCrO-4的形式存在;当pH大于7时,Cr(VI)以CrO24-的形式为主,可溶性Cr(VI)的总浓度保持稳定。

图2 水溶液中铬存在形态随pH变化图[10]Fig.2 Morphologies of chromium various with pH in aqueous solution 1 mol/L[10]
1.3 危害/毒性
电镀含铬废水中存在Cr(III)和Cr(VI)、氰化物、酸碱、添加剂等有毒有害污染物,当Cr(VI)质量浓度≥0.2 g/L,Cr(III)质量浓度≥1.0 g/L时均会对DNA 造成损伤[11]。这些性质复杂、组分迥异的污染物进入环境后难以被降解,长期在自然界中存在,可通过食物链在生物体内富集。
有机Cr(III)是胰岛素、葡萄糖、脂肪和氨基酸等代谢所必需的微量元素[12]。但无机铬毒性较大,对动物和人均有毒性作用,特别是无机Cr(VI)可以通过呼吸、皮肤接触、黏膜接触等途径被人体吸收,且Cr(VI)毒性是Cr(III)的10~100倍。Cr(VI)对人类具有明显的基因毒性,其基因毒性来源于Cr(VI)在细胞内的代谢产物;另外,Cr(VI)通过减少神经元细胞数量而显示出神经毒性[13],对肾脏、呼吸系统和神经系统等会造成永久性损害,甚至导致死亡[14]。高溶解性铬酸盐和低溶解性铬酸盐均是致癌物质,职业性吸入Cr(VI)会增大人体呼吸系统患癌的风险。对涉铬工厂的工人血液进行化验,发现发展中国家的工人受铬污染更严重[15]。
2 电镀含铬废水处理技术现状
长期以来,针对含铬电镀废水,研究人员提出了诸多处理技术方法,包括离子交换法、吸附法、化学沉淀法、电化学法、生物法等。归结起来,可以划分为物化处理技术、化学处理技术、生物处理技术和组合处理技术共4类。
2.1 物化处理技术
物化处理技术综合了物理和化学两门学科的技术方法,工艺过程相对稳定、可靠,运行成本较低[16]。离子交换法、膜分离法、吸附法是应用较广泛的物化处理技术。
2.1.1 离子交换法
具有选择性交换或吸附铬的离子交换树脂材料是离子交换法的关键[17−18]。离子交换分为阳离子型交换和阴离子型交换,Cr(III)和大部分金属离子可通过阳离子交换柱除去,以Cr(VI)存在的铬酸根可通过阴离子交换柱除去。例如,NAM 等[19]合成了阴离子交换剂PADD,在强酸性条件下,PADD中氨基正电荷增加,氨基与Cr(VI)的静电作用增强,对Cr(VI)的交换能力提高。
离子交换法处理含铬废水工艺流程示意图如图3所示。通过调节合适的pH 范围,酸型阳离子交换柱和碱型阴离子交换柱联用,可资源化回收电镀废水中的铬酐[20]。唐星星[21]采用两段洗涤法,低浓度含铬废水段经离子交换树脂吸附再解吸进行富集,与高浓度含铬废水合并后进行蒸发浓缩,实现了废水及铬酐回收。大孔N-甲基咪唑强碱阴离子交换树脂PCl、弱阴离子树脂Amberlite IRA 96 对Cr(VI)均有较好的去除效果[1,16]。另外,Diaion CR11 和Amberlite IRC86 等阳离子交换树脂[22]已商业用于处理Cr(III)。

图3 离子交换法处理含铬废水工艺流程示意图[2]Fig.3 Schematic diagram of processes for treating chromium-containing wastewater by ion exchange[2]
2.1.2 膜分离法
膜分离法借助外界能量或化学位差的推动作用,通过特定膜的渗透过程实现对废水中多组分的分离、纯化和富集。现有膜分离包括以压力驱动的反渗透(RO)、纳滤(NF)、超滤(UF)、微孔过滤(MF)、以电位差驱动的电渗析(ED)以及膜分离耦合生物降解的膜生物反应器(MBR)等[23]。
膜分离技术在水处理中应用广泛,既可对废水中有价组分进行浓缩预处理,又可将透过水循环回用。侯书芳等[24]介绍了超滤−反渗透处理含铬电镀废水的示范工程,含铬电镀漂洗水中Cr(VI)质量浓度约为142 mg/L,pH 约为10.5,经过预处理和三级反渗透膜系统循环处理,合格浓缩液进入镀槽回用;GIAGNORIO等[25]基于纳滤技术设计了符合生产饮用水标准的中试纳滤装置,处理后总铬质量浓度小于0.01 mg/L;SHI 等[26]通过两段烧结对316L 多孔不锈钢管原位氧化得到了机械强度和化学稳定性良好的磁铁矿膜,在pH 为4.0 时对Cr(VI)的吸附率达100%,在pH=13 时,0.1 mol/L Na2SO4溶液可脱附65%的Cr(VI),但吸附−解吸循环过程膜易出现阻塞,渗透性降低。
2.1.3 吸附法
吸附法是一种成本低、效率高且研究和应用广泛的处理方法,整体上更适用于处理低浓度含铬废水。目前,常用的吸附剂有活性炭、硅藻土、沸石、生物质吸附剂等。活性炭的高比表面积和大量的羟基、甲氧基等含氧基团决定了其对金属离子和有机物均具有优良的吸附性能,改性的活性炭在原有性能基础上可以进一步提升选择性吸附能力、吸附速度和吸附容量[27−28]。硫酸、硝酸锰、锰盐−铁屑、纳米银颗粒对活性炭改性后的除铬效果如表1所示[27−30]。

表1 活性炭基吸附剂对废水中重金属铬的去除效果Table 1 Removal effect of heavy metal chromium from wastewater by activated carbon based adsorbent
生物质吸附剂是活性炭之外被研究较多的吸附材料之一,具有来源广泛、易于再生、选择性较好等优点。李励殷[31]制备的磁性荔枝壳吸附剂在Cr(VI)初始质量浓度为100 mg/L,pH=3,吸附剂投加量为6 g/L 时,可去除95.9%的Cr(VI);KUSHWAHA 等[32]使用硫酸改性的棕榈壳,对Cr(VI)的吸附能力达到313 mg/g;LIU 等[33]利用咖啡渣作为吸附剂,在碱性条件下添加FeCl3絮凝剂沉淀金属离子,处理后Cr(VI)含量符合要求。
2.2 化学处理技术
化学处理技术往往通过改变废水中污染物的化学性质及状态,使其转变为无害或低毒物质而从水体中除去,在当前电镀废水治理中应用广泛[34]。化学处理技术主要包括化学还原法、化学沉淀法和电化学调控法。
2.2.1 化学还原法
化学还原法在具有氧化性污染物质的Cr(VI)废水处理中应用较多,毒性较大的Cr(VI)被还原成毒性次之的Cr(Ⅲ),总铬去除率进一步提高[10]。常用的还原剂有铁屑、硫酸亚铁、焦亚硫酸钠、硫化亚铁、多硫化钙等,调节pH 即可将Cr(Ⅲ)絮凝沉淀。在酸性条件下,将废铁屑作还原剂时,发生的还原反应为可表述为[35]:

调节pH 后,Fe(Ⅲ)和Cr(Ⅲ)可通过共沉淀除去[36]。同时,将铁屑作还原剂时可能形成微电解体系,进一步强化除铬效果[37]。前期研究表明:合适浓度的草酸盐可促进NaBH4对高浓度Cr(VI)的还原[38],低温环境可强化H2S 对Cr(VI)的还原过程[39]。此外,淀粉改性的纳米零价铁(S-nZVI)可以降低纳米颗粒间的团聚倾向,并且超声、曝气、芬顿等处理可以提升S-nZVI 对Cr(VI)的还原效果[40−41]。冯西平等[42]在pH为2时,使用NaHSO3理论用量的1.75倍还原去除了99.35%的Cr(Ⅵ)。
2.2.2 化学沉淀法
按照沉淀产物的不同,化学沉淀除铬可分为氢氧化物沉淀、钡盐沉淀、铬酸盐沉淀、铁氧体沉淀等。298 K时常见含铬难溶化合物及其溶度积如表2所示。

表2 298 K条件下常见含铬难溶化合物及其溶度积Table 2 Common chromium-containing insoluble compounds and solubility product at 298 K
利用溶度积越小越先沉淀的原理,调节pH 形成Cr(OH)3沉淀可以除去电镀废水中的Cr(III),常用的碱性调节剂有CaO,Na2HCO3和NaOH 等[43];在亚硫酸盐过量,温度为80 ℃,pH=2.0,PO34-与Cr(Ⅲ)的质量浓度比为1.1:1.0的条件下,磷酸盐可选择性分离铬和铁[44];此外,可向废水中加入PbSO4形成PbCrO4,加入BaCl2形成BaCrO4,以直接沉淀除去Cr(VI)[45−46]。当3价铬镀铬废水中存在柠檬酸或苹果酸等含羧基的配位剂时,常规碱性沉淀除铬效果不佳,Fe(II),Ca(II)和Al(III)等的协同作用可共沉淀除去Cr(III)[47−48]。
值得注意的是,铁氧体法是一种使用广泛的化学沉淀工艺,先后经过还原反应、共沉淀和生成铁氧体共3个阶段,Cr(III)替代了Fe3O4中的部分铁元素,生成具有尖晶石结构的复合氧化物,工艺流程如图4所示,主要反应式见式(3)~(5)[2],但无法单独回收有用金属,需额外消耗亚铁、碱与热能。超声波对铁氧体除铬有较强的促进作用[49];Cr(III)-Fe(III)共沉淀在磁赤铁矿(γ-Fe2O3)表面时[50],外加磁场有利于提高沉降效果。

图4 铁氧体法处理含铬电镀废水间歇式工艺流程[2]Fig.4 Intermittent process of treating chromium-containing electroplating wastewater by ferrite process[2]

2.2.3 电化学调控法
在电镀含铬酸性废液中,铁、碳、钛、铜、不锈钢等作为电极可直接或间接对Cr(Ⅵ)进行还原。当铁作电极材料时,铁在阳极被氧化成Fe(II)而进入溶液,Cr(Ⅵ)被Fe(II)还原为Cr(III),在电解过程中,氧还原和氢析出的副反应会降低电流效率[51−52]。同时,仅有少量Cr(Ⅵ)在阴极被直接还原,Fe(II)对Cr(Ⅵ)的还原起主要作用。随着H+被大量消耗,废水pH逐步升高到4.0~6.0,有利于Cr(III)-Fe(III)絮状共沉淀物析出[53−54]。
铁的价格虽较铝的价格低,但其电化学当量为铝的3倍多,故铁作电极时,阳极材料的消耗是铝的3倍多[55]。当铝板作电极材料电絮凝时,阴极产生的OH−易与Cr(III)等重金属离子形成沉淀,阳极产生的铝类聚合物可通过吸附架桥、沉淀网捕作用去除Cr(III)等重金属离子[56]。除此之外,钛电极做阳极同样可达到还原Cr(VI)的效果[51];当钛−铁双阳极协同电解含铬废水时,铁阳极附近的絮状物可吸附Cr(VI),辅助阳极钛将Cr(VI)还原为Cr(III),在电流为0.25 A,电解时间为1.5 h,pH=9时,Cr(Ⅵ)去除率大于90%[57];以钯纳米粒子改性的铜电极电解初始质量浓度为50 mg/L的Cr(VI)废水,当pH=1.5,电流为1 A时,99.63%的Cr(VI)被还原[58]。
2.3 生物处理技术
生物体具有静电吸附作用、酶的催化转化作用、络合作用、絮凝作用、积累富集作用等[14],可实现对重金属铬、高COD、氮磷等的净化,净化方法主要包括生物还原法、生物絮凝法、生物吸附法等。
2.3.1 生物还原法
具有降低Cr(VI)浓度的细菌统称为铬还原菌(CRB)[59],可从铬铁矿废水、制革厂、纺织工业、电镀制造业等用铬较多的环境中提取。与铬还原菌相似的还有铁还原菌(IRB),当IRB 将Fe(III)还原为Fe(II)时,Fe(II)将Cr(VI)还原为Cr(III),IRB间接还原铬的效果优于直接生物还原铬的效果[60]。ZHENG 等[61]把厌氧活性污泥中提取的Fe(III)还原菌Morganella sp包覆在零价铁上,得到RB-ZVI,在pH 为7,酵母粉质量浓度为6 g/L,葡萄糖质量浓度为4 g/L的最佳条件下,RB-ZVI对Cr(VI)的去除量达到26.86 mg/g,并可能存在吸附、还原、共沉淀和生物矿化等过程[62]。
在酸性条件下,生物质可以提供Cr(VI)还原为Cr(III) 所需的电子[63],以大型海藻Pelvetia canaliculata为例,其可以提供Cr(VI)还原为Cr(III)的天然电子供体,并作为锌、铁和Cr(III)螯合的天然阳离子交换剂[64];浮萍L.gibba对Cr(VI)的修复具有类似的效果[65]。Cr(VI)吸附在微生物细胞表面,细胞表面的官能团与金属离子可形成化学键,Cr(VI)作为末端电子受体,由铬酸还原酶催化或自发加速向Cr(III)转化,Cr(III)进一步被生物体吸附或络合成团[66]。
2.3.2 生物絮凝法
生物絮凝剂通常是带电的生物大分子,主要组成为蛋白质、多糖、纤维素和核糖等,根据物质组成不同,可分为利用微生物细胞的絮凝剂、利用微生物细胞提取物的絮凝剂、利用微生物细胞代谢产物的絮凝剂[67]。絮凝机理主要是桥联作用、中和作用和卷扫作用。与无机絮凝剂和合成有机絮凝剂相比,生物絮凝剂处理废水安全无毒,絮凝高效,用途广泛,不产生二次污染,但培养和保存困难,生产成本较高,在实际应用中受到限制[68]。
生物絮凝剂通过化学作用将絮凝物质集聚在一起,基本不受微生物个体和颗粒表面特性的影响。赵光等[69]以牛粪底物的中温厌氧发酵沼液为产絮基质,利用产絮菌F+制备的生物絮凝剂对Cr(VI)的絮凝效果良好,絮凝率达到83.8%。在碱性条件下,节杆菌sp.B4的胞外多糖具有一定自絮凝能力,通过调节合适的pH 可实现对Cr(VI)的去除;过量节杆菌sp.B4的胞外多糖可在无需调节pH的条件下直接将Cr(VI)还原为Cr(III),羧基和羟基在还原过程中占据主要作用[70]。利用芽孢杆菌Bacillus sp.在高盐条件下制备生物絮凝剂Na-Bsp,在宽pH范围和沸水处理下,絮凝效果良好,且絮凝剂表面的羟基、羧基和胺基可强化对重金属Cr(VI)的絮凝作用[71]。
2.3.3 生物吸附法
有些菌种能够在高浓度铬的条件下生长,在细胞内大量吸附或积累Cr(VI),并将其转化为毒性较小的Cr(III)。复合使用菌群或改性菌种可使不同菌种的优势特点最大化,但环境因素如微波、pH等对生物吸附过程影响较大[72−74]。
真菌在生命周期的所有阶段均可产生酶,其受污染物影响小,能在高金属浓度、高温、强酸碱等条件下稳定生长,被认为是积累铬等重金属的有效生物吸附剂[75]。酵母作为生物吸附剂,具有去除多种重金属的能力。MAHMOUD 等[76]将酵母细胞固定在海藻酸提取物中形成BPMB,对Cr(VI)的吸附能力达到200~1 000 mg/L。电镀废水中无机配体(CO23-,Cl−,F−和NO23-等)的竞争效应对酵母细胞等生物吸附铬影响较大[77]。藻类细胞壁表面的多孔结构由纤维素、果胶质、藻酸铵、岩藻多糖等多层微纤丝组成,氨基、羧基、硫基等官能团可被静电吸附或与金属离子配位形成稳定络合物,因此,藻类作生物吸附剂去除水溶液中重金属离子效果较好,且干藻相较活藻受金属离子毒害更小[78−80]。
2.4 组合处理技术
电镀废水种类繁多,成分复杂,每种处理方法均有一定的适用范围,常用处理技术及其优缺点如表3所示。单一的治理方法往往不易达到理想的处理效果和经济效益,且不同厂区不同批次的废水组分和含量也不尽相同,电镀废水的治理方法很难实现统一[26,50,81−82]。

表3 含铬电镀废水常用处理技术及其对比Table 3 Comparison of common treatment technologies of electroplating wastewater containing chromium
相对而言,多元优化的组合处理技术更有利于相互补充、协同作用,以深度净化含铬废水,达到最佳的经济技术指标。生物还原—混凝沉淀—离子交换的三级处理工艺示意图如图5所示[64],天然藻类提供电子供体以还原Cr(Ⅵ),调节pH 使Cr(III)和Fe(III)等金属阳离子在沉降槽混凝沉淀,褐藻小管藻作为天然阳离子交换剂可以净化95%的Zn(II),铬未检出。此外,光催化−生态修复法有效降低了高盐含铬废水中的COD 和BOD5质量浓度,提高了Cr(Ⅵ)还原效率并改善了出水水质[83];离子交换−铁氧体法可回用铬酐并深度净化Cr(III)等多种重金属离子,回用的水资源达到漂洗用水标准;电絮凝−活性炭吸附法为电镀污泥的安全处置提供了有效方法[52];电絮凝−膜分离法强化了重金属离子的去除效果[84];化学处理−超滤−反渗透法对混合电镀废水适用性强,有利于水资源的再生回用[85];多元组合技术与自动化控制结合有利于提高复杂混合电镀废水中金属的回收率,并有效回用水资源,使工艺流程和设备趋于小型化、模块化、简单化,节省处理成本。
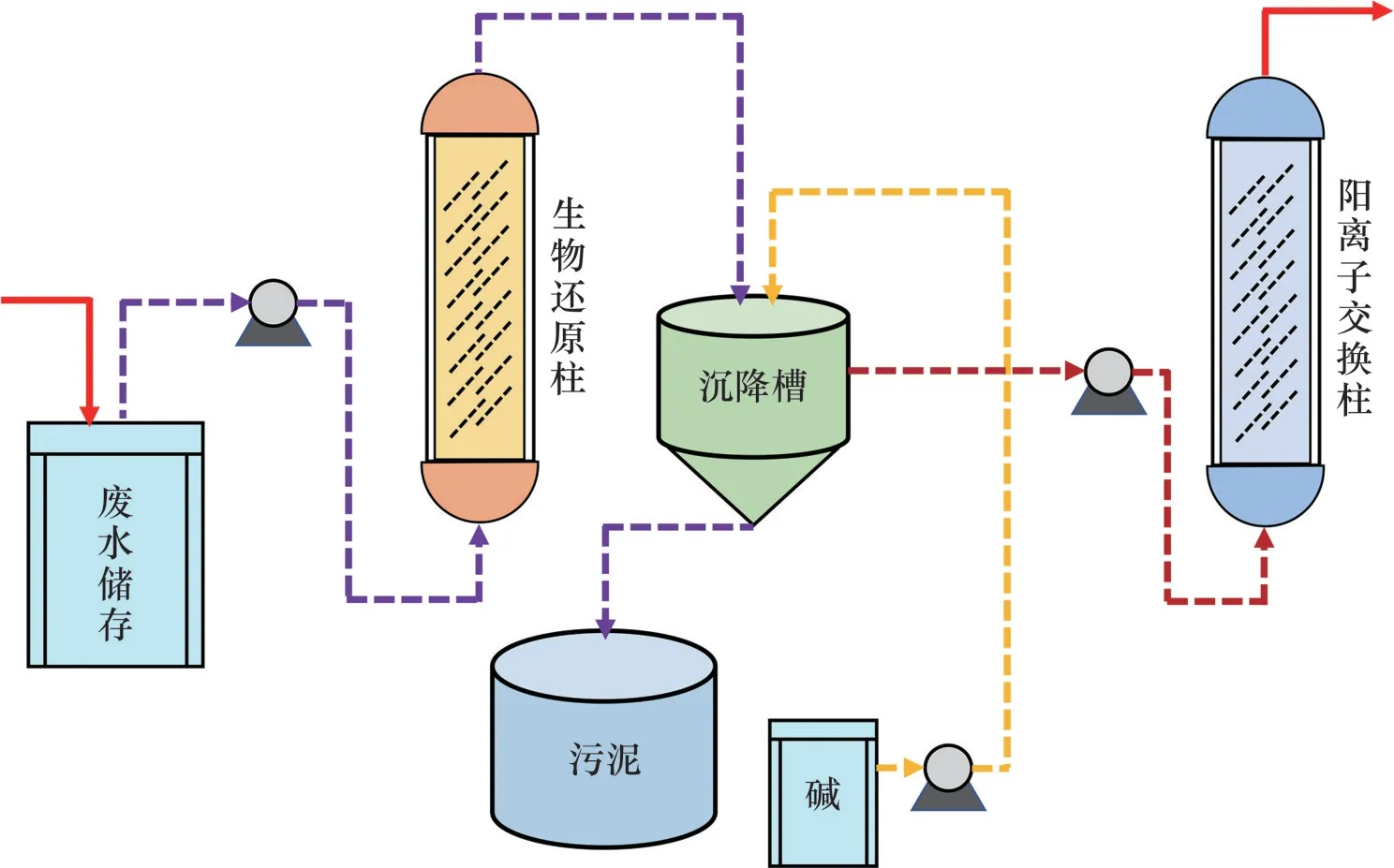
图5 生物还原—混凝沉淀—离子交换的三级处理工艺示意图Fig.5 Schematic diagram of three stage treatment processes of biological reduction-coagulation and sedimentation-ion exchange
3 电镀含铬废水污染防治过程中存在的问题
经过四五十年的持续发展,我国电镀废水治理先后经过了污染防治、环境保护、资源回收以及环境保护、经济效益和社会效益的有机结合几个阶段,取得了一定成果,但含铬电镀废水的源头处理、生态化治理、资源化回收等仍未达到预期目标,还存在一些问题:
1)电镀工业园区仓促筹划,匆忙投产,未能较好地结合地区实际,对园区设计中可能存在的不确定因素缺少充分的调研、论证和调试。
2)含铬电镀废水源头分类收集、分质处理意识淡薄,混排现象突出,重金属铬含量波动明显,加大了后续处理难度。
3)物化、化学、生物技术特点突出,缺点明显,对单一含铬漂洗水或模拟废水去除效果较好,对组分复杂的混合废水处理效果一般。
4)自动化程度偏低,药剂耗量大,运行成本高,废水回用率低等问题突出,铬资源化技术尚未推广,污泥成分复杂,安全隐患大等。
4 电镀含铬废水污染防治展望
当前,我国环境容量小、生态环境脆弱、环境风险高等问题日益凸显。未来含铬电镀废水防治需要聚焦于污水减量化、有价组分资源化、废水深度净化及近零排放。具体措施主要包括如下几个方面。
1)统筹规划电镀工艺与废水处理工艺,实现生产和处理的生态化改造。从源头上改革电镀技术,消除和减少污染,积极开发推广低浓度、低污染的电镀工艺;以电镀工业园区建设为契机,发展源头减量、过程管控和末端治理相结合的污染防治一体化技术,逐步实现“节能降耗、综合利用、减污增效”的电镀清洁生产目标。
2)采取分类回收—分质回用—深度净化工艺,确保有毒害物质近零排放。电镀废水分类分片回收、分质短流程回用,从源头控制可极大缓解后续治理压力;开发具有低能耗、抗污染、耐高温高压、选择性强、通用性好、具有特种分离等性能的集成工艺及配套设备,最终实现废水中有毒害物质的近零排放。
3)通过有价金属高值化回收—废水最大化回用—污泥安全处置利用,建立有用组分资源化综合利用机制。使用可控的电解技术回收再生电镀槽边液中的有价铬资源;发展具有耐酸碱、耐水浸、易再生等稳定化学性质的重金属铬吸附材料;研发具有高选择性、易于解吸、不易污染的离子交换树脂,实现铬酸回收和一水多用、循环使用的闭路循环流程;融合自动化控制技术提升药剂添加、在线监测、过程管理等智能化水平;逐步实现金属离子高值化回收,安全且广泛地利用污泥,回收回用90%以上水资源。
总体来说,含铬电镀废水的高效率、安全化治理和资源化利用仍是当前及今后发展的重要课题。加紧电镀行业的源头治理,筑牢含铬等废水减量化排放的闸口,强化工艺末端有价组分和水资源的回收回用,向着节能、高效、无二次污染的清洁生产方向改进,确保含重金属铬等有毒有害废水最终深度净化与无害化,是解决电镀废水污染问题和实现电镀行业可持续发展的重要保障,更是实现资源循环利用和改善生态环境质量的必然选择。

