紫杉醇脂质体与传统紫杉醇注射液治疗乳腺癌和非小细胞肺癌的疗效研究
翟美萍
由于生存环境的恶化以及生活压力的增加等多种因素导致各类恶性肿瘤的发生率持续升高,乳腺癌和非小细胞肺癌都是临床发病率极高的肿瘤,前者高居女性恶性肿瘤发病率的首位,后者则是最常见的肺癌类型[1]。治疗中考虑到患者对美观性要求或者受肿瘤本身分期因素的影响等,常会选择化疗非手术治疗的方式。紫杉醇是常用的化疗药物,其具有广谱抗肿瘤效果,而紫杉醇脂质体是用卵磷脂包裹紫杉醇后形成的一种新的紫杉醇剂型[2]。本文以本院收治的乳腺癌及非小细胞肺癌患者作为研究对象,对比采用紫杉醇脂质体和传统紫杉醇注射液治疗后的临床疗效与安全性。详情报告如下。
1 资料与方法
1.1一般资料 抽取本院2018 年10 月~2020 年10 月收治的38 例乳腺癌及非小细胞肺癌患者,以多中心、随机对照法分为A 组与B 组,每组19 例。A 组,男8 例,女11 例;年龄33~81 岁,平均年龄(54.5±8.9)岁;乳腺癌患者和非小细胞肺癌患者各为7、12 例。B 组,男7 例,女12 例;年龄31~79 岁,平均年龄(53.1±8.7)岁;乳腺癌患者和非小细胞肺癌患者各为8、11 例。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。本研究经本院伦理委员讨论通过,患者及患者家属签署知情同意书。
表1 两组一般资料比较(n,)
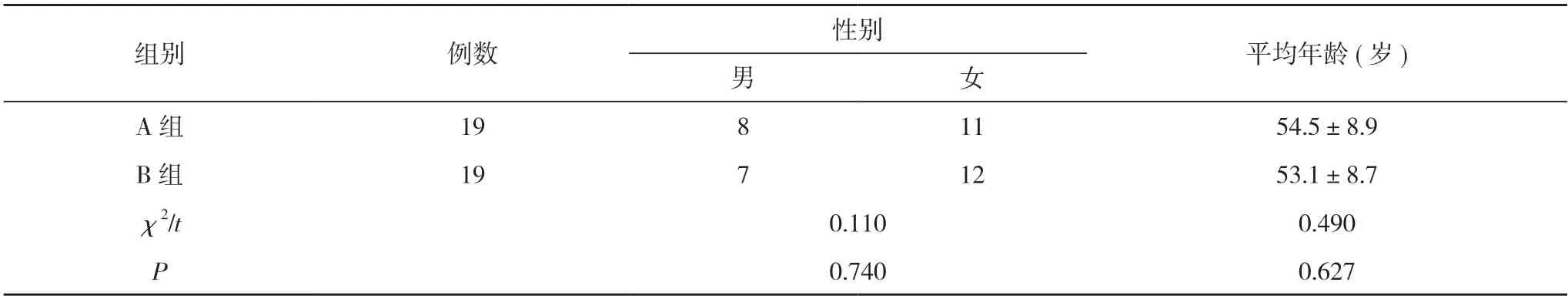
表1 两组一般资料比较(n,)
注:两组比较,P>0.05
1.2纳入及排除标准 纳入标准:患者均经细胞学和(或)病理学诊断确诊,且经影像学方法检测确定存在一个及以上可评价的病灶,病灶直径≥1 cm;患者的Karnofsky 功能状态评分>60 分,预计生存期>3 个月;患者为首次化疗或者既往有非紫杉醇化疗史但治疗失败,有非紫杉醇化疗史的患者,距离前次化疗的时间间隔在3 个月及以上;患者自愿参与本次研究,并在治疗中有良好的依从性。排除标准:患者合并其他恶性肿瘤的情况;患者合并重要脏器功能障碍的情况;患者合并精神或意识障碍,无法配合治疗的情况;患者合并表达障碍,无法准确传达治疗感受的情况。
1.3方法 A 组患者采用紫杉醇脂质体进行治疗,给药前30 min 为患者实施地塞米松及西咪替丁(给药剂量分别为10、300 mg)静脉注射、苯海拉明(给药剂量为50 mg)肌内注射,行常规预处理,预防过敏反应发生。然后在紫杉醇脂质体(南京绿叶制药有限公司,国药准字H20030357,规格:30 mg)瓶中加入10 ml 5%葡萄糖注射液,在专用振荡器中振荡摇动5 min,至紫杉醇脂质体充分溶解后再加入500 ml 5%的葡萄糖注射液中静脉滴注,紫杉醇脂质体的给药剂量为135 mg/m2,滴注时间为3 h 左右。
B 组患者则采用传统紫杉醇注射液(江苏红豆杉药业有限公司,国药准字H20067344,规格:30 mg)进行治疗,预处理方法和治疗方法同A 组。
根据患者肿瘤类型的不同,乳腺癌患者联合阿奇霉素静脉滴注治疗,给药剂量为40~60 mg/m2;非小细胞肺癌患者联合顺铂静脉滴注治疗,给药剂量为100~150 mg/m2。每3 周为1 个周期,治疗2 个周期。
1.4观察指标及判定标准 分别对两组患者的临床疗效及不良反应发生情况进行统计和比较。患者的临床疗效评价参加世界卫生组织制定的实体瘤治疗效果评价标准:以病灶完全消失,且维持时间超过4 周为完全缓解(CR);以实体瘤的瘤体体积缩小程度>50%,且维持时间在4 周以上为部分缓解(PR);以实体瘤体积缩小程度<50%或者增大程度<25%,病灶未见明显改变的情况为稳定(SD);以病灶体积增大程度>25%或出现新病灶的情况为病情进展(PD)。RR=(CR+PR)/总例数×100%。患者的用药不良反应参照世界卫生组织制定的抗癌药物毒性分度标准进行评价,不良反应发生率=(Ⅰ度+Ⅱ度+Ⅲ度+Ⅳ度)/总例数×100%。
1.5统计学方法 采用SPSS21.0 统计学软件处理数据。计量资料以均数±标准差()表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1两组临床疗效比较 A 组RR 为78.95%,高于B 组的47.37%,差异有统计学意义(P<0.05)。见表2。
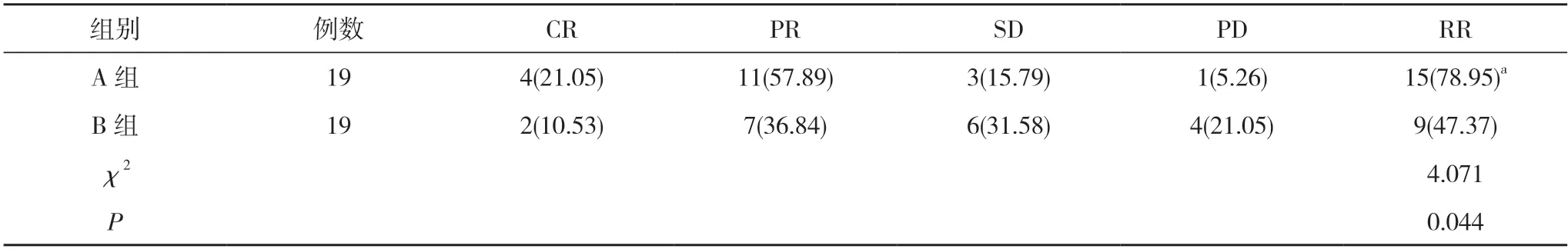
表2 两组临床疗效比较[n(%)]
2.2两组不良反应发生率比较 根据抗癌药物毒性分度标准分类,A 组Ⅰ度4 例、Ⅱ度1 例;B 组Ⅰ度9 例、Ⅱ度3 例、Ⅲ度1 例。A 组不良反应发生率为26.32%(5/19),低于B 组的68.42%(13/19),差异有统计学意义(P<0.05)。见表3。

表3 两组不良反应发生率比较[n,n(%)]
3 讨论
紫杉醇是一种抗微管制剂,其在治疗肿瘤过程中可以作用于微管蛋白系统,发挥促进微管二聚体结合而抑制其解聚,维持微管蛋白稳定性的功效[3];同时可引起细胞周期中微管排列异常,细胞分裂期间微管星状体产生,造成细胞分裂受阻;通过上述两种机制的共同作用发挥抑制肿瘤细胞分裂、增殖的效果[4]。研究显示,其在乳腺癌、非小细胞肺癌等多种恶性肿瘤的治疗中均可发挥重要治疗作用[5]。在乳腺癌治疗中,对于无法实施保乳术治疗但对美观性有较高需求的患者,通过紫杉醇化疗可以在治疗疾病的基础上最大程度保留患者的乳房,降低患者的负面情绪,促进其预后恢复;而在非小细胞肺癌治疗中,由于其发现时多为晚期,无法接受手术治疗,且对常规放疗的敏感性较低[6],紫杉醇化疗可以为患者提供新的治疗选择,为提高晚期患者生存率、延长生存时间提供更多可能[7]。
由于紫杉醇具有亲脂性好而难溶于水的特点[8],市售紫杉醇注射液往往将紫杉醇溶解在聚氧乙基代蓖麻油和无水乙醇混合溶媒中,溶媒中的聚氧乙基代蓖麻油在进入机体后会诱发多种过敏反应,影响患者的治疗依从性,降低患者的治疗效果。临床上常通过治疗前应用地塞米松、西咪替丁、苯海拉明等预处理方式降低治疗中不良反应发生率[9]。紫杉醇脂质体在这种情况下应运而生,该紫杉醇剂型通过卵磷脂的包裹,封闭在了类脂质双分子层内,大大增加了紫杉醇在体内的停留时间,同时也可以促进紫杉醇细胞毒性、药物毒性的降低[10]。本次研究结果显示,A 组RR 为78.95%,高于B 组的47.37%,差异有统计学意义(P<0.05)。所得结论与相关研究[11,12]具有一致性,提示紫杉醇脂质体治疗乳腺癌及非小细胞肺癌的临床效果更为理想。
本次研究两组患者治疗中均出现不同程度的恶心呕吐、厌食、乏力、关节疼痛、末梢神经炎、脱发、白细胞减少、血小板减少、血红蛋白降低、谷氨酸转氨酶及天冬氨酸转氨酶升高等消化道、血液、肝脏系统的不良反应,但是,从不良反应发生率及发生程度来看,采用紫杉醇脂质体治疗的A 组患者不良反应发生率仅为26.32%,且多为Ⅰ度和Ⅱ度不良反应,程度相对较轻。提示,紫杉醇脂质体治疗安全性优势明显。
综上所述,与传统紫杉醇注射液相比,采用紫杉醇脂质体治疗乳腺癌和非小细胞肺癌可以显著提高患者的治疗效果和安全性,患者不良反应程度较轻,值得在临床上推广应用。

