中期妊娠引产清宫后胚物残留致“动静脉瘘”两例探讨
杨润乔,邓姗
(1.盘锦市中心医院妇产科,盘锦 124010;2,中国医学科学院 北京协和医学院 北京协和医院妇科内分泌与生殖中心,国家妇产疾病临床医学研究中心,北京 100730)
病例1患者女,35岁,孕3产1(G3P1),因“中期妊娠引产后5月余,发现宫腔占位4月”于2021年12月10日入住北京协和医院。
初潮12岁,既往月经不规律,5 d/30~90 d,量中,无痛经。2009年自然受孕人工流产1次;2015年因继发不孕行宫腹腔镜手术,见宫腔两侧壁中下段内聚,行粘连分离术;2018年 因巨大儿剖宫产1次。
2021年7月1日自然妊娠后孕18周时发生难免流产行引产术+清宫术,术后阴道出血3周,量不多;术后6周余(2021年8月19日)外院复查超声示宫腔内异常回声4.3 cm×3.4 cm、子宫肌壁间血流丰富(局部动静脉瘘?),考虑出血风险大,建议咨询栓塞的必要性;术后8周左右(2021年8月30日)就诊于北京协和医院,查血激素水平:卵泡刺激素(FSH)6.17 U/L、黄体生成素(LH)4.80 U/L、雌二醇(E2)106.43 pmol/L、孕酮(P)<0.25 nmol/L、β-HCG 1.43 U/L。给予口服优思悦1个周期,同时加用生化颗粒、益母草颗粒。优思悦撤退性出血后(2021年10月11日)外院复查彩超:宫腔内异常回声1.4 cm×0.7 cm,与子宫后壁分界欠清,宫腔下段索条状强回声宽0.7 cm。2021年10月15日开始口服芬吗通2/10(早红片,晚黄片)×14 d。2021年11月5日再次月经后复查经阴道超声(图1A、B):内膜厚约0.6 cm,回声不均,内见多处点条状强回声,较大者直径约0.2 cm,后伴彗星尾;宫腔内见中低回声,大小0.8 cm×0.4 cm,形态规则,边界清;彩色多普勒血流显像(CDFI)未见明确血流信号,子宫肌层回声均。2021年11月15日口服地屈孕酮10 mg bid×10 d,停药于2021年11月29日出现撤退性出血,持续4 d,量中等,无痛经。2021年12月7日我院复查经阴道超声(图1C、D):内膜厚约0.6 cm,回声不均,宫腔及内膜处见多处点条状强回声,周围见少许无回声,较大强回声0.4 cm×0.2 cm;宫腔下段见无回声,1.1 cm×0.5 cm;子宫肌层回声尚均。考虑宫腔内疑似“动静脉瘘”的占位组织虽明显缩小,血流信号也消退,但宫腔内始终有异常回声,性质不明,患者仍有生育要求,行宫腔镜检查是合理的。
2021年12月13日宫腔镜术中(图1E、F)见宫腔深7.5 cm,中下段略内聚,宫底及后壁见片状疏松淡黄色组织,采用宫腔镜下刨削器械清除宫腔内上述淡黄色组织后,宫腔形态正常,双侧输卵管开口可见。术后病理:增殖期子宫内膜及平滑肌组织,局部可见退变物,免疫组化CD138+,符合胚物残留。术后口服优思悦,月经规律来潮,量中等。
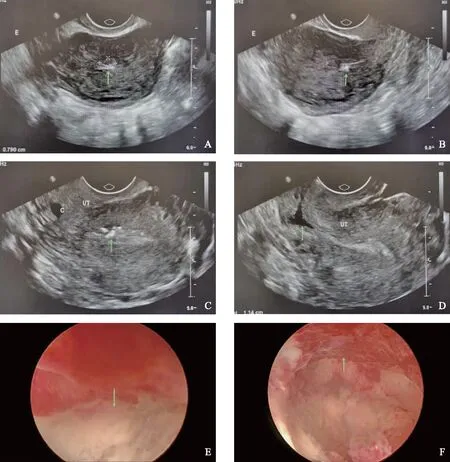
两次药物撤退性出血后超声,A:箭头示宫腔内中低回声,大小0.8 cm×0.4 cm,CDFI未见明确血流信号;B:箭头示宫腔内点条状强回声,后伴彗星尾。第3次药物撤退性出血后超声,C:箭头示宫腔及内膜处见多处点条状强回声,周围见少许无回声;D:箭头示宫腔下段无回声,1.1 cm×0.5 cm。宫腔镜探查,E:箭头示少许胚物残留主要位于宫底后壁,与肌层关系密切;F:箭头示前壁对应部位内膜光滑,继发粘连的风险小。
病例2患者女,28岁,G2P0,因中期引产后近2月、超声提示“肌层动静脉瘘”来诊。
既往月经规律。2021年9月因“孕12+周,胎儿NT增厚”行药物引产,9月17日流产,9月18日清宫;清宫术后出血半月余,因宫腔可疑占位,口服益母草和桂枝茯苓胶囊。2021年10月15日出现阴道流血,前7 d量正常,后淋漓一周。2021年10月29日复查超声:宫腔上段至前壁肌层可见3.7 cm×2.6 cm×1.7 cm不均质回声,前壁肌层最薄处0.38 cm,内可见丰富血流信号。予米非司酮25 mg bid × 8 d,期间第3天开始出血量似月经,淋漓不净近20 d。2021年11月8日复查超声:同部位不均质回声区3.6 cm×3.3 cm×2.0 cm,前缘几乎达浆膜,后缘紧贴宫腔。同期血HCG 4.1 U/L。当地考虑肌层内血流丰富的占位,可能需要子宫动脉栓塞治疗,建议转诊来至我院。2021年11月14日查盆腔增强MRI(图2A、B):子宫前壁下段肌层局限变薄,最薄约0.2 cm;宫腔及子宫前壁周边及内部可见多发迂曲增粗血管样流空信号,宫腔内见片状T1高信号,盆腔内多发迂曲血管影;盆底血管稍迂曲增粗,双侧附件区多发类圆形T1低T2高信号,增强未见明显异常强化。鉴于患者无活跃出血,予新生化颗粒、益母草、安坤颗粒等药物保守治疗观察,2021年11月28日月经来潮,前7 d似正常月经量,后淋漓不尽持续20余天,随后一次月经为2022年1月1日,量中,无明显痛经。2022年1月4日复查经阴道超声(月经第3天)(图2C、D):子宫大小5.5 cm×5.2 cm×4.1 cm,内膜厚约0.9 cm,回声不均,肌层回声欠均,CDFI见肌层内较多血流信号;右后壁见低回声区,范围约1.8 cm×1.4 cm,边界不清,内可见点状强回声,CDFI见内部及周边较多条状血流信号。给予优思悦每天1片口服2周期,月经规律,经期3天,此后间断偶有少许褐色分泌物,较用药前明显好转。停用优思悦后的末次月经为2022年2月27日,3月1日(月经第3天)复查性激素六项:FSH 23.11 U/L、LH 9.83 U/L、E2109.22 pmol/L、PRL 12.25 ng/ml、T 0.325 ng/ml、HCG(-);2022年3月13日月经后经阴道超声复查(图2E、F):子宫大小、形态正常,内膜0.8 cm,宫腔内未见明显肿块影像,下段后壁探及约1.4 cm×1.1 cm低回声区,边界欠清,CDFI肌壁间未见异常血流信号。考虑局限性腺肌病可能。
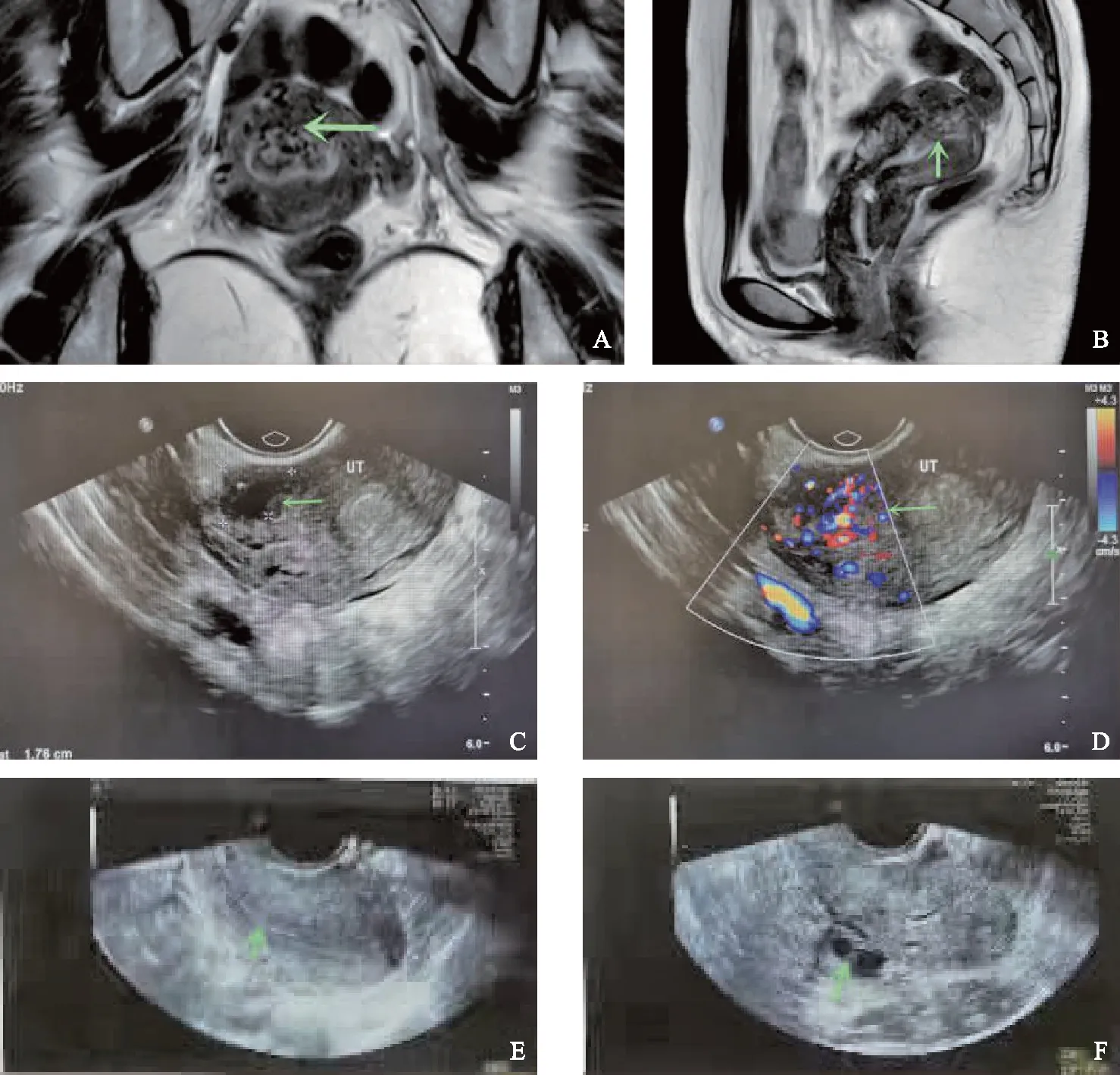
引产术后2月余盆腔增强MRI,A:箭头示宫腔内见片状T1高信号,前壁肌层似有浸润;B:箭头示宫腔内见片状T1高信号。中成药保守治疗2个月经周期后经阴道超声,C:箭头示子宫右后壁低回声区,范围约1.8 cm×1.4 cm,边界不清,内可见点状强回声;D:箭头示CDFI见低回声区内部及周边较多条状血流信号。两个药物周期后复查超声,E:箭头示宫腔内未见明显异常影像;F:箭头示子宫下段后壁1.4 cm×1.1 cm低回声区,边界欠清,未见异常血流信号,考虑局限性腺肌病可能。
结合患者目前检查结果来看,考虑宫腔内无异常占位,但子宫下段后壁低回声区性质仍不明确,无法明确鉴别是无活性的胚物残留还是局限性腺肌症。但目前月经规律,无异常出血,暂不考虑宫腔镜探查,可停用优思悦监测基础体温,观察排卵情况,并择期复查性激素六项(因前期检查提示有卵巢功能下降)。
讨 论
一、胎盘植入、残留等造成的动静脉瘘的自然转归规律
子宫动静脉畸形(uterine arteriovenous malformations,UAVM)是子宫供血动静脉间出现不经过毛细血管网的异常“短路”的病理现象,通常伴有血管增生及大量小瘘道形成[1],组织学检查显示壁内动脉分支和肌层静脉丛之间有多个小的动静脉瘘[2-3],血液从压力高的动脉血管通过动静脉瘘道或短路血管直接流入压力低的静脉血管,使局部血液循环阻力显著下降,导致血流速度明显加速,血流量异常增大,并随时间的延长逐渐加重,在瘘口部位局部静脉显著曲张,引起继发性出血及腹痛等临床症状。该疾病1926年首次由Dubreuil等[4]描述,当时命名为子宫蔓状动脉瘤。其后该疾病被冠以不同的名称,如子宫动静脉瘘、子宫肌层过度血管化、动静脉动脉瘤、海绵状血管瘤、静脉曲张性动脉瘤等,其中似乎子宫动静脉瘘最常用。
UAVM可分为先天性和获得性[5]。先天性UAVM 起源于胎儿血管形成期原始的毛细血管变异[6],是由于胚胎期原始的血管结构发育异常或停止发育而使原始的丛状结构持续存在所致。获得性UAVM常继发于子宫手术(如诊断性刮宫、剖宫产)、多次妊娠、复发性流产、分娩、胎盘植入、妊娠物残留、宫内节育器置入、子宫肿瘤、滋养细胞疾病、母体己烯雌酚暴露、感染等情况[7],平均发病年龄为33.4岁。有回顾性研究列举了UAVM患者的既往疾病和手术史,其中62%曾行诊断性刮宫术、26%曾行剖宫产术,宫腔镜或宫内节育器放 置术、子宫肌瘤剔除术、滋养细胞肿瘤者各占4%[7]。多数学者认为UAVM与损伤过程中的反常血管化或滋养细胞肿瘤及恶性肿瘤的血管侵袭性等有关,另外与高雌激素水平的作用引起血管内皮增殖和子宫内膜的变异、多次妊娠流产病理性的胚胎着床及产后子宫复旧不良及妊娠残留胎盘血管床复旧不全等都可能相关[8-10]。
胎盘植入、胚物残留等造成的动静脉瘘的临床转归受UAVM血管的位置和血管口径的大小的影响。部分患者可无明显临床表现,病灶可随时间延长在数周或数月内消退;部分患者可因子宫创伤、月经周期或妊娠引起的激素水平变化出现病情进展[11],表现为间断性的阴道流血、突发大量出血、月经过多等和盆腔痛;少数严重的患者在病变部位可触及或探及搏动感或血流震颤感;极少数患者可因严重出血导致休克[12]。
二、胚物残留的处理时机和策略
胚物残留(retained products of conception,RPOC)指自发性妊娠丢失(流产)、计划性终止妊娠或早产/足月产后胎盘和/或胎儿组织残留于子宫腔内。在足月产后的发生率约为1%[13],自然流产、习惯性流产或人工流产术后的患病率可高达6%[14]。
RPOC的主要危害是异常子宫出血和继发宫腔或宫体感染,少数情况下,残留组织仍有滋养细胞活性,可出现HCG下降不满意并合并月经延迟。
对于RPOC的处理时机及策略需结合患者的症状及病情是否稳定来选择:
1.子宫出血过多而导致血流动力学不稳定的患者:应根据需要补充液体和使用血液制品,并进行紧急手术干预。如清宫术后仍不能减缓出血,可尝试使用宫腔内球囊导管(如Foley、Bakri等)填塞;如仍无效,则可选择子宫动脉栓塞(UAE)术。当流产孕周及残留胚物较大,以及合并流产相关并发症时,更有可能发生阴道大出血,此时可行UAE术后宫腔镜下病灶切除[15]。子宫切除术是个别情况的极端抢救手段。
2.伴有脓毒血症(临床诊断为感染,同时满足以下至少2项:体温>38.5℃或<35℃;心率>90次/min;呼吸>20次/min或动脉二氧化碳分压<32 mmHg;白细胞>12×109/L、<4×109/L,或未成熟(杆状核)白细胞>10%)的患者:应给予静脉广谱抗生素治疗,情况稳定后尽早行清宫术,延迟清宫可能致命。
3.持续出血但生命体征平稳且不伴有感染的患者:可视出血的量及时间等具体情况,选择期待治疗或手术干预。对于自然流产的患者来说,期待治疗的成功率在随访1~2周时为50%~85%,在随访6周时高达90%[16-17]。手术干预用于出血时间长、量较多和/或有继发感染迹象的患者,具体方式包括刮匙刮宫或负压吸宫术,或宫腔镜定向清除术。宫腔镜手术,具有能同时诊断和治疗的优势[14,18],一项关于宫腔镜切除RPOC与刮除术清除RPOC的直接比较研究显示,宫腔镜操作后的子宫粘连发生率明显更低,这很可能是因为避免了对子宫内膜的整体造成损伤[18]。从宫腔粘连的发生角度来看,妊娠期(或近期妊娠过)的子宫进行刮宫术是发生宫腔粘连的主要危险因素,尤其在感染的情况下,并且风险似乎随着手术操作的次数增加而升高。研究显示,采用宫腔镜冷刀系统相较于传统清宫术对内膜的保护性更好、术后宫腔粘连的发生率更低[14],采用宫腔镜刨削系统清除RPOC相较于宫腔镜电切,手术时间更短,选择性更高,对周围子宫内膜没有热损伤及热效应,内膜损伤更小,术中并发症及术后子宫粘连的发生率更低[13,19-20]。宫腔镜抓取钳治疗RPOC也比传统刮宫术远期并发症少,术后妊娠结局较好[21]。因此,在适当的时机,采用定向宫腔镜,尤其是无能量器械清除RPOC是最佳的处理方法。
缩宫素类药物、米非司酮和/或米索前列醇常被用于RPOC的治疗,但具体方案(包括剂量和时间)均无明确的规范。也有不少医生愿意采用中药方法,如益母草、新生化颗粒等促进流产后宫腔的恢复。
本文中两例中期引产后宫腔及肌层占位,超声提示动静脉瘘,考虑为胎盘植入或胚物残留相关的继发性动静脉瘘,症状上均没有明显的大出血和继发感染征象,病情稳定,给了我们短期观察和药物保守治疗的时间。患者最初就诊时均有被告知需要子宫动脉栓塞治疗的可能,以预防潜在的大出血意外,但我们在处理上既未选择预防性子宫动脉栓塞,也没有选择积极地清宫处理,而是进行了3~4个周期的药物治疗,包括复方口服避孕药(COCs)、地屈孕酮、人工周期等。根据前人的经验,胚物残留最好能在流产后70 d左右或经超声多普勒显示无丰富血流信号的情况下再行宫腔镜择期手术,也就是说观察两个月经周期相对理想。药物治疗的目的是希望通过内膜脱落法消除病灶,病例1在每次月经后都可观察到宫腔内占位的明显缩小,也没有异常的子宫出血,于是选择继续观察,后来因超声还是提示宫腔内有不明确的微小占位,而她还有生育要求,故建议行宫腔镜检查和治疗。宫腔镜采用无能量刨削系统定向清除残留妊娠物,术程顺利,术后因患者同时合并有排卵障碍,给予优思悦调整月经。病例2则在经过3个周期的药物治疗后,宫内残留胚物消失,宫后壁异常回声虽然仍不明确,但患者无异常出血,病情稳定,暂不考虑宫腔镜检查,随访超声即可。
我们借鉴人流术后关怀项目(即人流术后即开始服用短效口服避孕药)以及COCs广泛用于异常子宫出血治疗的经验,经激素检测排除仍有明显绒毛HCG活性后,给予COCs并无禁忌,而临床实例获得的经验是可行的。当然,需要强调的是,需要跟患者做好风险告知,一旦出血活跃,应尽早急诊就诊,仍有再次清宫的可能。而如能顺利过渡,择期行宫腔镜检查和治疗是最理想的。

