改性活性炭对低浓度二氧化硫吸附动力学模型研究
王志强,张俊杰,刘相成,金梧凤
(天津市制冷技术重点实验室,天津商业大学机械工程学院,天津300134)
SO2作为主要的大气污染物之一,不仅会引起人体呼吸系统、肝脏肾脏等器官的病变,对人体健康造成严重威胁[1-3],还会加速电子元件中铜[4]、银等常用金属的腐蚀[5],在缩短电子设备使用寿命的同时,对芯片制造领域的品质控制亦会造成不良影响[6-7]。
在生产生活中常使用活性炭、沸石、金属有机骨架[8]等吸附剂对大气中的SO2进行吸附和脱除。为提高化学过滤器吸附SO2的能力,通常对填充在其中的活性炭进行改性[9],使其负载诸如氢氧化钾、氢氧化镁等专门针对性去除SO2的碱性物质,此类物质对酸性气体具有较强的吸附能力[10-11],已普遍被用于对吸附酸性气体的活性炭改性实验中。
虽然吸附床穿透实验可以有效评价吸附剂在特定吸附质浓度下的吸附能力[12-13],但是实验室得到的吸附实验结果并不能准确地反映吸附材料在实际应用中的性能,因为吸附剂的性能测试一般参照ANSI/ASHRAE 145.1—2008《Laboratory Test Method for Assessing the Performance of Gas-Phase Air-Cleaning Systems:Loose Granular Media》、ISO 9227—2017《Corrosion Tests in Artificial Atmospheres-Salt Spray Tests》和GB/T 10125—2012《人造气氛腐蚀试验:盐雾试验》进行,这3个标准测试吸附质的质量浓度通常设定为24 mg/m3,这样的浓度值远超过实际环境中SO2的浓度水平。气体吸附的最大特点在于整个吸附过程是吸附质的浓度在吸附剂内与主流空气之间的一种动态平衡,这种平衡会随着这两种浓度差的变化而改变[14-16]。具体来讲SO2初始浓度的高低将直接影响吸附剂的吸附性能,包括随操作时间的变化而变化的吸附效率以及特定穿透效率下的吸附容量。在实际运行条件下吸附剂的吸附特性无法通过高吸附质浓度的实验室测试直接得到,而如果开展低吸附质浓度的实验室测试则需要很长的时间才能得到结果,因此有必要开展一些相关的预测模型研究来分析低吸附质浓度下的吸附特性。
此外,以往对包括Langmuir模型、Freundlich模型和Dubin-Radushkevich(D-R)模型在内的气态污染物的吸附模型研究大多是在高浓度气态污染物工况下进行[17-18],而气态污染物的吸附性能与浓度并不一定呈线性相关规律,因此有必要对低浓度SO2吸附模型的适用性进行探究。另外,目前对SO2吸附机理的研究主要是基于烟气脱硫过程,此过程硫质量浓度为数千甚至数万mg/m3[19],对于低浓度SO2其吸附的特点和机理是否仍然适用还有待考究,因此有必要研究活性炭过滤材料对于低浓度SO2的吸附性能。笔者首先研究了3种碱改性活性炭对低浓度SO2的吸附性能,然后采用Langmuir模型、Freundlich模型和D-R模型拟合了碱改性活性炭对SO2的吸附特性曲线,最后通过不同吸附剂的特性曲线分析确定了SO2吸附过程中的主导因素以及核心机理。
1 实验部分
1.1 吸附材料
活性炭采购于3个不同的国产过滤介质生产商,并分别对3个活性炭样品使用KOH、CuO和Mg(OH)2进行改性得到CuO-KOH@AC、KOH@AC、Mg(OH)2@AC,3个改性活性炭样品相对负载碱基含量和孔结构信息见表1。一般认为微孔结构总的吸附势是不均匀的,吸附过程中往往按照吸附势的强弱进行吸附和填充,孔径越小的地方吸附势越强,较小孔吸附饱后,稍大的孔再填充。氮吸附等温线测试结果表明,3种被测样品的吸附等温线均为可逆Ⅰ型等温线[20],3个样品的孔径主要集中在2 nm以下,也就是说3个样品均属于微孔材料。有资料表明,吸附剂表面的微孔水平会直接影响其吸附性能[21]。从表1看出,3个样品的微孔比表面积为774~790 m2/g,微孔体积为0.336~0.368 cm3/g,总比表面积为817~1 124 m2/g,其中负载氢氧化镁的活性炭比表面积最大,为1 124 m2/g。因此,这3个样品的比表面积、微孔孔隙体积非常接近,差异主要体现在活性炭负载组分的种类和数量上。

表1 3种改性活性炭的比表面积与孔容Table 1 Specific surface area and pore volume of three kinds of modified activated carbon
1.2 表征方法
使用ASAP 2020型比表面积与孔隙分析仪在-196℃直接测量样品并获得氮吸附等温线,并分别通过Brunauer-Emmett-Teller(BET)方法、Barrett-Joiner-Halenda(BJH)方法、Dubin-Radushkevich(DR)方法获得比表面积、微孔和中孔体积以及孔径分布。使用Axios型X射线荧光光谱仪(XRF)对活性炭的成分进行分析(将实验样品研磨成粉末状,在马弗炉中以700℃燃烧6 h以消除C的影响)。采用ESCALAB 250Xi型X射线光电子能谱仪(XPS)以AlKα为激发源对吸附SO2后的活性炭样品进行分析,以检测样品表面S的化合价(在此过程前用284.8 eV的C 1s峰结合能对光谱进行校准)。采用Nexus 470型傅里叶变换红外光谱仪(FT-IR)对吸附SO2后活性炭样品表面的吸附物种进行分析,并对在400~4 000 cm-1的物质以4 cm-1的分辨率进行记录(将样品在玻璃研钵中研磨成粉末,然后与溴化钾混合)。
1.3 SO2吸附实验
吸附测试是根据ANSI/ASHRAE 145.1—2008《Laboratory Test Method for Assessing the Performance of Gas-Phase Air-Cleaning Systems:Loose Granular Media》和ISO 9227—2017《Corrosion Tests in Artificial Atmospheres-Salt Spray Tests》的要求在固定床流动系统中进行的。SO2吸附实验系统示意图见图1。测试系统的主要材料为聚四氟乙烯和304不锈钢,避免了对SO2吸附的干扰;洁净空气和SO2的流量由高精度质量流量控制器控制,保证了实验的准确性。测试样品均被装入厚度为10 mm的吸附管(容积约为0.785 mL,内径为10 mm)中。由于3种碱改性活性炭的原始形状不同,既有颗粒状也有柱状,因此将所有样品粉碎并筛分到粒度小于19 μm后进行吸附实验。为研究低浓度SO2环境下不同相对湿度(RH)对吸附性能的影响,在吸附温度为(25±2)℃和RH分别为1%、50%、75%条件下对CuO-KOH@AC进行了3组吸附实验,分别模拟极端干燥、一般潮湿和潮湿条件下碱改性活性炭对SO2的吸附性能。实验中RH由温控加湿器控制,使其根据需要保持在不同水平;SO2进出口浓度则由T100型紫外荧光SO2分析仪实时测量。吸附剂对SO2的去除率和吸附容量由式(1)(2)计算得出:
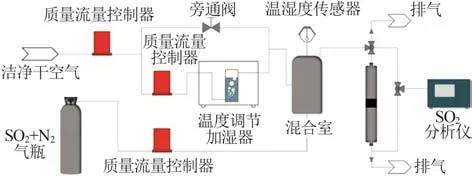
图1 SO2吸附实验系统示意图Fig.1 Schematic diagram of SO2 adsorption experiment system


式中:Ec为SO2去除率,%;ρinlet、ρoutlet分别为进、出口SO2质量浓度,mg/m3;ms为吸附剂对SO2吸附容量,mg/g;Q为总气流速率,m3/h;mad为吸附剂质量,g;tend为吸附实验中Ec下降到最终去除率Eend的总时长,h。
2 结果与讨论
2.1 改性活性炭对SO2的吸附性能
3种碱改性活性炭去除SO2的效率曲线见图2。实验条件:25℃,RH=50%,迎面速度为0.6 m/s,ρinlet=2 612 mg/L。从图2看出,KOH@AC和Mg(OH)2@AC对SO2的初始去除率分别为94.53%和90.08%,CuOKOH@AC对SO2的初始去除率最低,为84.41%,并且在开始吸附后其去除率下降速度明显快于其他两个样品。另外,计算了KOH@AC、Mg(OH)2@AC、CuO-KOH@AC 3组改性活性炭在穿透率达到40%时对SO2吸附量分别为64.17、64.09、7.98 mg/g。
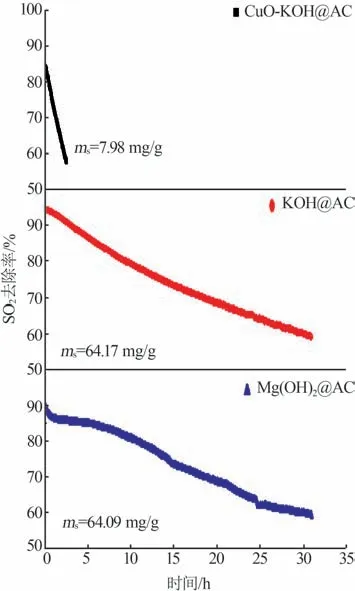
图2 负载不同碱基的活性炭去除SO2的效率曲线Fig.2 Efficiency curves of SO2 removal by activated carbon loaded with different bases
研究表明[22],未改性活性炭微孔的比表面积越大则吸附能力越强。而对于碱改性活性炭,相较于与其吸附性能没有明显相关性的微孔比表面积,其孔结构特性对活性炭吸附特性的影响更为明显。从表1看出,负载CuO-KOH的活性炭与负载KOH的活性炭孔结构相似,推断这两种样品的吸附能力相差不大。但是从图2可知,负载KOH的活性炭具有远高于负载CuO-KOH活性炭的初始吸附效率。也就是说,相对于负载改性物质的活性炭的孔结构,其吸附性能与所负载物质的种类和数量的关联性更大,这与前人的研究结果[15]非常吻合。
文献表明[23],负载铜元素对吸附SO2有良好的促进作用。在其他条件相近的情况下,负载CuO的改性活性炭的吸附能力明显高于未负载CuO的活性炭。这是因为,在活性炭上添加包括CuO在内的酸性物质、碱性物质、过渡金属盐类和氧化物等,可以利用配位吸附或其他化学作用来增强挥发性有机物的吸附效果,甚至可能代替活性炭表面的官能团成为吸附SO2的活性位点[24]。在负载CuO的改性活性炭吸附SO2的过程中,CuO通过铜金属基团将目标气体引入改性活性炭表面的同时,还充当着过渡金属的催化作用。同样地,用KOH、Mg(OH)2等碱液处理也能使活性炭吸附SO2的性能有一定程度的提高。其原因可能是碱性基团的引入与SO2发生化学反应以及以CO2形式释放的含氧官能团受热分解形成的空隙共同作用的结果。与KOH、Mg(OH)2等碱改性活性炭相比,在存在CuO颗粒的情况下某些活性炭微孔可能被堵塞,导致比表面积显著降低。当微孔被CuO颗粒阻塞时,可能会通过CuO的聚集形成介孔和大孔[25]。然而,SO2气体的吸附归因于微孔和引入CuO载体的离子相互作用的结合[26],这直接导致负载CuO的吸附效率可能低于KOH、Mg(OH)2等碱改性活性炭。
2.2 改性活性炭对SO2吸附等温线拟合
为在有限的实验时间内在低浓度SO2工况下获得更好的吸附数据,选择了代表性更好的CuOKOH@AC作为实验对象,并将迎面速度调至0.36 m/s。图3a为不同SO2浓度下CuO-KOH@AC对SO2的穿透率曲线。图3a表明,吸附剂在高SO2浓度下失效快,随着SO2浓度的降低,吸附剂的使用寿命显著增长。在相同的穿透率条件下,吸附剂在各SO2浓度下的吸附量存在较大差异。也就是说,吸附剂在目前常用的高SO2浓度(SO2质量浓度为23.5~235 mg/m3)条件下的吸附量并不能反映其在真实环境浓度下的吸附性能。通过实验得到的吸附结果以散点图的形式呈现在图3b中,并用3种等温吸附模型进行拟合。Langmuir模型(式3)、Freundlich模型(式4)和D-R模型(式5)的具体表述如下[18]:

图3 不同SO2质量浓度下CuO-KOH@AC对SO2的穿透率曲线(a);Langmuir模型、Freundlich模型和D-R模型拟合曲线(b)Fig.3 Breakthrough rate curves of CuO-KOH@AC at different SO2 concentrations(a)and the fitting curves of the Langmuir model,the Freundlich model and the D-R model(b)
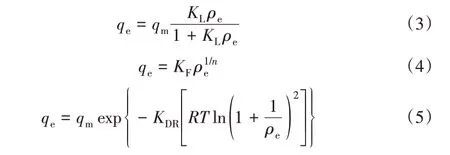
式中:qe、qm分别为拟合、实际测量中的吸附量,mg/g;ρe为入口SO2质量浓度,mg/m3;KL为吸附平衡常数,m3/mg;KF为吸附常数,mg1-1/n·m3/n·g-1;KDR为吸附常数,mol2/kJ2;n为无因次参数,与吸附作用推动力大小和吸附位能量有关,1/n表示吸附强度或表面不均匀性,为0~1的常数。
3种模型的拟合和预测结果见表2。由表2看出,D-R吸附等温线模型拟合效果最差。文献表明[27],该模型将分子吸附行为描述为微孔填充理论,认为吸附着重点在物理吸附。活性炭吸附SO2包括物理吸附和化学吸附,物理吸附产物中硫价态主要为+4价,化学吸附产物中硫价态主要为+6价。通过XPS分析两种价态的硫元素,结果为物理吸附引起的168.3 eV峰位面积占比和催化氧化吸附引起的169.4 eV峰位面积占比分别为4.42%和95.58%,证明低浓度SO2环境化学吸附是主要的吸附方式。而且,较差的拟合结果表明物理吸附在低浓度SO2时可能不占主导地位。而Freundlich模型给出的预测值与实际测量吸附量最接近,偏差最小。这表明吸附剂表面吸附位点可能分布不均匀,强度也不尽相同。此外,特征系数(1/n)小于1,进一步说明低浓度SO2吸附可能以化学吸附为主。

表2 3种模型的拟合和预测结果Table 2 Fitting and prediction results of three models
2.3 相对湿度对改性活性炭吸附SO2的影响
图4为不同RH条件下CuO-KOH@AC吸附SO2的性能。从图4看出,3种RH条件下穿透率曲线之间的差异非常明显。在RH为1%条件下,CuO-KOH@AC对SO2的去除效率随着时间的推移而迅速下降,穿透率达到70%时耗时仅为6.76 h,此时吸附剂对SO2的吸附量为14.75 mg/g。在RH为50%条件下,吸附剂对SO2的吸附量为27.52 mg/g,穿透率达到70%时耗时为12.42 h。在RH为75%条件下,吸附剂对SO2的吸附性能最好,穿透速率变化最慢,吸附剂对SO2的吸附量高达127.33 mg/g,穿透率达到70%时耗时达到56.72 h。值得注意的是,在RH为75%时吸附剂对SO2的吸附能力约为RH为50%时的4.6倍,相当于RH为1%时8.6倍,可以认为水分子参与反应促进吸附,有利于进行不可逆的化学反应。从不同RH条件下CuO-KOH@AC吸附SO2后的XPS分析结果(2.4节的图6)也可以看出,由于水分子参与化学吸附和洗刷被占据的活性位点继续氧化吸附,随着RH增加S6+价态的占比增大,证明环境中RH的增加将提高活性炭吸附剂对SO2的吸附能力。这与早期工业烟气处理研究中发现空气中的水会促进高浓度SO2在活性炭上的吸附相一致[28]。这意味着在建筑环境控制应用中,使用的活性炭式SO2过滤设备可以放置在高湿度环境下的空气处理流程中,以获得更好的过滤性能,进而延长其使用寿命。
与现有文献[28]高浓度SO2穿透率曲线相比,低浓度SO2在改性活性炭中的吸附穿透率曲线趋势与之一致,各RH条件下的最终穿透率均随着湿度的增加而升高,穿透时间也与湿度成正比。但是,与高浓度SO2情况不同的是,较之于高浓度SO2的穿透率曲线,低浓度时达到饱和时间所需的时长更长、穿透率更高。此外,在高浓度SO2穿透率曲线中,在RH达到一定水平(30%)后,继续增大RH对穿透率的影响将不再明显。而在本实验中,即使RH达到50%,或者继续增加RH依旧对降低穿透率有显著作用(见图4)。也就是说在低浓度SO2吸附过程中湿度的影响更大、效果更为显著。
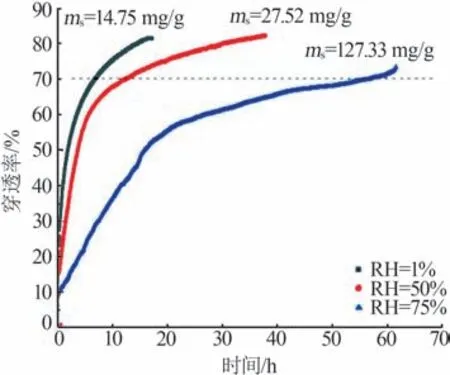
图4 不同RH条件下CuO-KOH@AC对SO2的穿透率曲线Fig.4 Breakthrough rate results of CuO-KOH@AC under different RH conditions
2.4 改性活性炭吸附SO2表面吸附物种类分析
在SO2质量浓度为1 306~13 400 mg/L的环境中CuO-KOH@AC吸附SO2后的FT-IR图见图5。有资料表明,吸附SO2后的吸附剂在1 130 cm-1处观察到—SO3基团的强带,在610~630 cm-1处观察到—SO2基团的弱带[29]。本次实验结果表明,气态SO2在CuO-KOH@AC表面主要转化为—SO2基团和—SO3(或SO42-)化合物作为吸附产物。另一方面,这也表明—SO2基团在化学吸附作用下会被氧化生成SO3,符合以往的研究结论[30]。在不同RH条件下CuOKOH@AC吸附SO2后S 2p的XPS图见图6。从图6看出,S 2p有169.4 eV和168.3 eV两个峰,分别属于S的+6价态和+4价态[31]。
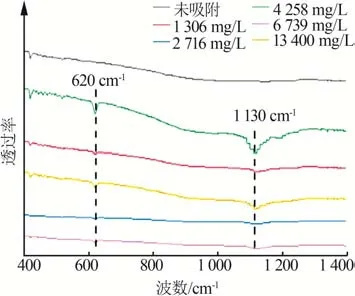
图5 CuO-KOH@AC吸附SO2后的FT-IR图Fig.5 FT-IR spectra of CuO-KOH@AC after SO2 adsorption

图6 CuO-KOH@AC吸附SO2后的XPS图Fig.6 XPS spectra of the CuO-KOH@AC after SO2 adsorption
综上所述可以得到以下结论:首先,该吸附剂表面的亚硫酸产物为S6+和S4+,这与FT-IR的分析结果一致;第二,在RH为1%时S6+的峰面积占比为80.35%,表明即使在湿度很低的情况下吸附剂表面的吸附活动仍以硫的氧化物为主,这也说明在干燥环境下吸附过程中发生的氧化反应仍可以进行;第三,在RH为1%和50%时,穿透率达到60%所耗的时间差别不大,容污量无显著差异,这可能是因为在极低SO2浓度和低湿情况下,水分子会与SO2竞争活性位点,其量也不能高到刷新活性位点,因此被过滤空气的湿度并不是表面吸附的SO2发生氧化反应的必要条件,但是高湿度的环境会明显加剧这种氧化过程;第四,在3种不同湿度条件下S的化合价80%以上是S6+,说明碱改性活性炭对SO2的吸附主要是在吸附-氧化过程中完成的;第五,SO2的高氧化比且氧化后生成的SO3(或SO42-)比SO2更稳定、不易被解吸,表明吸附剂具有良好的吸附性能,特别是吸附容量大,这与变湿实验的台架试验结果一致。
2.5 表面吸附机理探讨
根据台架试验和表征结果可以认为,在低SO2浓度条件下碱改性活性炭表面的吸附过程以化学吸附为主,此外在吸附过程中大部分SO2被氧化成高价硫化物,这意味着碱改性活性炭对低浓度SO2的吸附过程可能遵循类似于高浓度(超过几千mg/m3)时的氧化行为。前人研究提出了活性炭氧化吸附过程的机理,涉及的主要反应如下[27]:
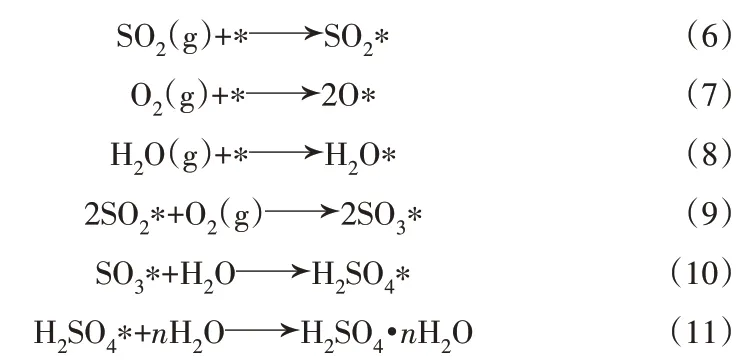
这一过程的总反应方程式可表示为:
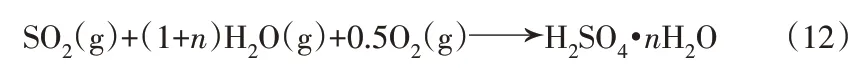
在上述完整的吸附过程中,(6)(7)(8)分别代表空气中的SO2、O2、水蒸气首先分别被吸附在吸附剂表面的中心(*)上,均属于物理吸附过程;(9)(10)(11)表示吸附态的SO2与同处于吸附态的O2、H2O反应,最终生成硫酸水合物并释放到活性吸附位点附近,从而保证了吸附剂吸附的连续性、持久性,这几个过程属于化学吸附过程,其中(10)(11)均有H2O参与,但是H2O发挥的作用不同,(10)中H2O溶解、吸附被氧化而成的SO3*,(11)中H2O进一步吹脱改性活性炭表面的H2SO4*。从这个角度看,活性炭化学吸附SO2过程的主要参与者是O2和H2O。在大气环境中的低浓度SO2脱除过程中,相对于SO2含量,氧含量是非常充足的,这使得湿度对吸附性能的影响十分显著。从反应式(10)和(11)或总反应方程式(12)来看,H2O的量越多越有利于反应的正向进行。这也就解释了为什么湿度越高吸附的SO2被氧化成高价态的比例也越高。对于未改性活性炭来说,水分对吸附的促进作用可以被认为是水对吸附产物的溶解,以确保吸附点重新获得吸附能力[30]。在高浓度SO2情况下,一部分SO2没有散布到活性炭内部,进而导致SO2吸附效率降低。对于碱改性活性炭,SO2则会被碱金属组分吸附,然后参与进一步的氧化产生硫酸盐物种,如硫酸钾和硫酸镁。值得注意的是,这些硫酸盐产品是水溶性盐类,这意味着有水参与的活性位置更新过程很可能会溶解表层形成的硫酸盐并与湿空气中的水分继续结合、吹脱,这一系列过程不仅释放了活性中心,同时也暴露了其中的基本官能团。这一结论表明,在高湿度条件下工作的活性炭,其表面的碱组分将更充分地参与SO2的吸附过程。
3 结论与展望
选取了3种常用的SO2过滤用碱改性活性炭进行低浓度SO2吸附性能测试。用3种等温吸附模型拟合了不同SO2浓度下的吸附性能。此外,还在不同环境湿度、SO2浓度较低的条件下,对碱改性活性炭吸附剂表面的吸附物种进行了表征和分析。主要结论:1)碱改性活性炭对SO2的吸附以吸附-氧化过程为主,气态SO2主要以SO42-的形式吸附在碱改性活性炭表面,由于碱改性活性炭对SO2有较强的化学吸附作用,其吸附容量对碱负荷的含量可能比对表面孔结构更为敏感;2)在低浓度SO2条件下,Freundlich模型比Langmuir模型和D-R模型具有更好的拟合效果和预测效果,偏差最小,结合Freundlich模型的特征系数(1/n)小于1和吸附势不一致的假设,可得知表面吸附位点分布不均匀是由于化学吸附占主要因素造成的;3)环境湿度的增加将增强碱改性活性炭对低浓度SO2的去除能力,这种促进的潜在原因是,当可溶性硫酸盐产物被吸附剂表面上的水带走时,内部碱性官能团被暴露出来并参与到吸附过程。

