新型冠状病毒保存液开发与应用*
余 辉,钟德优,范月珍,黄丽芳
(福州长庚医疗器械有限公司,福建 福州 350100)
有学者从1例患者呼吸道样本分离出一种新型β冠状病毒,并对其基因组进行了测序[1-2]。这种新型冠状病毒(SARS-CoV-2)因其与急性呼吸道综合征冠状病毒的遗传同源性而被命名为SARS-CoV-2,而该病毒是引起新型冠状病毒肺炎(COVID-19)的主要病原体[3-6]。距今为止,全球各地均发现COVID-19并有蔓延扩散的趋势,其带来的诊断、治疗、死亡等对全球人民经济、公共健康均造成了沉重负担。
国家卫生健康委员会发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》指出,将实时荧光定量聚合酶链反应(qPCR)与病毒基因测序作为病原学确诊证据[7]。但病毒基因测序操作复杂,检验周期较长,国内缺乏相关专业人才,所以,qPCR核酸检测成为阻止疫情蔓延扩散的主要手段[8-9]。然而病毒样本从采集送至实验室检测的过程中总存在着各种问题,使样本中的病毒核酸降解或变异,影响了实验数据的准确性。因此,作者研发了一种不仅能完整保存病毒的原始性状及活性使病毒核酸不被降解,并优化待测样本的存储条件与保存时间尽量延长的病毒样本保存液——长庚病毒样本保存液(CG保存液),并与常规保存液对比分析了CG保存液的存放效果,现报道如下。
1 材料与方法
1.1材料
1.1.1研究对象 采用常规保存液(常规保存液组)和CG保存液(CG保存液组)存放新型冠状病毒阳性对照品。
1.1.2试剂与仪器 达安新冠病毒检测试剂阳性对照(滴度为10×105IU/mL),核酸提取或纯化试剂购自中山大学达安基因股份有限公司,SARS-CoV-2核酸检测试剂盒(荧光PCR法)购自中山大学达安基因股份有限公司,常规保存液、CG保存液均由福州长庚医疗器械有限公司提供,qPCR仪采用罗氏LightCycler®480。
1.2方法
1.2.1阳性质控品制备 将50 μL阳性对照品分别用常规保存液或CG保存液稀释至5 mL,混匀后分装至采样管中备用。
1.2.2稳定性分析
1.2.2.1室温(25 ℃) 抽取2组保存液采样管各3支,室温存放6、12、18、24 h,收集样本后进行核酸提取与qPCR扩增反应,检测循环数(Ct)值。
1.2.2.24 ℃ 抽取2组保存液采样管各3支,4 ℃存放1、2、3、5、7 d,收集样本后进行核酸提取与qPCR扩增反应,检测Ct值。
1.2.2.3-20 ℃ 抽取2组保存液采样管各3支,-20 ℃存放2、4、6、8周,收集样本后进行核酸提取与qPCR扩增反应,检测Ct值。
1.2.3核酸提取 根据中山大学达安基因股份有限公司核酸提取或纯化试剂中说明书操作步骤取200 μL待测样本进行核酸提取。
1.2.4qPCR扩增反应 根据中山大学达安基因股份有限公司SARS-CoV-2核酸检测试剂盒(荧光PCR法)说明书操作步骤取5 μL待测样本核酸,加入20 μL反应液,混匀后转移至核酸扩增区进行检测。扩增反应参数:50 ℃、2 min,95 ℃、2 min,1个循环;95 ℃、5 s,60 ℃、35 s,10个循环;95 ℃、5 s,60 ℃、35 s,45个循环。ORFlab基因基础值为34.65,N基因基础值为33.93。
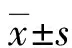
2 结 果
2.12组保存液室温存放检测结果比较 CG保存液组室温存放6、12、18、24 h靶基因Ct值比较,差异均无统计学意义(P>0.05);常规保存液组室温存放第12小时后N基因Ct值明显上升,室温存放第18小时后ORFlab基因Ct值明显上升,差异均有统计学意义(P<0.05)。见表1。

表1 2组保存液室温存放检测结果比较值)
2.22组保存液4 ℃存放检测结果比较 2组保存液4 ℃存放1、2、3、5、7 d靶基因Ct值比较,差异均无统计学意义(P>0.05)。见表2。

表2 2组保存液4 ℃存放检测结果比较值)
2.32组保存液-20 ℃存放检测结果比较 2组保存液-20 ℃存放2、4、6、8靶基因Ct值比较,差异均无统计学意义(P>0.05)。见表3。

表3 2组保存液-20 ℃存放检测结果比较值)
3 讨 论
COVID-19流行期间采用qPCR是检测COVID-19患者SARS-CoV-2的“金标准”[10]。但持续增长的检测需求导致有效的待测样本收集和运输介质极度缺乏[11-12]。因此,本研究通过评估CG保存液保存效果,以期替代常规保存液,并快速、准确地检测SARS-CoV-2,确保适当的患者管理、疫情控制及更好地了解该病毒的全球流行病学[13-14]。
实验室早期应用生理盐水替代病毒样本保存液运输保存时发现,生理盐水无法达到较长时间保持病毒的完整性状及活性,因此,生理盐水不适用于替代病毒样本保存液。GARNETT等[15]将阳性对照品分别放入各种转运介质后检测SARS-CoV-2分子发现,生理盐水组室温放置可检测的RNA大量损失。随着保存液研究的深入,科研人员在培养基中添加Hank′s平衡液、稳定蛋白质组、抗生素、缓冲剂等多种物质组成常规保存液以应对疫情期间运输介质短缺[16-17]。当将常规保存液保存阳性对照品时发现,-20 ℃放置8周或4 ℃放置7 d靶基因稳定性未受影响;然而室温放置24 h后靶基因Ct值明显上升;说明常规保存液能保持病毒在体外的活性及核酸的完整性,提高病毒核酸阳性检出率;但其保存待测样品后对环境温度具有较严格的限制,表现出常规保存液存在局限性。本研究结果与此结论一致。MCAULEY等[18]将阳性对照品使用常规保存液室温保存24 h后病毒RNA含量显著下降。基于上述原因,CG保存液添加了合适的核酸裂解液,快速破坏细胞膜,使蛋白变性沉淀,游离出核酸及减少Mg2+、Ca2+、Mn2+等二价金属离子对核酸质量的影响;并加入合适的显色试剂,使操作人员便于观察采样前与采样后的区别[19]。本研究结果显示,采用CG保存液保存阳性对照品时发现,CG保存液在不同环境温度下靶基因稳定性均未受显著影响。
总之,选择氯化铵、乙二胺四乙酸盐、焦磷酸二乙酯、十二烷基硫酸钠、吐温20、二硫苏糖醇等成分使CG保存液能迅速消除SARS-CoV-2感染性,防止病毒核酸降解,降低运输与检测人员感染率;另外,保存液包含核酸RNA酶抑制剂,保护病毒核酸稳定不被降解,增加了核酸提取效率,更适用于因繁忙的临床环境而延误送样本到实验室检测。

