Catalyst6颅内支撑导管联合支架取栓术治疗急性缺血性脑卒中的疗效观察
童 贵,范 进,汪子琪,张松格
(成都西区医院神经内科,四川 成都 610036)
目前,急性缺血性脑卒中(AIS)已成为国内首要致残及致死原因,残疾率高达75%;对时间窗内具备手术指征的AIS患者通过静脉溶栓及桥接机械取栓手术以到达靶血管成功再通、更好地挽救缺血半暗带使患者最大获益及最大限度地改善预后、减少致死率及致残率是目前临床研究的主要方向[1]。自从2015年新英格兰杂志等公布五大AIS血管内机械取栓随机对照试验(RCT)临床研究结果[2-4],以及2018年中国急性缺血性卒中血管内治疗指南明确指出时间窗内静脉溶栓治疗后桥接血管内取栓手术治疗为目前最高级别推荐方案以来[5],目前,血管内机械取栓治疗技术已迅速成为我国AIS重要的治疗手段。而目前指南推荐的取栓手术主要包括单纯支架取栓技术、直接一次性抽吸取栓技术、支架拉栓+负压抽吸联合取栓技术(SWIM)三大技术。SWIM集合了支架拉栓和一次性负压抽吸取栓技术2种手术优点。但在具体手术中采用何种手术方案及流程目前尚无固定模式,探索一种操作简单、手术时间短、低血栓逃逸率低,研究更低的术后24 h颅内出血、脑疝发生率的手术模式及流程为患者带来更大的获益是目前研究重点。本研究分析了成都西区医院及西部战区总医院5年来收治的AIS患者的临床资料,比较了单纯支架取栓及Catalyst6颅内支撑导管负压抽吸联合Solitare FR支架取栓2种取栓手术操作模式和流程,旨在为AIS患者机械取栓术中具体操作流程和技术改进提供参考依据。
1 资料与方法
1.1资料
1.1.1一般资料 收集2017年1月至2022年1月成都西区医院和西部战区总医院神经内科收治的132例住院AIS患者的临床资料,按不同手术方式分为观察组(采用Catalyst6颅内支撑导管联合支架取栓,67例)和对照组(采用单纯支架取栓,65例)。2组患者年龄、性别、合并疾病等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。本研究符合成都西区医院及西部战区总医院医学伦理委员会相关规定,

表1 2组患者一般资料比较
1.1.2纳入标准 (1)发病6 h内AIS并接受取栓手术的患者;(2)术前快速完成CT平扫并进行卒中CT评分大于或等于6分的患者;(3)术前采用磁共振、CT灌注成像检查等多模式影像学检查评估存在可挽救的缺血半暗带;(4)手术采取Catalyst6持续负压抽吸联合Solitare FR支架和单纯Solitare FR支架拉栓操作模式的患者;(5)同意参与本研究的患者。
1.1.3排除标准 (1)前循环大血管为慢性狭窄基础上合并急性栓塞(术后证实或术前3.0 T高分辨磁共振证实为原位慢性狭窄并栓塞);(2)大脑前动脉栓塞或后循环系统栓塞;(3)3.0 T高分辨磁共振或CT血管成像证实为串联病变(急性颈内动脉近端血管栓塞合并大脑中动脉等远端栓塞或近端颈内动脉慢性狭窄合并远端血管急性栓塞)。
1.2方法
1.2.1治疗方法 2组患者均予以相同临床治疗路径、术后90 d回访。
1.2.2手术操作
1.2.2.1SWIM技术 患者取平卧位,全身麻醉满意后常规消毒铺巾,以右侧腹股沟下缘1.0 cm处股动脉搏动明显处为穿刺点,并予利多卡因0.1 g局部浸润麻醉,麻醉满意后经右侧腹股沟下缘1.0~1.5 cm股动脉搏动明显处行改良seldinger技术穿刺插管并植入8 F股动脉穿刺鞘,在150.0 cm泥鳅造影导丝引导下将5 F(125 cm)多功能造影导管分别置于主动脉弓、颈总动脉开口处、按对应剂量予造影剂注入,同时行脑血管造影,明确血管栓塞部位及侧支血管代偿情况,选择相应尺寸取栓支架及手术方案。阅片满意后予以同轴技术泥鳅导丝带5 F多功能造影导管外带6FNeuro Max TM0.88长鞘或8 F guiding指引导管送至颈内动脉C1段远端。于路径图(Roadmap)指引下利于同轴技术微导丝(Synchro-14)外带微导管(Rebar18或27)缓慢通过靶血管栓塞段并向前送至靶血管栓塞段远端并越过栓塞段(颈内动脉虹吸段或大脑中动脉水平段远端或M2段),然后回撤出微导丝,经微导管手推造影剂证实微导管远端在血管真腔内。经微导管送入相应尺寸的取栓支架(Solitare FR 4 mm×20 mm或6 mm×30 mm),回撤微导管将支架释放于靶血管栓塞段(支架远端标记点跨过血栓,应用 Solitare 支架有效取栓段覆盖血栓),待支架展开并停留观察5 min后(快速恢复栓塞段血管前向血流并使支架充分展开并嵌入血栓)。此时关闭所有肝素生理盐水灌洗通道,缓慢前推Catalyst6颅内支撑导管使其头端充分接触血栓近端(当支撑导管负压增大或抽吸时无回抽血液提示头端已与血栓接触),助手经Catalyst6颅内支撑导管予以双50 mL卡扣注射器保持负压吸引状态。Solitare FR取栓支架及Catalyst6颅内支撑导管一并回撤入8 F guiding或6 F Neuro Max长鞘内。当取栓支架和Catalyst6颅内支撑导管一体撤出至邻近8 F guiding或6 F Neuro Max长鞘尾端时连同Y阀一同撤出体外。在回撤过程中使用双50 mL卡扣注射器分别回抽8 F指引导管及Catalyst6颅内支撑导管以防止导管内有残存血栓。取栓完成后即刻造影复查靶血管开通情况,如未成功开通则重复上述取栓手术过程,但取栓次数不宜超过3次。术后予以颈内动脉造影,采用改良脑血流灌注分级情况(mTICI)评估靶血管开通情况。术后拔除8 F股动脉鞘,并予以右侧股动脉压迫止血器压迫穿刺点并加压包扎止血,术后即刻复查CT提示颅内无术后继发出血及高灌注损伤。具体操作流程,见图1。
1.2.2.2单支架取栓 患者取平卧位,全身麻醉后常规消毒铺巾,经右侧腹股沟下缘股动脉搏动明显处行改良seldinger技术穿刺并植入8 F股动脉穿刺鞘,在150.0 cm泥鳅造影导丝引导下将5 F(125 cm)多功能造影导管分别置于主动脉弓、颈总动脉开口处、按对应剂量予行脑血管造影,明确责任血管栓塞部位及侧支血管代偿情况,选择相应尺寸取栓支架及手术方案。阅片满意后予以同轴技术泥鳅导丝带5 F多功能造影导管外带8 F guiding指引导管置于颈内动脉C1段远端。路图指引下利于同轴技术微导丝(Synchro-14)外带微导管(Rebar18或27)缓慢通过靶血管栓塞段并向前送至栓塞血管远端,撤出微导丝,经微导管手推造影剂证实微导管远端在血管真腔内。经微导管送入相应尺寸的取栓支架(Solitare FR 4 mm×20 mm或6 mm×30 mm),回撤微导管将支架释放于靶血管栓塞段,待支架充分展开并停留观察5 min,此时关闭所有肝素生理盐水灌洗通道,助手经8 F guiding导管予以50 mL卡扣注射器保持负压吸引状态。Solitare FR取栓支架及微导管一并回撤入8 F guiding指引导管内。当取栓支架和微导管整体撤出至邻近8 F guiding尾端时连同Y阀一同撤出体外。取栓完成后即刻造影复查靶血管开通情况,如未成功开通则重复上述取栓手术过程,但取栓次数不宜超过3次。
1.2.3观察指标
1.2.3.1有效性指标 (1)统计比较2组患者术中栓塞血管只取栓1次、血管成功开通率等。采用取栓1次手术完成后即刻行靶血管手推造影,采用改良mTICI进行脑梗死溶栓灌注分级,mTICI达到2b/3级血流灌注评价为靶血管成功开通。(2)统计比较2组患者术后90 d 改良Rankin评分(mRS),评价患者长期预后,mRS 0~2分为预后良好。(3)统计比较2组患者术后90 d内病死率,以评价患者术后短期内预后。(4)统计比较2组患者从股动脉穿刺成功置鞘至栓塞血管成功开通总手术用时或栓塞血管未能成功开通的患者手术结束时间。
1.2.3.2安全性指标 (1)统计比较2组患者术中血栓逃逸并发血管远端栓塞发生例数,计算血栓逃逸发生率。(2)统计比较2组患者术后24 h内颅内出血、脑疝发生率,以及病死率。将手中发生血栓逃逸和术后24 h内颅内出血评价为一般不良事件,术后24 h内出现脑疝或死亡评价为严重不良事件。
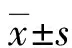
2 结 果
观察组患者取栓1次责任血管成功开通率、术后90 d良好预后率均明显高于对照组,术后90 d内死亡率、血栓远端逃逸率均明显低于对照组,差异均有统计学意义(P<0.05);总手术时间、术后24 h内颅内出血率、术后24 h内脑疝形成率、术后24 h内病死率与对照组比较,差异均无统计学意义(P>0.05)。见表2、3。

表2 2组患者有效性指标比较

表3 2组患者安全性指标比较[n(%)]
3 讨 论
2015年至今国际国内多项RCT均明确证实,运用Solitare FR支架取栓在AIS中运用安全、有效[6];如DAWN及DEFUSE-3等血管内机械取栓研究均提示良好预后率及不良安全事件发生率与本研究结果基本一致。但由于取栓支架原理:支架释放径向展开过程中,支架网眼对血栓的切割作用容易造成红色血栓破碎,破碎小栓子易发生远端逃逸。而颈内动脉在直径上相较于大脑中动脉较大,血栓体积相应更大,且前向血流冲击力更大,加上支架对血栓切割作用,更容易使小直径血栓远端逃逸。在取栓手术过程中无球囊导管阻断前向血流的情况下采用Catalyst6颅内支撑导管持续负压抽吸下联合支架拉栓能最大限度地降低血栓逃逸率。负压抽吸联合支架拉栓具有以下几点已经明确的优势[7]:(1)在大脑中动脉M1段取栓手术中不能完全阻断前向血流情况下利用Catalyst6头端顺应性及到位能力跨过大脑前动脉开口,可以很好地避免血栓逃逸至大脑前动脉。(2)联合取栓可以增加血栓一次抓取概率增加成功开通率,减少取栓操作次数,最大限度地减少小栓子逃逸,提高手术效率及手术安全性。但SWIM联合取栓技术在具体手术操作流程中可以通过Catalyst6支撑导管回收取栓支架以增加支撑导管内负压抽吸强度,且支撑导管在原位保留以利于取栓通路的保持、缩短第2次取栓操作时间[8-11];但也可以不通过支撑导管回收支架,而是采用和本研究一样的手术方法支架连同Catalyst6支撑导管一起回撤入8 F指引导管[12-15]。
本研究术中均采用Solitare FR支架不回收入Catalyst6颅内支撑导管内,而是取栓支架连同Catalyst6颅内支撑导管一并回撤入8 F guiding指引导管后一并回收,该方法优点是避免取栓支架上所附着的血栓通过Catalyst6头端时血栓变形碎裂,能最大限度地减少血栓逃逸[16-19]。不可否认上述针对不同手术方案及流程的研究影响因素众多,故存在一定的不足和局限性:(1)手术主刀医师操作技术水平及熟练程度等因素对手术效果及开通时间、血栓逃逸及预后等均存在一定影响,但该影响因素无法量化及评价。(2)如何降低术后24 h死亡和脑疝等严重并发症,综合分析与充分术前评估、严格把关手术适应证、术中及术后血压管理、术中谨慎操作有关。(3)本研究为AIS手术患者的回顾性研究,但受限于时间窗内患者数量及手术患者例数较少,对术中操作模式的比较尚需要更大样本量及更多RCT研究结果进一步证实[20-21]。
综上所述,对血管内治疗时间窗内AIS患者单从手术操作技术的角度分析与单支架取栓术比较,Catalyst6颅内支撑导管联合支架取栓技术在术后24 h颅内出血、术后24 h脑疝、术后24 h内死亡等安全性指标方面无显著差异,且没有明显增加总手术时间,观察组患者显著提高了靶血管1次成功开通率,减少了术中血栓逃逸,并具有更低的90 d内死亡率和更高的术后90 d良好预后率,更好的短期内及长期预后。

