血管性痴呆患者社区获得性肺炎的相关因素分析
王玉,褚静鑫
(重庆市急救医疗中心,1.临床技能中心;2.全科医学科,重庆 400010)
血管性痴呆(vascular dementia,VD)是老年期痴呆的主要类型之一,约占全部老年期痴呆病例的16%,我国VD患病率约为1%~3%[1]。超过1/3的65岁以上脑卒中患者可在发病后3个月内进展为VD,且随着我国脑卒中发病率的逐年升高,VD发病率也不断上升[2]。VD患者临床表现以记忆和认知功能缺损为主,可同时伴有语言、运动、视觉、空间感知等方面的认知功能异常,不仅严重影响患者的生活质量,而且由于存在明显的神经功能损害且具有多种风险因素,患者的肺部感染发生率较高。近年来,既往报道[3-4]也证实VD患者易发生多重耐药菌感染,治疗难度较高,患者预后较差,但在VD患者社区获得性肺炎(community acquired pneumonia,CAP)相关因素研究方面分歧较多[5],导致针对此类感染的预防控制难以深入。因此,本研究采用回顾性方法分析VD患者CAP的相关因素。
1 资料与方法
1.1 一般资料
连续选取2019年1月至2021年6月在重庆市急救医疗中心住院治疗、符合入选标准的126例VD患者作为研究对象。纳入标准:(1)符合《2016中国血管性认知障碍诊疗指导规范》[6]中VD的诊断标准;(2)患者临床资料完整,可供回顾性研究采集资料。排除标准:(1)合并恶性肿瘤、肝肾功能不全、血液系统疾病、自身免疫疾病、免疫缺陷病者;(2)长期应用免疫抑制剂或糖皮质激素者;(3)由外伤、毒物接触等非血管性因素引起认知功能障碍者;(4)入组时明确诊断合并肺外局部感染或全身性感染的患者。
1.2 观察指标
1.2.1 CAP情况 通过查阅病案对纳入患者的CAP情况进行调查和分析,CAP的诊断标准参照中华医学会呼吸病学分会制订的《中国成人社区获得性肺炎诊断和治疗指南》中的CAP诊断标准[7],具体标准为:感染为社区发病或明确潜伏期社区获得性感染的医院内发病,患者均具有新近出现的咳嗽、咳痰等呼吸道症状或原有症状加重,伴有脓性痰、胸痛、发热等感染症状,胸部X线影像学检查可见斑片状浸润阴影或间质性改变,部分患者伴有胸腔积液,查体可闻及明显的肺部干湿性啰音,实验室检查可见血常规白细胞计数升高或降低。根据是否发生肺部感染将患者分为感染组和未感染组。
1.2.2 相关因素调查 设计调查表并通过查阅病案对纳入患者的肺部感染相关因素进行调查和分析,主要包括:(1)一般资料:年龄、性别、吸烟史、饮酒史、营养状态、卧床情况。(2)脑血管疾病及相关危险因素:糖尿病、高血压、高甘油三脂血症、冠心病。(3)临床症状和体征。在调查之前对所有参与调查者进行培训,明确纳入和排除标准,确定数据采集录入过程中具体问题的解决方法,采集数据采用双人分别录入,由第3人进行逻辑复核,出现分歧时由第3人最终确定。
1.3 统计学分析
2 结果
2.1 VD患者的CAP情况及单因素分析
21例患者发生CAP,感染率为16.67%。在一般资料方面,感染组患者的吸烟史、营养不良、长期卧床比例高于未感染组,差异有统计学意义(P<0.05)。在脑血管疾病及相关危险因素方面,感染组患者的糖尿病比例高于未感染组,差异有统计学意义(P<0.05)。在临床症状和体征方面,感染组患者的球麻痹比例高于对照组,差异有统计学意义(P<0.05)。见表1。
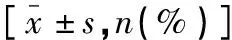
表1 两组患者临床资料比较
2.2 VD患者合并CAP的多因素分析
将单因素分析中差异有统计学意义的因素作为自变量纳入Logistic多元回归模型进行分析,结果显示,VD患者合并CAP的发生与吸烟史、糖尿病、球麻痹具有相关性(P<0.05)。见表2。
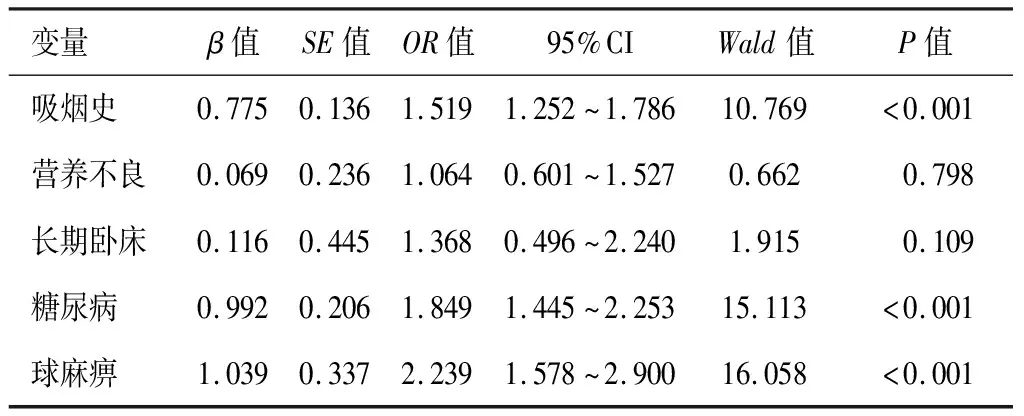
表2 VD患者合并CAP相关因素的Logistic多元回归分析
3 讨论
VD和阿尔茨海默症(Alzheimer’s disease,AD)是老年人群最常见的痴呆类型,而VD患者一般具有明显的脑血管疾病病史,且多合并有高血压、冠心病、糖尿病等基础疾病,虽然可能同时存在脑组织退行性病变因素,但血管性因素在其发病机制中仍占据主要地位[8],故合并CAP的比例较高。VD患者较高的肺部感染风险来自四个方面:(1)VD患者因罹患脑血管疾病而遗留有偏瘫、吞咽困难、震颤等后遗症,易出现误吸,部分重症患者在急性期后仍需要长期卧床,导致了肺部感染的多发[9];(2)VD患者一般具有高龄、基础疾病多、器官储备能力弱、营养状态不佳的特点,导致了其对病原微生物的抵御能力不足[10];(3)脑卒中的应激损害会进一步导致患者的免疫功能下降,相关研究[11-12]结果显示,脑血管疾病患者存在着明显的外周血T淋巴细胞计数降低,主要表现为CD8+T淋巴细胞、调节性T细胞(Treg)/CD4+T淋巴细胞比例升高,CD4+T淋巴细胞、CD4+/CD8+T淋巴细胞比值降低、辅助性T 细胞17(Th17)/CD4+T淋巴细胞、自然杀伤细胞(NK细胞)、B细胞比例均下降,血清免疫球蛋白水平、血清补体水平、血清白细胞介素、肿瘤坏死因子、干扰素等炎症因子水平紊乱,脾脏体积也显著缩小,且上述变化与脑血管疾病的病情程度呈正相关关系,虽然患者的免疫功能可在急性期之后逐渐得到恢复,但短期免疫功能失调仍导致了肺部感染风险的升高;(4)脑血管病变后细胞外液易在白质内潴留从而对神经功能产生影响,而合并严重脑白质病变VD患者的神经功能水平通常难以得到较好恢复[13],部分患者在急性期后甚至无法自理,更易出现肺部感染。本研究显示,VD患者的肺部感染率较高,故临床医生对于入院的VD患者应认真评价和诊断其肺部感染风险,对于未感染者应采取有效措施预防感染的发生,对于已感染者应及时给予抗感染治疗以改善其临床预后。
近年来,关于VD患者肺部感染相关的报道极少,尽管针对脑血管疾病患者肺部感染相关因素的研究[14-15]较多,但结果存在分歧,其中,报道的急性脑梗死肺部感染相关因素包括年龄、既往肺部疾病、完全卧床、侵入性治疗、糖尿病、病情程度、意识状态、炎症因子基因多态性、低蛋白血症、住院时间等,多发性腔隙性脑梗死肺部感染相关因素则包括年龄、糖尿病、血清白蛋白及β2微球蛋白水平、D二聚体水平等。本研究中,吸烟史、糖尿病及球麻痹可对VP患者肺部感染风险产生影响。吸烟已成为一项世界性的健康问题,全世界吸烟总人口已超过15亿[16],吸烟可引起气道和肺泡发生炎性反应,导致巨噬细胞、中性粒细胞、T淋巴细胞等异常激活,进而上调白细胞介素、白三烯、肿瘤坏死因子等炎性因子水平[17],并诱导肺组织的氧化损伤[18],其病理变化主要包括肺组织基质、肺实质细胞外基质的降解,气道出现粘液分泌增加、阻塞、纤维化、纤毛清除功能破坏、肺泡壁损伤等改变[19],使肺组织和气道对感染的防御和清除系统破坏,肺部感染风险明显提升。相关研究[20-21]显示,具有吸烟史颅脑病变患者的肺部感染率明显偏高,吸烟是诱发肺部感染的主要原因,患者的吸烟时间越久,其肺感染风险越大,而且其肺部感染的治疗难度和病死率也越高,同时,吸烟还会使患者术中高碳酸血症风险、术中氨茶碱应用率、术后雾化治疗率升高,提升术后感染风险。糖尿病对肺部感染风险的影响已被学术界广泛认可,糖尿病患者的肺部感染主要包括大叶性感染、小叶性感染、真菌性感染及肺结核,糖尿病病程越长,其痰标本中革兰阴性菌和真菌的检出比例越高,产超广谱β-内酰胺酶菌株、多重耐药菌株的检出率也越高[22]。同时,糖尿病合并肺部感染患者的多器官功能障碍综合征风险还与其空腹血糖情况有关,积极控制血糖和合理选用抗菌药物能够促进肺部感染的病情转归[23-24]。50%~70%的脑卒中后存活者会遗留不同程度的后遗症,而卒中相关性肺炎的发生率高达50%,其主要原因以吞咽困难、饮水呛咳、发音障碍为特征的球麻痹较为常见[25]。因此,针对合并球麻痹的VD患者,应加强振动排痰、营养支持、吞咽困难筛查、吞咽功能训练等临床护理措施,以降低肺部感染的发生率;对于已发生感染的患者,应在积极治疗原发疾病的基础上足量、早期应用敏感性抗菌药物,必要时可考虑及早鼻饲和建立人工气道,从而提高感染的控制效果,达到改善患者预后的目的。
综上,VD患者的肺部感染率较高,且吸烟史、糖尿病及球麻痹与VP患者肺部感染风险密切相关。VD患者的CAP风险与行为因素、基础疾病、脑血管疾病后遗症多种因素有关,对患者的感染风险应开展全面评价,及时预防干预。

