琥珀酸在哌柏西利片中的应用研究
钱进,霍立茹,*,张倩倩(.徐州医科大学,江苏 徐州 000;.南京济群医药科技股份有限公司,南京 00)
哌柏西利片是治疗乳腺癌晚期的主要药物。其片剂因主药含量大,可压性及流动性不佳而较难制剂化,且主药在pH 4.5介质中溶解度差而难以产业化,故需选用适宜的辅料进行制备[1-3]。琥珀酸常作为片剂的助溶剂、润滑剂等,具有抗结块、改善流动性及提高药物稳定性和溶解度等作用。不同目数的琥珀酸具有不同特性,能够从结合性、溶解性及稳定性等多方面影响片剂的质量,因此琥珀酸目数的筛选尤为重要。本试验通过对比不同目数琥珀酸的主要功能性指标,分别制备处方研究其对哌柏西利片制备过程中物料流动性、可压性及包衣片的溶出曲线、有关物质的影响,筛选出合适目数(粒径范围)的琥珀酸用于哌柏西利片的制备[4-6]。
1 材料
1.1 仪器
AL104型电子天平(Mettler Toledo),6S-OCEDM微量电子天平(Sartorius),U3000高效液相色谱仪(DIONEX),BM2000 显微镜(江南永新光学仪器有限公司),GL2-35 干法制粒机(张家港市开创机械制造有限公司),ZPS-8压片机(上海信源制药机械有限),S250SMART高速压片机(山东新马制药装备有限公司),三维混合机(南京锐霸科技有限公司),YD-35 硬度仪(天津市鑫洲科技有限公司),MB-35 水分测定仪(奥豪斯仪器有限公司),HELOS/BR-RODOS/T4 激光粒度测定仪(Sympatec),UV-2600 紫外分光光度计(日本岛津),FADT-1202 自动取样溶出仪(Focs),高效包衣机(深圳信宜特科技有限公司),药品强光照射试验箱(重庆永生实验仪器厂),恒温恒湿箱(施都凯仪器设备有限公司)。
1.2 试药
哌柏西利片(辉瑞公司,批号:EW2912,规格:125 mg/片);哌柏西利片(南京济群医药科技股份有限公司,规格:125 mg/片,批号分别为210320、210402、210411、210422、210506-1/-2);对照品哌柏西利(批号:20091201,纯度:99.90%)、杂质A(批号:21416,纯度:99.31%)、杂质B(批号:21446,纯度:99.31%)(中国食品药品检定研究院);琥珀酸(南京化学,批号:201030083C、201040091C、201030062C);微晶纤维素(旭化成,批号:2624,型号:PH102);羧甲基纤维素钠(德国瑞登梅尔,批号:3201081037);胶态二氧化硅(德国Evonik,批号:159011814);硬脂酸镁(湖州展望,批号:20200103);薄膜包衣预混剂(上海卡乐康包衣技术有限公司)。
2 方法及结果
2.1 琥珀酸功能性指标测定
结合原料流动性及可压性较差的性质并查阅产品介绍,选择4种具有代表性的琥珀酸(30目、40目、60目、80目)进行考察,通过其相关指标特性进行筛选。
2.1.1 粒径分布的测定 使用激光粒径仪干法进样测定琥珀酸的粒径分布,分散压力为4 bar,进样速率70%,使用RAOXO 2.0 软件对不同目数筛分的琥珀酸粒度分布进行分析,结果见图1、表1。
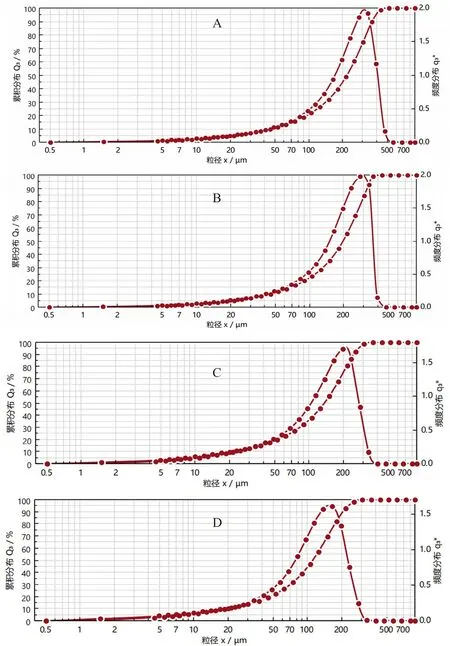
图1 琥珀酸粒度分布图Fig 1 Particle size distribution of succinic acid
2.1.2 流动性的测定 测定琥珀酸的休止角以考察其流动性,具体方法为将漏斗固定于水平铁架台上,从漏斗中缓慢加入物料至物料圆锥体高度不再增加,量取物料垂直高度及圆锥体半径,以物料垂直高度及圆锥半径比为正切值计算休止角[7],每批样品测量 3 次取平均值,结果见表 1。
2.1.3 堆密度、振实密度及压缩性指数 参照2020年版《中国药典》(ChP2020)四部通则0993[8],测定不同目数琥珀酸的堆密度及振实密度,根据公式压缩性指数=100×(堆密度-振实密度)/堆密度,计算压缩性指数,结果见表 1,不同目数琥珀酸的各指标均存在一定差异,将其作为哌柏西利片组成成分,分别制备成制剂后进一步确定其影响片剂的关键指标及选择最终的目数。
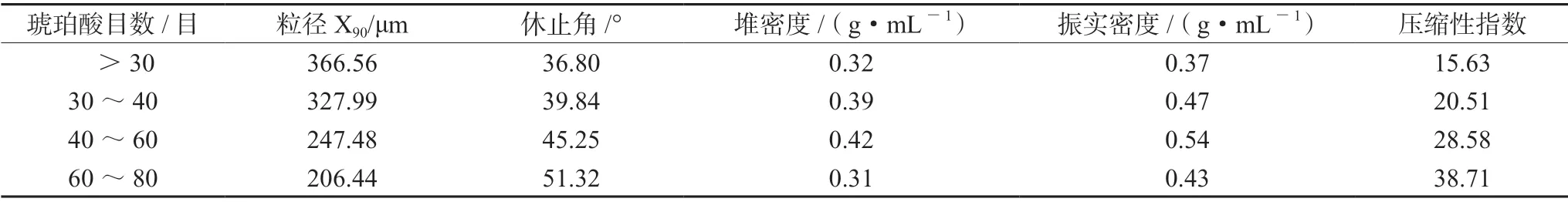
表1 琥珀酸功能性指标测定Tab 1 Functional indexes of succinic acid
2.2 制剂相关指标的测定
分别用目数为>30、30~40、40~60、60~80的琥珀酸与原料、微晶纤维素、羧甲基纤维素钠、胶态二氧化硅、硬脂酸镁过筛后称重混合,混合后物料进行干法制粒,样品批号对应为 210320、210402、210411、210422,4 批样品其他辅料种类、用量以及制备工艺均不变。
2.2.1 混粉相关指标的测定 ① 休止角的测定:取4批样品混粉参照“2.1.2”项下方法测定休止角,每批样品测量3次取平均值,结果见表 2。
② 压缩性指数的测定:取4批样品混粉参照“2.1.3”项下方法测定压缩性指数,每批样品测量3次取平均值,结果见表 2。
③ 颗粒率的测定:参照 ChP2020 四部通则0982单筛分法[8]测定 4批样品预混粉60目以上的颗粒率,每批样品测量3次,取平均值,结果见表2。使用60~80目的琥珀酸所制备的混粉休止角明显大于45°,流动性较差,需关注其片剂含量均匀度是否符合要求。
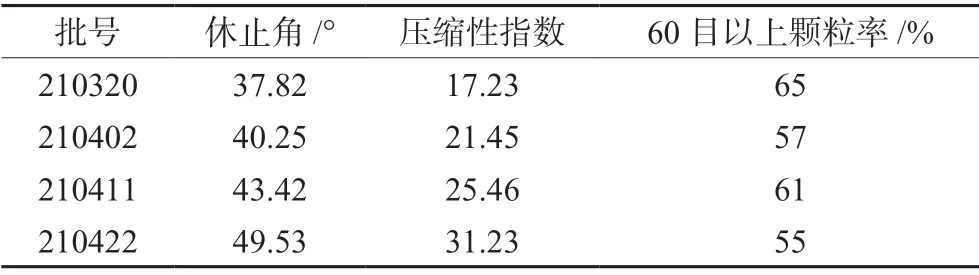
表2 混粉相关指标的测定结果Tab 2 Related indexes of powder mixture
2.2.2 片芯相关指标的测定 将 4 批样品在同一压片环境及设备条件下分别压片后进行片剂相关指标的考察。
① 外观及断层:在压片过程中观察各批样品的外观性状及断层现象。4 批样品在实验室压片数量为 500 片左右时均未出现断层现象,片剂片重稳定。继续进一步放大批量(2000片)并使用工厂设备压制片剂,考察压片是否断层,以确定处方工艺的可行性,结果见表 3及图2。

图2 片芯外观(批号:210402)Fig 2 Core appearance(batch No.210402)
② 硬度的测定:每批样品在连续压片过程中随机取样20片使用 MB-35 硬度仪测量片芯硬度,结果见表 3。
③ 含量均匀度的测定:参照 ChP2020 四部通则含量均匀度检查法[8],每批样品取10片片芯检测样品的含量均匀度,结果见表 3。60~80目琥珀酸流动性差,出现断层,故而含量均匀度不合格;>30目琥珀酸压片时,硬度只有120 N,可压性不好。因此下一步重点考察30~40目和40~60目琥珀酸所制制剂溶出曲线。

表3 片芯相关指标测定结果Tab 3 Related indexes of chip core
2.2.3 溶出曲线的测定
① 溶出试验条件:溶出方法为桨法,分别以水、pH 1.0 盐酸溶液、pH 4.5 醋酸盐缓冲液、pH 6.8 磷酸盐缓冲液为溶出介质,转速均为 75 r·min-1,溶出介质体积均为 900 mL,溶出介质温度均为(37±0.5)℃[9]。
② 溶液的配制:精密称取哌柏西利片对照品约12 mg置100 mL 量瓶中,加入少量溶出介质超声溶解并定容,再精密移取5 mL置50 mL量瓶中,加入溶出介质定容,得对照品溶液。分别于各取样时间点取出溶液10 mL,并补充同等温度的溶出介质10 mL,将所取样品溶液过滤,取续滤液1 mL 用介质稀释定容至10 mL作为供试品溶液。
③ 溶出曲线的测定:将210402 及210411批片芯均使用同一批薄膜包衣预混剂进行包衣,测定2批样品包衣片及参比制剂(各12片)在4种介质中的溶出曲线,具体方法为取各对照品及供试品溶液,参照 ChP2020 四部通则0401紫外-可见分光光度法[8]在353 nm处测量吸光度,按外标法计算溶出量,绘制溶出曲线,计算相似因子f2[10]。
结果表明 2 批自制样品在 pH 1.0、水、pH 6.8介质中的溶出曲线均与参比制剂相似,在pH 4.5中210402 批样品溶出曲线与参比制剂相似,f2>85,而210411批样品溶出速率慢于参比制剂,f2只有61,故接下来对210402 批样品进行影响因素试验,考察初步稳定性。溶出曲线见图3。
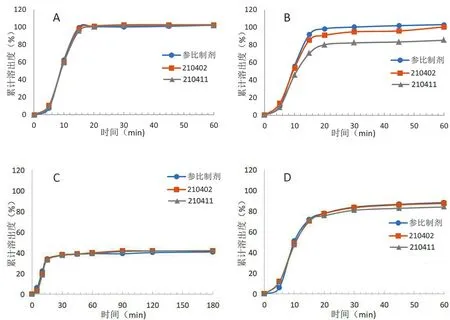
图3 参比制剂与 2 批自制样品在不同介质中的溶出曲线Fig 3 Dissolution curve of the reference preparation and 2 batches of self-made samples in different dissolution media
2.2.4 有关物质的测定
① 色谱条件:色谱柱为十八烷基硅烷键合硅胶为填充剂(250 mm×4.6 mm,5 μm);柱温为45℃;流速为 1.0 mL·min-1;进样量为 20 μL;检测波长为 250 nm;流动相A为0.03%三氟乙酸水,B为0.03%三氟乙酸乙腈;稀释溶剂为0.1 mol·L-1HCl-乙腈(80∶20),梯度洗脱,洗脱程序如下:0~10 min,90%A;10~40 min,90%~70%A;40~65 min,70%~15%A;65~66 min,15%~90%A;66~75 min,90%A。
② 溶液的制备:取包衣片研磨后细粉50 mg,精密称定,置100 mL量瓶中,超声溶解,用稀释溶剂稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。取哌柏西利、杂质A、杂质B,精密称定,用稀释溶剂稀释成每1 mL含哌柏西利0.5 mg及杂质A、杂质B各含5 μg的系统溶液。取各溶液进样测定,各成分分离度符合药典要求,见图4。
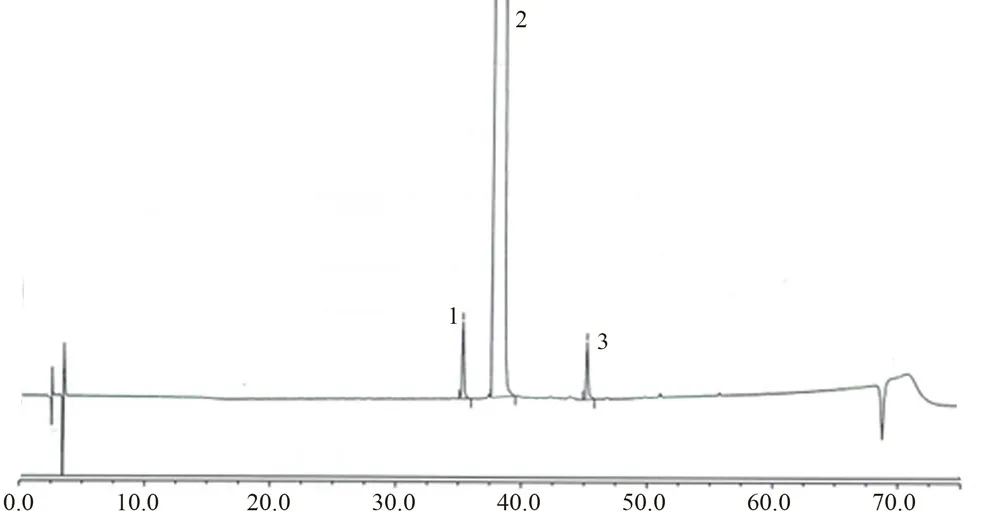
图4 系统溶液色谱图Fig 4 Chromatogram of system solution
取 210402 批自制样品及参比制剂进行影响因素试验,将各样品分别放置于高温(60℃)、高湿(RH 92.5%)以及光照[(4500±500)lx]条件下于 5、10、30 d取样检测有关物质。结果表明自制样品各杂质含量均不高于参比制剂,且杂质增长趋势与参比制剂基本一致,结果见表 4。
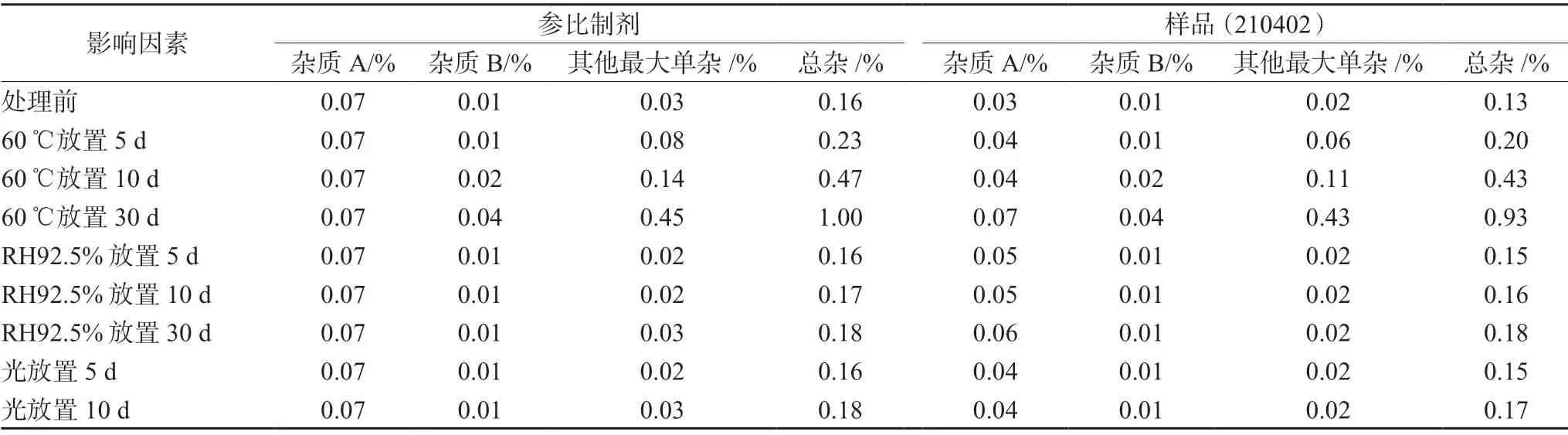
表4 有关物质测定结果Tab 4 Related substances
2.3 不同批次琥珀酸(30~40目)主要功能性指标一致性考察
选用2批不同批号(批号:201030083C、201040091C)琥珀酸(30~40目)参照“2.1”及“2.2”项下方法测定主要功能性指标并制备样品(批号分别为 210506-1、210506-2)进行研究,以考察不同批次辅料功能是否具有一致性,并确定不同批次辅料制备的样品质量是否一致。结果表明,不同批次的琥珀酸(30~40目)主要功能性指标检测结果及制剂相关检测结果均无明显差异,表明该辅料无明显批间差异,制备的样品质量基本一致(见表5~7及图5)。
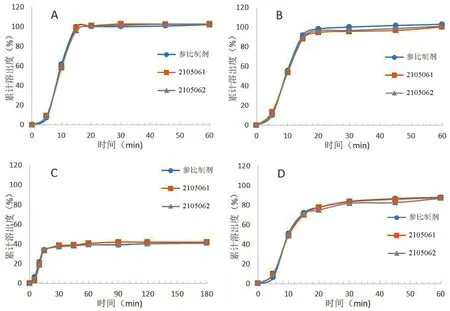
图5 参比制剂与 2 批自制样品在不同介质中的溶出曲线Fig 5 Dissolution curve of the reference preparation and 2 batches of self-made samples in different dissolution medium

表5 不同批次琥珀酸(30~40目)功能性指标测定结果Tab 5 Functional indexes of different batches of succinic acid (30~40 mesh)
3 讨论
3.1 流动性
从流动性角度分析,不同目数的琥珀酸因粒径大小差异导致流动性不同,从而影响制剂混粉的流动性。筛分得到60~80目的琥珀酸,粒径小,批量放大后,压片出现断层,混粉流动性差,不适合进一步研究。小于60目的琥珀酸,粒径较大,没有出现断层现象,适合进一步研究。

表6 不同批次琥珀酸(30~40目)制剂相关指标测定结果Tab 6 Related indexes of different batches of succinic acid (30~40 mesh) preparations

表7 有关物质测定结果Tab 7 Related substances
3.2 可压性
从可压性角度分析,>30目的琥珀酸,粒径大,批量放大压片时,主压片厚调至最小后,片芯硬度仍然只有120 N,达不到参比制剂的目标硬度(150~180 N)。故不适合进一步研究。
3.3 崩解特性
崩解特性角度分析,筛分得30~40目琥珀酸所制得制剂在区分力介质中(pH 4.5)崩解现象与参比制剂相似,在12 min左右崩解。但是40~60目琥珀酸所制得制剂在18 min左右崩解,且终点累计溶出度只有80%左右[5]。
综上所述,琥珀酸(30~40目)不同批次样品主要功能性指标检测的结果基本一致,功能具有一致性,所制备的3 批哌柏西利混粉流动性、可压性均较好,片剂溶出行为与参比制剂相似,产品质量与参比制剂一致,故适合作为哌柏西利的组成成分并进一步用于放大生产[11-12]。

