足月新生儿黄疸与维生素D及NADSYN1基因多态性的相关性研究
李国旭,王萍,周伟玮,崔晓玉,张芳,舒剑波,刘洋△
新生儿黄疸是新生儿时期常见的症状之一,可见于60%以上的正常新生儿[1]。较高的胆红素水平可产生不可逆的脑损伤,远期常遗留严重的神经系统后遗症,重者可导致死亡[2]。因此,对于新生儿高胆红素血症及其高危因素进行早期识别和干预尤为重要。维生素D(VD)在儿童生长发育及疾病进程中均起到了非常重要的作用[3]。VD缺乏与新生儿黄疸均是新生儿期常见的问题,但有关新生儿黄疸与VD关系的研究较少。烟酰胺腺嘌呤二核苷酸(NAD)参与线粒体代谢、细胞分裂、免疫应答等过程[4]。NADSYN1基因编码的NAD合成酶1是NAD合成的关键酶,近年逐渐成为研究VD遗传因素的热点之一[5]。高分辨熔解曲线(HRM)由于其操作简单、特异性高等优点,常用于疾病诊断、耐药基因筛查等领域[6]。本研究利用HRM检测VD相关基因单核苷酸多态性。国内外关于VD与新生儿黄疸的研究较少,且结果存在一定差异。有研究证实高胆红素血症患儿的VD水平低于正常新生儿[7-8],但也有研究证实两者间无明显差异[9]。本文通过研究足月新生儿黄疸、维生素D水平及NADSYN1基因rs12785878位点单核苷酸多态性之间的关系,及新生儿高胆红素血症的危险因素,为查找新生儿黄疸的病因提供新思路,以提高医务人员对足月新生儿高胆红素血症的认识。
1 对象与方法
1.1 研究对象 收集2019年5月—2020年8月于天津市儿童医院新生儿内科住院的216例伴有黄疸的足月新生儿作为研究对象,包括男117例,女99例,日龄1~30 d,出生体质量2 750~4 000 g,出生孕周37~41+5周。纳入标准:(1)入院查体存在皮肤黄染表现。(2)胎龄≥37周,且<42周。(3)出生体质量≥2 500 g,且<4 000 g。排除标准:(1)严重缺氧。(2)新生儿败血症、新生儿化脓性脑膜炎等重症感染。(3)先天性肝胆疾病,如先天性胆汁淤积、胆道闭锁等。(4)由同族免疫性溶血、红细胞膜或酶异常性疾病等引起的高胆红素血症。(5)先天免疫性疾病。(6)甲状腺功能异常。(7)肝、肾功能衰竭等重大疾病。(8)遗传代谢性疾病,如甲基丙二酸血症、Citrin缺陷病等。本研究获得本院伦理委员会审批(审批号:KY2020-40)。
1.2 方法
1.2.1 分组标准 参照《实用新生儿学》及《实用儿科学》的相关表述,足月儿生理性黄疸多于2周内消退,且总胆红素不超过221μmol/L。根据患儿的入院日龄(≤14 d、>14 d)和总胆红素(TBIL)水平进行分组如下:(1)日龄≤14 d组,包括高胆组1(TBIL>221μmol/L)和对照组1(TBIL≤221μmol/L);(2)日龄>14 d,包括高胆组2(TBIL>34.2μmol/L)和对照组2(TBIL≤34.2μmol/L)。
1.2.2 血清VD水平检测 采用液相色谱-串联质谱法(LC-MS/MS)对血清维生素D水平进行检测。根据《儿童微量营养素缺乏防治建议》规定:新生儿VD≤15μg/L为VD缺乏,>15μg/L且≤20μg/L为VD不足,>20μg/L为VD正常[10]。
1.2.3 临床相关指标采集(1)患儿的性别、日龄、出生体质量、胎次、感染因素、血糖、血浆蛋白、白蛋白、血酸碱度、血清VD、TBIL、直接胆红素、间接胆红素情况。(2)孕母的年龄、受教育程度、孕周、剖宫产史、母乳喂养情况。
1.2.4 应用PCR-HRM进行基因分型 通过文献复习,选择与VD相关的NADSYN1基因rs12785878位点作为研究位点[11]。采用PCR-HRM法检测rs12785878位点基因型。首先设计PCR引物:上游5′-GAATACCACCTTCAAATAGGGC-3′,下游5′-AGCATCTGGGCAACATCAG-3′,产物大小339 bp。经PCR扩增后,将扩增产物送Sanger测序以获得GG、GT、TT基因型。设计HRM引物:上游5′-CCTAAGTGCCAAGGGATCTA-3′,下游5′-AGGCTCACGAGACGATCAG-3′,产物大小122 bp。利用已测序基因型样本检验建立的HRM的准确性、特异性。
1.3 统计学方法 利用SPSS 25.0软件分析数据。符合正态分布的计量资料用均数±标准差(±s)描述,2组比较采用独立样本t检验;非正态分布数据采用M(P25,P75)描述,组间比较采用Mann-WhitneyU检验。计数资料用例(%)描述,组间比较采用χ2检验。采用二分类Logistic回归分析新生儿高胆红素血症的影响因素。样本群体代表性分析采用Hardy-Weinberg平衡检验。以P<0.05为差异有统计学意义。
2 结果
2.1 总体情况 ≤14 d组104例(48.1%),>14 d组112例(51.9%)。216例患儿VD水平平均(14.98±7.62)μg/L;其中≤14 d组VD水平平均(11.56±4.89)μg/L;>14 d组VD水平平均(18.15±8.31)μg/L。
2.2 ≤14 d组新生儿的临床资料及高胆红素血症影响因素分析 高胆组1较对照组1剖宫产率、母乳喂养率、感染发生率和TBIL水平高,血浆蛋白水平低(P<0.05),2组间VD水平差异无统计学意义,见表1。经HRM共检测104例患儿NADSYN1基因的基因型。以是否发生高胆红素血症作为因变量(是=1,否=0),以剖宫产、母乳喂养、感染(二分变量均赋值为:是=1,否=0)及血浆蛋白、VD水平作为自变量,分析104例≤14 d组新生儿发生高胆红素血症的影响因素。结果显示,感染、剖宫产与母乳喂养为高胆红素血症的危险因素,见表2。
2.3 >14 d组新生儿的临床资料及高胆红素血症影响因素分析 高胆组2较对照组2妊娠天数少、血浆蛋白水平和VD水平低,感染发生率高、TBIL水平高(P<0.05),见表3。经HRM共检测112例患儿NADSYN1基因的基因型,以是否发生高胆红素血症作为因变量(是=1,否=0),以感染(是=1,否=0)、妊娠天数、血浆蛋白和VD水平等为自变量,分析>14 d组112例新生儿发生高胆红素血症的影响因素。结果显示,血浆蛋白降低、感染为高胆红素血症的危险因素,VD水平不是发生高胆红素血症的影响因素。见表4。

Tab.1 Comparison of clinical data between the hyperbilirubinemia group and the control group in neonates with jaundice≤14 d表1 ≤14 d新生儿高胆组与对照组的临床资料比较
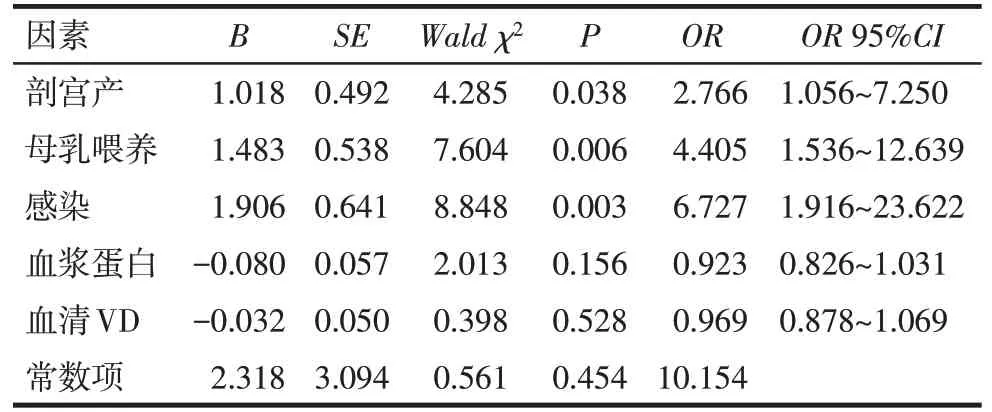
Tab.2 Analysis of risk factors of hyperbilirubinemia in neonates≤14 d表2 ≤14 d新生儿发生高胆红素血症的影响因素分析
2.4 黄疸、VD及NADSYN1基因多态性三者间的关系 本研究共检查了216例患儿rs12785878位点基因型,其中GG型54例,TG型101例,TT型61例,高胆组与对照组所选样本均具有群体代表性,符合Hardy-Weinberg平衡(P>0.05),见表5。
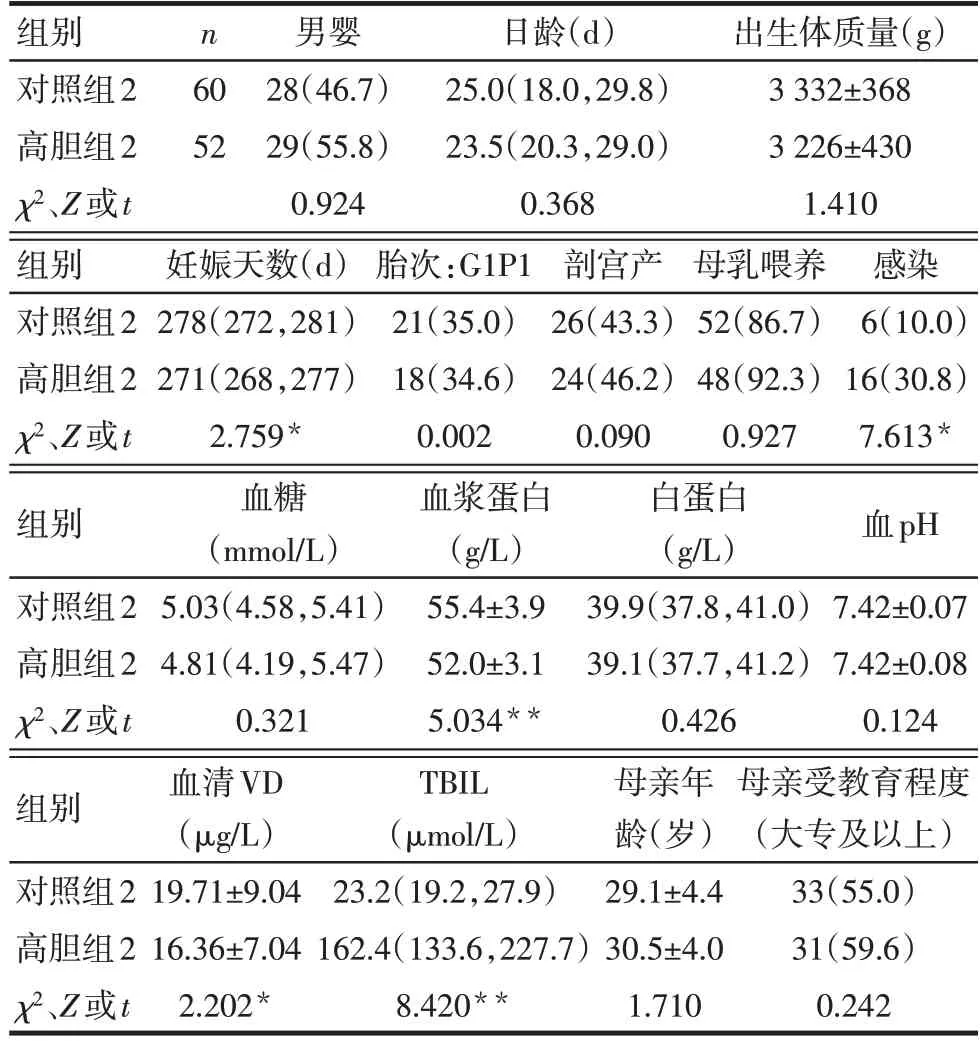
Tab.3 Comparison of clinical data between the hyperbilirubinemia group and the control group in neonates with jaundice>14 d表3 >14 d新生儿高胆组与对照组的临床资料比较
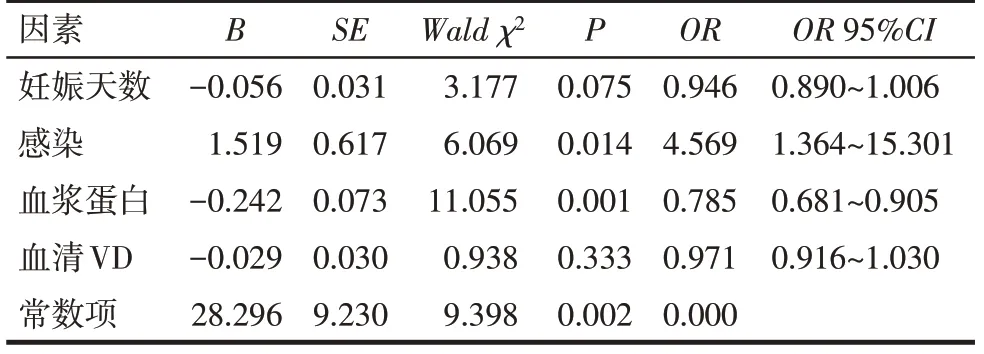
Tab.4 Analysis of risk factors of hyperbilirubinemia in neonates>14 d表4 >14 d新生儿发生高胆红素血症的影响因素分析
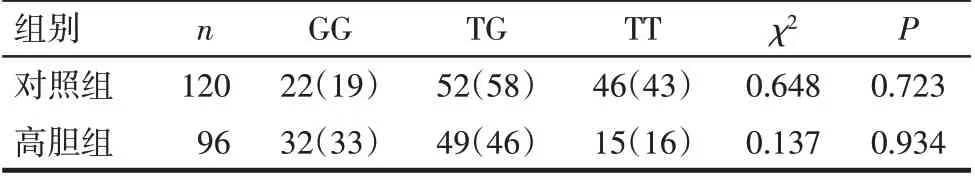
Tab.5 Hardy-Weinberg Equilibrium test at rs12785878表5 rs12785878位点基因型Hardy-Weinberg平衡检测[实际值(理论值)]
2.4.1 高胆组与对照组rs12785878位点基因型及等位基因比较 ≤14 d组,高胆组1与对照组1间基因型、等位基因分布差异均有统计学意义(P<0.05);>14 d组,高胆组2与对照组2间基因型、等位基因分布差异均有统计学意义(P<0.05),均表现为高胆组患儿GG型、G等位基因比例较高,见表6。
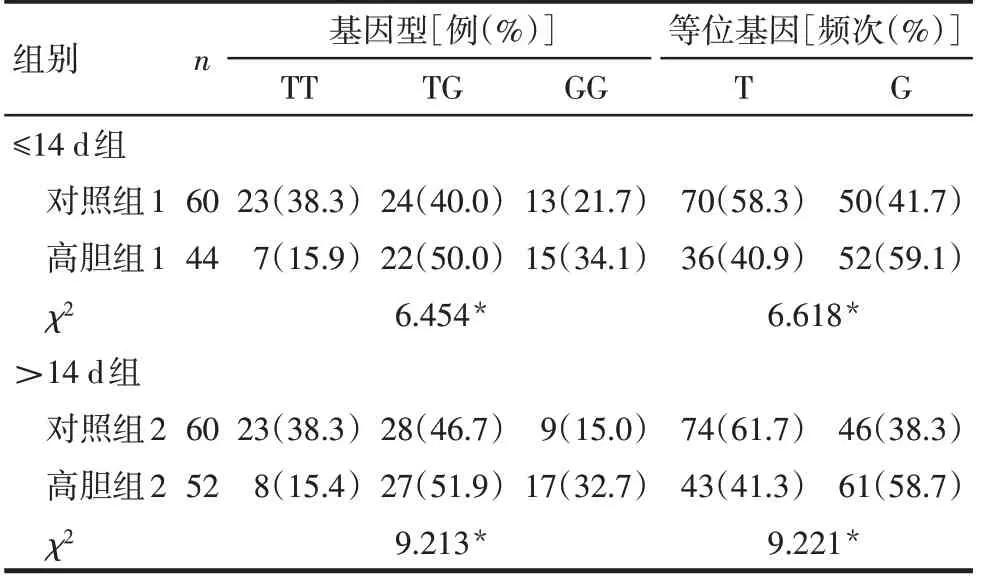
Tab.6 Comparison of rs12785878 genotype between the hyperbilirubinemia group and the control group表6 高胆组与对照组rs12785878位点基因型比较
2.4.2 rs12785878位点不同基因型VD水平的比较 ≤14 d组TT和TG基因型患儿维生素D水平明显高于GG基因型患儿;>14 d组中GG、TG、TT基因型新生儿的VD水平差异无统计学意义,见表7。
Tab.7 Comparison of VD levels between neonates with different genotypes at RS12785878 locus表7 rs12785878位点不同基因型及等位基因VD水平的比较 (μg/L,±s)

Tab.7 Comparison of VD levels between neonates with different genotypes at RS12785878 locus表7 rs12785878位点不同基因型及等位基因VD水平的比较 (μg/L,±s)
*P<0.05;a与GG基因型比较,P<0.05。
基因型GG型TG型TT型F n n 28 46 30≤14 d组VD水平9.62±4.24 12.05±4.81a 12.61±5.23a 3.239*26 55 31>14 d组VD水平17.28±7.57 17.79±8.30 19.53±9.00 0.621
3 讨论
新生儿黄疸的发生与种族、孕周、分娩方式、喂养方式、感染、生后体质量下降等多种因素有关[12-13]。患儿母亲的受教育程度及社会习俗与患儿黄疸的发生发展也有着重要的关系[13],但国内相关研究较少。本研究通过不同日龄高胆组与对照组的研究,验证与高胆红素血症有关的高危因素,为临床医生早期识别高胆红素血症提供思路。同时,本研究分析了高胆红素血症、VD及NADSYN1基因rs12785878位点三者间的关系,为临床医生诊治高胆红素血症提供一定帮助。
3.1 高胆红素血症的危险因素 本研究对≤14 d组新生儿的分析显示,感染、剖宫产、母乳喂养为高胆红素血症的危险因素。>14 d组中感染、低血浆蛋白为高胆红素血症的危险因素。感染是黄疸的诱发及加重因素之一,一方面患儿进食量减少,可供能量代谢减少,肠蠕动减慢,肠肝循环增加;另一方面,体内毒素可破坏细胞膜正常结构,导致细胞膜通透性增加,进而导致溶血,同时还可抑制葡萄糖醛酸转移酶的活性,导致机体内间接胆红素蓄积,诱发或者加重新生儿黄疸[15]。剖宫产引起高胆红素血症的机制可能与术中麻醉药物通过胎盘进入胎儿体内有关,麻醉药物不仅可导致血浆红细胞膜通透性增加,还可抑制胃肠蠕动[16]。母乳内葡萄糖醛酸苷酶含量及活性升高,可通过促进肠肝循环导致TBIL升高,同时母乳可影响葡萄糖醛酸转移酶活性,进一步导致TBIL升高[17]。但国外也有研究表明完全母乳喂养与新生儿黄疸无相关性[18]。本研究结果表明,母乳喂养为≤14 d组新生儿发生高胆红素血症的危险因素。由于日龄≤14 d新生儿可能存在母乳喂养不足、肝肠循环增加等情况,这些因素亦可以增加高胆红素血症的风险[19]。因此,家长及医务人员应注意评估≤14 d新生儿母乳喂养是否充足以及新生儿的体质量增长情况,以正确对待患儿的高危因素。血浆蛋白由肝细胞合成,主要由球蛋白和白蛋白组成。白蛋白承担转运游离胆红素至肝脏完成代谢的作用,低白蛋白可能影响游离胆红素的转运和代谢,从而加重黄疸[20]。本研究经多因素分析后证实,血浆蛋白水平升高是>14 d新生儿发生高胆红素血症的保护因素,但是单因素分析未发现低血浆白蛋白为发生高胆红血症的危险因素,后期还应增加样本量进一步研究。
3.2 高胆红素血症与VD水平的关系 相关研究证实高胆红素血症与VD有着密切的关系。Mutlu等[7]比较了30例足月高胆红素血症婴儿与21例对照足月婴儿的VD水平(日龄3~10 d),发现高胆组VD水平明显低于对照组(P=0.01)。Aletayeb等[8]同样发现高胆组患儿VD水平显著降低(P<0.001)。但是,2018年伊朗的一项研究将30例足月高胆红素血症婴儿与30例健康非黄疸足月婴儿的VD水平进行比较发现两者间差异无统计学意义(P=0.11)[9]。本研究显示,≤14 d患儿,高胆组1和对照组1之间VD水平差异无统计学意义;>14 d患儿,高胆组2和对照组2之间VD水平差异有统计学意义,当纳入多因素回归时VD并非发生高胆红素血症的影响因素,本研究得到的结论支持高胆组与对照组在VD水平上无差异,但是考虑到生后14 d内VD主要由母亲VD水平决定,14 d后多从外界摄入VD,且VD在人体代谢周期大约为14 d[21-22],因此可能存在一定的研究误差,未来可进一步完善相关变量控制,以进一步明确两者的关系。
3.3 rs12785878位点与VD水平的关系 全基因组关联分析研究证实NADSYN1/DHCR7基因座与VD水平有关[11,23]。rs12785878位于NADSYN1基因内含子区域,位于DHCR7基因附近,碱基突变类型为G>T,突变后与VD水平升高有关[24-25]。DHCR7基因编码7-脱氢胆固醇还原酶,该酶催化7-脱氢胆固醇生成胆固醇,7-脱氢胆固醇是VD合成的底物,因此当该基因功能受到影响时,VD合成底物相对增多,进而导致VD水平升高[26-27]。本研究中,≤14 d的TT基因型患儿VD水平明显高于GG基因型,>14 d患儿组则无差异,考虑理由同上文所说,>14 d患儿多从外界摄入VD从而对结果造成影响。本研究显示≤14 d患儿rs12785878位点GG基因型更易表现为低VD水平。
3.4 高胆红素血症与rs12785878位点SNP的关系 对高胆组患儿rs12785878位点不同基因型的分析显示,高胆红素血症发生的风险与不同基因型、等位基因组间差异有统计学意义,笔者发现高胆组携带GG基因型、G等位基因的比例更高。NAD是胆红素合成过程中的辅酶之一,当NADSYN1基因rs12785878位点发生G>T时,胆红素合成减少[28]。另有研究显示细胞内NAD水平下降时会导致细胞发生衰老等变化,因此NAD对细胞有一定的保护作用,在一定程度上可以减少红细胞的破坏,从而减少胆红素的生成[29]。因此推测NADSYN1基因rs12785878位点携带GG基因型、G等位基因的患儿更易发生高胆红素血症。
总之,母乳喂养、感染、剖宫产、低血浆蛋白水平为不同日龄足月新生儿发生高胆红素血症的危险因素。临床医生应正确识别这些高危因素,以提高诊治水平。患儿rs12785878位点携带GG基因型、G等位基因更易发生高胆红素血症。≤14 d患儿rs12785878位点携带TT基因型的VD水平更高。本研究较之前国内外关于新生儿高胆红素血症与VD关系的研究在一定程度上扩大了样本量,并包括了整个新生儿期,同时本研究有助于为新生儿黄疸的个体表型差异提供分子遗传学水平的解释,丰富了对新生儿高胆红素血症病因学的研究,可为严重高胆红素血症的预防和早期识别与诊疗提供参考。

