AlH3与MgH2对高氯酸铵热分解的影响
龙茂豪,崔立明,黄可奇,夏良洪,王彦娜,张同来
(1.北京理工大学 爆炸科学与技术国家重点实验室,北京 100081;2.淄博市产品质量检测研究院,山东 淄博 255000)
引 言
高氯酸铵(AP)作为氧化剂被广泛应用于固体火箭推进剂中,其热分解性能对推进剂的燃烧过程有重要的影响[1-4],通常应用于火箭推进剂中的催化剂是依靠催化高氯酸铵的分解来实现对火箭推进剂燃烧性能的改进[5-7]。
在过去的十多年中,氢作为清洁、高效的能源载体引起了广大学者的关注。轻金属氢化物作为储氢材料之一,因其优异的容积效率和安全性使其成为新能源领域的热门研究对象[8-9]。在轻金属氢化物中,目前研究较多的是MgH2和AlH3。镁基氢化物因其高含氢量和稳定性在火箭推进剂中有着良好的应用前景。刘磊力等[10-11]研究发现,MgH2对AP的催化作用强于镁粉,能显著降低AP的低温和高温分解温度,增大表观反应热。在AP/Al/HTPB复合推进剂中,MgH2通过催化AP的分解起到降低推进剂的热分解温度作用,同时推进剂反应热得到增强。姚淼等[9]将MgH2运用到炸药配方中,发现MgH2使RDX的表观活化能和安定性都有所降低。AlH3利用其高燃烧热、高比冲、高密度、无毒害性和良好成气性等特点成为固体推进剂和固液混合推进剂中的高能添加剂组分[12-14]。相应地,AlH3的加入可能会引起固体推进剂感度偏高、流变性变差等问题。Deluca等[15]将AlH3代替Al粉引进推进剂体系,发现推进剂比冲得到显著提高。俄罗斯Ermilov等[16]报道了含AlH3的高能固体推进剂,铝含量达6%~27%,该推进剂具有较好的热安定性和感度性能。程新丽等[17-18]研究发现,AlH3和GAP之间存在相互作用,与含硝酸酯黏结剂组成的混合体系中,其感度受硝酸酯的结构和硝酸酯中硝基的数量影响。
本研究通过差示扫描量热法(DSC)、热烤爆法、动态测压热分析法 (DPTA) 对AlH3/AP、MgH2/AP体系的热分解作用、热感度及安定性进行了系统性分析,并与纯AP进行了对比,以期为AlH3与MgH2应用于固体火箭推进剂配方设计和安全使用过程提供参考。
1 实 验
1.1 样 品
实验样品均由西安近代化学研究所提供,样品的信息如表1所示。分析测试用混合试样按各组分1∶1质量比进行研磨混合,操作过程需注意防潮和安全防护。
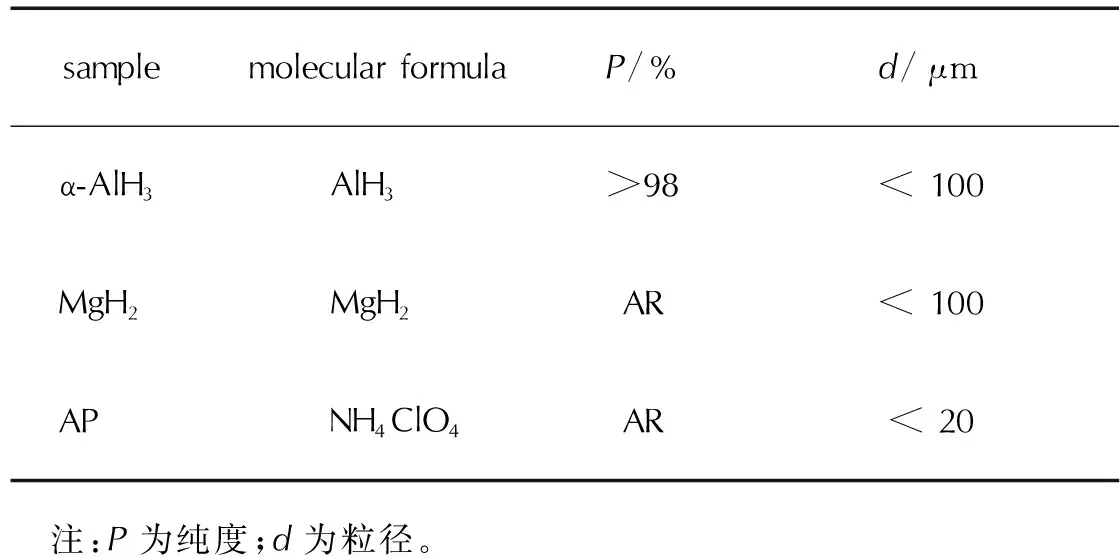
表1 实验样品Table 1 Experimental samples
1.2 仪器与测试条件
CDR-4P型差示扫描量热仪,上海申乐仪表电子有限公司;在产品测试前,用高纯的In、Sn和Zn对仪器的测量温度进行标定;测试环境温度25℃,相对湿度61%。
FCY-1型5s爆发点测试仪,陕西应用物理化学研究所;测试环境温度25℃,相对湿度61%。
动态测压热分析(DPTA)仪,本课题组研制;由热分解反应单元、程序控温加热单元、数据采集处理单元组成;依赖于高精度、高灵敏度、内置式微型压力传感器和温度传感器,能够对含能材料在定容、真空、加热的密闭环境中的分解放气反应过程进行实时、连续、在线的检测;集成高强度防爆防护反应单元、精密程序控温加热单元、微机数据采集和处理单元。测试环境温度25℃,相对湿度61%。
1.3 性能测试
采用DSC法,使用密闭坩埚,测试试样的分解放热过程;每次称取质量各约0.5mg的AlH3、MgH2、AP,作为单独组分;按质量比1∶1称取总药量约1.0mg,以AlH3和AP、MgH2与AP作为混合组分;升温速率分别为5、10、15和20℃/min。
采用热烤爆法,测试试样的5s爆发点温度;每次称取AIH3/AP、MgH2/AP和AP试样约20mg;采用DPTA法,测试试样在真空条件下的分解放气过程;根据国军标GJB 5891.12-2006火工药剂测试方法第12部分《真空安性测试——压力传感器法》,称取质量100mg的AP作为单独组分,按质量比1∶1称取总药量100mg,以AlH3和AP、MgH2与AP作为混合组分;将试样干燥后,均匀平铺在3组试管底部,抽真空至20Pa以下,静置30min,确保试样管内无压力变化,保证体系的密封性,然后直接放入加热炉均温块腔体内。仪器按照预置程序完成试样的加热及恒温保持,加热温度设置为100℃,恒定温度48h。
2 结果与讨论
2.1 DSC热分析
AlH3/AP和MgH2/AP体系试样在升温速率10℃/min时的DSC曲线如图1所示。
由图1 (a) 中AP的DSC测试结果分析可以看出,AP在251℃出现一个吸热峰,在这个温度区间AP发生晶形转变,由斜方晶转化为立方晶[19];在389℃处有一个明显的放热峰温,是AP的高温受热分解阶段。由图1(a) 所示,AlH3的热分解主要表现为一个放热过程,在190℃出现放热峰温。AlH3在发生受热分解、释氢反应时没有对应的吸热峰出现,是因为在空气气氛中,相较于AlH3分解释氢引起的吸热量,释氢形成的铝核所发生的氧化钝化反应放热量更为剧烈,所以在图1(a)中AlH3表现为明显的放热过程。在AP加入AlH3组成混合体系后,混合体系表现为两个放热过程,第一个放热峰在218℃附近出现,比起AlH3单独体系的放热峰推迟了约20℃,可见AP的加入使AlH3的热稳定性有一定程度的提高。在AlH3/AP混合体系中,AP分解的外推起始温度由351℃提前到了300℃,热分解温度提前了近50℃。分析认为,AlH3在195℃时已经进入热分解阶段,生成的活性铝核和H2都是缺电子结构,促进了AP分子中N—H键的断裂;同时,AlH3的分解产生较多的热量,进一步推进AP的分解反应进程,导致混合体系的放热过程相较AP单组分热分解过程有了明显的提前。

图1 AlH3/AP和MgH2/AP体系在10℃/min的 DSC曲线Fig.1 DSC curves of AlH3/AP and MgH2/AP series at 10℃/min
由图1(b)可知,MgH2的热分解过程为单一的吸热过程,吸热峰出现在400.5℃,这一阶段发生的是MgH2的分解释氢反应。与AP组成混合体系后,混合体系吸热峰温为245.8℃,与AP单组分的吸热峰对应,可知MgH2低温分解阶段对AP的晶形转变行为影响较小。在升温至310℃时,MgH2受热分解,AP也开始受热分解。与AlH3相似,MgH2的分解产物H2对AP的分解也有促进作用,混合体系较AP纯组分的分解放热峰温由389.9℃提前至351.2℃,提前了48.7℃。
对AIH3/AP、MgH2/AP和AP试样分别在5、10、15和20℃/min升温速率下进行DSC测试,测试结果如图2所示。
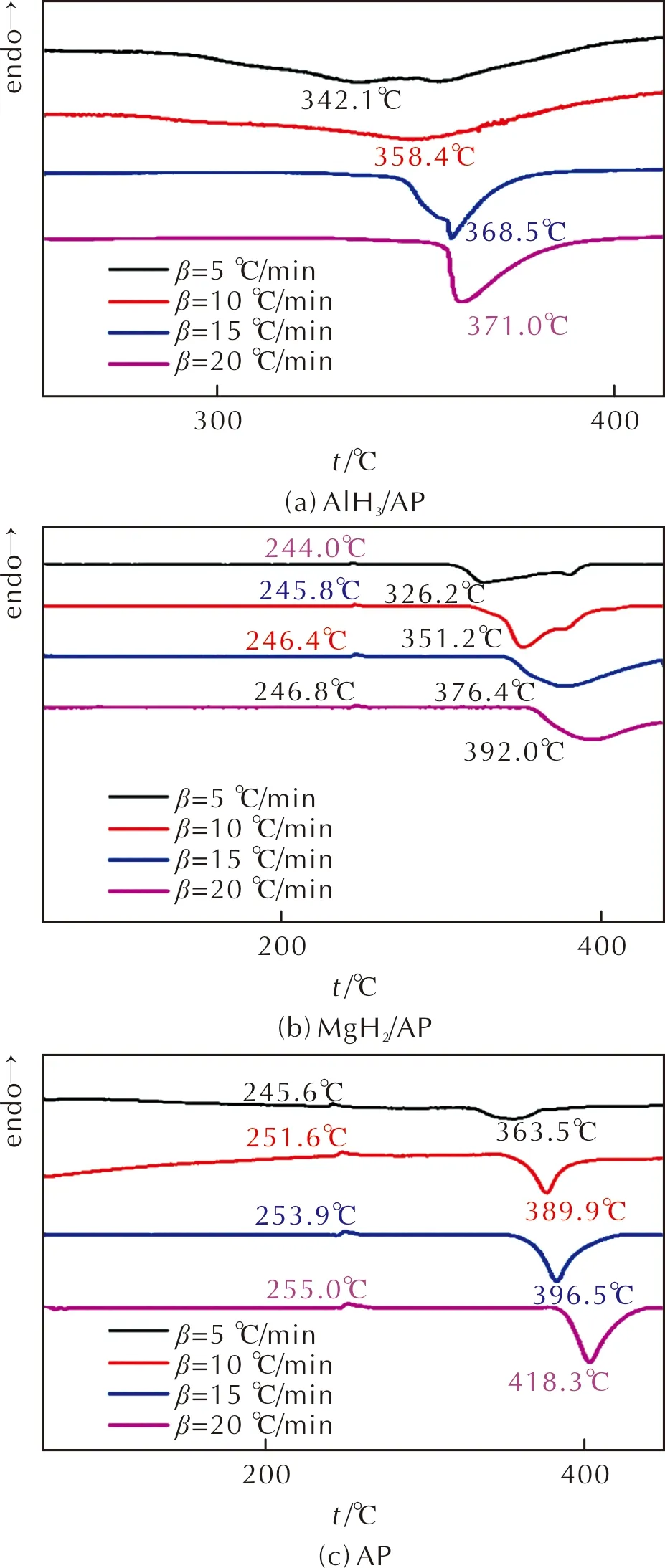
图2 不同升温速率下AlH3/AP、MgH2/AP和AP的DSC曲线Fig.2 DSC curves of AlH3/AP, MgH2/AP and AP at different heating rates
将获得的不同试样基于不同升温速率下的DSC曲线的第一分解放热峰峰温,采用Kissinger法[20]和Ozawa法[21]计算试样的非等温动力学参数,结果列于表2,式(1)和式(2)分别为Kissinger法和Ozawa法的计算方程式:

表2 非等温动力学计算参数Table 2 Calculation results of non-isothermal kinetic parameters
lnβ/Tp=lnAR/Ek+EK/RTp
(1)
lgβ=lgAEO/G(α)R-0.4567EO/RTp-2.315
(2)
式中:Tp为第一分解放热峰的峰顶温度,K;R为气体常数,8.314J/(K·mol);β为线性升温速率,K/min;G(α)为反应动力学函数;A为指前因子,s-1;EK和EO为Kissinger法和Ozawai法中计算的表观活化能,kJ/mol。
通过张-胡-谢-李方程[22]可计算得到热爆炸临界温度(Tb)。含能化合物的活化自由能(ΔG≠)、活化熵(ΔS≠)和活化焓(ΔH≠)等热力学参数可通过式(3)~式(7)计算得到:
Tpi=Tp0+aβ+bβ2+cβ3
(3)
(4)
A=(KaTp0/h)exp(1+ΔS≠/R)
(5)
ΔH≠=Ek-RTp0
(6)
ΔG≠=ΔH≠-Tp0ΔS≠
(7)
式中:a、b、c为常数;kB为玻尔兹曼常数,1.381×10-23J/K;h为普兰克常数,6.626×10-34J·s;Tp0为升温速率β→0K/min时的放热峰温,K;Tpi为升温速率β=iK/min时的第一放热峰温。
按上式计算了AP及混合样品的热力学参数,其计算结果如表3所示。
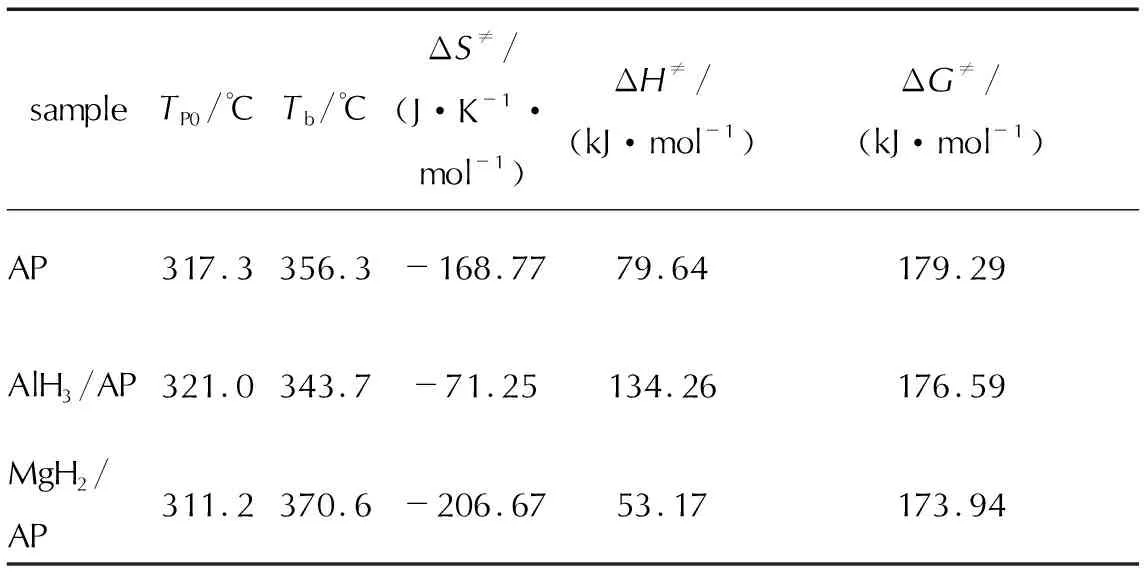
表3 试样热力学参数Table 3 Thermodynamic parameters of samples
从表3可知,热爆炸临界温度Tb由高到低的顺序为MgH2/AP、AlH3/AP、AP,Tb越高表明材料的热安定性越好。因此,MgH2/AP的热安定性好于AlH3/AP。过渡态理论认为,ΔH≠活化焓为正值则表明正向的活化反应是吸热的,ΔG≠活化自由能为正值则表明反应是非自发的。表3结果中,ΔH≠、ΔG≠均大于零,说明热分解过程是吸热反应且不自发进行,分解需要外界热能的提供。ΔS≠表示活化过渡态与反应物之间的混乱度之差,ΔS≠<0表明活化过渡态的混乱度比反应物低,其反应点位的活性也更低。在表3结果中,ΔS≠均为负值,表明研究的体系中各过渡态混乱度较高,反应活性较强。
2.2 热烤爆法分析
对AlH3/AP、MgH2/AP和AP分别进行热烤爆测试,将获得的各试样的测试温度和延迟爆发时间进行拟合,所得结果如图3所示,并根据式(8)拟合计算出热烤爆法试样分解过程的活化能和常数C。热烤爆法特征数据见表4。

表4 热烤爆法特征数据Table 4 Characteristic data of thermal roasting method for each sample
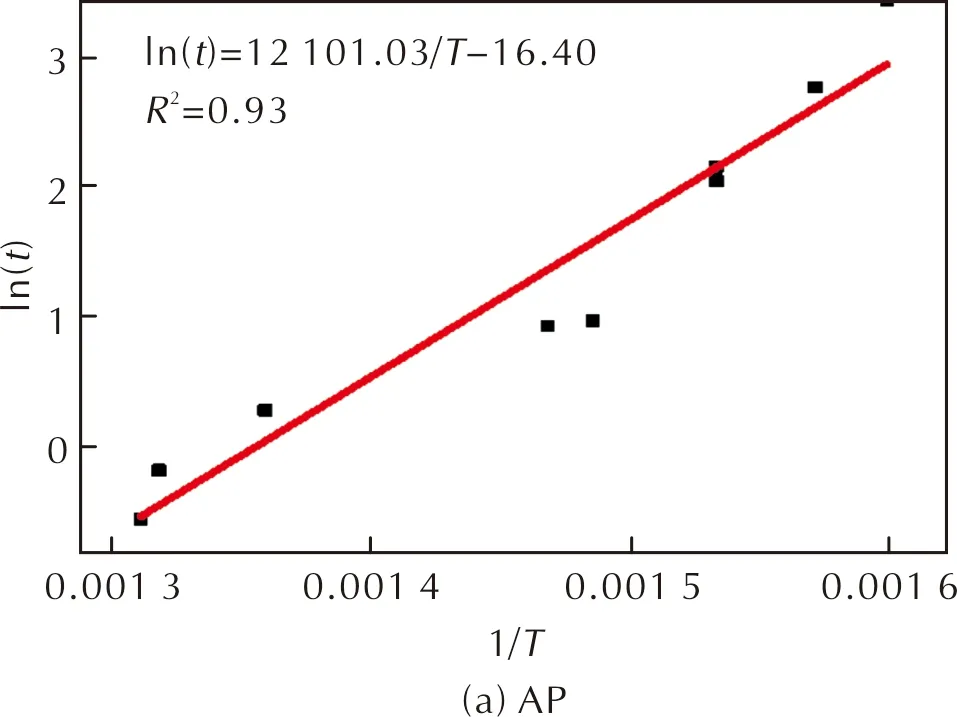

图3 AP、AlH3/AP和MgH2/AP的5s爆发点曲线Fig.3 5s burst point curves of AP, AlH3/AP and MgH2/AP
ln(t)=E/(RT)+C
(8)
式中:T为测试爆发点的温度,K;E为试样热烤爆分解爆炸过程的活化能,kJ/mol;t为试样从开始加热至爆发需要的时间,s;C为常数;R为理想气体常数,8.314J/(mol·K)。
由表4可知,在AP中分别引入AlH3和MgH2组成混合体系后,其5s爆发点和表观活化能E相对于单组分AP均有不同程度的减小。AlH3/AP体系表观活化能相较AP单组分降低了近41kJ/mol,MgH2/AP体系表观活化能相较AP单组分降低了近21kJ/mol,表明这两单质轻金属氢化物对AP的热分解起到很好的促进作用;AlH3与AP的混合体系5s爆发点和MgH2与AP的混合体系均低于AP单组分662.65K,表明引入这两种物质提高了体系的热感度。
2.3 DPTA分析
对AlH3/AP、MgH2/AP和AP试样进行DPTA测试,获得了AlH3/AP、MgH2/AP和AP试样的DPTA曲线,如图4所示。在DPTA曲线中,黑色曲线代表的是经标准化后的净增气体压强p与加热时间t的变化关系,包括加热阶段与恒温阶段。蓝色曲线为黑色曲线的曲率函数,曲率函数的极大值点,即拐点,反映了净增气体压强p的压力变化过程从快速增加转向缓慢增加所需的时间。拐点越小,即表示反应体系能更早进入放气量平衡阶段,则表明该试样的安定性也就越好。
由图4可知,各试样的DPTA热分解由两个阶段组成:第一阶段为初始升温阶段,分解气体压强随温度的升高而明显增大;第二阶段为恒温阶段,随着反应时间增加,分解气体压强仍逐渐增大,但增速明显放缓,分解过程趋向一个缓慢、平稳的放气过程。
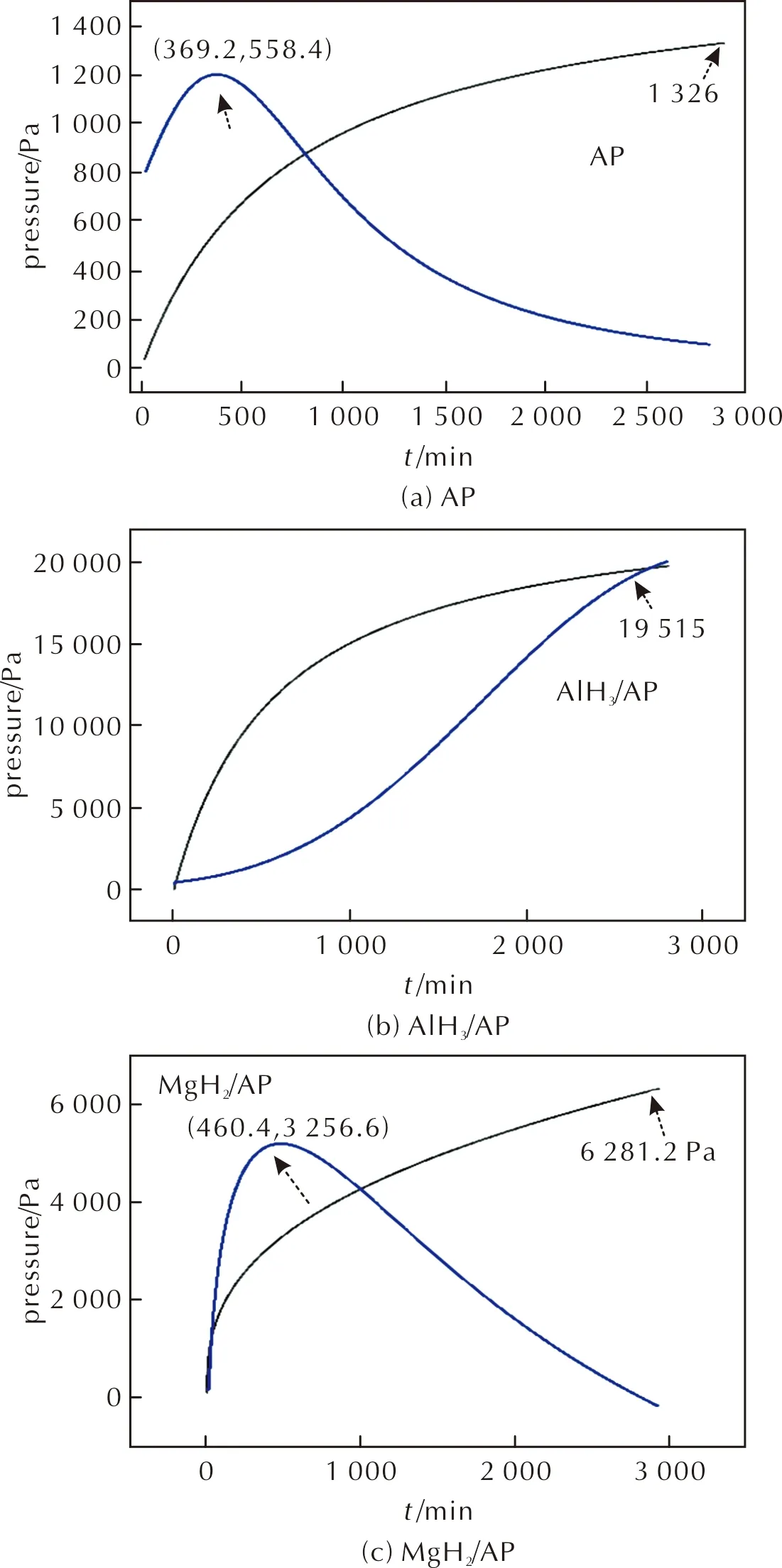
图4 AP、AlH3/AP和MgH2/AP的DPTA曲线Fig.4 DPTA curves of AP,AlH3/AP and MgH2/AP
通过放气量计算,将标准状态的净增气体压强(p)换算成气体净增体积(V),即放气量的值列于表5中。由表5可见,AP和AP/MgH2混合体系的放气量均小于2.0mL/g,按相关标准规定,表明这两种试样都有良好的安定性。AlH3/AP的DPTA曲线中,曲率函数在测试范围内没有出现极值点,说明在测试温度下、在48h内,该体系没有达到放气平衡,且其放气量很高,认为该体系的安定性差。从两组混合体系的放气量与单组分AP差值ΔV对比看:AlH3与MgH2对AP的热分解都明显的促进作用。根据放气量越小、安定性越好的原则,试样在DPTA条件下的热安定性由高到低依次为AP、MgH2/AP、AlH3/AP。
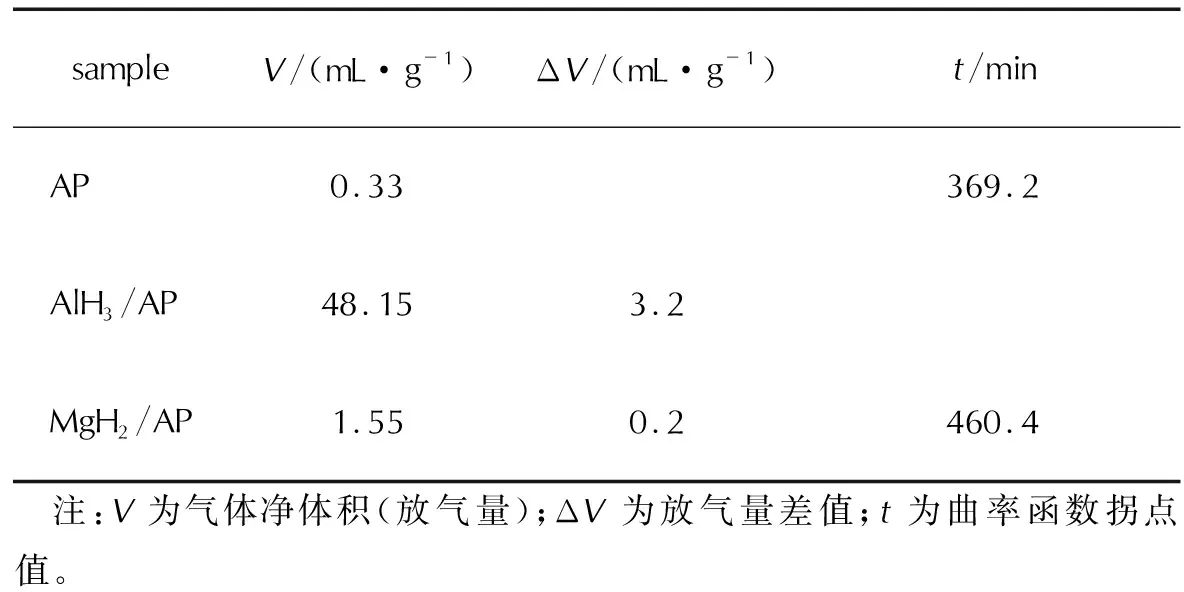
表5 100℃下48h试样的DPTA放气量Table 5 DPTA released gas volume of samples at 100℃ for 48h
3 结 论
(1)用密闭坩埚法对AP、AlH3/AP和MgH2/AP进行热分解行为研究,发现AlH3和MgH2对AP的热分解均有促进作用,均使AP的放热分解峰提前近50℃。
(2)热烤爆法测试研究求得AP、AlH3/AP和MgH2/AP混合体系的5s爆发点和表观活化能,发现AlH3和MgH2的引入引起了AP混合体系的热感度升高,热感度由高到低的顺序为:AlH3/AP、MgH2/AP、AP。
(3)通过DPTA测试法对AP、AlH3/AP和MgH2/AP混合体系进行测试研究,发现AP及MgH2/AP的放气量均小于2mL/g,而AlH3/AP的放气量超过2mL/g, 安定性由好到差的顺序为:AP、MgH2/AP、AlH3/AP。

