影像组学在肺结节诊断的研究进展⋆
随着胸部CT分辨率的提高以及人工智能的发展,肺结节的检出率明显上升。近年来,影像组学在鉴别肺结节性质、组织学分型、基因表达、治疗及预后等方面显示出良好的性能,为个体化治疗方案提供最有价值的诊断信息。本文就影像组学在肺结节诊断的研究进展进行综述。
1 影像组学概述
影像组学首次由荷兰学者Lambin P于2012年提出
,是指从计算机断层(computed tomography,CT)、正电子发射断层(positron emission tomography,PET)或磁共振成像(magnetic resonance imaging,MRI)等获得的医学图像中高通量提取和分析大量定量成像特征,然后挖掘这些特征与疾病诊断/预后之间的关联。
所有的数字成像方式都可以应用于影像组学分析,不同成像方式的工作流程本质上是相同的。工作流程主要包括医学图像获取与重建、图像分割、特征提取、数据分析等四个步骤,如图1
所示。
特质是指人们在认识、理解甚至改造事物的过程中表现出来的区别他人的个性心理特征。根据本项目的研究需要,一级指标的“特质”下设个性、品质和价值观等三个二级指标。在品质下特别设置了“职业的坚守”和“中医药文化的虔诚度”三级指标;而“价值观”下则特设了“育人观”。这些指标的设计主要是出于中医药院校的特点以及教师这一特定的职业身份,如何加强坚守自己的职业,教好书育好人也是归国外语教师跨文化能力的重要考量。
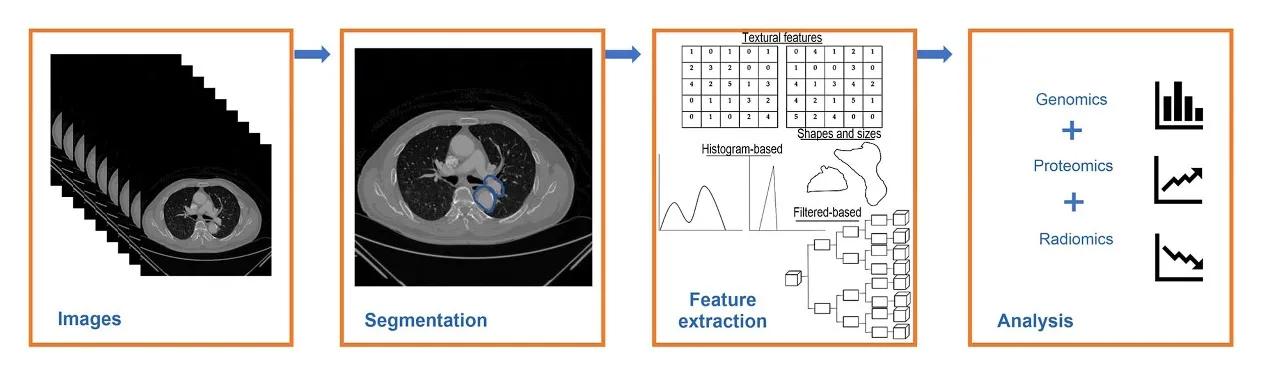
1.2.1 图像获取与重建 图像获取与重建是影像组学工作的基础,图像采集和标准化操作程序有助于生成高质量的数据集。理想情况下,研究中使用的所有图像都应该使用相同的机器和程序。但由于不同医疗设备之间的参数不同、使用不同技术得到的组学特征也可产生不同的分析结果。目前最常见的是从CT或PET图像中获取肺结节患者的图像。
随着肺癌诊断和治疗的进步以及分子检测的出现,基因突变的预测已成为临床个体化和精准治疗以改善生存期和提高生活质量的关键。肺癌的病理分型中,肺腺癌中表皮生长因子受体(epidermal growth factor receptor,EGFR)是最常见的基因突变类型,驱动基因的改变与患者的预后密切相关,准确识别致癌基因突变对肺腺癌患者至关重要。多项研究强调了影像组学在无创性鉴定肺癌基因突变方面的作用,CT影像组学可能成为选择基因突变患者进行侵袭性取样的非侵袭性替代生物标志物。Zhang等
结合常规临床特征使用影像组学分析预测EGFR突变型NSCLC对酪氨酸激酶抑制剂的反应,表明影像组学特征比CT影像特征或临床变量更能预测EGFR突变。有学者
研究构建了基于影像组学特征与临床和影像学特征相结合的列线图,使用SVM分类器获得了最佳影像组学特征模型,影像组学特征与临床和影像组学特征的联合模型在预测EGFR突变状态方面具有最佳区分能力,可为靶向治疗候选者提供有用的基于图像的生物信息,以预测EGFR突变状态。Weng等
回顾性分301名NSCLC患者的胸部CT平扫图像,研究表明基于临床特征和影像组学特征的联合模型在NSCLC患者EGFR激活突变的个体化、无创预测方面表现出良好的性能。
早期肺癌以肺腺癌为主,在临床和组织学上表现为从惰性(非侵袭性)到侵袭性病变。组织学上按浸润程度可分为原位腺癌、微浸润性腺癌和浸润性腺癌。组织病理浸润程度与患者预后密切相关,其中原位腺癌或微浸润性腺癌切除后5年生存率接近100%
。研究表明
,基于CT的影像组学能够确定表现为实性或亚实性的肺腺癌的病理分型,且AUC均在0.77~0.90之间。Wu等
采用影像组学分析预测非小细胞肺癌(non-small cell lung carcinoma,NSCLC)的组织病理学类型,从350例肺结节患者的术前CT图像提取了440个影像组学特征,发现53个组学特征与肿瘤组织学具有显著相关性,通过结合基于小波的特征分析,能较为准确的预测肿瘤组织学类型(AUC 72%)。影像组学特征结合其他变量,如临床、术中病理特征,可以提高最终病理的准确性
。此外,结节内及结节周围影像组学特征相结合比单纯结节的影像组学特征更具有良好的预测效能
。影像组学也可通过预测早期肺腺癌有无侵犯邻近淋巴血管、胸膜及气腔扩散,从而促进患者的个体化治疗
。
CT是肺结节诊断应用最广泛的影像检查技术,可观察结节CT形态学征象。随着低剂量胸部CT筛查和CT后处理技术的发展,肺结节的检出率显著上升。影像组学通过计算机从医学图像中提取定量且理想情况下可重现的信息,包括人眼难以识别或量化的复杂模式。CT是目前影像组学分析中最常见的成像方式,目前多项研究表明CT影像组学方法在鉴别肺结节性质、预测肺结节的侵袭性或病理分型、恶性结节的基因表达中显示出潜在的价值。
与空白组比较,模型组和各给药组大鼠血清中IL-1β、TNF-α水平均显著升高,差异均有统计学意义(P<0.01)。与模型组比较,各给药组大鼠血清中IL-1β、TNF-α水平均显著下降,且八角枫水提液高剂量组大鼠血清中IL-1β水平显著低于阳性组,阳性组和八角枫水提液高剂量组大鼠血清中TNF-α水平均显著低于其低、中剂量组,差异均有统计学意义(P<0.05);其余各给药组组间比较,差异均无统计学意义(P>0.05),详见表4。
2 CT影像组学在肺结节良恶性的研究
1.2.4 数据分析 影像组学的目标是利用选定的影像组学特征构临床结果的预测模型。影像组学特征数据通常分为实验数据和验证数据。实验数据用于建立预测模型;验证数据则被用来验证模型的效能,以显示其临床应用价值,独立的、外部的、经过验证的模型被认为可靠性更高。数据分析的方法有多种,常用的包括支持向量机(support vector machine,SVM)、logistic回归、随机森林等
。
肺结节的CT形态学特征仅通过肉眼识别,存在较大的主观性,且部分良恶性结节影像征象存在交叉重叠,准确诊断困难。影像组学通过提取并筛选医学图像中具有代表性的组学特征,以显示良恶性肺结节之间的差异。Xu等[
分析了373例肺结节患者的薄层CT平扫图像,根据第8版肺癌TNM分期系统,按直径(cm)分为3组,T
a (0 b(1 c(2 对875名肺结节患者进行回顾性分析,使用影像组学评分和临床变量构建逻辑回归模型和影像组学列线图,从训练组(AUC 0.836)和验证组(AUC 0.809)中获得对肺结节性质的良好区分,列线图也表现出出色的辨别和校准能力。Zhao等 基于CT影像组学对孤立性肺实性结节患者的肺隐球菌病和肺腺癌进行分类并评估其鉴别能力,构建了具有临床特征、影像学征象和影像组学评分的列线图模型,AUC值分别为0.91和0.89,有助于临床决策。Beig N等 和Wu等 报道通过结合肺结节周围及结节内的影像组学特征,也有助于区分肺结节的良恶性,具有良好的预测价值。 1.2.3 特征提取 影像组学中“特征”一词是指具有预测价值的特征集合,也称为定量成像生物标志物 。影像组学特征包含了大量的客观潜在信息,主要有两大类:语义特征和非语义特征 。语义特征可定义为影像科医生提出的定性描述的经验特征,非语义特征是用数学表达式定量描述的成像特征。影像特征提取需要计算机软件进行处理,从而得到大数据集的特征并对其进行筛选,选取相关性最高的组学特征进行建模分析 1.2.2 图像分割 图像分割是指将图像从正常组织结构中勾画感兴趣区域的过程,是影像组学研究流程的重要步骤,决定了需要进一步分析的区域。图像分割技术包括手动分割、半自动分割和全自动分割,其中手动分割是目前较为认可的标准,但自动分割比手动分割更具有可重复性和快速性 。图像分割算法包括基于阈值的分割方法、基于边缘的分割方法和基于区域的分割方法等三大类,不同的算法各有其优缺点 。 (1)实验组患者的治疗有效性明显高于对照组患者的治疗有效性,两组比较差异显著,P<0.05,有统计学意义;(2)实验组内有4例患者出现头晕问题、3例患者出现恶心问题、3例患者出现呕吐问题、3例患者出现皮肤瘙痒问题,还有1例患者出现了其他问题,共涉及9例患者。对照组内有28例患者出现头晕问题、25例患者出现恶心问题、19例患者出现呕吐问题、16例患者出现皮肤瘙痒问题,还有8例患者出现了其他问题,共涉及48例患者。实验组患者的不良问题发生率明显低于对照组患者的不良问题发生率,两组比较差异显著,P<0.05,有统计学意义,详见表2。 PET/CT是在CT的基础上引入了功能成像原理,是一种非侵入性全身性检查,能够在分子水平上可视化和量化肿瘤特征,可通过放射性浓聚程度或病灶的标准摄取值(standardized uptake value,SUV)对结节良恶性进行评估 。18F-FDG PET/CT最大标准摄取值(SUVmax)>2.5已被广泛接受为区分肺部恶行肿瘤和良性疾病的临界值 。然而,18F-FDG PET/CT的准确性并不完全可靠。多项研究表现,PET/CT影像组学可提高诊断效率,在检测肺结节,区分其良、恶性,表征其组织学、分期和基因预测方面效果显著。一项研究 评估了111名孤立性肺结节患者,测试了18个3D成像特征,包括来自 PET 和 CT 的常规、纹理和形状特征,以确定良性和恶性组之间的差异,研究结果表明 F-FDG PET/CT的形状和纹理特征可以通过显着提高预测模型的准确性来更好地区分良性和恶性肺结节。Kang等 在CT、薄层CT、PET、PET/CT四组影像组学模型中,运用PET/CT影像组学模型鉴别良恶性肺结节的结果比单纯从CT获得的形态学数据更具优势。Kirienko等 研究发现,PET/CT影像组学模型能显著的区分原发性肺病变和肺转移,且CT特征在鉴别肿瘤亚型方面有局限性,而PET/CT具有较高的鉴别能力。ZHANG等 对248例NSCLC患者进行回顾性研究,通过PET和CT图像提取组学特征构建的影像组学模型,能很好地区分EGFR突变和野生型;同时结合临床变量和组学特征,具有更高的EGFR突变预测效能。一项回顾性的多中心研究表明 ,PET/CT影像组学特征是接受立体定向体放射治疗的早期NSCLC患者局部复发的独立预测因素,可以提供与复发相关的信息,并有助于临床决策,尤其是在增加剂量方面。 第一个问题,关于大力发展有效灌溉面积。刚才我也说到了,应该说这些年,我国灌溉农业的发展还是取得了长足的进展,中央的投入和地方的投入都在逐步增加。2011年中央的农田水利投入资金达到了659亿元,地方的农田水利投入达到了600亿元,加起来一共1 200多亿元,增幅是非常大的。特别是国家明确从土地出让收益中提取10%用于农田水利建设以后,我想我们国家的灌溉农业还会迎来更快的发展。按照“十二五”规划,到“十二五”末要新增4 000万亩(266.67万hm2)的有效灌溉面积。从目前我们的投入和正在实施的项目来说,以及从各地的规划实施来说,是能够实现这个目标的。 与CT图像相比,MRI检查无放射剂量、具有更好的软组织对比性能,并且可进行功能成像,胸部MRI在临床实践中越来越受到重视,在肺结节的检测、诊断等方面具有很好的应用价值 。研究表明 ,与低剂量CT相比,MRI检测直径<6mm的实性结节以及直径<8mm的亚实性结节的灵敏度相对较低,对直径>6mm实性结节的敏感性超过95%,特异性超过99%。且MRI更容易受到心脏和呼吸运动伪影的影响,并受低质子密度、极短T 值和肺内磁场不均匀性的影响,因此对肺部病变MRI影像组学的研究报道较少。Wang等 首次建立了一个基于多参数MRI的肺部病变分类影像组学模型,研究共纳入了201例患者的MRI图像,其中143个恶性病变和58个良性病变,提取多参数MRI的影像组学特征,包括T WI、T WI和ADC图。研究结果显示,使用SVM的递归特征消除算法,T WI、T WI和ADC的联合模型表现出最高的性能,在鉴别肺部恶性肿瘤和良性病变方面有很好的表现。Yan等 基于MRI T -mapping定量技术提取影像组学特征建立诊断模型,结果表明纹理特征有助于鉴别肺部良恶性病变,对于需要长期随访的肺结节患者,T -mapping定量技术可作为一种有效的检查方法。 随着肺结节的检出不断增多,影像组学在肺结节诊断研究也越来越受到重视。相对于影像形态特征,影像组学特征是通过高通量的图像数据挖掘技术而获得的人眼无法识别的量化特征,为个体化临床决策提供最有价值的诊断信息。但是,未来的影像组学研究应着眼于克服目前的局限性 ,如图像采集缺乏标准化、影像组学方法不一致、缺乏重现性;数据冗余,易产生过拟合;大多都是单中心回顾性研究,需要外部验证数据集和前瞻性研究来评估影像组学方法的稳健性和实际临床应用价值。随着人工智能、深度学习的发展,影像组学与之结合也逐渐在肺结节的应用研究中发挥重要的作用。 [1]Lambin P,Rios-Velazquez E,Leijenaar R,et al.Radiomics:extracting more information from medical images using advanced feature analysis[J].Eur J Cancer,2012,48(4):441-446. [2]Fornacon-Wood I,Faivre-Finn C,O'Connor JPB,et al.Radiomics as a personalized medicine tool in lung cancer:Separating the hope from the hype[J].Lung Cancer,2020,146(8):197-208. [3]Guiot Julien,Vaidyanathan Akshayaa,Deprez Louis,et al.A review in radiomics:Making personalized medicine a reality via routine imaging[J].Med Res Rev,2021. [4]吴佩琪,刘再毅,何兰,等.影像组学与大数据结合的研究现状[J].中华放射学杂志,2017,51(7):554-558. [5]Avanzo M,Stancanello J,El Naqa I.Beyond imaging:The promise of radiomics[J].Phys Med,2017,38(6):122-139. [6]Lahos I,Stefanidis K,Sheard S,et al.Lung cancer screening:nodule identification and characterization[J].Transl Lung Cancer Res,2018,7(3):288-303. [7]Xu Y,Lu L,E LN,et al.Application of radiomics in predicting the malignancy of pulmonary nodules in different sizes[J].AJR Am J Roentgen ol,2019,213(6):1213-1220. [8]Liu A,Wang Z,Yang Y,et al.Preoperative diagnosis of malignant pulmonary nodules in lung cancer screening with a radiomics nomogram[J].Cancer Commun (Lond),2020,40(1):16-24. [9]Zhao J,Sun L,Sun K,et al.Development and validation of a radiomics nomogram for differentiating pulmonary cryptococcosis and lung adenocarcinoma in solitary pulmonary solid nodule[J].Front Oncol,2021,11:759840. [10]Beig N,Khorrami M,Alilou M,et al.Perinodular and intranodular radiomic features on lung CT images distinguish adenocarcinomas from granulomas[J].Radiology,2019,290(3):783-792. [11]Wu L,Gao C,Ye J,et al.The value of various peritumoral radiomic features in differentiating the invasiveness of adenocarcinoma manifesting as ground-glass nodules[J].Eur Radiol,2021,31(12):9030-9037. [12]Travis W D,Brambilla E,Noguchi M,et al.International association for the study of lung cancer/american thoracic society/european respiratory society international multidisciplinary classification of lung adenocarcinoma[J].J Thorac Oncol,2011,6(2):244-285. [13]Sun Y,Li C,Jin L,et al.Radiomics for lung adenocarcinoma manifesting as pure ground-glass nodules:invasive prediction[J].Eur Radiol,2020,30(7):3650-3659. [14]Wang X,Li Q,Cai J,et al.Predicting the invasiveness of lung adenocarcinomas appearing as ground-glass nodule on CT scan using multi-task learning and deep radiomics[J].Transl Lung Cancer Res,2020,9(4):1397-1406. [15]Wu W,Parmar C,Grossmann P,et al.Exploratory study to identify radiomics classifiers for lung cancer histology[J].Front Oncol,2016,6(3):71. [16]Wu G,Woodruff HC,Sanduleanu S,et al.Preoperative CT-based radiomics combined with intraoperative frozen section is predictive of invasive adenocarcinoma in pulmonary nodules:a multicenter study[J].Eur Radiol,2020,30(5):2680-2691. [17]Wu G,Woodruff HC,Shen J,et al.Diagnosis of invasive lung adenocarcinoma based on chest CT radiomic features of part-solid pulmonary nodules:A multicenter study[J].Radiology,2020,297(2):451-458. [18]Yang G,Nie P,Zhao L,et al.2D and 3D texture analysis to predict lymphovascular invasion in lung adenocarcinoma[J].Eur J Radiol,2020,129(8):109111. [19]Yuan M,Liu J Y,Zhang T,et al.Prognostic impact of the findings on thin-section computed tomography in stage I lung adenocarcinoma with visceral pleural invasion[J].Sci Rep,2018,8(1):4743. [20]Chen D,She Y,Wang T,et al.Radiomics-based prediction for tumour spread through air spaces in stage I lung adenocarcinoma using machine learning[J].Eur J Cardiothorac Surg,2020,58(1):51-58. [21]Zhang L,Chen B,Liu X,et al.Quantitative biomarkers for prediction of epidermal growth factor receptor mutation in non-small cell lung cancer[J].Transl Oncol,2018,11(1):94-101. [22]Zhang G,Cao Y,Zhang J,et al.Predicting EGFR mutation status in lung adenocarcinoma:development and validation of a computed tomographybased radiomics signature[J].Am J Cancer Res,2021,11(2):546-560. [23]Weng Q,Hui J,Wang H,et al.Radiomic feature-based nomogram:A novel technique to predict EGFR-Activating mutations for EGFR tyrosin kinase inhibitor therapy[J].Front Oncol,2021,11:590937. [24]Wang L,Chen Y,Tang K,et al.The value of F-FDG PET/CT mathematical prediction model in diagnosis of solitary pulmonary nodules[J].Biomed Res Int,2018,2018:9453967. [25]Palumbo B,Bianconi F,Palumbo I,et al.Value of shape and texture features from F-FDG PET/CT to discriminate between benign and malignant solitary pulmonary nodules:An experimental evaluation[J].Diagnostics (Basel),2020,10(9):696. [26]Niyonkuru A,Chen X,Bakari KH,et al.Evaluation of the diagnostic efficacy of 18 F-Fluorine-2-Deoxy-D-Glucose PET/CT for lung cancer and pulmonary tuberculosis in a Tuberculosis-endemic Country[J].Cancer Med,2020,9(3):931-942. [27]Kang F,Mu W,Gong J,et al.Integrating manual diagnosis into radiomics for reducing the false positive rate of 18F-FDG PET/CT diagnosis in patients with suspected lung cancer[J].Eur J Nucl Med Mol Imaging,2019,46(13):2770-2779. [28]Kirienko M,Cozzi L,Rossi A,et al.Ability of FDG PET and CT radiomics features to differentiate between primary and metastatic lung lesions[J].Eur J Nucl Med Mol Imaging,2018,45(10):1649-1660. [29]Zhang J,Zhao X,Zhao Y,et al.Value of pre-therapy F-FDG PET/CT radiomics in predicting EGFR mutation status in patients with non-small cell lung cancer[J].Eur J Nucl Med Mol Imaging,2020,47(5):1137-1146. [30]Dissaux G,Visvikis D,Da-Ano R,et al.Pretreatment F-FDG PET/CT radiomics predict local recurrence in patients treated with stereotactic body radiotherapy for early-Stage non-small cell lung cancer:A multicentric study[J].J Nucl Med,2020,61(6):814-820. [31]Yu N,Yang C,Ma G,et al.Feasibility of pulmonary MRI for nodule detection in comparison to computed tomography[J].BMC Med Imaging,2020,20(1):53. [32]Meier-Schroers M,Homsi R,Schild HH,et al.Lung cancer screening with MRI:characterization of nodules with different non-enhanced MRI sequences[J].Acta Radiol,2019,60(2):168-176. [33]Meier-Schroers M,Homsi R,Skowasch D,et al.Lung cancer screening with MRI:results of the first screening round[J].J Cancer Res Clin Oncol,2018,144(1):117-125. [34]Wang X,Wan Q,Chen H,et al.Classification of pulmonary lesion based on multiparametric MRI:utility of radiomics and comparison of machine learning methods[J].Eur Radiol,2020,30(8):4595-4605. [35]Yan Q,Yi Y,Shen J,et al.Preliminary study of 3T-MRI native T1-mapping radiomics in differential diagnosis of non-calcified solid pulmonary nodules/masses[J].Cancer Cell Int,2021,21(1):539. [36]石镇维,刘再毅.影像组学研究的困境和出路[J].中华放射学杂志,2022,56(1):9-11.3 PET/CT影像组学在肺结节诊断的研究
4 MRI影像组学在肺结节诊断的研究
5 总结与展望

