恩替卡韦治疗慢性乙型病毒性肝炎的效果观察
赵云太
乙肝是我国常见传染疾病之一。临床症状包括肝功能异常、身体乏力、肝区疼痛和黄疸等,该病的发生对患者身心健康造成了一定影响,因此需要针对性的治疗方法,如护肝治疗,确保肝功能正常,但是为更好的控制乙肝病毒(HBV),通常需要结合抗病毒药物[1]。现阶段主要采用抗病毒药物治疗,其具有抗乙肝病毒功效,但是长时间服用会导致患者耐药性增加,无法取得理想效果。恩替卡韦对乙肝病毒抑制效果明显,采用低剂量治疗即可发挥显著效果,且具有较低的耐药性,进而被广泛用于治疗乙肝患者[2]。基于此,本次对恩替卡韦治疗乙肝的效果及对患者HBV-DNA、肝功能和肝纤维化的影响进行简单阐述,详情报告如下。
1 资料与方法
1.1 一般资料 选取2019 年1 月~2021 年1 月本院60 例乙肝患者为研究对象,以随机数字表法分为对照组和观察组,各30 例。对照组男18 例,女12 例;年龄最小20 岁,最大69 岁,平均年龄(45.26±9.32)岁;病程1~9 年,平均病程(3.87±1.95)年;文化水平:小学6 例,初中9 例,高中8 例,大专及大专以上7 例。观察组男19 例,女11 例;年龄最小20 岁,最大67 岁,平均年龄(45.31±9.29)岁;病程1~8 年,平均病程(3.76±1.52)年;文化水平:小学5 例,初中10 例,高中7 例,大专及大专以上8 例。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。经医院医学伦理委员会批准。纳入标准:①与《慢性乙型肝炎防治指南》中慢性乙型病毒性肝炎诊断标准相符;②自愿签署研究同意书;③研究资料齐全、完整;④意识清晰;⑤具备良好的用药依从性。排除标准:①具有本次研究药物过敏史;②合并认知功能障碍或者具有精神疾病史;③因为人类免疫缺陷病毒、药物等导致的肝炎;④存在腹水及黄疸等重要器官损伤;⑤哺乳期或者妊娠期妇女;⑥合并其他传染疾病史;⑦伴有凝血功能障碍或者意识模糊;⑧短时间内采用干扰素及核苷类药物治疗者;⑨拒绝参与本次研究或者中途选择退出者。
1.2 方法
1.2.1 对照组 采用常规治疗,甘草酸二铵肠溶胶囊(正大天晴药业集团股份有限公园,国药准字H20040628,规格:50 mg×24 粒)150 mg/次,3 次/d 口服;水飞蓟宾葡甲胺片(江苏中兴药业有限公司,国药准字H32026233,规格:50 mg)200 mg/次,3 次/d 口服。接受为期6 个月的治疗。
1.2.2 观察组 采用恩替卡韦片(北京百奥药业有限责任公司,国药准字H20193077,规格:0.5 mg×7 片×4 板)治疗,0.5 mg/次,1 次/d 口服。接受为期6 个月的治疗。
1.3 观察指标及判定标准 ①治疗前后肝功能指标,包括ALB、TBiL 和ALT。②治疗效果,判定标准[3]:肝功能异常、身体乏力、肝区疼痛和黄疸等症状全部消失,肝功能指标均正常,为显效;肝功能异常、身体乏力、肝区疼痛和黄疸等症状基本缓解,肝功能指标改善明显,为有效;肝功能异常、身体乏力、肝区疼痛和黄疸等症状未发生改变或者加重,肝功能指标未发生改变,为无效。治疗总有效率=(显效+有效)/总例数×100%。③治疗前后HBV-DNA 水平。④治疗前后肝纤维化指标,包括LN、Ⅳ-C 和HA。⑤不良反应发生情况,包括恶心、头晕、腹泻和头痛。
1.4 统计学方法 采用SPSS22.0 统计学软件进行数据统计分析。计量资料以均数±标准差 ()表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组治疗前后肝功能指标比较 治疗前,两组ALB、TBiL 和ALT 水平比较差异无统计学意义(P>0.05);治疗后,观察组ALB、TBiL 和ALT 水平均优于对照组,差异具有统计学意义(P<0.05)。见表1。
表1 两组治疗前后肝功能指标比较 ()
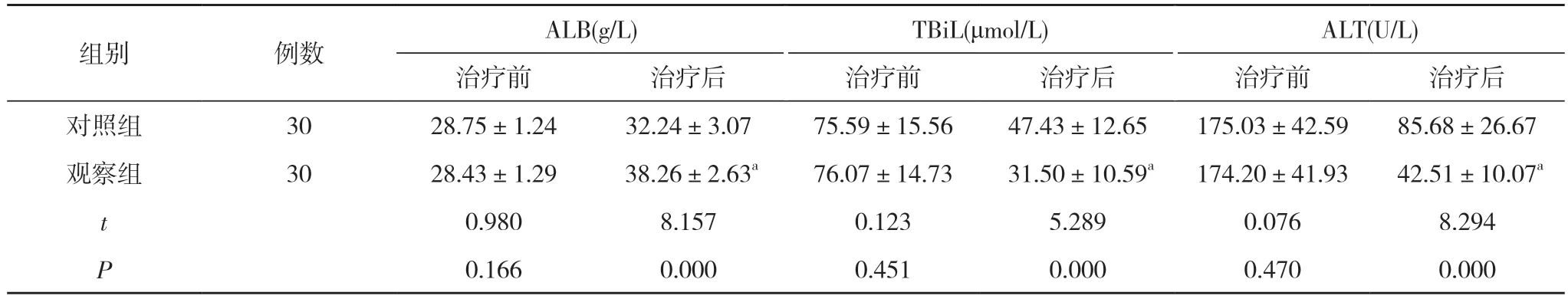
表1 两组治疗前后肝功能指标比较 ()
注:与对照组比较,aP<0.05
2.2 两组治疗效果比较 观察组治疗总有效率高于对照组,差异具有统计学意义(P<0.05)。见表2。

表2 两组治疗效果比较(n,%)
2.3 两组治疗前后HBV-DNA 水平比较 治疗前,对照组HBV-DNA 水平为(6.47±1.26)×103copies/ml,观察组为(6.41±1.23)×103copies/ml;治疗后,观察组HBV-DNA 水平为(2.59±0.23)×103copies/ml,对照组为(3.50±0.29)×103copies/ml;治疗前,两组HBV-DNA水平比较差异无统计学意义(t=0.187,P=0.426>0.05);治疗后,观察组HBV-DNA 水平低于对照组,差异具有统计学意义(t=13.467,P=0.000<0.05)。见表3。
表3 两组治疗前后HBV-DNA 水平比较(,×103copies/ml)

表3 两组治疗前后HBV-DNA 水平比较(,×103copies/ml)
注:与对照组比较,aP<0.05
2.4 两组治疗前后肝纤维化指标比较 治疗前,两组LN、Ⅳ-C 和HA 水平比较差异无统计学意义(P>0.05);治疗后,观察组LN、Ⅳ-C 和HA 水平均低于对照组,差异具有统计学意义(P<0.05)。见表4。
表4 两组治疗前后肝纤维化指标比较()
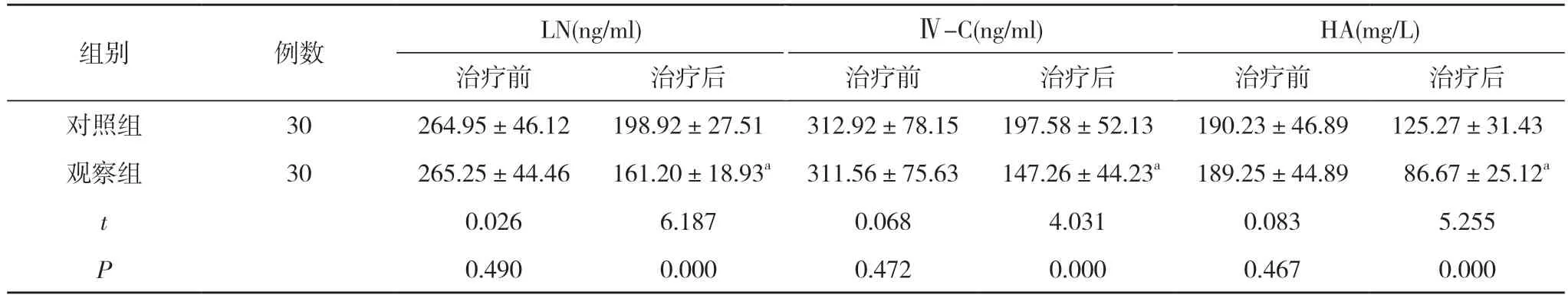
表4 两组治疗前后肝纤维化指标比较()
注:与对照组比较,aP<0.05
2.5 两组不良反应发生情况比较 对照组发生2 例恶心,1 例头晕,1 例腹泻,1 例头痛,不良反应发生率为16.67%;观察组发生1 例恶心,1 例头晕,1 例腹泻,不良反应发生率为10.00%。两组不良反应发生率比较差异无统计学意义(P>0.05)。见表5。
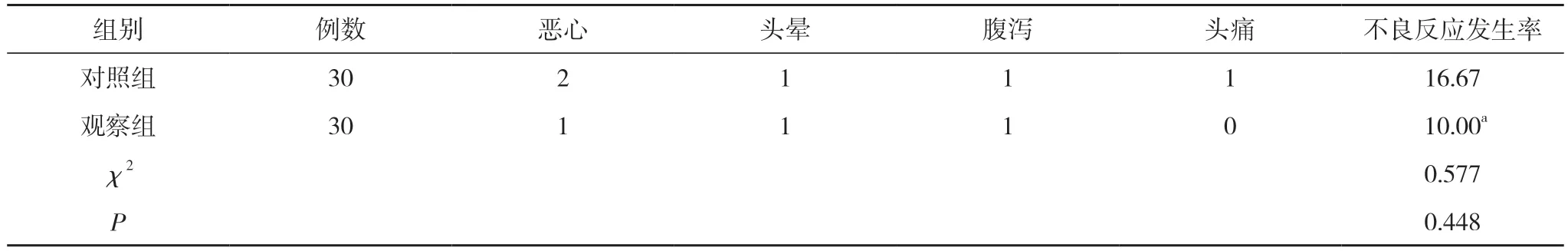
表5 两组不良反应发生情况比较(n,%)
3 讨论
乙肝是当前临床发生率较高的一种传染性疾病,该病从不同程度上影响了患者日常生活及工作等。到目前为止,有关乙肝疾病的诱发机制尚不明确。但是,大部分研究认为[3],乙肝病毒持续复制是推动疾病发展的主要因素。乙肝病毒复制具有一定的特殊性,其治愈时间较长,但是持续性的病毒复制极易加快病情发展,损伤患者肝功能,随着疾病的发展很可能形成肝癌、肝硬化等,其同样是导致乙肝患者死亡的主要因素[4]。
经研究发现[5],近年我国乙肝患者发病率呈增加趋势,每年都有因为乙肝而死亡的患者。若治疗不及时,极易导致病毒再次复制,进而对肝脏功能造成损伤,导致肝功能失代偿。处于失代偿期的乙肝患者,疾病发展速度相对较快,同时也提高了并发症发生率,严重威胁到患者生命安全[6]。因为该病病情相对严重,再加之危险性高,所以治疗方法的选择特别重要。现阶段,主要采用抑制乙肝病毒持续复制的方法和抗病毒方法进行治疗[7]。据有关研究显示[8],通过抑制乙肝病毒能够减少病毒的复制,从而对肝硬化病情发展有效控制,此外,其有助于降低肝硬化发病率。当前对于乙肝患者的治疗方法有很多,但是由于病毒复制持续时间较长,长期用药很容易导致患者出现耐药性,单一用药也可能推动疾病的发展,所以临床上大部分采用联合用药治疗[9]。
本次研究结果显示,治疗后,观察组ALB、TBiL和ALT 水平均优于对照组,差异具有统计学意义(P<0.05)。由此可见,经过恩替卡韦治疗后乙肝患者的肝功能得到明显改善,该药物能够对机体免疫功能进行调节,及早恢复免疫功能,从而获取良好的治疗效果。观察组治疗总有效率高于对照组,差异具有统计学意义(P<0.05)。治疗后,观察组HBV-DNA 水平低于对照组,差异具有统计学意义(P<0.05)。根据以上结果分析,应用恩替卡韦后能够有效清除病毒,乙肝患者自身病毒数量越来越少,在控制病情发展中具有显著效果,而且其有助于肝组织病变减少,通过免疫调节有助于机体自我调节功能改善,减少肝炎症状,确保良好的治疗效果。本研究结果还显示,治疗后,观察组LN、Ⅳ-C 和HA 水平均低于对照组,差异具有统计学意义(P<0.05)。恩替卡韦属于鸟嘌呤核苷类似物,通过对病毒的复制有效抑制,从而控制疾病的发展。据有关资料显示,与其他抗乙肝病毒药物相比,恩替卡韦具有较低的耐药性,而且有关资料显示,该药物有助于肝细胞炎症减少,使肝功能改善,有效控制疾病发展,避免其形成肝硬化或者肝纤维化[10-12]。有关研究人员经过研究发现,乙肝治疗过程中采用恩替卡韦能够对外周血结缔组织生长因子的表达水平进行抑制[13]。恩替卡韦耐药屏障较高,能够长期用于抗病毒治疗,其可以与三磷酸脱氧鸟嘌呤核苷相互竞争,从而将转录酶抑制作用充分展现出来,避免HBV-DNA 的合成,充分发挥抗病毒功效[14-16]。采用常规方法治疗乙肝,也可有效抑制乙肝病毒,控制HBV-DNA,但是相关资料显示,常规药物具有较低的病毒活性,起效相对偏慢。而且长期用药,患者耐药性也随之提高,有些则会产生病毒反弹复制,不仅影响整体治疗效果,也会导致肝脏恶变程度增加,形成肝功能衰竭,所以建议采用恩替卡韦[17-19]。本次研究结果还显示,观察组与对照组不良反应发生率比较差异无统计学意义(P>0.05)。根据该结果分析,长时间应用恩替卡韦治疗能够充分发挥抗病毒作用,避免HBV-DNA 连续复制,而且其在肝功能改善方面具有显著效果,此外,该药物具有较高的安全性,其能够尽量减少不良反应的发生,确保良好的治疗效果。
综上所述,恩替卡韦在乙肝临床治疗中具有较高的应用价值,不仅能够改善肝功能、肝纤维化,同时可促进整体治疗效果的提高,有效控制HBV-DNA,此外,该药物具有安全性高等特点,值得临床进一步采纳与推广。

