肉桂人参颗粒的含量测定、指纹图谱建立及差异标志物筛选Δ
高欢,胡北,李想,陈莹,许子华(中国人民解放军北部战区总医院药剂科,沈阳 110003)
肉桂人参颗粒为中国人民解放军北部战区总医院的院内制剂,是在古籍经典名方桂枝人参汤的基础上制得,主要由肉桂、炙甘草、人参、白术、干姜5味药材组成。方中肉桂温里散寒、通利血脉,为君药,桂皮醛、肉桂酸为其主要活性成分,具有抗氧化、抗炎、解热镇痛、抗肿瘤和保护神经等作用[1-3];炙甘草益气和中[4],合肉桂辛甘化阳以扶卫,为臣药,甘草苷、甘草酸铵为其主要成分,具有抗炎等作用[5];人参、白术益气健脾[6-7],助甘草大补元气[8];干姜辛热,温中散寒、守而不走[9],同为佐药;诸药合用,共奏和解表里之功效,治太阳病因误下而成协热下利、表里不解者[10]。该药临床上可用于治疗外寒直中、营卫凝滞、血脉流行不利之证,常用于感冒、流行性感冒及胃溃疡、急慢性胃肠炎等属中阳不足者[11-12],疗效确切且不良反应较少。目前该药相关的质量标准尚未建立。由于中成药成分复杂,单一成分难以全面地反映中成药的整体质量,故质量标准需测定多个指标成分,且需综合考虑药物所含的活性成分、君药臣药的特征成分以及含量较高成分等。本研究采用高效液相色谱(HPLC)法以肉桂人参颗粒中君药肉桂(含桂皮醛、肉桂酸)和臣药炙甘草(含甘草酸铵、甘草苷)中的主要成分为指标进行定量分析,建立其指纹图谱并进行相似度评价,同时结合化学模式识别分析筛选影响肉桂人参颗粒质量的差异标志物,旨在为该药的质量评价及后续上市提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器有LC-16型HPLC仪、AUW120D型十万分之一电子分析天平、AEL-160型万分之一电子分析天平(日本Shimadzu公司),KQ3200型超声波清洗机(杭州微米派科技有限公司)等。
1.2 主要药品与试剂
甘草苷对照品(批号111610-201908,纯度93.1%)、肉桂酸对照品(批号110786-201604,纯度98.8%)、桂皮醛对照品(批号110710-202022,纯度99.5%)均购自中国食品药品检定研究院;甘草酸铵对照品(批号wkq21021808,纯度≥98%)购自四川维克奇生物科技有限公司;甲醇、乙腈为色谱纯,其余试剂均为分析纯,水为蒸馏水。
肉桂(批号11321004)、人参(批号39021005)、干姜(批号00320015)、炙甘草(批号05721001)、白术(批号07020042)5种药材均于2021年2月11日购自河北仁心药业有限公司。上述药材经沈阳药科大学中药学院陆金财教授鉴定,分别为樟科植物肉桂Cinnamomum cassia Presl的干燥树皮、五加科植物人参Panax ginseng C.A.Meyer的根、姜科植物姜Zingiber officinale Rosc.的干燥根茎、豆科植物甘草Glycyrrhiza uralensis Fisch.的干燥根和根茎(经蜂蜜烘制而得)、菊科植物白术Atractylodes macrocephala Koidz的干燥根茎。
10批(编号S1~S10)肉桂人参颗粒[批号分别为20210228、20210309、20210312、20210425、20210426、20210427、20210428、20210429、20210430、20210501,规格为每袋装15 g(无糖型)]均为中国人民解放军北部战区总医院自制。
2 方法与结果
2.1 色谱条件
以Agilent C18(250 mm×4.6 mm,5µm)为色谱柱,以0.1%磷酸溶液(A)-乙腈(B)为流动相进行梯度洗脱(0~20 min,10%B→17%B;20~30 min,17%B→20%B;30~70 min,20%B→26%B;70~112 min,26%B→40%B;112~120 min,40%B→50%B;120~130 min,50%B→10%B;130~140 min,10%B);流速为1.0 mL/min;检测波长为265 nm;柱温为30 ℃;进样量为10 µL[6,13-14]。
2.2 甘草酸铵等4种成分的含量测定
2.2.1 混合对照品溶液的制备 分别取甘草酸铵、甘草苷、肉桂酸、桂皮醛对照品适量,精密称定,加甲醇溶解,制成上述4个成分质量浓度分别为0.852、1.224、1.132、3.036 mg/mL的单一对照品贮备液。取各单一对照品贮备液适量,加甲醇,制成上述4个成分质量浓度分别为898.85、550.80、28.30、167.00 µg/mL的混合对照品贮备液;取1 mL,置于10 mL量瓶中,加60%甲醇定容,即得上述4个成分质量浓度分别为89.89、55.08、2.83、16.70µg/mL的混合对照品溶液。
2.2.2 供试品溶液的制备 取肉桂人参颗粒约2 g,研成细粉,精密称定,置于具塞锥形瓶中,精密加入60%甲醇30 mL,称定质量,超声(功率250 W,频率25 kHz)处理30 min,放至室温,再次称定质量,用60%甲醇补足减失的质量,滤过,取续滤液,即得。
2.2.3 阴性对照溶液的制备 按肉桂人参颗粒的处方和制备工艺分别制备缺肉桂、甘草的阴性颗粒样品,再按“2.2.2”项下方法制得各阴性对照溶液。
2.2.4 系统适用性试验 分别取上述混合对照品溶液、供试品(编号S1)溶液、阴性对照溶液,按“2.1”项下色谱条件进样测定,记录色谱图。结果显示,在供试品色谱与对照品色谱相同的保留时间处有吸收峰,分离度均大于1.5,理论板数均不低于5 000,阴性对照对测定无干扰。结果见图1。
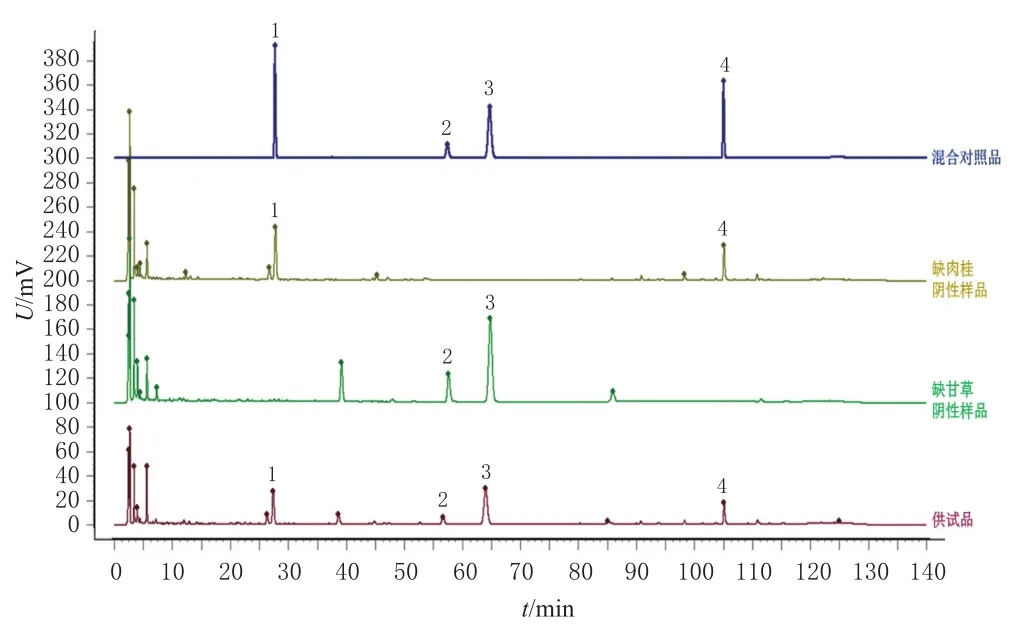
图1 系统适用性试验的HPLC图
2.2.5 线性关系考察 精密吸取“2.2.1”项下混合对照品贮备液,用甲醇逐级稀释,得系列质量浓度的工作溶液(甘草酸铵质量浓度分别为17.98、35.95、89.89、179.77、359.54 μg/mL,甘草苷质量浓度分别为 11.02、22.03、55.08、110.16、220.32 μg/mL,肉桂酸质量浓度分别为0.57、1.13、2.83、5.66、11.32 μg/mL,桂皮醛质量浓度分别为3.34、6.68、16.70、33.40、66.80 μg/mL)。取上述系列工作溶液和混合对照品贮备液,按“2.1”项下色谱条件进样测定,记录峰面积。以各待测成分的质量浓度为横坐标(X)、峰面积为纵坐标(Y)进行线性回归。结果见表1。
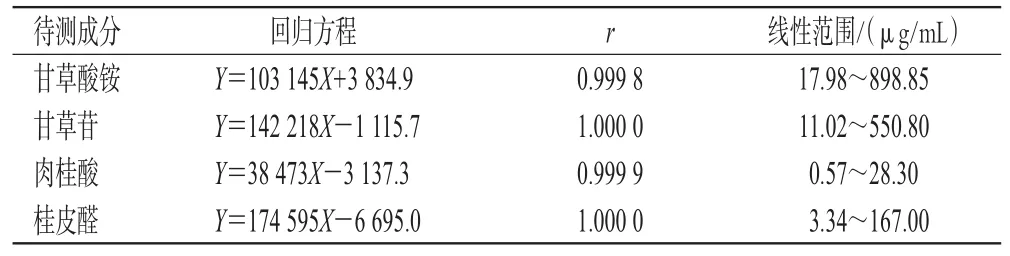
表1 甘草酸铵等4种成分的回归方程与线性范围
2.2.6 精密度试验 精密吸取“2.2.1”项下混合对照品溶液,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果显示,甘草酸铵、甘草苷、肉桂酸、桂皮醛峰面积的RSD分别为0.10%、0.09%、0.10%、0.10%(n=6),表明仪器精密度良好。
2.2.7 稳定性试验 取“2.2.2”项下供试品溶液(编号S1),分别于室温下放置 0、4、8、12、16、20、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果显示,甘草酸铵、甘草苷、肉桂酸、桂皮醛峰面积的RSD分别为0.78%、1.14%、0.62%、0.77%(n=7),表明供试品溶液于室温下放置24 h内基本稳定。
2.2.8 重复性试验 精密称取肉桂人参颗粒(编号S1)共6份,每份约1 g,精密称定,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并按外标法计算样品含量。结果显示,甘草酸铵、甘草苷、肉桂酸、桂皮醛含量的RSD分别为1.21%、1.72%、1.92%、2.31%(n=6),表明方法重复性良好。
2.2.9 加样回收率试验 取已知量的肉桂人参颗粒1 g(编号S1),分别精密加入各单一对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率。结果见表2。

表2 甘草酸铵等4种成分的加样回收率试验结果(n=6)
2.2.10 样品含量测定 取10批肉桂人参颗粒(编号S1~S10)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并按外标法计算样品含量。每样品平行测定3次。结果见表3。
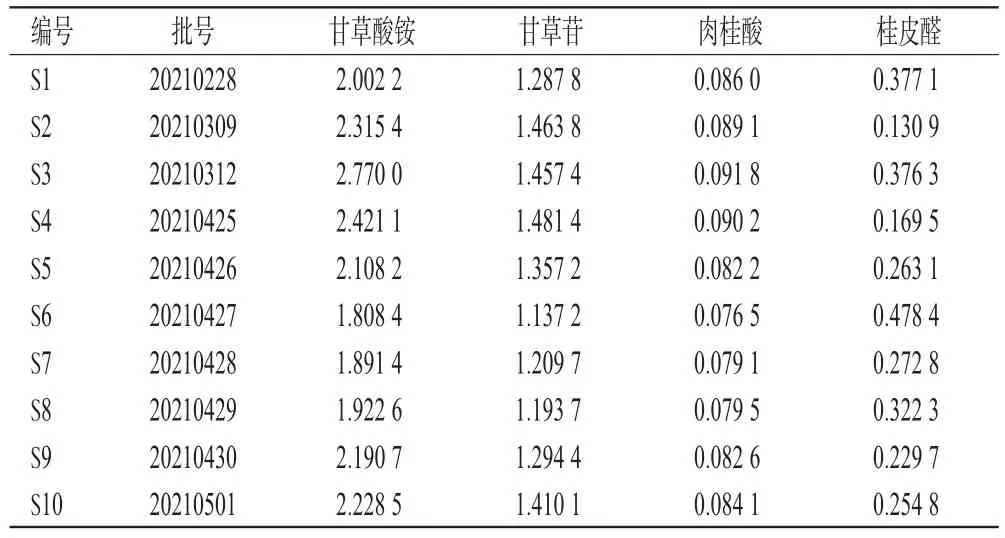
表3 甘草酸铵等4种成分的含量测定结果(n=3,mg/g)
2.3 肉桂人参颗粒HPLC指纹图谱的建立
2.3.1 精密度试验 取“2.2.2”项下供试品溶液(编号S1),按“2.1”项下色谱条件连续进样测定6次,记录色谱图。以桂皮醛为参照峰(分离度好、峰面积大、保留时间适中),计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间的RSD≤2.02%(n=6),相对峰面积的RSD≤2.04%(n=6),表明仪器精密度良好。
2.3.2 重复性试验 取“2.2.2”项下供试品溶液(编号S1),共6份,按“2.1”项下色谱条件进样测定,记录色谱图。以桂皮醛为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间的RSD≤0.36%(n=6),相对峰面积的RSD≤4.36%(n=6),表明方法重复性良好。
2.3.3 稳定性试验 取“2.2.2”项下供试品溶液(编号S1),分别于室温下放置 0、4、8、12、16、20、24 h时按“2.1”项下色谱条件进样测定,记录色谱图。以桂皮醛为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间的RSD≤0.86%(n=7),相对峰面积的RSD≤4.01%(n=7),表明供试品溶液于室温下放置24 h内稳定性良好。
2.3.4 指纹图谱的生成 取10批肉桂人参颗粒(编号S1~S10)样品,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,记录色谱图。将得到的图谱导入《中药色谱指纹图谱相似度评价系统(2012版)》,以各成分色谱响应均较强的S1样品为参照,采用中位数法,时间窗宽度为0.3 min,经多点校正后进行Mark峰匹配,生成肉桂人参颗粒的HPLC叠加指纹图谱和对照图谱(R)。结果显示,10批肉桂人参颗粒共有16个共有峰。结果见图2。
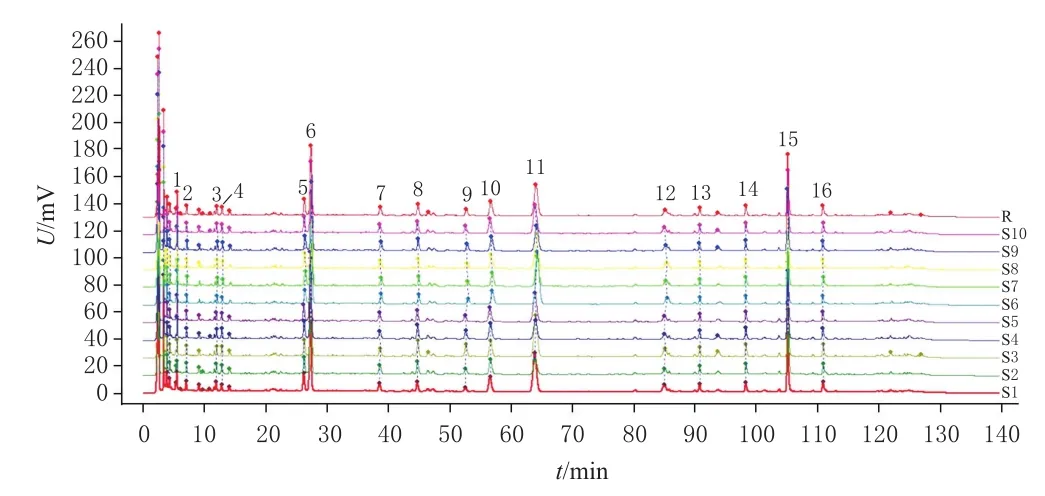
图2 10批肉桂人参颗粒的HPLC叠加指纹图谱和对照图谱
2.3.5 共有峰的指认 分别取“2.2.1”项下混合对照品溶液和“2.2.2”项下供试品溶液,按“2.1”项下色谱条件进样测定,记录色谱图(见图3)。通过与混合对照品比对,共指认了4个共有峰,分别为甘草苷(6号峰)、肉桂酸(10号峰)、桂皮醛(11号峰)、甘草酸铵(15号峰)。
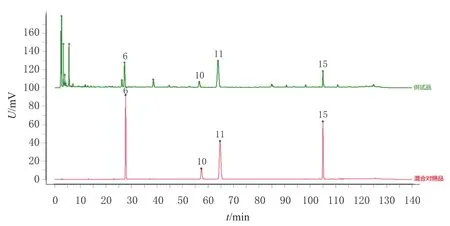
图3 混合对照品溶液与供试品溶液的HPLC图
2.3.6 相似度评价 采用《中药色谱指纹图谱相似度评价系统(2012版)》对10批肉桂人参颗粒指纹图谱的相似度进行评价。结果显示,10批样品的指纹图谱与对照图谱的相似度均大于0.95,表明不同批次样品的成分种类稳定,所建指纹图谱可以反映肉桂人参颗粒的整体特征。结果见表4。
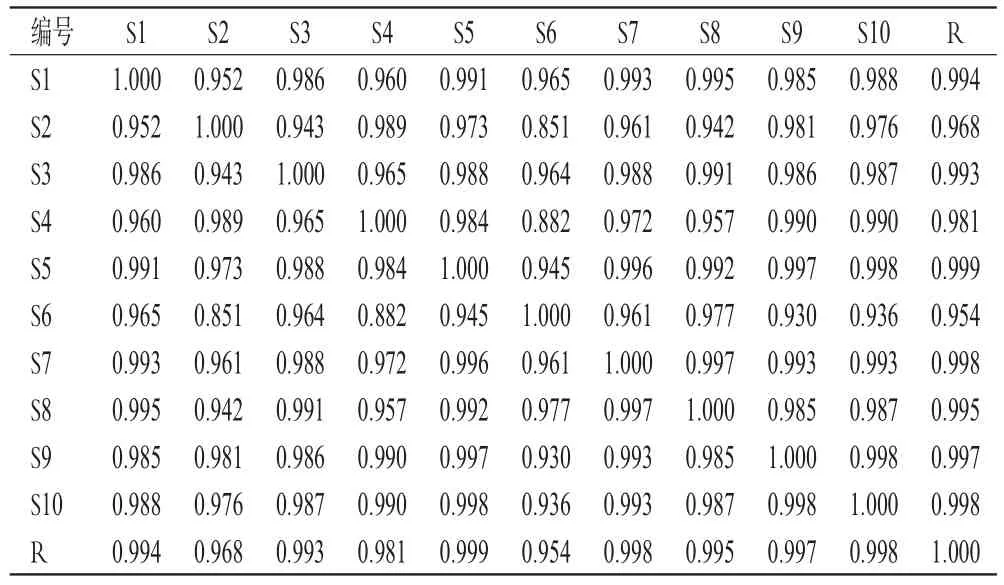
表4 10批肉桂人参颗粒的相似度评价结果
2.4 聚类分析
以16个共有峰的峰面积为变量,以平方欧氏距离为度量标准,采用SPSS 25.0软件进行聚类分析。结果显示,当类间距离为10时,10批样品可聚为3类,其中S3为一类,S1~S2、S4~S5、S10为一类,S6~S9为一类,表明不同批次样品中各成分含量存在差异。结果见图4。
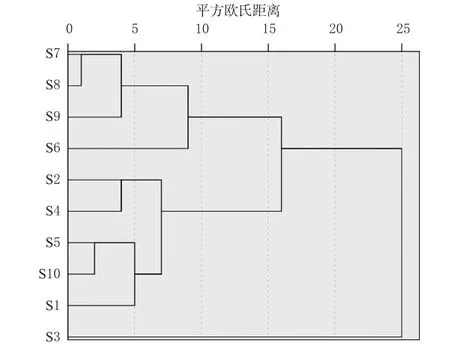
图4 10批肉桂人参颗粒的聚类分析树状图
2.5 主成分分析
以16个共有峰峰面积为原始数据进行标准化处理,以主成分的特征值及贡献率为依据,采用SPSS 25.0软件进行主成分分析。结果显示,前3个主成分的特征值大于1,累计方差贡献率为91.918%。结果见表5(表中仅展示前3个主成分的数据)。
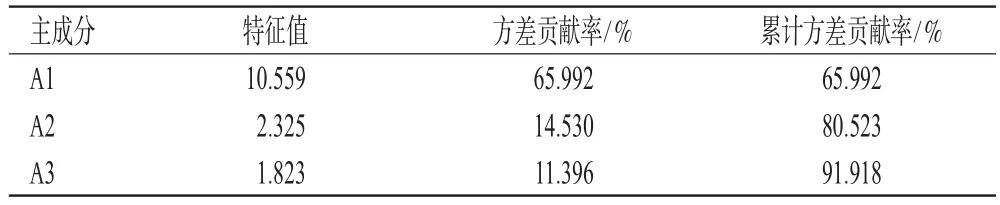
表5 主成分的特征值及方差贡献率
2.6 正交偏最小二乘法-判别分析
以16个共有峰的峰面积为变量,采用SIMCA 14.1软件进行正交偏最小二乘法-判别分析。变量重要性投影(variable importance in projection,VIP)值可用来衡量各共有峰的表达模式对样本分类判别的影响强度和解释能力,以辅助筛选质量差异标志物[15]。结果显示,10批样品数据均落在95%置信区间内,10批样品可分为3类,其中S3为一类,S1~S2、S4~S5、S10为一类,S6~S9为一类,与聚类分析结果一致。以VIP值大于1为标准筛选影响样品质量的差异标志物[15],结果显示,有4个共有峰的VIP值大于1,分别为11号峰(桂皮醛)、15号峰(甘草酸铵)、6号峰(甘草苷)、9号峰(成分未知)。结果见图6、图7。
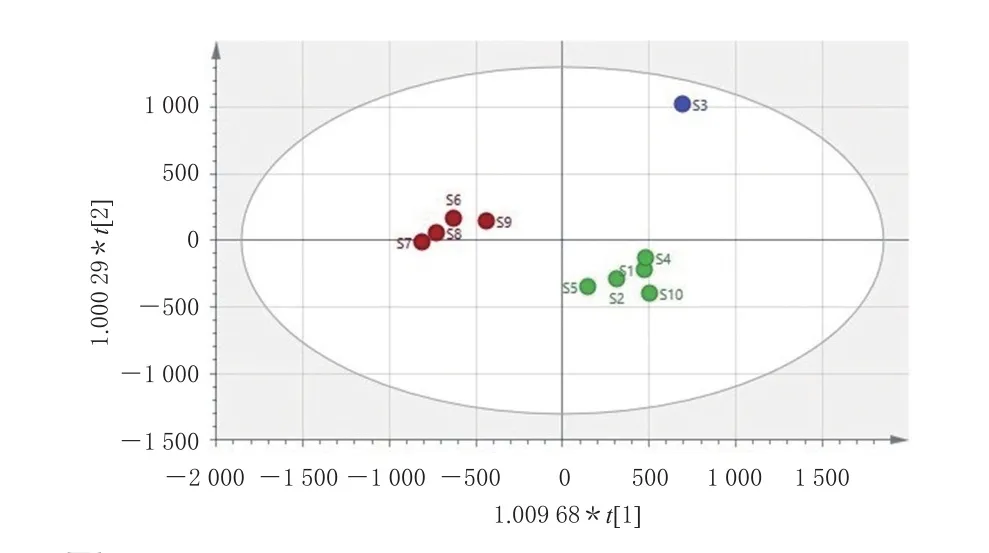
图6 正交偏最小二乘法-判别分析的得分散点图
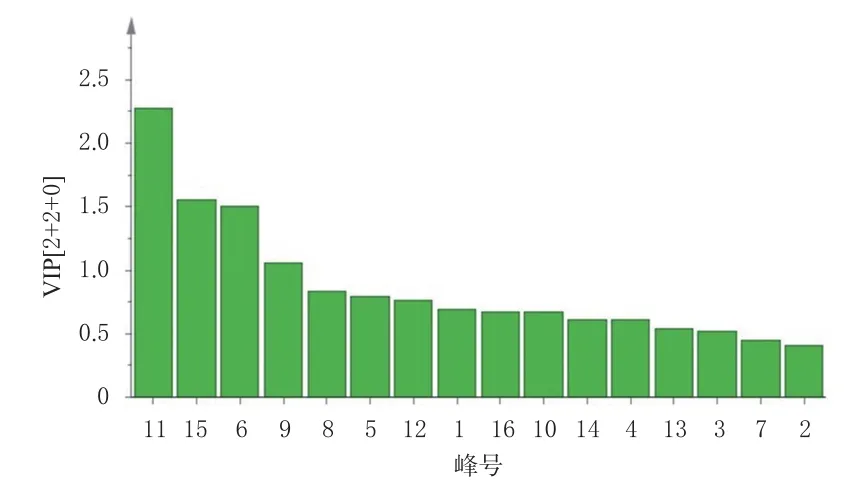
图7 共有峰的VIP值
3 讨论
3.1 检测波长的选择
参考2020年版《中国药典》(一部),甘草苷和甘草酸铵的检测波长为237 nm、桂皮醛为290 nm[6]。基于此,本研究分别考察了不同检测波长(210、254、265、280、290 nm)对各色谱峰峰面积和分离度的影响。结果显示,当检测波长为265 nm时,各色谱峰的峰面积和分离度均较好,故选择检测波长为265 nm。
3.2 提取条件的优化
本研究考察了供试品溶液的制备方法,采用不同体积分数甲醇(50%、60%、70%、80%、100%甲醇)来提取样品,结果显示,以60%甲醇为提取溶剂时,各色谱峰的峰形较好,含量较高,故选择提取溶剂为60%甲醇。本研究还考察了不同超声时间(15、30、45 min)的提取效果,结果显示,各成分含量可随超声时间增加而逐渐升高,但超声30 min与超声45 min对各成分含量的影响较小,考虑到实验效率,故选择超声提取时间为30 min。
3.3 含量测定结果分析
含量测定结果显示,10批肉桂人参颗粒中甘草酸铵、甘草苷、肉桂酸、桂皮醛的含量分别为1.808 4~2.770 0、1.137 2~1.481 4、0.076 5~0.091 8、0.130 9~0.478 4 mg/g,表明不同批次样品间各成分含量存在差异,以桂皮醛的差异较大,这可能与制备过程中的加热导致桂皮醛挥发有关。相似度评价结果显示,不同批次样品的相似度均大于0.95,其中S2、S4、S6样品的相似度相对较低,这可能与药材在贮藏或生产过程中造成的含量差异有关[16]。
3.4 指标成分的选择与化学模式识别分析
10批肉桂人参颗粒共有16个共有峰,共指认出了4个共有峰,分别为甘草苷(6号峰)、肉桂酸(10号峰)、桂皮醛(11号峰)、甘草酸铵(15号峰)。桂皮醛和甘草苷均为2020年版《中国药典》(一部)单味药项下规定的指标成分[6]。通过主成分分析发现,前3个主成分的特征值大于1,表明这3个成分能够概括样品中的绝大部分信息。聚类分析结果显示,10批样品可聚为3类,其中S3为一类,S1~S2、S4~S5、S10聚为一类,S6~S9聚为一类;正交偏最小二乘法-判别分析结果显示,11号峰(桂皮醛)、15号峰(甘草酸铵)、6号峰(甘草苷)、9号峰的VIP值大于1,表明甘草酸铵、桂皮醛、甘草苷和9号峰代表的化学成分可能是影响肉桂人参颗粒质量的差异标志物。
综上所述,本研究所建指纹图谱及含量测定方法准确度高、重复性好,可用于肉桂人参颗粒的质量评价;甘草酸铵、桂皮醛、甘草苷等成分可能是影响肉桂人参颗粒质量的差异标志物。

