地塞米松联合盐酸氨溴索在分泌性中耳炎中的应用效果研究
涂澄宇
(南昌大学第四附属医院耳鼻喉科 江西南昌 330003)
分泌性中耳炎(SOM)是耳鼻咽喉科多发疾病,会引起耳痛、耳鸣等,对日常工作、生活造成严重影响[1]。SOM 病情易反复发作,若不及时治疗,会引发鼓室粘连、听骨链坏死等病变情况,影响听力,甚至造成耳聋[2]。临床治疗SOM 多采用糖皮质激素,地塞米松是糖皮质激素受体激动剂,具有抗炎、抗过敏等作用,但药效持续时间较短,单一用药整体治疗效果欠佳[3]。盐酸氨溴索具有良好的促黏液溶解作用,有利于呼吸道内部黏稠分泌物排出,在呼吸系统相关疾病治疗中广泛应用,但在SOM 治疗中的应用效果还有待进一步研究[4]。本研究分析地塞米松联合盐酸氨溴索治疗SOM 的临床效果。现报道如下:
1 资料与方法
1.1 一般资料 纳入医院2020 年3 月至2022 年3 月收治的78 例SOM 患者,按随机数字表法分为对照组和观察组,各39 例。对照组男20 例,女19例;年龄 21~53 岁,平均年龄(37.51±6.25)岁;病程1~8 个月,平均病程(4.31±1.25)个月;气导听阈值24~43 dB,平均气导听阈值(34.11±4.15)dB。观察组男21 例,女18 例;年龄22~52 岁,平均年龄(38.53±6.27)岁;病程 1~8 个月,平均病程(4.36±1.17)个月;气导听阈值24~43 dB,平均气导听阈值(34.05±4.18)dB。对比两组一般资料无显著差异(P>0.05)。本研究经医院医学伦理委员会审批(伦理审批号:K201914)。
1.2 入选标准 (1)纳入标准:SOM 诊断标准符合《分泌性中耳炎的临床诊断与处理指南》[5];均为单侧发病;精神正常,基本认知、沟通无障碍;对本研究所用药物耐受;患者及家属均知情,且签署知情同意书。(2)排除标准:伴有心功能不全;入组前4 周有服用糖皮质激素、抗生素治疗;伴有肝、肾功能障碍;既往存在听力损伤史;患有感染性疾病;临床资料不完整,研究无法持续进行。
1.3 治疗方法 两组患者均取坐立位,医师正对患侧耳朵,采用碘伏对外耳道进行消毒,并采用10 ml注射器(带有鼓膜穿刺针头)穿刺,选取鼓膜前下象处距鼓膜边缘约2 mm 左右作为穿刺点,抽取可能存在的积液,若难以吸出,则使用9 号长针头再次抽取。对照组于患者中耳腔内注入1 ml 地塞米松磷酸钠注射液(国药准字H22020042),1 次/d。观察组于鼓膜穿刺抽液后,将0.5 ml 地塞米松和0.5 ml 盐酸氨溴索注射液(国药准字H20103255)与浓度为0.9%氯化钠溶液(1 ml)混合,之后注入鼓室内,1 次/d。以7 d 为一个治疗周期,首先治疗一个周期,若未痊愈则开始下一个周期,最多4 个周期。
1.4 观察指标 比较两组临床疗效、血管通透性、炎症反应、免疫功能及不良反应。(1)临床疗效:患者自觉症状消失,听力水平与健耳水平无异,鼓室导抗图显著改善视为痊愈;患者临床相关症状明显改善,听力水平提高>20 dB,但尚未接近健耳水平视为显效;患者临床症状较治疗前部分改善,15 dB≤听力水平提高≤20 dB 视为有效;患者临床症状较治疗前均无改善,听力水平提高<15 dB 视为无效。均于治疗4 个周期后评估,痊愈、显效、有效之和为总有效。(2)血管通透性:抽取患者治疗前后5 ml 静脉血(清晨空腹),离心分离血清,通过酶联免疫法检测纤维连接蛋白(Fn)、透明质酸(HA)、血小板活化因子(PAF)水平。(3)炎症反应:抽取患者治疗前后5 ml静脉血(清晨空腹),分离出血清,通过酶联免疫法检测白介素 -2(IL-2)、白介素 -6(IL-6)水平。(4)免疫功能:治疗前后抽取患者5 ml 静脉血(清晨空腹),至于抗凝管中送检,分离出血液中免疫细胞,采用流式细胞仪(贝克曼库尔特商贸有限公司,型号:XL-MCL)检测 CD8+、CD4+,并计算 CD4+/CD8+。(5)不良反应。
1.5 统计学方法 采用SPSS 20.0 软件分析数据,计数资料用%表示,采用χ2检验,计量资料以()表示,采用t 检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组治疗总有效率高于对照组(P<0.05)。见表 1。
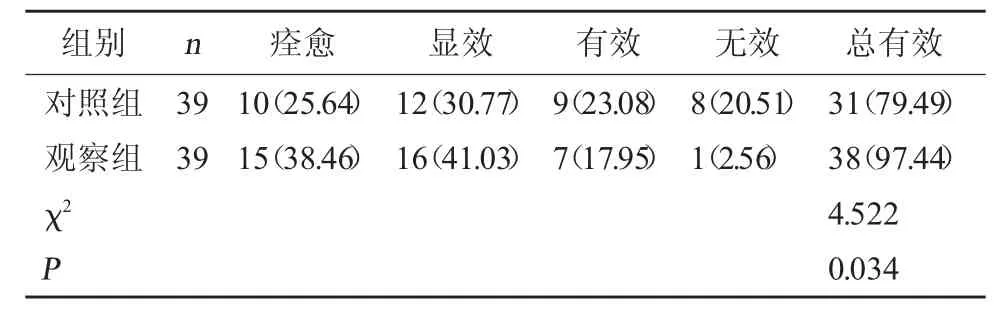
表1 两组临床疗效比较[例(%)]
2.2 两组血管通透性比较 治疗前两组血管通透性对比无显著差异(P>0.05);治疗后两组Fn 水平均高于治疗前,HA、PAF 水平均低于治疗前,且观察组Fn 水平高于对照组,HA、PAF 水平低于对照组(P<0.05)。见表 2。
表2 两组血管通透性比较()
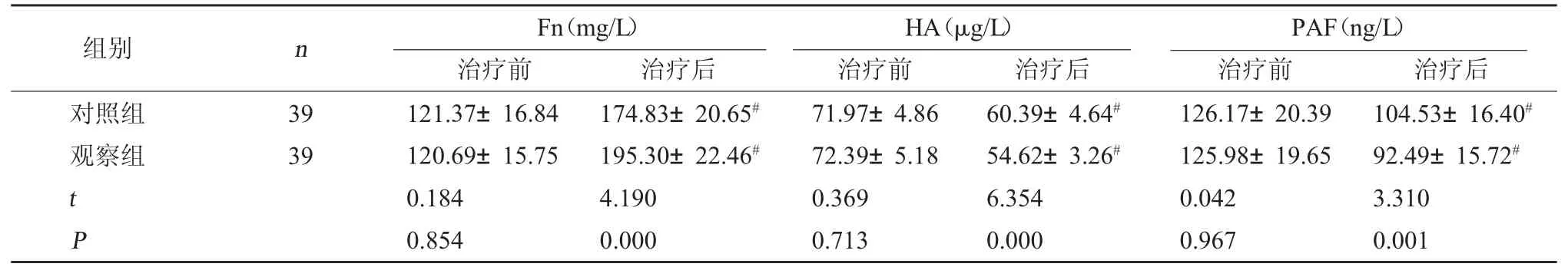
表2 两组血管通透性比较()
注:与同组治疗前比较,#P<0.05。
PAF(ng/L)治疗前 治疗后对照组观察组组别 n Fn(mg/L)治疗前 治疗后HA(μg/L)治疗前 治疗后39 39 t P 121.37±16.84 120.69±15.75 0.184 0.854 174.83±20.65#195.30±22.46#4.190 0.000 71.97±4.86 72.39±5.18 0.369 0.713 60.39±4.64#54.62±3.26#6.354 0.000 126.17±20.39 125.98±19.65 0.042 0.967 104.53±16.40#92.49±15.72#3.310 0.001
2.3 两组免疫功能比较 治疗前两组免疫功能对比无显著差异(P>0.05);治疗后两组CD8+均低于治疗前,CD4+、CD4+/CD8+均高于治疗前,且观察组CD4+、CD4+/CD8+较高于对照组,差异有统计学意义(P<0.05);治疗后两组CD8+水平比较无显著差异(P>0.05)。见表 3。
表3 两组免疫功能比较()

表3 两组免疫功能比较()
注:与同组治疗前比较,#P<0.05。
CD4+/CD8+治疗前 治疗后对照组观察组组别nCD8+(%)治疗前 治疗后CD4+(%)治疗前 治疗后39 39 t P 34.57±3.09 33.97±2.93 0.880 0.382 26.52±2.48#25.63±2.37#1.620 0.109 34.69±2.26 34.24±2.66 0.805 0.423 41.62±3.85#44.89±4.52#3.439 0.001 1.22±0.06 1.19±0.09 1.732 0.087 1.48±0.11#1.94±0.15#15.444 0.000
2.4 两组炎症反应比较 治疗前两组炎症反应对 比无显著差异(P>0.05);治疗后两组IL-2、IL-6 水平均低于治疗前,且观察组低于对照组(P<0.05)。见表4。
表4 两组炎症反应比较(pg/ml,)
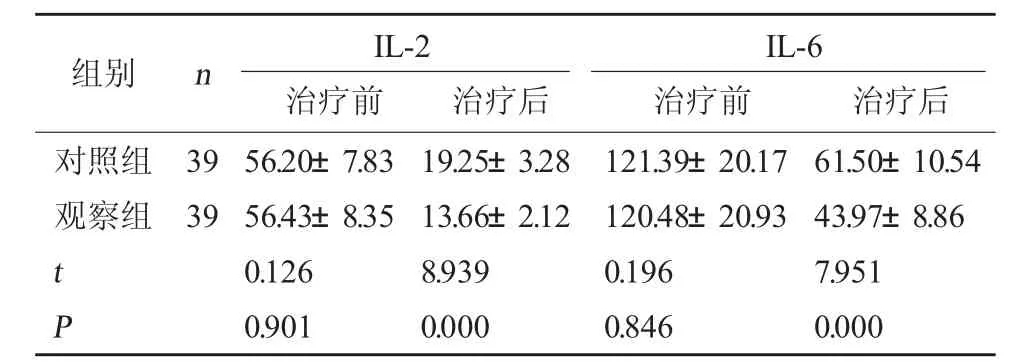
表4 两组炎症反应比较(pg/ml,)
注:与同组治疗前比较,#P<0.05。
IL-6治疗前 治疗后对照组观察组组别 n IL-2治疗前 治疗后39 39 t P 56.20±7.83 56.43±8.35 0.126 0.901 19.25±3.28 13.66±2.12 8.939 0.000 121.39±20.17 120.48±20.93 0.196 0.846 61.50±10.54 43.97±8.86 7.951 0.000
2.5 两组不良反应比较 两组不良反应比较,差异无统计学意义(P>0.05)。
3 讨论
SOM 属非化脓性炎性病变,临床尚未明确其发病机制,认为与机体免疫密切相关。患者咽鼓管、中耳腔等表面活性物质分泌大量减少,导致咽鼓管压力急剧增加,中耳腔内出现积液,最终发展为SOM,严重影响患者听力[6]。
地塞米松为临床治疗SOM 的常用药物,抗免疫、抗炎效果较好,机体易于吸收,能够使得免疫球蛋白与其受体结合力降低,进而减少T 淋巴细胞转化。但单一用药地塞米松难以稳定控制病情,停药后易复发,而大剂量用药存在较多不良反应,临床应用受限[7]。本研究观察组治疗总有效率高于对照组,Fn水平、CD4+、CD4+/CD8+均高于对照组,HA、PAF、IL-2、IL-6 水平均低于对照组,对比两组不良反应无显著差异,表明地塞米松+盐酸氨溴索治疗SOM患者疗效确切。其原因为盐酸氨溴索主要成分是氨溴索,属黏液溶解剂,给药后能够改善咽鼓管生理功能,刺激咽鼓、中耳表面活性物质分泌,利于改善中耳通气效果[8]。同时,盐酸氨溴索能够溶解中耳分泌物,使其黏性降低,最终排出鼓室内积液,改善听力。SOM 患者血管通透性增加,其清除功能会相应降低,不利于中耳分泌物排出,影响听力改善效果[9~10]。Fn 在组织液、血浆中广泛分布,若其水平降低,会使得清除外界刺激物质能力降低,促使血管通透性增加;HA 为酸性黏多糖,在血管壁通透性、免疫应答方面具有重要作用;PAF 增加血管壁通透性,促使中耳黏液纤毛清除功能减弱[11~12]。IL-2、IL-6 为重要细胞因子,参与机体免疫应答、炎症反应,故该类指标在SOM 诊断评估中敏感性较高,可有效反映患者病情变化[13]。盐酸氨溴索能够加快纤毛摆动,提高其对分泌物清洁能力,并可降低炎症介质释放,有效抑制机体炎症反应,进而减轻血管内皮损伤,达到改善血管内皮通透性的目的[14]。CD4+、CD8+共同完成T细胞免疫调节,CD4+对细胞、体液免疫具有辅助作用,而CD8+对细胞则具有杀伤作用,CD4+、CD8+的相对稳定在维持机体正常免疫功能中意义重大。而地塞米松、盐酸氨溴索均具有免疫调节作用,联合应用能够协同增效,更好的改善机体免疫功能,有利于病情的转归[15]。从安全性角度分析,两组不良反应比较,差异无统计学意义,提示联合用药安全性高。
综上所述,在SOM 患者中采用地塞米松与盐酸氨溴索联合治疗效果更佳,能够有效降低血管通透性,减轻炎症反应,改善免疫功能,安全可靠。

