新型扩皮送鞘法在同步放化疗肿瘤病人PICC置管中的应用
张明洁,张珍珍,焦姗姗,范丹丹
经外周静脉置入中心静脉导管(peripherally inserted central catheters,PICC)为需要长期静脉输液或化疗用药的病人提供了必要的血管通路。美国血管通道学会推荐的PICC操作标准为:在血管超声(US)引导下应用改良赛丁格技术(MST)于上臂行PICC置管术[1-2]。2017年起我科引进了该项技术,此后的临床实际工作及操作中发现存在一些弊端,因我科多是行同步放化疗的肿瘤病人,自身血管条件较差[3],MST在扩皮过程易损伤皮下淋巴管,相较传统盲穿法,术后穿刺点的渗血量以及带管期间穿刺点的渗液量均较明显。本研究针对扩皮送鞘法进一步探索,利用新型小切口联合盲穿针外鞘、扩张器组装钝性分离法应用于PICC置管,旨在优化置管过程,减少PICC置管术中、术后并发症。现作报道。
1 资料与方法
1.1 一般资料 选取2019-2020年在我科行PICC置管的同步放化疗肿瘤病人120例。纳入标准:(1)首次行PICC置管的同步放化疗肿瘤病人,出血、凝血功能正常且符合置管要求;(2)能正常交流并可以配合的病人;(3)签署本研究及PICC置管知情同意书。排除标准:(1)血小板减少症及出血、凝血功能异常者;(2)昏迷,无法取得配合的病人;(3)存在以下PICC置管禁忌证的病人:既往有血栓病史,上腔静脉压迫综合征,乳腺癌患侧肢术中改变贵要静脉、头静脉走向,淋巴结压迫的患肢,穿刺部位破溃或感染。按照随机数字表法将病人分为 A、B、C 3组,各40例,3组病人性别、年龄、穿刺静脉差异均无统计学意义(P>0.05)(见表1),具有可比性。
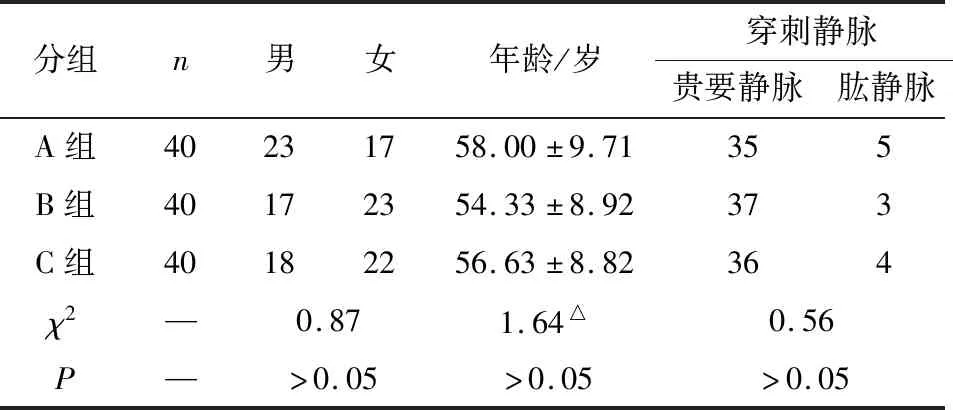
表1 3组病人一般资料比较(n)
1.2 方法
1.2.1 材料及置管方法 3组病人均采用巴德或舒贝康4Fr三向瓣膜硅胶PICC及其套件,便携式B超机、MST组件。由我科熟练掌握置管基本流程且具有PICC置管资质的3名护士,在US引导下找到靶血管,然后辅助穿刺针进入,随后置入导丝,导丝置入成功后使用2%利多卡因 0.1~0.3 mL局麻。A组采用常规纵向扩皮法,将扩皮刀的刀刃向上与皮肤垂直,刀尖纵向刺入皮肤2~3 mm进行扩皮,到达真皮后将微插管鞘沿导丝经皮下推进血管。B组采用钝性分离法,在微插管鞘中分离扩张器与导管鞘,将扩张器沿导丝旋转扩张穿刺点后送入血管,分离成功后取出扩张器再套上导管鞘,沿导丝边旋转边推送边将该组件再次推进血管行钝性分离。C组采用新型小切口联合盲穿针外鞘、扩张器组装钝性分离法,在微插管鞘中分离扩张器与导管鞘,组装传统盲穿针外鞘与扩张器,用扩皮刀纵行切开1 mm的小切口,将组装好的套件穿过导丝,继而全部推进血管行钝性分离。3组均在扩张器与外鞘成功送入血管后同时退出导丝及扩张器,保留外鞘在血管内,再经外鞘将导管缓慢送入上腔静脉,最后退出外鞘。置管完成后将一块5 cm×5 cm大小的藻酸盐敷料经过对折2次(4层)后,覆盖在穿刺点上,局部按压15 s,使用无菌透明贴膜固定导管,然后弹力绷带加压包扎2 h,同时进行健康宣教,术后避免剧烈活动、拎重物等。
1.2.2 评价方法 由经过统一培训的非置管操作的研究人员进行评价。(1)将导管鞘组件一次性送入血管判定为:一次性送鞘成功。将需扩张器或手术刀进行二次扩皮判定为:一次性送鞘失败。一次性送鞘成功率(%)=一次性送鞘的成功例数/穿刺总例数×100%。(2)置管术中疼痛程度评估:采用NRS 数字评分法,0分代表无痛,10分代表最剧烈疼痛,1~3分、4~6分、7~10分依次为轻度、中度、重度疼痛。置管操作完毕后以病人的主诉为参照,由病人个人选择一个最能代表自身疼痛程度的数字。(3)穿刺点渗血情况:穿刺点的渗血量判断参照国内既往研究使用标准[4],观察记录置管后48 h藻酸盐敷料的渗血层数以及7 d内换药次数。48 h为置管病人常规换药时间,若48 h内肉眼发现穿刺点藻酸盐敷料有4层渗血时,则需及时更换敷料,并且将4层藻酸盐敷料累计入渗血层数中,将本次换药累计入7 d内所需换药次数中。若未发现穿刺点藻酸盐敷料4层有渗血,则按48 h常规换药。7 d内换药次数为4层藻酸盐敷料可见渗血时换药次数加48 h常规换药1次。
1.3 统计学方法 采用方差分析、q检验、χ2检验和行乘列(R×C)的χ2检验。
2 结果
2.1 3组病人一次性送鞘成功率比较 A组及C组病人均一次性扩皮送鞘成功,成功率为100%;B组病人3例钝性扩皮失败后改扩皮刀再次扩皮送鞘成功,成功率为92.5%;3组病人的一次性送鞘成功率差异无统计学意义(χ2=6.15,P>0.05)。
2.2 3组置管疼痛评分的比较 3组置管疼痛评分比较,差异有统计学意义(P<0.01),A组评分高于B组和C组,C组高于B组(P<0.05~P<0.01)(见表2)。
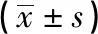
表2 3组置管疼痛评分比较
2.3 3组病人术后渗血情况比较 C组病人48 h穿刺点渗血藻酸盐敷料层数及置管后7 d内换药次数均低于A组和B组(P<0.05)(见表3)。
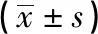
表3 3组病人穿刺点渗血情况比较
3 讨论
3.1 传统扩皮技术存在缺陷 一般而言,传统的PICC置管术通常采用纵切法扩皮,术者使用扩皮刀纵向扩皮2~3 mm,扩皮范围较大,需切开皮肤的表皮层、真皮层甚至皮下组织层,较多的弹力纤维、组织及毛细血管遭到破坏,造成伤口不易愈合、穿刺点渗血量较多[5]。若病人皮肤组织疏松,此类现象更甚,从而容易引发病人依从性差,难以配合操作。
3.2 钝性分离法扩皮可明显减少置管后穿刺点渗血量 钝性分离法相比于传统的解剖刀破皮法,其采用直接扩张穿刺点而不需使用扩皮刀,沿着皮纹方向将已组装好的导管鞘组件直接推进表皮、真皮及皮下组织,不会对周围血管、神经等组织造成切割性损伤,且无关乎操作者手法及经验[6]。本研究结果显示,钝性分离法(B组)与小切口联合钝性分离法(C组)相比较于传统扩皮送鞘方法(A组),均可减少PICC置管后穿刺点渗血量,使得穿刺点局部皮肤损伤小。
3.3 盲穿针外鞘钝性分离法有利于提高送鞘成功率 在临床实践中大部分病人穿刺点的皮肤存在角质层厚,而操作者发现,用扩张器与导管鞘组件直接钝性分离过程中,进针和送鞘阻力较大,需大气力将外鞘、扩张器在左右旋转配合下加以推进,外鞘变形在所难免,增加了置管的操作风险与难度系数。若操作者首次钝性分离不能完成,用扩皮刀纵向切开1 mm 后,则再行之,这样带来的结果就是皮下组织、血管损伤较大,扩张器退出后,穿刺位置存在不同程度的出血。阮玉华等[7]研究发现,利用小切口联合扩张器钝性分离技术一次置管成功率较高,出血量少,减少置管后维护次数。但是该技术存在的弊端即是对皮下组织产生二次创伤,是因为在使用扩张器与导管鞘组件进行钝性分离时,要先使用扩张器扩张穿刺点,继而两者组装后再推进。在皮肤钝性分离时,通常使用两种组装器,第一种是盲穿针外鞘与扩张器组装,第二种是可撕裂鞘与扩张器组装。盲穿针外鞘的特点是:长度约为3.2 cm,管壁较薄且柔软,与扩张器的贴合度高,鞘前端与鞘身过渡段约2 mm,在推进过程中可减小皮肤阻力。而可撕裂鞘长度达5.1 cm,进入血管部分相对较长,势必对血管的损伤范围较大,相较于盲穿针管壁,质地也略坚硬,鞘前端与鞘身过渡段仅为0.5 mm,进穿刺点时推进阻力瞬间增大造成送入困难或外鞘变形。本研究显示,新型小切口联合盲穿针外鞘、扩张器组装钝性分离法(C组),不仅能提高PICC置管术中一次性送鞘成功率,而且可降低术中疼痛及术后渗血等相关并发症的发生率。
3.4 不同扩皮方法一次性送鞘成功率比较分析 在本研究中,A组和C组的病人一次性扩皮送鞘成功率均为100%,B组有3例病人在第一次置管操作时出现送鞘失败。分析失败原因如下:3例病人均为男性,皮肤表皮层过于厚实,扩张器均能顺利推进血管,拔出扩张器套上导管鞘后,再次去推进血管,但不能成功扩张穿刺点。B组3例病人改用新型小切口联合钝性分离法后,再次送鞘均为一次性送鞘成功。本研究中传统穿刺针在巴德4Fr三向瓣膜硅胶PICC及其套件包内均有配备,临床上采取此种钝性分离法不额外增加成本耗材支出[8]。
综上,该项新技术值得推广,为后续临床工作中肿瘤病人PICC置管提供了新的实践思路。但受样本量大小、研究时间等限制,此结论仍需要通过更大的样本量、更长久的临床观察验证,以进一步改进、优化PICC置管操作流程。

