CMC浮选分离萤石与方解石作用机理研究
马 强 李育彪 李万青 杨 旭
(武汉理工大学资源与环境工程学院,湖北 武汉 430070)
萤石矿是战略性矿产资源,是氟工业的基础原料[1-2],广泛应用于新能源、新材料、国防军工、制冷、冶金、化工等领域[3-4]。我国萤石资源较丰富,常与多金属硫化矿、碳酸盐矿物及重晶石等共(伴)生,一般品位较低、伴生矿多、嵌布粒度细,给萤石的开发利用造成了极大困难[3,5-8]。
萤石常与方解石等含钙脉石矿物伴生,其高效浮选分离一直是世界性难题[2,9-12]。Mulliken布居分析表明[13],萤石中F—F键及方解石中O—Ca键均具有较大离子性,易断裂形成离子键。方解石表面存在价键不饱和的Ca2+,而萤石表面F—F键断裂时,由于F-水化自由能小于Ca2+,F-优先脱离矿物表面进入溶液,在萤石表面产生不饱和价键Ca2+,由此造成方解石与萤石相近的表面物化性质[14],难以有效浮选分离。工业生产中,浮选萤石时常选择水玻璃为方解石抑制剂[6-7,15-18],尽管价格低廉,但需在高碱环境下作业,且药剂用量很大,给后续水处理及成本控制带来了困难。除了传统的无机抑制剂,高分子抑制剂如古尔胶[18]、腐殖酸钠[19]、聚丙烯酸钠[14]等也常被用作抑制剂,但效果较差。因此,寻找一种对环境友好、具有高选择性、能实现萤石与方解石高效分离的抑制剂具有重要的科学及现实意义。
羧甲基纤维素(CMC)属阴离子型醚类,可溶于水,水溶液呈中性或弱碱性,具有一定黏度[20-21]。研究表明,CMC可作为硫化矿、硅酸盐矿物抑制剂[22-23],但其在萤石与方解石浮选分离中应用较少,且抑制机理尚不明确。本文通过纯矿物、人工混合矿浮选试验研究了CMC对萤石、方解石浮选的影响,并采用接触角测试、Zeta电位检测、吸附量及微量热分析揭示了CMC对方解石选择性抑制的作用机理,构建了吸附模型,为弱碱性条件下实现萤石与方解石的高效浮选分离提供了理论基础。
1 试验原料及方法
1.1 试验原料
萤石、方解石均取自湖南。首先将试验样品敲碎,手工挑选去掉杂质,然后用陶瓷罐棒磨,湿筛取粒级0.074~0.038 mm样品烘干、装袋。取样品化验可知,萤石CaF2含量94.62%,方解石CaCO3含量92.52%。XRD分析结果(图1)显示,2种纯矿物XRD图中未出现其他杂质衍射峰,其纯度满足试验要求。
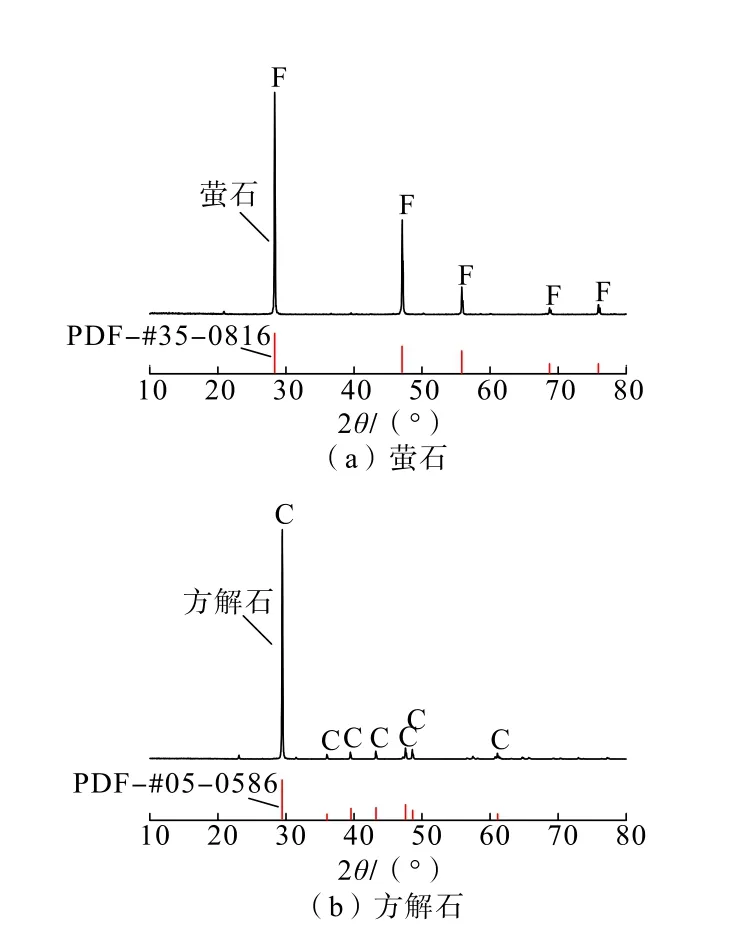
图1 萤石及方解石样品XRD图谱Fig.1 XRD patterns of fluorite and calcite sample
试验所用pH调整剂为NaOH,分析纯;抑制剂为CMC(黏 度:800~1 200 mPa·s,分 子 式 为:[C6H7O2(OH)2OCH2COONa]n,取代度(DS):1),分析纯;捕收剂为油酸钠,分析纯;试验用水为超纯水。
1.2 试验方法
1.2.1 浮选试验
采用容积为40 mL的XFG型挂槽式浮选机,其中,纯矿物浮选试验每次称取2.0 g萤石或方解石样品;人工混合矿浮选试验按照萤石与方解石质量比1∶1称取4.0 g,并加入适量超纯水搅拌。浮选流程如图2所示,其中,固定捕收剂油酸钠用量为95 mg/L,浮选采用人工刮泡。纯矿物浮选中将所得泡沫产品与槽内产品分别烘干、称量并计算回收率;人工混合矿浮选中将所得泡沫产品与槽内产品分别烘干、称量、化验,并计算回收率。
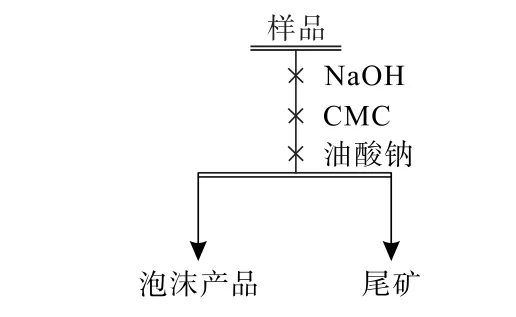
图2 浮选试验流程Fig.2 Flotation test flowsheet
1.2.2 接触角测试
将萤石、方解石平整块状样品分别置于浓度为20 mg/L的CMC溶液中,并调节溶液pH=8,浸泡30 min,然后取出洗涤3次、烘干,采用KRUSS DSA 1005型接触角测定仪测试2种矿物表面与CMC作用前后接触角,每个样品测量3次,取平均值。
1.2.3 Zeta电位测试
用玛瑙研钵将萤石、方解石单矿物研磨至粒径小于5 μm,使用超纯水配成0.01%质量浓度的矿浆,按照浮选流程加入浮选药剂,在磁力搅拌器上搅拌10 min,取上述样品加入样品池,采用JS94H型Zeta电位测定仪测量CMC作用前后萤石、方解石表面的动电位,每个样品测量3次,取平均值。
1.2.4 吸附量测试
分别称取2.0 g萤石、方解石置于40 mL浮选槽中,加入适量超纯水,控制CMC用量分别为0、5、10、15、20、25 mg/L,按照浮选流程加入药剂,搅拌20 min,然后以6 000 r/min转速离心3 min,取上清液待测,采用TU-1810型紫外可见光分光光度计分析仪对萤石、方解石表面吸附油酸钠后的上清液进行油酸钠含量测定,计算油酸钠吸附量。
1.2.5 微量热测试
采用RD496-2000型微量热仪进行微量热测试。通过微量热法测量萤石、方解石吸附油酸钠/CMC热动力学变化,将萤石、方解石样品分别置于pH=8的NaOH溶液中,取悬浮液2 mL置于玻璃外管,往内管中加入1 mg/L油酸钠/0.6 mL CMC溶液。将内管套入外管,再将套管置于不锈钢套筒,放入测量池待测。参考池玻璃外管不加萤石、方解石样品,只在内管分别加入等量相同溶液。设定温度参数298.15 K,待基线平稳,捅破玻璃内管,测量微量热动力学参数,每组试验重复3次,取平均值。依据下式[10]进行数据处理。式中:k为反应速率常数,n为反应级数,Hi为t时刻曲线积分面积,H∞为曲线总积分面积。
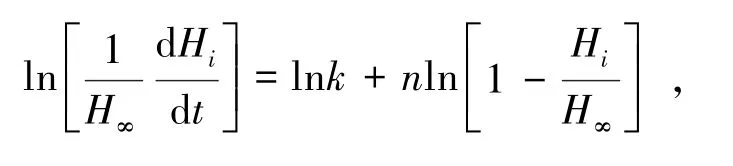
2 试验结果与讨论
2.1 纯矿物浮选试验
2.1.1 CMC用量的影响
在pH=7、油酸钠用量为95 mg/L的条件下,考察CMC用量对萤石、方解石回收率的影响,结果见图3。
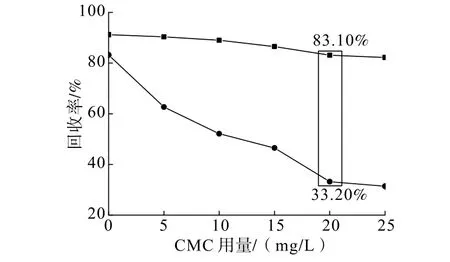
图3 CMC用量对纯矿物浮选回收率的影响Fig.3 Effect of CMC dosage on recovery rate of the pure mineral in flotation
由图3可知,CMC用量对萤石回收率影响较小,但强烈抑制方解石。CMC用量为20 mg/L时,萤石浮选回收率为83.10%,而方解石浮选回收率仅为33.20%,表明在此浓度下,CMC对方解石抑制作用更强,且对2种矿物的抑制差异达到了最大值。
2.1.2 pH值的影响
在油酸钠用量为95 mg/L的条件下,考察添加(用量为20 mg/L)和不添加CMC 2种条件下pH值对萤石、方解石回收率的影响,结果见图4。
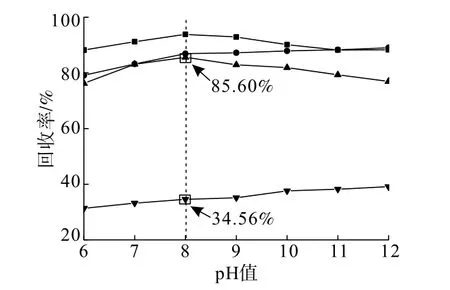
图4 pH值对纯矿物浮选回收率的影响Fig.4 Effect of pH value on recovery rate of the pure mineral in flotation
由图4可知,未添加CMC时,萤石回收率随pH值的增加先升高后降低,pH=8时达到最大值93.80%;方解石回收率随pH值的增加一直缓慢升高。添加CMC后,萤石最大回收率为85.60%,而此时方解石回收率仅34.56%。由此可知,控制CMC用量为20 mg/L、pH=8,有望实现两者浮选分离。
2.2 人工混合矿浮选分离试验
控制CMC用量为20 mg/L、矿浆pH=8,进行人工混合矿浮选试验,结果如表1所示。
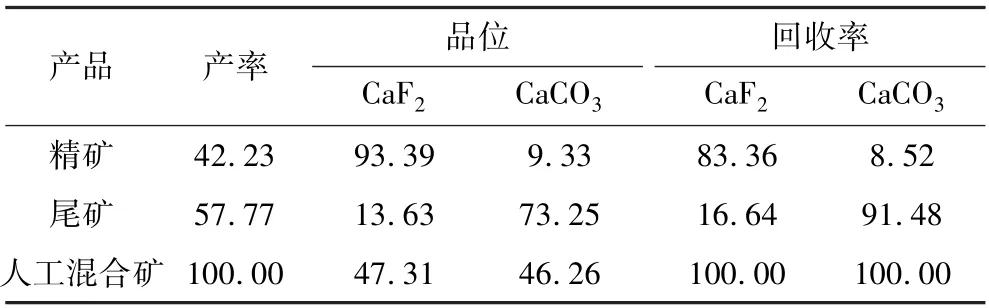
表1 人工混合矿试验结果Table 1 Test results of the artificial mixed ore %
由表1可知,精矿中萤石品位为93.39%,萤石回收率为83.36%,但精矿中方解石品位仅为9.33%,其回收率为8.52%。表明人工混合矿中方解石被强烈抑制,最终得到了高品位、高回收率的萤石精矿。
3 机理分析
3.1 接触角分析
图5为CMC作用前后萤石、方解石接触角的变化。
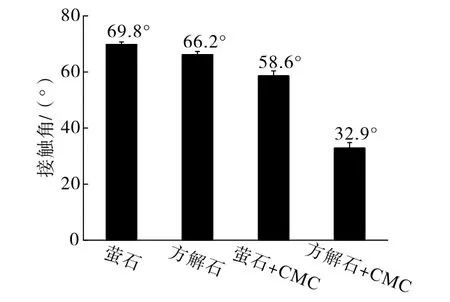
图5 CMC对纯矿物接触角的影响Fig.5 Effects of CMC on contact angle of the pure minerals
由图5可知,萤石、方解石纯矿物自然接触角分别为69.8°、66.2°,与CMC作用后,分别减小11.2°、33.3°。结果表明,CMC对萤石接触角影响较小,但能显著减小方解石接触角,增大其亲水性。
3.2 Zeta电位分析
图6为CMC对纯矿物表面Zeta电位的影响。
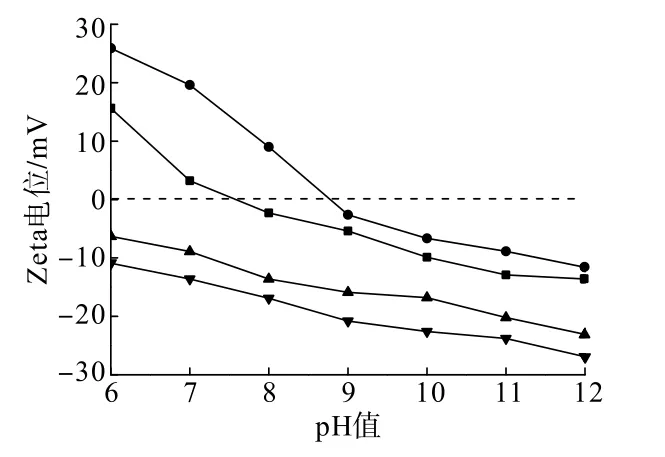
图6 CMC对纯矿物表面Zeta电位的影响Fig.6 Effect of CMC on Zeta potentials of the pure minerals
由图6可知,萤石、方解石的零电点分别为7.4、8.7,当2种矿物分别与CMC作用后,均在pH为6~12范围内整体呈电位负移。当矿浆pH>6时,CMC主要电离出—RCOO-(图7),即—RCOO-占优势[9,21],表明—RCOO-在萤石、方解石表面吸附是造成2种矿物Zeta电位负移的原因。但方解石Zeta电位负移程度更大,表明CMC优势组分—RCOO-大量吸附在方解石表面。
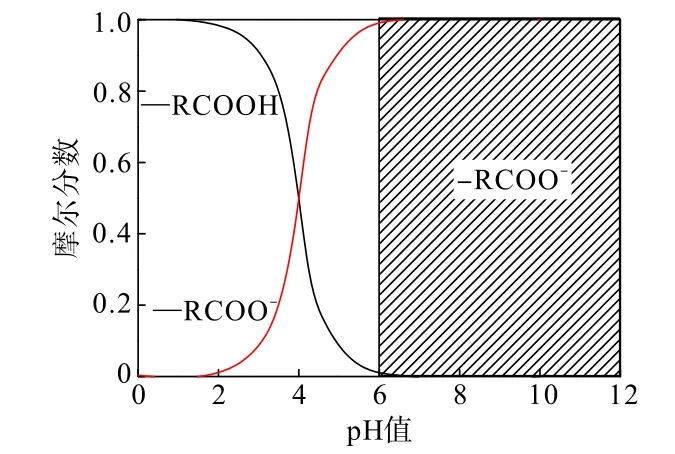
图7 不同pH条件下CMC组分Fig.7 CMC components at different pH
3.3 吸附量分析
图8为CMC对2种矿物表面油酸钠吸附量的影响。
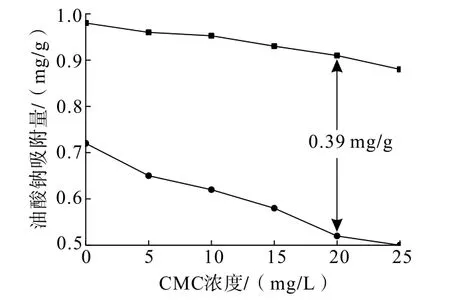
图8 CMC对矿物表面油酸钠吸附量的影响Fig.8 Effect of CMC on the adsorption of sodiumoleate on mineral surface
由图8可知,在不添加CMC时,萤石表面油酸钠吸附量明显高于方解石,这是由于2种矿物常见解离面的Ca2+活性位点密度不同(DFT模拟表明,萤石常见解离面(111)、(100)上Ca2+密度分别为12.9、11.1 μmol/m2,方解石常见解离面(104)上Ca2+密度为8.24 μmol/m2),导致萤石表面油酸根离子的吸附密度大于方解石表面[3]。因此,油酸钠体系下萤石的可浮性大于方解石。
随着CMC用量增加,2种矿物表面吸附油酸钠量随之降低,且方解石减少幅度明显大于萤石。研究表明,在pH>6时,油酸钠主要电离出阴离子基团—RCOO-、—(RCOO-)22-,均易在萤石、方解石表面Ca2+活性位点吸附[9,21],且在萤石表面吸附量明显大于方解石,导致萤石表面可供CMC吸附的Ca2+活性位点明显减少,使得CMC对萤石的抑制作用减弱,即CMC大量吸附于方解石表面,使其表面亲水被抑制。研究表明[9],萤石、方解石与CMC作用后,2 938.49 cm-1处存在—CH3、—CH2的C—H振动吸收峰,且方解石与CMC作用后形成的C—H振动吸收峰强度明显大于萤石,表明方解石更易与CMC发生作用。同时,方解石表面Ca2+活性位点大量减少,难以继续吸附油酸根离子,这可能是CMC强烈抑制方解石的原因。
3.4 微量热分析
图9为CMC对油酸钠与矿物作用时的热速率曲线的影响。
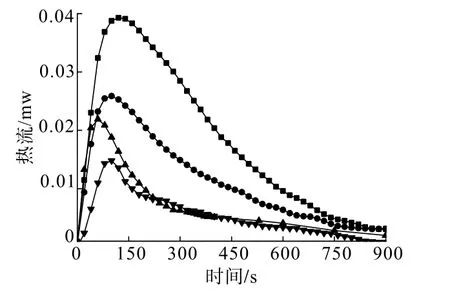
图9 CMC对油酸钠与矿物作用时热速率曲线的影响Fig.9 Effect of CMC on the heat rate curve of sodium oleate interacting with minerals
由图9可知,热速率曲线均为正,表明体系均为放热反应。
将图9所得微量热数据分别计算,得到添加CMC前后油酸钠与矿物作用时的热动力参数(见表2)。由表2可知,萤石与油酸钠作用时热速率反应热最大Q=86.66 mJ,方解石与油酸钠作用时热速率反应热次之,萤石与油酸钠、CMC溶液作用时热速率反应热Q=51.93 mJ,而方解石与油酸钠、CMC溶液作用时热速率反应热Q=33.69 mJ。表明CMC均能降低萤石、方解石与油酸钠作用的反应热。添加CMC后,方解石与油酸钠反应速率常数k值(1.69)低于萤石与油酸钠反应速率常数k值(1.86),说明CMC抑制了2种矿物与油酸钠的化学吸附速率,且对方解石更明显。反应级数(n)大致等于1,表明此反应体系为一级反应。
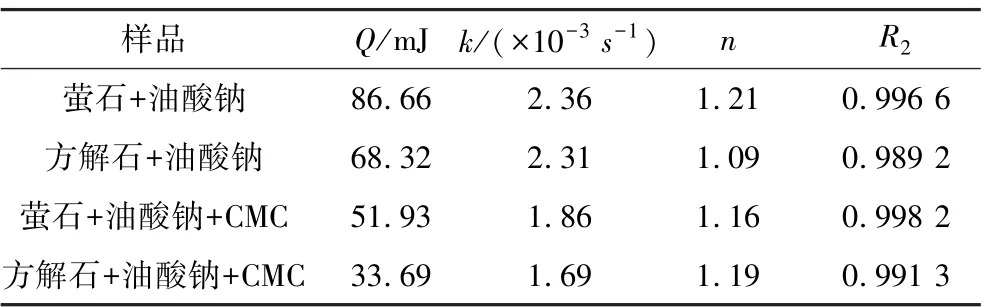
表2 CMC与矿物作用热动力学参数Table 2 Thermodynamic parameters of interaction between CMC and mineral
3.5 吸附模型
图10为CMC对矿物表面油酸钠吸附影响模型。首先,萤石、方解石表面都存在荷正电的Ca2+,与抑制剂CMC作用后,在萤石表面吸附少量CMC,而方解石表面吸附较多CMC,导致方解石表面Ca2+活性位点数量急剧减少。当添加捕收剂油酸钠时,由于萤石表面吸附了少量CMC,存在更多Ca2+,导致萤石与更多油酸钠作用,而方解石表面只有少数Ca2+活性位点可与之作用。因此,CMC能高效选择性分离萤石、方解石。
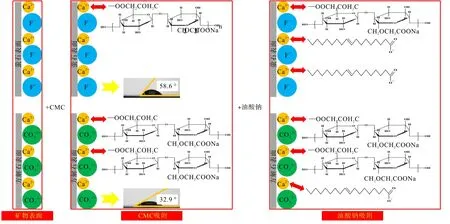
图10 CMC对矿物表面油酸钠吸附影响模型Fig.10 Model of the effect of CMC on the adsorption of sodium oleate on mineral surfaces
4 结 论
(1)CMC对方解石有更强烈的抑制作用,在CMC用量为20 mg/L时能高效抑制方解石。pH=8时,萤石浮选回收率达到最大值85.60%,而方解石浮选回收率为34.56%。人工混合矿试验所得精矿中含萤石93.39%、回收率为83.36%,可最大化实现两者浮选分离。
(2)CMC能造成方解石Zeta电位显著负移,归因于CMC优势组分—RCOO-大量吸附于方解石表面,使得方解石矿物表面相较于萤石表面具有更小接触角,从而难以吸附油酸钠。CMC可有效降低方解石与油酸钠溶液作用时的反应热。热动力学数据表明,方解石与油酸钠、CMC溶液作用后有更低的反应速率常数,且反应体系为一级反应。
(3)吸附模型表明,CMC主要电离组分—RCOO-会大量吸附在方解石表面,使方解石表面Ca2+活性位点大量减少,难以继续吸附油酸根离子,这是CMC强烈抑制方解石的原因。

