创新海洋生物科技,推动我国海洋生物产业高质量发展
焦炳华 刘小宇 卢小玲 于豪冰 胡 波
1.海军军医大学 基础医学院生物化学与分子生物学教研室 上海200433
2.海军军医大学 海军特色医学中心海洋生物与极地医学研究室 上海200433
海洋生物医药与生物制品产业是我国发展海洋战略性新兴产业的重点领域, 也是实现我国“蓝色经济” 高质量发展的重要内容。 近年来, 我国的海洋生物医药与制品产业的发展取得了长足的进步, 壳聚糖、 海藻酸钠的产量占世界的80%以上[1]。 在国家863 和重点研发等计划支持下, 特别是通过“十二五”“十三五” 两轮国家海洋经济创新发展示范项目的支持, 一批科技成果产业化落地, 海洋生物酶类制剂如溶菌酶、 蛋白酶、 脂肪酶、 酯酶等实现了产业化; 具有止血、 愈创、 抗菌和手术防粘连的海洋功能材料产品进入了产业化实施阶段; 海洋绿色农用制剂寡糖农药展开了全面应用; 海洋动物疫苗如鳗弧菌疫苗、 迟钝爱德华菌疫苗、 虹彩病毒疫苗等实现了自主研发;以系列鱼油制品、 高附加值肽类制品为代表的海洋功能食品品种丰富; 海洋糖类药物研发率进入世界领先水平, 原创抗阿尔茨海默病新药GV-971 (商品名“九其一”) 成功上市[2]。 据2020 年中国海洋经济统计公报显示, 我国海洋生物医药研发力度不断加大, 产业增势稳健, 原料药延续较快发展态势, 全年实现增加值451 亿元, 比上年增长8.0%[3]。 以上成果, 体现出我国海洋生物经济产业各方面稳步发展, 在中国海洋经济总产值中的比例不断上升, 呈现出十分强劲的发展态势。
1 海洋药物
1.1 海洋药物研发概况
世界上近60%的临床应用药物都直接或间接来源于天然产物。 海洋高盐、 高压、 缺氧、 少光照等特殊生境使海洋生物的次生代谢途径与陆地生物有着巨大的差异, 导致海洋生物能够产生一些化学结构新颖、生物活性多样的次级代谢产物, 这些化合物为海洋创新药物的研发提供了大量的模式结构和药物前体[4]。从20 世纪90 年代开始, 海洋天然产物相关研究进入快速增长阶段, 特别是从2008 年开始, 每年有超过1 000 个海洋天然产物被发现[5]。 截至目前, 各国科研人员已从不同海洋生物资源中发现超过2 万个海洋天然产物, 其中包含数百个结构新颖、 具有显著广谱生物学活性和重要应用前景的海洋分子[6]。 美国是世界上最早开展海洋药物研究的国家, 在这一研究领域占据绝对优势, 其次为西班牙、 德国和日本。 据资料显示, 现阶段基于海洋天然产物或其衍生物开发而成功上市的药物有17 种, 进入III 期、 II 期、 I 期临床研究的活性物质分别有8 种、 12 种、 8 种, 约75%的海洋创新药物出现在21 世纪之后, 并且绝大多数是国外的研发产品, 我国相对落后[7]。 不难看出, 海洋药物相关研究已经成为国际研究热点, 基于“蓝色海洋药库” 的创新药物研制已成为当今医药工业发展的重要方向, 各国也纷纷成立了海洋药物研究机构, 并对海洋天然产物的研究投入大量科研资金。 例如美国国立卫生研究院(National Institutes of Health, NIH) 每年投于海洋药物研究的科研经费占全部天然药物研究经费的一半以上, 巨大的投入已获得丰厚的回报, 牢牢占据海洋创新药物研究的第一把交椅, 近几年除了一大批有应用前景的海洋候选药物外, 正在进行临床疗效评价的海洋抗癌药物至少有7 个[6]。 尽管我国很早就有海洋药物的使用历史和经验, 但目前我国的海洋创新药物研制水平落后于西方发达国家。 为壮大海洋经济, 加强海洋生物医药、 海洋生物制品、 海洋生物材料的研究发展, 建立了以青岛、 长三角、 厦门、广州为中心的海洋生物技术和海洋药物研究机构, 以加快我国海洋天然产物研究的步伐, 目前, 每年有超过200 个活性新分子从中国海域被发现, 这些海洋活性新天然产物的发现, 为我国后续海洋创新药物研发的腾飞打下了坚实的基础[6-7]。
1.2 已上市的海洋药物的情况
头孢菌素C (Cephalosporin C) 实际上是最早发现的海洋药物, 来源于海洋真菌, 目前已发展成系列的头孢类抗生素, 在临床上得到广泛应用。 20 世纪60 年代的抗结核一线药物利福霉素(Rifamycin) 亦源自海洋细菌。 此后, 欧洲、 美国、 日本等发达国家和地区的药品监管机构相继批准了一系列海洋生物药物上市[8]。 截至2021 年6 月, 国外批准上市的海洋药物大约有13 种(见表1), 含10 种小分子, 1 种多糖及2 种蛋白类, 聚焦于抗肿瘤、 抗病毒、 抗菌、 镇痛等领域[9-14]。
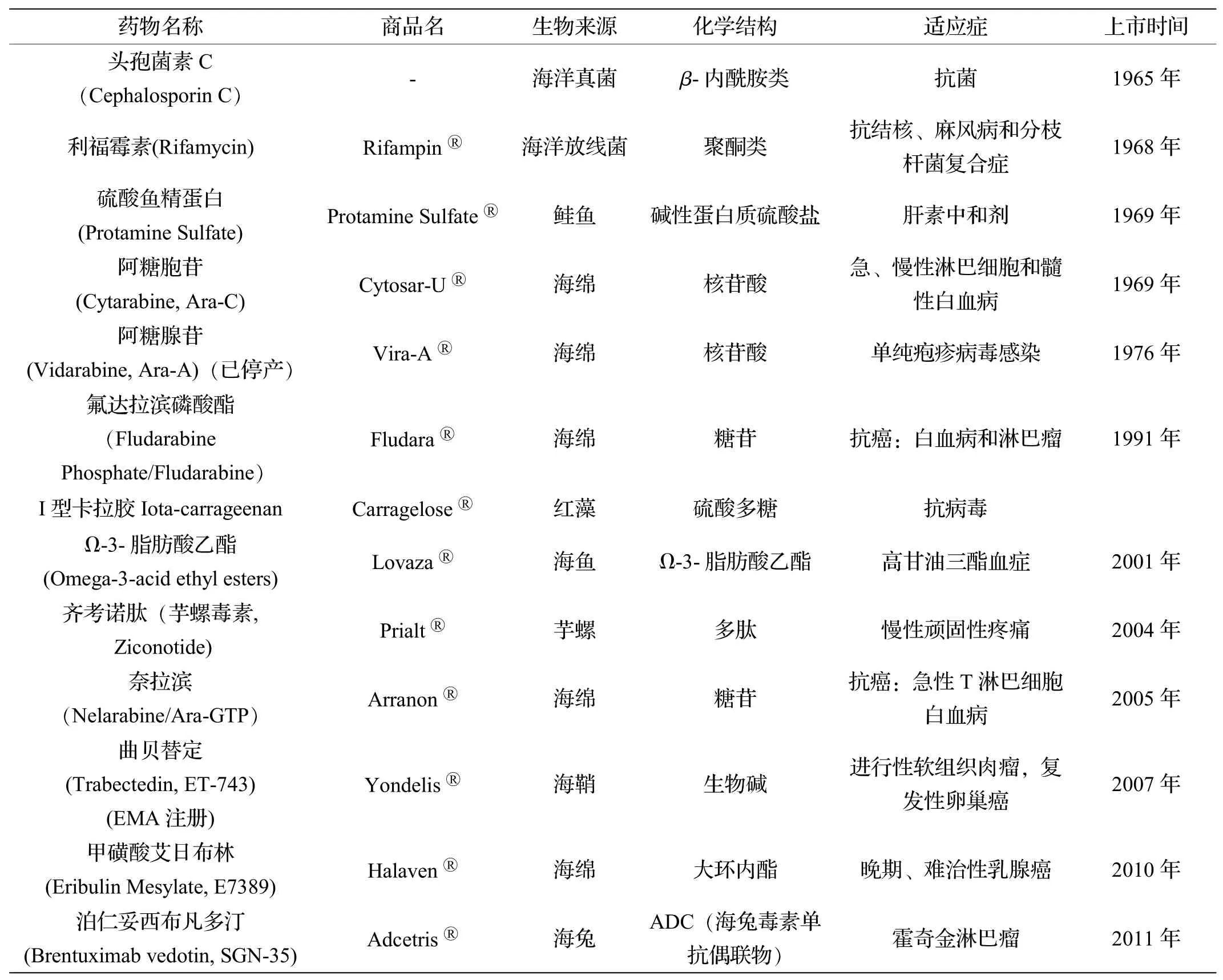
表1 全球批准上市的海洋药物(统计至2021 年6 月)
另外, 除了已上市的海洋药物外, 还有几十种海洋活性物质或其衍生物进入临床试验。 这些药物源于海洋真菌、 放线菌的化合物有2 个, 均进入II 期临床试验; 来自海洋藻类的活性物质有1 个进入III 期临床试验, 1 个进入I 期临床试验; 来自海绵有11 个,5 个进入II 期临床试验, 4 个进入I 期临床试验, 2 个停滞于I 期临床试验; 来自海洋软体动物的化合物有8 个, 1 个进入III 期临床试验, 4 个进入II 期临床试验, 3 个进入I 期临床试验; 来自棘皮动物门的活性物质1 个进入III 期临床试验; 从海洋尾索动物门发现的化合物有2 个, 1 个进入III 期临床试验, 1 个止步于II 期临床试验; 提取自节肢动物门的化合物有2个, 均进入II 期临床试验; 从海洋纽形动物门提取的活性物质有1 个, 但止步于II 期临床; 在海洋脊椎动物发现的化合物有3 个, 2 个进入III 期临床试验,1 个进入II 期临床试验。 这些药物的治疗涉及临床不同的疾病, 显示出独特疗效[4,7]。
许多海洋来源的天然活性物质, 具有极其强烈的细胞毒活性, 但正因为如此, 实际应用中有可能存在着治疗窗口窄等问题, 限制了该类药物的进一步开发和利用。 近些年来, 抗体偶联药物( Antibodyconjugated Drugs, ADC) 的提出, 使大量的细胞毒类海洋天然活性物质有了更好的用武之地。 2011 年上市的海洋药物泊仁妥西布凡多汀AdcetrisR是第一个海洋ADC 药物, 它利用具有强烈细胞毒性的海兔毒素作为癌细胞杀伤弹头, 发挥了很好的治疗作用, 成为海洋ADC 药物成功开发的典范。 目前已上市和进入临床的ADC 药物中, 主要是以海兔毒素及其衍生物作为“弹头” 的详情见表2[15]。

表2 已上市和进入临床的海洋来源抗体偶联药物概况(统计至2021 年6 月)
2021 年6 月18 日, 百时美施贵宝和卫材达成了独家全球战略合作意向, 共同合作开发ADC 药物MORAb-202。 MORAb-202 的弹头部分为已上市的海洋药物艾日布林, 目前研究尚在继续中。
1.3 我国海洋药物研究现状
我国已上市的海洋药物共有10 种, 化学结构类型以多糖类为主, 自1985 年藻酸双酯钠片成为我国首个具有知识产权的海洋类功能原创肝素药物后, 相继又上市了用于降血脂的甘露六烟酯片、 甲壳胺、 角鲨烯、 海麒舒肝、 海昆肾喜、 甘糖酯、 甘露醇烟酸酯片和甘露特钠胶囊(GV-971) 等, 主要用于心脑血管疾病、 肝病、 慢性肾衰竭及阿尔兹海默症等的治疗(表3)[16-17]。
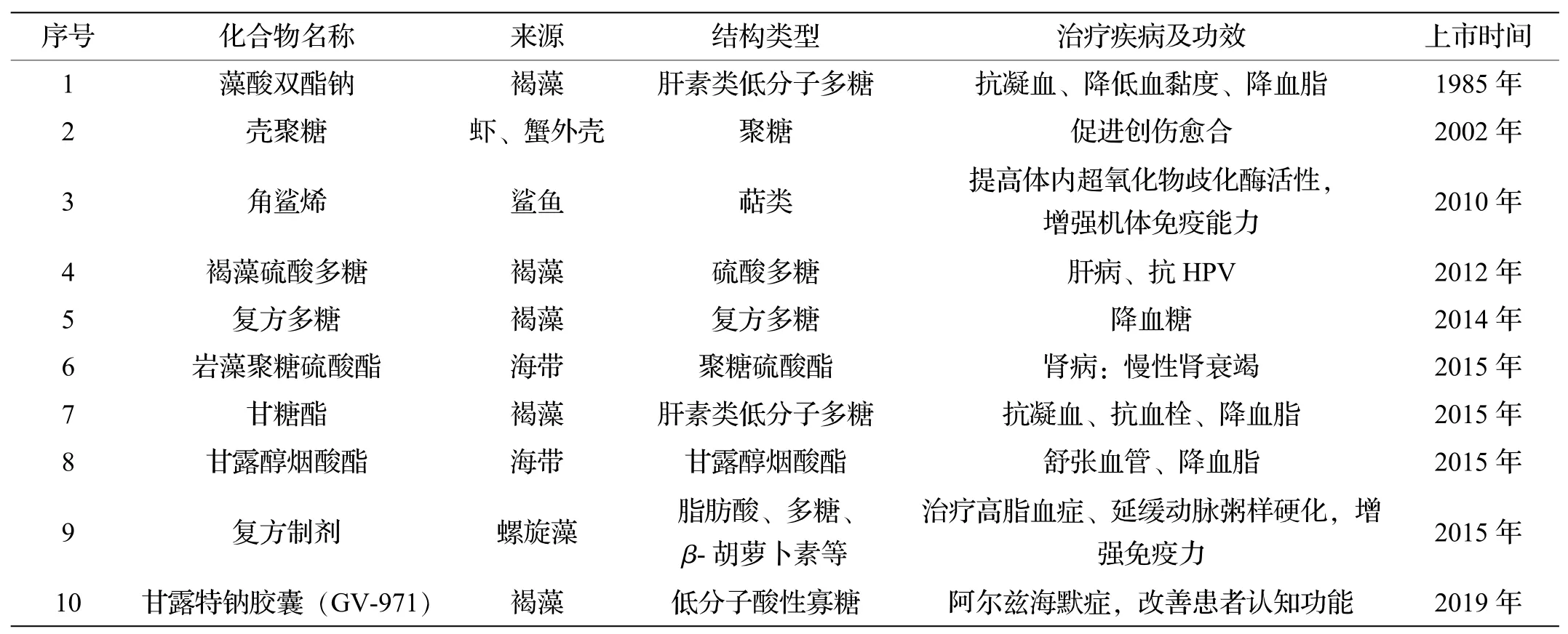
表3 国内自主研发批准上市的海洋药物
此外, 一些低分子量海洋硫酸多糖药物几丁糖酯、 螺旋藻糖肽( K-001) 、 D- 聚甘酯和玉足海参多糖等均进入Ⅲ期临床研究, 主要用于动脉粥样硬化、 晚期胰腺癌和防治脑缺血等的治疗。 另外, 紧跟国际药物开发潮流, 我国海洋来源ADC 药物的研发也正蓬勃兴起, 目前也有数款以海兔毒素为弹头的ADC 药物进入临床研究(表4)[15]。
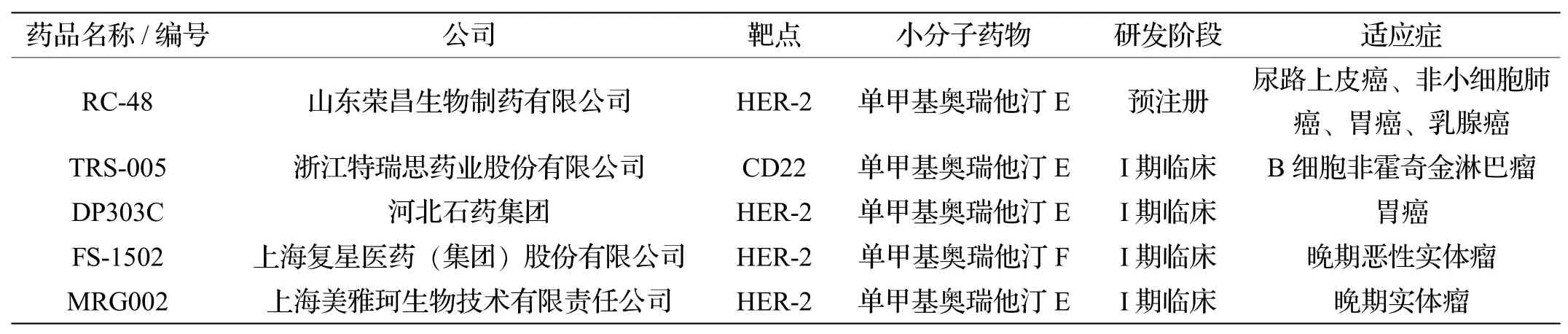
表4 国内在研的海洋小分子弹头抗体偶联药物
与世界其他国家不同的是, 海洋中药是我国海洋药物研究的一大特色和亮点。 海洋中药是指来源于海洋、 在中医药理论指导下用于防治疾病的药物, 我国从20 世纪70 年代开始进行现代海洋药物研究, 先后对1 667 种海洋药用动植物和18 种海洋矿物开展了现代药理学、 化学研究, 取得了系列研究成果, 并据此修订了12 种海洋中药的质量标准, 新的质量标准部分收录于2020 版的《中国药典》 中。 在成方制剂方面, 2020 版《中国药典》 收录了145 首方剂, 涉及10 余味海洋中药, 以珍珠母、 珍珠、 牡蛎的使用频次最多, 含牡蛎的成方制剂如乌鸡白凤丸等216 个, 含珍珠的成方制剂如安宫牛黄丸等125 个, 含珍珠母的成方制剂如清开灵等41 个。 内服制剂占比94.44%,丸剂数量最多, 功效以清热解毒、 止痛、 安神为主,临床应用报道2 539 篇[18]。
2 海洋生物制品
2.1 海洋生物酶和功能蛋白
生态环境和产业结构的调整使我国酶制剂市场显示了比世界市场高得多的增长速度(年平均增长率达21%), 酶制剂用于催化和转化的生物制造产业被列为我国中长期科技规划发展纲要优先支持发展的重点领域[19]。 自“九五” 时期开始, 我国对海洋生物酶的开发利用开展了系统的研究, 经过多年的积累, 目前, 获得了多种活性强、 理化性质特殊, 具有优良应用前景的海洋生物酶类, 这些海洋生物酶与现有的陆地来源酶相比具有低温和室温下活性高、 抗氧化、 在复杂体系中稳定性良好等优越的性质, 在国内外市场具有较强的竞争优势, 其中已有部分酶制剂在开发和应用关键技术方面取得重大突破, 进入产业化实施阶段[20]。
目前我国重点开发工业用、 食品用、 医药用等海洋新型酶类及酶制剂。 工业用酶制剂主要包括低温碱性脂肪酶、 低温碱性蛋白酶、 低温中性纤维素酶等;食品用酶制剂主要包括淀粉酶、 蛋白酶、 脂肪酶等;医药用酶制剂主要包括尿素酶、 胶原酶、 溶菌酶等;饲料用酶制剂主要包括多糖酶、 纤维素酶、 蛋白酶、中性植酸酶等[21]。 此外, 嗜冷、 嗜热、 嗜碱及耐有机溶剂等海洋极端酶在手性合成中的应用前景十分广阔, 将是未来绿色化学工业发展的重要方向之一[22-23]。
蛋白质是生命的物质基础, 是生物有机体生长、繁殖及新陈代谢不可缺少的营养物质。 海洋生物的多样性及海洋环境复杂性使得海洋生物成为地球上最大的天然蛋白质库。 海洋生物中不同种类蛋白质的识别功能研究及规模制备工艺等是海洋生物资源高值化综合利用的重要研究内容, 也是海洋蛋白质资源深度开发的基础。 目前, 我国在海洋渔业部分副产物中的蛋白质资源的综合利用已达到相当大的规模, 制备了多种海洋胶原蛋白、 贝类蛋白、 海藻蛋白、 海洋微藻蛋白等, 作为食品原料、 营养补充剂、 黏合剂、 材料表面改性剂以及应用在再生医学和组织工程、 生化试剂或诊断材料等领域[24]。
2.2 海洋生物材料
甲壳素/壳聚糖、 海藻酸盐、 琼胶、 卡拉胶、 胶原蛋白、 褐藻酸等海洋生物大分子具有独特的结构和功能, 在生物材料开发应用方面具有诸多优点[25-26]。甲壳素、 壳聚糖及其衍生物具有成胶性、 成膜性、 可纺性等, 可制成适合临床应用的不同形态、 性质和功能的材料产品。 目前, 国内以壳聚糖及其衍生物开发生产生物医用材料产品的企业超过80 家, 获产品批文超过100 个, 其中生产三类医疗器械产品的企业为6 家, 产品功能涉及手术止血和防术后粘连两个品种,其他属二类医疗器械产品, 用于皮肤损伤创面的止血、 愈创、 抑菌、 消炎等。 目前国家食品药品监管部门共颁发180 个壳聚糖相关的注册证, 其中以上海昊海生物科技有限公司生产的用于防粘连及骨科的壳聚糖产品、 杭州协合医用品有限公司生产的生物外科手术用防粘连冲洗液以及山东赛克赛斯生物科技股份有限公司生产的产品手术防粘连液(赛必妥) 等为代表产品。
海藻酸钠是从褐藻中获得的海洋生物大分子,其结构中的β-D-甘露糖醛酸和α-D-甘露糖醛酸, 具有明显的抗肿瘤活性作用, 基于此特性开发的肿瘤血管栓塞剂“海藻酸钠微球栓塞剂” 三类医疗器械投入市场应用多年, 除此之外, 以褐藻酸钙纤维生产皮肤创面功能敷料的生产厂家有30 余家, 褐藻酸盐用于组织工程的细胞支架材料、 载药缓释微球材料也有研究[25]。 但是, 褐藻酸盐在体内没有有效的水解酶类, 体内降解时间长。 褐藻酸盐在生物医用材料方面的应用, 现尚不及甲壳素/ 壳聚糖研究得深入, 使得其应用面还不够广。 因此, 还需结合褐藻酸盐的性质特点, 进行系统深入的基础研究和应用评价。
海洋动物的胶原蛋白也是生物医用材料研究发展的一个重要资源。 这种材料相对易于提取纯化, 无陆地哺乳动物原料可能携带病毒传播的风险, 目前在创伤止血材料方面有一定的研究, 还未能形成有效的产业前景。
2.3 农用生物制剂
我国是农业大国, 利用丰富的海洋生物资源, 尤其是海洋中的甲壳素、 壳聚糖、 褐藻胶等多糖资源,各种微生物资源及其代谢产物, 海洋微藻等各种生物资源等, 可以开发出系列绿色高效的农用制剂, 作为生物肥料、 生物农药、 饲料添加剂和饵料应用于农业的各个方面。
近年来, 我国已开发出甲壳寡糖、 壳寡糖等一系列海洋寡糖、 农肥产品, 并成功实现产业化, 针对粮食作物、 水果、 蔬菜和经济作物进行了大规模推广应用, 累计推广面积近亿亩, 创造了直接和间接经济效益数百亿元, 部分产品已销往国外(表5)。 除了传统的防病抗病、 促生长作用之外, 在研究与实际应用推广过程中抗逆(低温、 干旱)、 保花保果、 提高品质、降低农残、 采后保鲜等新功能也被发现, 这使得寡糖产品的应用面越来越广, 前景越来越广阔, 为后期开发高端产品奠定基础。 此外, 在国际上率先提出了糖链植物疫苗的概念, 认为此类产品作用“防胜于治”,为其应用模式及应用方法提供了理论依据。

表5 我国主要的海洋来源农用生物制剂
另外, 在海洋微生物农药研发领域, 我国近年来也取得了较大成绩。 海洋枯草芽孢杆菌、 海洋链霉菌和海洋细菌生物制剂等蔬菜真菌病害防治药剂均已上市推广或已进入产品报批阶段。 也发掘了海洋木霉、海洋放线菌、 萎缩芽孢杆菌等新资源, 获得了新的有效品种。
但是, 在农用生物制剂方面, 我国还存在诸多需要解决的问题, 已上市的产品种类少、 产能有限, 在研的海洋生物农用制品规模化生产工艺尚有待改进,海洋生物农用制品作用机制尚不明确, 海洋生物农用制品应用技术体系还不完善, 海洋生物农用制品市场认知度不足等问题。
2.4 疫苗及佐剂
我国虽是世界水产养殖大国, 但鱼类疫苗学研究起步较晚, 也十分薄弱, 特别是商业化开发迟迟难以取得实质性突破。 近年来, 随着我国以海水鱼类养殖为代表的水产养殖业向工业化转型的加速, 以及国内外消费市场对于安全水产品的消费认知度日趋提高,我国对于水产品安全问题的管控愈发严格。 这给以疫苗接种为核心的新型水产养殖病害防控技术的加速发展提供了充分的产业机遇。 在过去的10 年间, 经过国家“十二五” 时期和“十三五” 时期各项研发计划的支持, 我国的海水鱼类疫苗的基础研发和商业开发都取得了长足发展和推进。
2011 年, 海洋鱼类鳗弧菌基因工程减毒活疫苗获得我国首例鱼用活疫苗《农业转基因生物安全证书(生产应用)》, 开启了我国海洋动物基因工程活疫苗的商业化开发基础。 2015 年国际上首个商业许可的大菱鲆迟缓爱德华菌活疫苗获得国家一类兽药注册证, 随后2016 年该疫苗获得生产文号, 准予商业化生产应用, 实现了我国海水鱼类疫苗商品化零的突破。 2016 年, 大菱鲆鳗弧菌基因工程活疫苗正式向农业农村部提交新兽药注册申报。 同时, 一大批新的海水鱼类疫苗相继完成临床前研发, 进入临床阶段和产品注册环节。 未来5 年里, 我国的海水鱼类疫苗的商品化将迎来井喷式成果, 这些疫苗的陆续上市, 将为我国以海水鱼类为代表的水产养殖业的可持续健康发展提供可靠的病害防控技术与配套产品支持, 从而助力我国由水产养殖大国向强国转变。
目前研究的疫苗佐剂中, 壳聚糖是报道最多的多糖材料。 壳聚糖可以激活巨噬细胞分泌细胞因子, 而且具有很好的黏膜黏附性及促渗透吸收性, 可以促进抗原的渗透吸收[27]。 褐藻酸是另一种重要多糖材料,褐藻酸盐可以与二价阳离子形成凝胶, 可作为抗原储库, 通过缓慢释放抗原, 延长抗原的作用时间, 以获得更好的免疫效果。 褐藻酸还可作为口服疫苗的抗原载体, 避免抗原受到较强酸性胃液的破坏, 实现在肠道的定点释放。 此外, 研究发现多种来源于海洋的多糖及皂苷等物质同样具有免疫调节作用。 在未来, 伴随对海洋生物资源的进一步发现和深人研究, 将有助于开发更多的天然药物佐剂, 并为海洋生物材料的高值化利用开辟新的途径。
2.5 海洋功能食品
海洋生物多样性决定海洋生物活性组分的多样性, 海洋生物活性物质具有储量大、 种类繁多、 活性强及副作用小等特点, 为研制开发海洋功能食品提供了有利条件[28-30]。 随着基础研究工作取得的相关成绩,海洋功能食品产业逐渐发展成为海洋经济的重要组成部分。 多生物活性蛋白、 多肽、 多糖和脂肪酸等已经实现规模化生产并成为功能食品的重要组成部分, 产生了巨大的经济效益和社会效益(表6)。
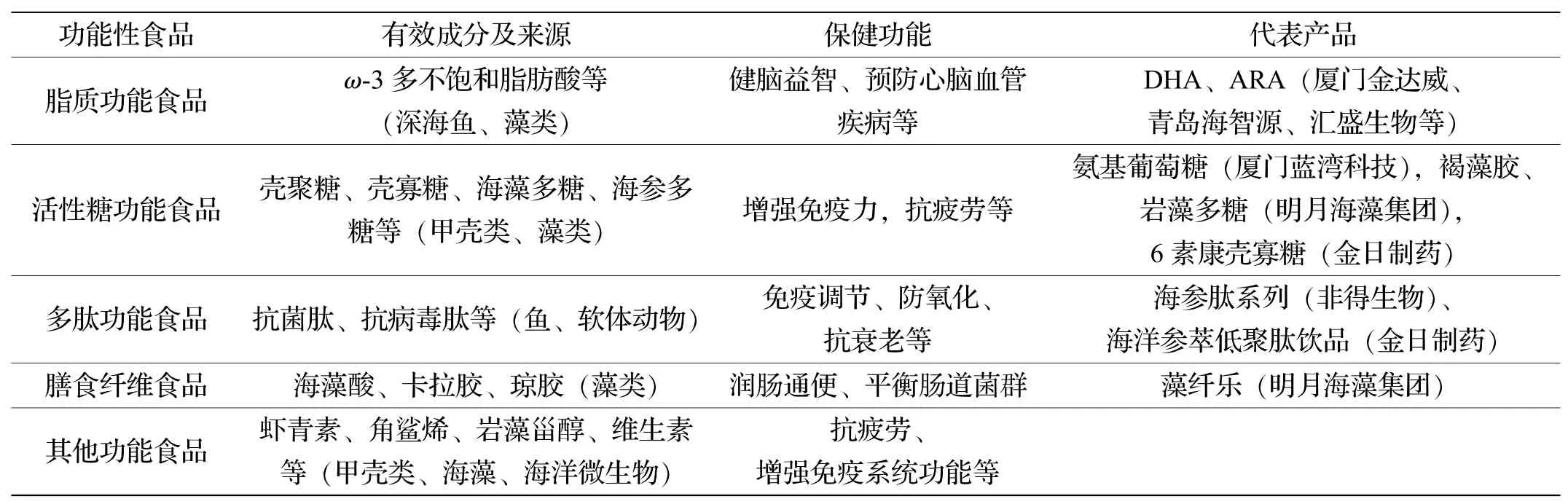
表6 我国主要的海洋功能食品
另外, 许多海洋多糖还用于胶凝剂、 稳定剂、 增稠剂、 分散悬浮剂或成膜剂等, 起着增加食品黏度、赋予食品黏滑而富有弹韧性的口感等功能, 如由红藻中提取的琼脂主要用于增稠和胶凝; 皱波角藻等提取的卡拉胶主要用于增稠、 乳化和成膜, 以改善食品外观; 褐藻胶也在多种食品中用作助剂等。
3 未来发展展望
近年来, 我国的海洋生物经济呈现出蓬勃的发展势头, 但与欧美、 日本等发达国家和地区相比, 我国仍然存在很多不足。 首先, 我国拥有的具有自主知识产权和重要创新性的海洋生物制品核心关键技术相对较少, 需要进一步加强源头创新; 其次, 海洋生物资源的高值化开发利用的比率偏低, 急需加大研究力度与扩大开发范围, 提高新型高端海洋生物制品的种类和数量; 第三, 海洋生物经济是一项系统工程, 目前我国在前期的基础研究、 后期的技术集成和企业的参与度不够。 基础研究的缺乏, 使得创新驱动力不足, 技术集成和企业参与度不够, 制约了技术和成果的产业化进程。
当前, 海洋生物资源的高效、 深层次开发利用,尤其是海洋高端生物产品的研究与产业化已成为发达国家竞争最激烈的领域之一。 随着“海洋强国” 战略的实施和面向海洋战略性新兴产业发展的国家需求,发展海洋生物产品创新技术, 实施海洋生物资源高值化开发战略, 建设高技术密集型海洋生物新兴产业,是我国海洋生物资源开发利用发展的必然之路。
3.1 指导思想
面向人口健康、 资源环境、 工业和农业领域的国家重大需求, 利用可持续发展的海洋生物资源, 瞄准重大产品和关键技术的国际前沿, 突破海洋生物资源高效、 可持续利用的核心和关键技术, 研制具有显著海洋资源特色、 拥有自主知识产权和国际市场前景良好的海洋创新药物和高值化海洋生物制品; 建立国际先进的海洋生物资源开发利用技术、 符合国际规范的产品创新体系、 功能完备的产品研发技术平台与产业化基地, 形成在国际技术前沿具有创新能力和影响力的研发队伍。 为建成2035 年世界中等海洋生物科技强国、 2050 年世界强国提供高技术支撑。
3.2 总体目标
围绕海洋生物科学前沿和蓝色经济发展需求, 本着“深远近海联动、 保护开发并重、 科学技术融合”的原则, 针对海洋特有的群体资源、 遗传资源、 产物资源, 在科学前沿、 关键技术、 产业示范3 个层面,一体化布局海洋生物资源开发利用重点任务创新链,全面提升海洋生物资源可持续开发创新能力, 培育与壮大我国海洋生物产业。 通过重点任务的部署和实施, 将显著提高我国深海生物资源勘探、 获取和开发能力; 全面提升远洋渔业资源开发能力, 促进南极磷虾产业健康发展, 构建远海养殖示范模式, 拓展养殖空间, 实现“屯渔戍边”; 在我国典型海域建立一批生物资源养护示范区和生态牧场, 开发一批创新海洋药物, 推进一批高端海洋生物制品和功能食品产业化, 发展和壮大我国海洋生物战略性新兴产业。
4 战略部署
(1) 深海生物资源。 重点突破深海生物及其基因资源的原位检测、 样品采集、 培养、 保藏等关键技术瓶颈; 开展深海生物多样性全球性调查与评估; 获得一批具有研究和潜在开发价值的深海生物和基因资源, 完善深海生物及其基因资源库; 开展深海(深部生物圈) 生命起源与适应性机制、 与地球系统进化和演化以及全球变化关系等前沿基础研究; 系统开展深海生物基因资源应用潜力评价研究, 发展和壮大有国际影响力的深海生物产业。
(2) 海洋创新药物。 重点发展海洋天然化合物的发现、 活性筛选、 靶标确认、 规模化制备、 成药性评价等新技术, 形成完善的海洋药物发现—中试—产业化研发链; 创制一批针对重大疾病、 具有广阔市场前景的创新海洋药物, 建成若干个全球有影响力的海洋药物企业。
(3) 海洋生物制品。 重点发展海洋生物来源功能分子的发现、 活性确认、 规模化制备、 产业化工程等技术, 研制和开发一批有广阔市场前景的高附加值海洋生物制品(海洋生物功能材料、 海洋新型生物酶制剂、 海洋动物疫苗、 海洋健康相关食品等); 建成若干个全球有影响力的海洋生物制品企业。
目前我国正大力推动科技体制改革, 加强和推动海洋生物制品的基础研究、 技术研究和产业化开发的全创新链设计, 一体化组织实施, 将极大地推动我国海洋生物制品的研究、 开发和产业化, 推动我国海洋生物产业的健康高质量发展。

