7例促肾上腺皮质激素非依赖性双侧肾上腺大结节样增生患者的临床特点
郝聪,李玲,史峥,林苗,张会娟
(郑州大学第一附属医院 内分泌科,河南 郑州 450000)
库欣综合征(Cushing’s syndrome,CS)是由各种病因造成肾上腺分泌过多皮质醇的临床综合征,根据病因可分为促肾上腺皮质激素(adrenocorticotropic hormone,ACTH)依赖性和非ACTH依赖性两大类。ACTH非依赖性双侧肾上腺大结节样增生(ACTH independent macronodular adrenal hyperplasia,AIMAH)是CS的少见类型,在内源性CS中的比率为2%~3%[1]。AIMAH临床表现多样,部分患者可有CS的典型体征,而有些患者仅有高血压、糖代谢异常、骨代谢异常等非特异性表现。因此,AIMAH诊断较困难,易发生漏诊。本研究对7例AIMAH患者的临床资料进行回顾性分析,以加强对该疾病的认识。
1 对象和方法
1.1 研究对象回顾性分析2012年5月至2021年7月就诊于郑州大学第一附属医院的7例AIMAH患者的临床资料。AIMAH诊断标准参考Lacroix等[2]总结的特点:(1)伴或不伴CS的特征性表现;(2)实验室检查符合非ACTH依赖性CS或者亚临床CS(subclinical Cushing’s syndrome,SCS)的诊断;(3)影像学检查提示双侧肾上腺大结节样增生;(4)病理证实肾上腺皮质结节样增生;(5)除外原发性色素性结节性肾上腺皮质病、先天性肾上腺皮质增生、肾上腺皮质转移癌、库欣病、原发性醛固酮增多症、嗜铬细胞瘤等其他可致双侧肾上腺增生或结节样改变的疾病。SCS诊断标准[3-4]:(1)无CS的特征性表现;(2)1 mg过夜地塞米松抑制试验或小剂量地塞米松抑制试验(low-dose dexamethasone suppression test,LDDST)后测定早上8:00血清皮质醇>50 nmol·L-1但≤138 nmol·L-1;(3)另外至少有以下1项异常检测结果,包括24 h UFC水平升高,ACTH水平偏低或低于正常范围,皮质醇分泌节律消失。
1.2 评估方法
1.2.1患者的一般资料 包括性别、就诊年龄、病程、临床表现等。
1.2.2实验室检查及试验 采用化学发光法测定血清皮质醇(参考值:8:00为171~536 μg·L-1,16:00为64~327 μg·L-1)、血清ACTH(参考值:8:00为7.2~63.3 ng·L-1,16:00为4~32 ng·L-1)水平,采用高压液相法测定24 h尿游离皮质醇(24 hours urinary free cortisol,24 h UFC)(参考值73~372 nmol·d-1)水平。试验包括LDDST、大剂量地塞米松抑制试验(high-dose dexamethasone suppression test,HDDST)等。
1.2.3影像学检查及其他 包括肾上腺CT平扫及增强、骨密度检查等。
1.2.4异常受体表达筛查试验 包括体位试验、标准混合餐试验、垂体后叶激素试验、促性腺皮质激素释放激素(gonadotrophin-releasing hormone,GnRH)激发试验和甲氧氯普胺/莫沙必利试验,每项试验前测定血清皮质醇作为对照,试验开始后2~3 h内每隔30~60 min测定血清皮质醇水平,皮质醇水平较基础值升高<25%为无反应,皮质醇水平较基础值升高25%~49%为部分阳性反应,≥50%为阳性反应[5]。
2 结果
2.1 一般情况和临床表现7例AIMAH患者中,男2例,女5例,年龄39~69岁,中位年龄53岁,病程4~20 a,中位病程10 a。5例患者具有CS特征性表现,2例无CS特征性表现。具体资料见表1。

表1 AIMAH患者的临床资料
2.2 实验室检查6例皮质醇节律紊乱,1例(例4)皮质醇节律基本正常;6例8:00皮质醇升高,1例(例2)8:00皮质醇虽在正常范围内,但0:00皮质醇高于16:00。5例8:00 ACTH水平低于正常,2例(例2、例4)8:00 ACTH在正常范围内。1例(例2)24 h UFC正常,其余患者24 h UFC均升高。见表2。地塞米松抑制试验中,7例患者LDDST均未被抑制;7例中1例未做HDDST,5例HDDST未被抑制,1例(例4)HDDST被抑制。见表2。异常受体筛选试验见表3。

表2 AIMAH患者的实验室检查

表3 异常受体筛选试验
2.3 影像学检查及病理检查结果7例患者肾上腺CT均提示双侧肾上腺结节样增生改变,增强扫描呈轻到中度强化。5例患者接受垂体MRI检查,1例未见明显异常,3例垂体信号欠均匀,1例垂体饱满。见图1。7例患者术后大体标本为金黄或灰黄,质软或质中,病理学检查均提示肾上腺皮质结节状增生。见图2。
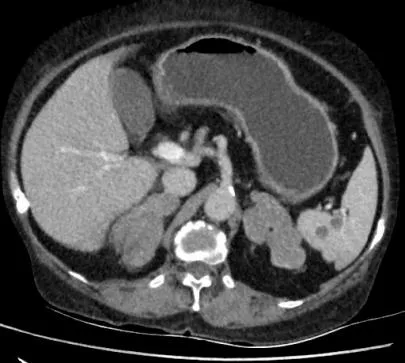
图1 AIMAH患者肾上腺CT表现
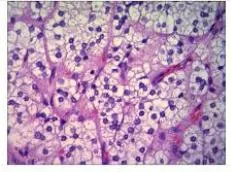
图2 AIMAH患者肾上腺病理学表现
2.4 治疗及预后AIMAH患者的手术及预后相关资料见表4。

表4 AIMAH患者的手术及预后
3 讨论
AIMAH由Kirschner等[6]于1964年首次报道,是CS的少见特殊类型。本研究7例患者中5例具有CS特征性表现,其皮质醇昼夜节律消失,ACTH降低,LDDST均未被抑制,除1例未行HDDST外,余 4例HDDST均未被抑制;2例无CS特征性表现,ACTH正常,其中例2皮质醇节律消失,仅在病程中记载LDDST和HDDST均未被抑制,未能找到LDDST的血清皮质醇结果,无法判断其是否符合SCS;例4皮质醇节律基本正常,LDDST未被抑制,HDDST被抑制,LDDST后的血皮质醇水平为95.6 μg·L-1,高于138 nmol·L-1(1 μg·L-1=2.77 nmol·L-1),故不符合SCS。7例患者术后病理均证实为肾上腺皮质结节状增生。因此,对于影像学检查显示双侧肾上腺大结节样增生同时合并高血压、糖代谢异常、骨代谢异常等表现的患者,即使无典型CS的临床表现,也应考虑AIMAH的可能,及时检测ACTH、皮质醇水平及其他肾上腺皮质、髓质激素,行LDDST、HDDST和异常受体筛选试验协助诊断。
有研究表明AIMAH分泌过多皮质醇并非是细胞合成能力增强,而是细胞数量增多[7-8],这可解释AIMAH病情进展缓慢,部分患者虽有肾上腺结节样增生,临床表现却不典型。Ohashi等[9]对1例亚临床AIMAH患者随访7 a后,该患者才出现CS表现。本组7例患者中位年龄为53岁,病程平均22个月,如例6就诊时52岁,CS症状已有6 a,有高血压、糖尿病、骨质疏松等代谢异常及心功能不全。因此,对于AIMAH患者应力争早诊断、早治疗,以改善预后。
目前AIMAH的病因尚未完全明确。最初认为AIMAH是垂体分泌过多ACTH刺激双侧肾上腺大结节样增生,最终导致肾上腺自主分泌皮质醇增多,从而抑制垂体ACTH分泌[10]。如今认为AIMAH分泌皮质醇增多是某些激素激活了肾上腺皮质束状带异常表达的G蛋白偶联受体导致的,包括异位受体如抑胃肽受体、β-肾上腺素能受体、血管升压素V2及V3受体、5-羟色胺受体和血管紧张素Ⅱ受体,以及原位受体如血管升压素V1受体、黄体生成素/人绒毛膜促性腺激素受体、5-羟色胺受体和瘦素受体,这些受体表达增加,活性增强,这为AIMAH的药物治疗提供了思路:抑制相关内源性激素或用特异性拮抗剂阻断受体[11]。本研究中,例2患者体位试验部分阳性(血清皮质醇较基础值升高46%)和垂体后叶激素试验阳性,由于2项试验均可作用于精氨酸加压素受体,其反应存在重叠,推测该患者可能同时存在血管紧张素Ⅱ受体、β-肾上腺素受体、精氨酸加压素受体。Louiset等[12]对30例AIMAH患者的肾上腺组织标本进行检测,发现肾上腺静脉血中ACTH水平高于外周,由增生肾上腺中的类固醇生成细胞亚群产生,这提示外周ACTH受体即黑素皮质素2型受体拮抗剂靶向治疗AIMAH或是一种新型药物治疗方案。
既往认为AIMAH的标准治疗方案是双侧肾上腺切除术,但术后需糖皮质激素和盐皮质激素终身替代治疗,发生肾上腺危象的风险增加[13]。张学斌等[14]报道了82例接受单侧肾上腺切除术的AIMAH患者,短期内多数获得缓解,在长期随访(>6个月)中,63例患者复发,其中29例接受对侧肾上腺切除术。冒永鑫等[15]报道了46例AIMAH,单侧肾上腺切除术后平均随访23.96个月,29例缓解,13例复发患者接受对侧了肾上腺切除术。本组7例患者均先接受单侧肾上腺切除术,2例患者缓解;4例无缓解,其中1例因术后心力衰竭、消化道大出血要求出院失去随访,2例接受对侧肾上腺次全切术,1例接受对侧肾上腺全切术;1例患者复发,接受对侧肾上腺次全切术。接受双侧肾上腺切除术者术后均接受激素替代治疗。国外也有不少关于AIMAH单侧肾上腺切除术的研究,样本量虽较小,但均报道多数患者获得长期缓解[16-18]。因此,AIMAH患者可行单侧肾上腺切除术,但术后应密切随访,若症状不缓解或复发,再行对侧肾上腺全切或次全切术。

