BiPAP 联合牛肺表面活性物质对早产儿呼吸窘迫综合征患儿的临床治疗效果
博海平
RDS 本身作为一种呼吸道疾病,是儿科中一种较为常见的疾病类型。引发早产儿出现RDS,与肺发育不完善有直接关系,由于肺泡产生肺表面活性物质不足,从而在气体交换阶段出现低氧现象,会出现严重的脑损伤,对早产儿的生命安全造成了极大的威胁,为了能够改善早产儿的低氧情况,可采用呼吸机及肺表面活性物质来进行治疗。近年来,早产儿RDS 疾病发病几率逐年递增,疾病本身具有氧合指标差、病情进展速度快等特点,在发病后若不能及时接受治疗,将会对早产儿的身心健康造成极大的影响。在以往RDS 疾病临床治疗中主要是采用机械通气治疗方法,但是该种治疗方法会对早产儿造成极大的创伤,并且在治疗后易引发早产儿出现支气管肺发育不良,对肺的正常发育造成了极大的影响[1]。因此,在早产儿RDS 临床治疗中选取一种科学有效的治疗措施尤为重要。当前,倡导将BiPAP 联合牛肺表面活性物质治疗法用于早产儿RDS 治疗中,BiPAP 治疗方法具有简便、体积小、操作灵活及安全性高等优势,但是该种治疗方法单独使用临床治疗效果不好,临床上倡导与牛肺表面活性物质联合使用。本次研究,观察BiPAP 联合牛肺表面活性物质所取得的临床治疗效果,报告如下。
1 资料与方法
1.1 一般资料 选取2019 年1 月~2021 年12 月早产儿RDS 患儿40 例,通过随机分组的方式分成对照组和观察组,各20 例。对照组中男10 例,女10 例;胎龄27~36 周,平均胎龄(30.6±2.0)周;出生体重1.4~3.7 kg,平均出生体重(2.6±0.6)kg。观察组中男9 例,女11 例;胎龄26~35 周,平均胎龄(31.5±1.9)周;出生体重1.3~3.5 kg,平均出生体重(2.5±0.5)kg。两组患儿的一般资料比较,差异无统计学意义(P>0.05),具有可比性。本次研究活动在经过医院伦理委员会的批准通过后进行,患儿家属知情本次研究活动,同意参加。
1.2 纳入及排除标准
1.2.1 纳入标准 ①在本次研究中选取的所有患儿均被诊断为早产儿RDS;②非遗传性及先天性畸形疾病者;③进入到医院接受治疗的时间为出生后1 d 内。
1.2.2 排除标准 ①免疫性疾病者;②心肝肾功能不全者;③先天性疾病者;④重度窒息者;⑤吸入胎粪者。
1.3 方法
1.3.1 对照组 行BiPAP 治疗。将气道正压维持在12~15 cm H2O(1 cm H2O=0.098 kPa),呼气末正压控制在4~6 cm H2O,吸气时间控制在0.5 s,呼吸频率控制在20~40 次/min。患儿的经皮血氧饱和度控制在88%~93%。对于经皮血氧饱和度<88%的患儿,应上调吸入氧浓度40%~60%。对于经皮血氧饱和度>93%的患儿,应下调吸入氧浓度21%~40%。
1.3.2 观察组 行BiPAP 联合牛肺表面活性物质治疗。BiPAP 治疗法与对照组一样,在此基础上增加牛肺表面活性物质治疗,当早产儿被确诊为RDS 疾病后,需要在确诊1 h 内对其进行气管插管治疗,在最开始阶段将用药剂量控制在70 mg/kg,当注射工作完成后,对患儿进行气囊加压通气治疗,将治疗时间控制在≥5 min,保证药液能够均匀分布在患儿的肺内。对于病情较为严重的患儿,用药剂量同上,应每隔12~24 h给药1 次,给药次数控制在2~3 次。
1.4 观察指标及判定标准 ①血气指标,包括PaO2、PaCO2,使用血气分析仪进行检测。②MAP、SpO2及HR。③临床治疗效果,在评估过程中以《实用新生儿学》为参考依据,对患儿的体征和临床症状改善情况进行观察,显效:患儿的体征及呼气性呻吟症状全部消失,具有稳定的呼吸频率,患儿具有红润的肤色,通过对患儿进行X 线胸片检查,结果完全恢复正常;有效:患儿的体征及呼气性呻吟症状明显改善,呼吸频率急促,唇部颜色为微紫,通过对患儿进行X 线胸片检查,结果显示有所好转;无效:患儿的体征及呼气性呻吟症状未改善或加重,呼吸频率不稳定,通过对患儿进行X 线胸片检查,结果显示未恢复[2]。总有效率=(显效+有效)/总例数×100%。④并发症发生率,包括呼吸暂停、肺部感染、肺出血、支气管肺发育不良。
1.5 统计学方法 采用SPSS22.0 统计学软件进行统计分析。计量资料以均数±标准差()表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组治疗前后的血气指标比较 治疗前,两组PaO2、PaCO2比较,差异无统计学意义(P>0.05);治疗后,观察组PaO2高于对照组,PaCO2低于对照组,差异具有统计学意义 (P<0.05)。见表1。
表1 两组治疗前后的血气指标比较 (,mm Hg)

表1 两组治疗前后的血气指标比较 (,mm Hg)
注:与对照组治疗后比较,aP<0.05
2.2 两 组MAP、SpO2、HR比较治疗前,两组MAP、SpO2、HR 比较,差异无统计学意义(P>0.05);治疗后,观察组MAP、SpO2高于对照组,HR 低于对照组,差异具有统计学意义 (P<0.05)。见表2。
表2 两组MAP、SpO2、HR 比较()

表2 两组MAP、SpO2、HR 比较()
注:与对照组治疗后比较,aP<0.05
2.3 两组治疗效果比较 观察组临床治疗总有效率高于对照组,差异具有统计学意义 (P<0.05)。见表3。
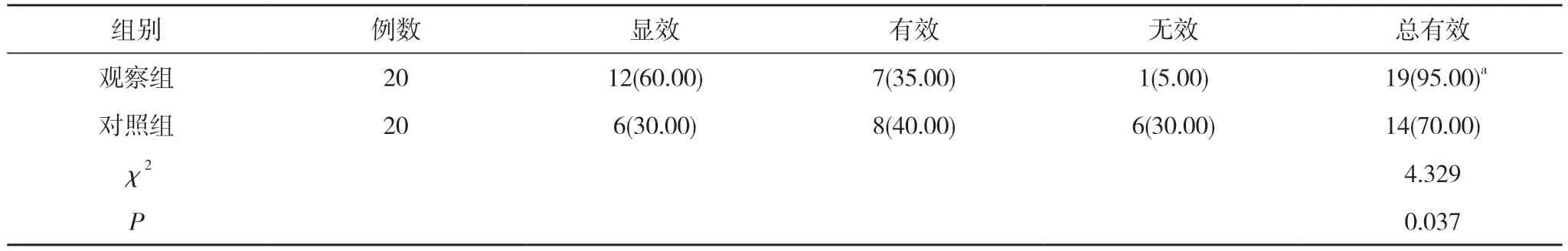
表3 两组治疗效果比较[n(%)]
2.4 两组并发症发生率比较 观察组并发症发生率低于对照组,差异具有统计学意义 (P<0.05)。见表4。

表4 两组并发症发生率比较[n(%)]
3 讨论
早产儿极容易出现RDS 疾病,引发该种疾病的产生与缺乏肺表面活性物质及肺发育不成熟有直接关系,进而导致生后肺泡浸润性不张等情况的产生,从而形成透明膜,降低了肺的残气量及顺应性,一些病情严重者还会有死亡风险。早产儿RDS 患儿的临床症状主要表现为呼吸衰竭及呼吸困难,发病时间一般集中在出生后4~12 h。医学上相关的数据显示,早产儿RDS患儿在出生后2 d 有着较高的死亡率。早产儿在患有RDS 疾病之后应及时接受治疗,在疾病治疗中通过给予患儿外源性肺表面活性物质,有助于降低肺泡表面张力,肺泡顺应性明显提升,氧合改善效果好,疾病临床治疗效果好[3]。
在早产儿RDS 疾病的早期治疗过程中主要是使用大剂量的牛肺表面活性物质进行治疗,疾病临床治疗效果显著。同时辅助使用BiPAP 治疗方法,该种治疗方法在疾病治疗中应用,主要是使用微处理器控制的阀门来提供双水平压力支持,从而产生高流速气体,参数设置包括呼气相正压(EPAP)和吸气相正压(IPAP)两个压力水平,吸气相通由患儿出发,当患儿呼吸频率较慢时,会出现时间循环触发情况,在该种模式下以流速及时间为周期[4]。BiPAP 作为早产儿RDS 中一种常用的无创呼吸模式,该种治疗方法在无创通气条件之下,流量出发从而促使压力支持通气模式得以开启,以此来取得良好的呼吸支持效果。患儿在每次呼吸时,呼吸机可为患儿设置不同的吸气相及呼气相参数,并且能够将压力支持通气和呼吸末正压有机的结合起来,使每分钟的潮气量及通气量得以增加。另外,BiPAP 治疗方法完成了对肺泡正压的有效维持,有助于防止肺泡出现萎缩,确保气道能够始终维持在一种扩张状态中,对肺泡气体交换具有促进作用,患儿氧合水平明显提升。在双水平正压通气之下,使肺内的分流得以减少,气体交换面积大大增加[5]。BiPAP 治疗方法下无需切开气管,避免患儿气道遭受到严重的损坏,完成了对气道防御系统的有效保护,有助于避免患儿在疾病治疗期间出现躁动不安心理情绪,使肺气漏疾病发生率得以降低[6]。牛肺表面活性物质是一种价格较为昂贵的物质,主要分布在肺泡表面,所展现出来的作用包括稳定肺泡容积、降低肺表面张力和快速清除肺液等,使肺泡表面张力得以降低,在早产儿RDS 疾病治疗中应用有助于改善机体的氧合状态,能够取得一定的临床治疗效果[7]。为了能够进一步提升早产儿RDS 的治疗效果,倡导将牛肺表面活性物质与BiPAP 治疗方法同时使用,有助于降低患儿的并发症发生率,医疗开销明显减轻,院内感染危险性大大降低[8]。
本次研究结果显示,治疗后,观察组PaO2高于对照组,PaCO2低于对照组,差异具有统计学意义(P<0.05)。治疗后,观察组MAP、SpO2高于对照组,HR 低于对照组,差异具有统计学意义 (P<0.05)。观察组临床治疗总有效率高于对照组,差异具有统计学意义 (P<0.05)。观察组并发症发生率低于对照组,差异具有统计学意义 (P<0.05)。可见在早产儿RDS 患儿治疗中使用BiPAP 联合牛肺表面活性物质治疗法展现出了较高的临床应用效果,两种治疗方法同时使用有助于改善患儿的血气指标,肺气漏发生风险明显降低[9-11]。之所以能够取得良好的临床治疗效果,是因为BiPAP治疗方法的气道压力值可在上限及下限压力间出现变动,并且在实际的治疗期间,会以患儿病情的实际情况为依据,对压力水平及持续时间进行合理制定,具有体积小、无创、安全性高、简便及操作灵活等优势[12]。另外,BiPAP 治疗方法主要是运用鼻面罩使用双水平气道正压来提供压力支持通气,使用涡轮供气的方式,每分钟所产生的持续气流为40~50 L,以此来完成对漏气的补偿,完成了对预设压力水平的有效维持,有助于防止鼻面罩出现漏气而对疾病临床治疗效果造成极大的影响[13]。
在对早产儿RDS 疾病进行治疗期间,需要结合患儿病情的实际情况有针对性的对患儿进行治疗[14]。肺表面活性物质本身作为一种脂蛋白,由肺泡Ⅱ型上皮细胞分泌而产生,其成分由60%的二棕榈酰卵磷脂及10%的表面活性物结合蛋白构成,所展现出来的药理作用主要表现为,能够使肺泡气-液界面表面张力得以降低,完成了对患儿肺泡稳定性的有效维持,防止出现肺不张疾病的产生[15]。若早产儿出现呼吸困难情况,肺表面活性物质能够展现出扩张及稳定肺泡作用,使肺的气体交换及顺应性得以明显改善,肺泡通气功能、临床症状及氧合状态得以明显改善[16]。
吴志兴[17]在2021 年提出,BiPAP 治 疗法,显效率为30.00%,有效率为43.33%,无效率为26.67%,总有效率为73.33%;BiPAP 联合牛肺表面活性物质治疗法,显效率为56.67%,有效率为40.00%,无效率为3.33%,总有效率为96.67%;BiPAP 联合牛肺表面活性物质治疗法临床治疗总有效率高于BiPAP 治疗法,差异具有统计学意义 (P<0.05)。BiPAP 治疗法,PaO2治疗前为(46.13±3.72)mm Hg,治疗后为(68.02±3.80)mm Hg;PaCO2治疗前为(52.57±7.01)mm Hg,治疗后为(46.14±4.26)mm Hg。BiPAP 联合牛肺表面活性物质治疗法,PaO2治疗前为(46.91±3.84)mm Hg,治疗后为(81.53±5.96)mm Hg;PaCO2治疗前为(52.38±6.77)mm Hg,治疗后为(35.19±4.15)mm Hg。BiPAP 治疗法和BiPAP 联合牛肺表面活性物质治疗法治疗前两组PaO2和PaCO2对比,差异无统计学意义(P>0.05)。BiPAP 联合牛肺表面活性物质治疗法治疗后PaO2高于BiPAP 治疗法,PaCO2低于BiPAP 治疗法,差异具有统计学意义 (P<0.05)。从以上既往研究结果中可知与本文的研究结果具有较强的一致性,充分认证了本次研究结果的科学性,并且说明了本次研究结果的价值,可为同类型文章写作提供可靠的依据。
综上所述,在早产儿RDS 患儿治疗中使用BiPAP联合牛肺表面活性物质治疗法,有助于改善患儿的血气指标,氧合状态改善效果好,体征及临床症状改善效果突出,降低并发症发生率,疾病临床治疗效果显著,推荐在临床上大力使用。

