基于Levey-Jennings质控图联合Westgard多规则理论建立万古霉素治疗药物监测的室内质控评估方法
李会婷,吴 妍,张哲弢,史天陆
(中国科学技术大学附属第一医院/安徽省立医院药剂科,合肥 230001)
万古霉素为糖肽类抗菌药物,用于治疗耐甲氧西林金黄色葡萄球菌(MRSA)、肠球菌及耐甲氧西林凝固酶阴性葡萄球菌等革兰阳性菌感染。美国感染病学会发布的有关MRSA感染治疗指南[1]和《万古霉素临床应用中国专家共识(2011版)》[2]指出,万古霉素治疗金黄色葡萄球菌感染成败与其血药谷浓度高低有关,同时不良反应(尤其是肾毒性)的发生与其血药浓度过高有关。2020年美国万古霉素治疗严重MRSA感染的治疗药物监测指南[3]和《中国万古霉素治疗药物监测指南(2020更新版)》[4]推荐,对于重症监护病房患者、肥胖患者、烧伤患者、应用肾损害药物患者及肾功能不全患者、新生儿/儿童患者、接受肾脏替代治疗等患者,应进行万古霉素监测。目前,万古霉素的治疗药物监测方法包括荧光偏振免疫分析法、微生物法等[5]。但高效液相色谱法(high-performance liquid chromatography,HPLC)仍是使用最普遍的方法[6-7]。其较为经济,但步骤繁琐,结果影响因素较多,而国内没有配备定值质控品,对于万古霉素室内质控研究较少且不够完整。因此,本研究在已有实验室条件下,对 HPLC法测定万古霉素血药浓度的室内质量控制评价体系进行了相关探索。
1 材料
1.1 仪器
Shimadzu LC-2010A型高效液相色谱仪(紫外检测器,LabSolutions Version 5.51 色谱工作站,日本岛津公司);MS205DU型十万分之一分析天平(瑞士Mettler Toledo公司);SB-5200D型超声波清洗器(宁波新芝生物科技股份有限公司);TGL-16B型高速台式离心机(上海安亭科学仪器厂)。
1.2 药品与试剂
万古霉素对照品(批号:130360-201302),去甲万古霉素(批号:130338-201704,含量87.7%),均购于中国食品药品检定研究院;甲醇(HPLC级,西陇科学股份有限公司);水为超纯水;健康人空白血清由我院输血科提供。
2 方法与结果
2.1 色谱条件
色谱柱:Hypersil ODS色谱柱(4.6 mm×250 mm,5 μm);流动相:磷酸二氢钾-甲醇(V∶V=87∶ 13);检测波长:230 nm;流速:1 mL/min;柱温:35 ℃;进样量:20 μL。
2.2 万古霉素工作液的配制
精密称取万古霉素适量至5 mL容量瓶中,以超纯水稀释至刻度得到1 mg/mL万古霉素储备液。取适量注射用水,依次将储备液稀释为25、50、100、250和500 μg/mL系列浓度的万古霉素工作液,于4 ℃冰箱备用。
2.3 去甲万古霉素工作液的配制
精密称取去甲万古霉素5 mg至25 mL容量瓶中,以注射用水稀释至刻度,溶解后得到200 μg/mL去甲万古霉素内标溶液。
2.4 自制血浆质控品的制备
参考文献[8],取健康人血清90 μL,分别加入25 μg/mL、50 μg/mL、100 μg/mL、250 μg/mL、500 μg/mL和1 mg/mL万古霉素工作液10 μL,得到新鲜配制的自制质控品,质量浓度分别为2.5、5、10、25、50和100 μg/mL。
2.5 方法学验证
2.5.1 专属性考察:按照“2.1”项下色谱条件下进样,去甲万古霉素、万古霉素保留时间分别12.793 、17.707 min,与血清内其他成分分离良好,空白血清无干扰,见图1。

A.空白血清样品;B.血清+内标+万古霉素;1.去甲万古霉素内标;2.万古霉素A.blank serum; B.serum+internal standard+vancomycin; 1.norvancomycin; 2.vancomycin
2.5.2 标准曲线及最低定量限的建立:取“2.4”项下各质量浓度的自制血浆质控品,分别加入去甲万古霉素20 μL,混匀30 s后加入10%高氯酸溶液100 μL,涡旋1 min,12 000 r/min离心10 min(离心半径6 cm),取上清液80 μL,按照“2.1”项下色谱条件进样并测定。以万古霉素浓度(X,μg/mL)为横坐标,以万古霉素峰面积与内标峰面积比值(Y)为纵坐标进行线性回归,得回归方程,Y=0.059 4X-0.082 4,r=0.999 8,结果表明,万古霉素血清质量浓度在2.5~100 μg/mL线性良好,血清中最低定量限为0.5 μg/mL。
2.5.3 精密度及回收率测定:取新鲜配制的高、中、低浓度质控品(质量浓度分别为50、25、10 μg/mL),按照“2.1”项下色谱条件进样分析。每个浓度平行操作6次,计算日内精密度;连续测定3 d,计算日间精密度。同时,取新鲜配制的高、中、低浓度质控品,按照“2.1”项下色谱条件进样分析,万古霉素色谱峰面积与内标色谱峰面积比值代入相对应的随行标准曲线中,每个浓度平行操作6次,计算日内回收率;连续测定3 d,计算日间回收率。结果均满足《中华人民共和国药典:四部》(2020年版)[9]中生物样品检测的要求,见表1。

表1 万古霉素血药浓度监测室内质控精密度和回收率结果(n=6)
2.5.5 绘制Z-分数质控图:由于选择了3个质控浓度,为了多水平、更直观准确地进行质量控制,在Levey-Jennings质控图基础上,将低、中、高浓度质控样品转换成Z-分数形式,绘制在单张质控图进行比较。转换公式为,Z=(x-xmat)/s,x为质控品测定值,xmat为同一水平质控品测定值的平均值,s为该质控品的标准差[10]。运用Excel软件绘制Z分数图(见图2),结合Westgard 12 s/13 s/22 s/R4 s/41 s/10x多规则质控原则,当出现1次2<|Z|<3时,违反12 s规则,提出警告1次,当出现1次|Z|>3时,违反13 s规则,提出失控1次;当连续2次出现2<|Z|<3时,违反22 s规则,或连续2次Z之间差值>4,违反R4 s规则,提示失控;连续4次|Z|>1,违反41 s规则,或连续10次|Z|>0,违反10x规则,均提示失控。结果显示,高浓度质控品第22次、第23次2次Z差值为4.08,违反R4 s规则,提示失控1次,经分析考虑为随机误差所致。查找原因发现为操作人员不同所致,后调整操作人员重新操作测定后未有误差出现。
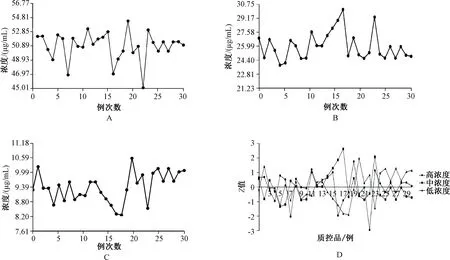
A.高浓度质控品Levey-Jennings质控图;B.中浓度质控品Levey-Jennings质控图;C.低浓度质控品Levey-Jennings质控图;D.高、中、低浓度质控品Z-分数质控图A. Levey-Jennings chart of high concentration quality control samples; B. Levey-Jennings chart of medium concentration quality control samples; C. Levey-Jennings chart of low concentration quality control samples; D. Z-score charts of high, medium and low concentration quality control samples
2.6 万古霉素血药浓度监测数据
2020年6—8月测定万古霉素39例次,共29例患者,其中6例患者测定2次,1例患者测定5次。首次总体监测结果显示,仅41.38%的万古霉素血药谷浓度在正常范围内,低于正常范围的有9例,高于正常范围的有8例;万古霉素血药谷浓度监测≥2次的7例患者中,4例经剂量调整后,万古霉素血药谷浓度恢复至正常范围;万古霉素治疗期间,共2例患者发生肾损伤,其万古霉素质量浓度均>20 μg/mL,见表2。
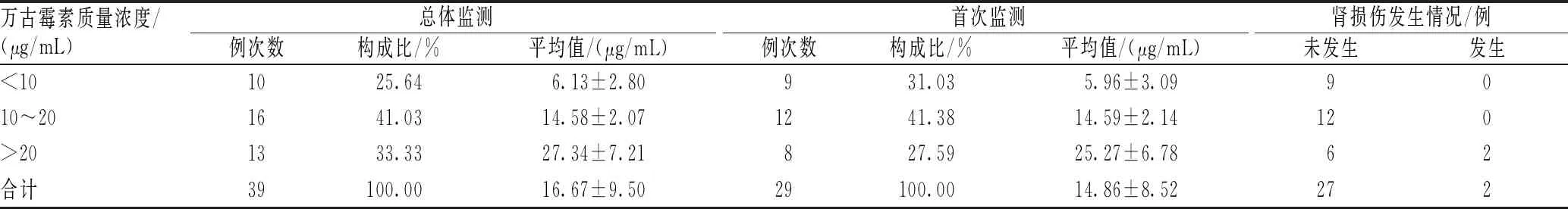
表2 万古霉素血药谷浓度总体监测和首次监测浓度分布及肾损伤发生情况
3 讨论
万古霉素是治疗MRSA感染的主要药物之一,但其治疗指数窄,个体差异较大[11-12]。若血药浓度过低,达不到治疗效果,易产生耐药;血药浓度过高,则易引起不良反应(如肾毒性、耳毒性等),因此,根据万古霉素血药浓度监测结果进行个体化用药方案的调整,保证患者达到安全、有效的治疗效果尤为重要[13-14]。而治疗药物监测结果的准确性是临床制定和调整个体化给药方案的重要影响因素之一,质控方法的建立在一定程度上可以保证样品测定的准确性及稳定性,因此,建立一套完整的质控体系以保证监测结果的准确性是非常重要的。
自制万古霉素质控血清制备方法简单、成本低廉,其可行性已有文献报道[8]。绘制Levey-Jennings质控图是实验室常用于判断质控样本合格与否的方法,其通过上下警戒线、失控线来对质控结果进行简单判定,但只对随机误差敏感,且只能显示单个浓度测定的精密度。而Z-分数质控图可用于多水平的质控物,全面反映多个浓度的质控结果[15]。Westgard多规则质控规则中的13 s规则和R4 s规则可及时发现随机误差,22 s规则、41 s规则和10x规则可及时发现系统误差,Westgard多规则质控规则与Levey-Jennings质控图和Z分数质控图联合,不仅可以更为准确地判定测定结果的准确性,还可以在发生失控时,确定失控类型,为失控原因的确定提供帮助[16-18]。
通过本实验室连续性质控评价发现,本批次自制万古霉素质控血清共发生警告4次,失控1次,失控发生于高浓度质控品,第22次、第23次2次Z差值为4.08,违反R4 s规则。当发生失控时,及时查明原因,排除误差,分析可能存在的影响因素并及时纠正,以保证血药浓度检测结果的准确性是十分必要的。因此,实验中应详细记录试剂批号、操作人员、定标日期、实验室环境、冰箱温度、测定中的异常现象、仪器的校正及故障等信息,以便及时发现造成误差的原因。根据我院实验室情况,分析产生随机误差的原因主要为环境温度改变、操作人员不同等;产生系统误差的原因主要为试剂的“瓶底效应”、移液枪的校正等[19-20]。
目前,国内外指南推荐成人万古霉素有效谷浓度为10~20 μg/mL,新生儿/儿童患者万古霉素谷浓度维持在5~15 mg/L[21]。指导剂量调整最关键和实用的为万古霉素血药谷浓度[22]。按照常规剂量(15 mg/L,每12 h给药1次)给药时,其导致肾功能损害的发生率为1%~5%[2,23]。本研究初步统计了2020年6—8月29例患者万古霉素血药浓度测定结果,结果显示,仅有41.38%的患者万古霉素血药浓度在正常范围内,与文献中的达标率基本一致[24]。多次进行万古霉素血药谷浓度监测的7例患者中,4例通过调整用药方案再次监测血药浓度恢复至正常范围,肾损伤发生率为6.90%,略高于文献报道[2,23]。分析原因,首先,本研究分析例数偏少;其次,我院万古霉素监测人群均为老年人及危重症患者,该人群脏器功能差,联合用药较多,发生肾损伤患者的万古霉素血药浓度均>20 μg/mL,可知肾毒性的发生与血药浓度过高有着密切联系[25-26]。
本研究较为全面地建立了HPLC法测定万古霉素血药浓度的质控评价方法,应用Levey-Jennings质控图联合Westgard多规则理论进行质控评估,能够提高误差的检测灵敏度并提示误差的性质,以便发现各种测定误差并及时纠正,保证血药浓度测定的准确性,为临床制定合理的个体化给药方案提供准确参考。

