水热法合成CTAB改性污泥生物炭对酸性橙Ⅱ的吸附去除
牛 芳 , 李国亭 , 周永康 , 陈 焕 , 张树德 , 刘迎旭
(1.华北水利水电大学 环境与市政工程学院 , 河南 郑州 450011 ; 2.郑州污水净化有限公司 , 河南 郑州 450000)
全球每年生产大量的染料并应用于许多不同的行业,包括纺织、化妆品、造纸、皮革、制药和食品行业等[1]。染料废水的处理和排放成为工业废水处理中的一个重要问题。处理染料废水最常用的工艺方法有吸附、絮凝、过滤和沉降等,在这些技术中,吸附因其有效、高效、经济的优点被广泛使用。近年来,一些新型的复合吸附剂因其对特定污染物的去除特别有效而备受关注 ,这些复合吸附剂集合各部分物质的优点和特性,具有良好的应用前景[2-3]。
研究发现,生物炭具有丰富的孔隙结构、较大的比表面积和丰富的官能团,这些结构特点使生物炭具备良好的吸附能力[4-5]。随着工业企业数量和城市规模日益扩大,工业废水和生活污水的排放量随之增加,作为污水处理副产物的污泥产量逐年递增,在污泥处置方式中将污泥变废为宝,实现资源化利用是当前研究的热点。污泥生物炭是以污水厂的污泥为原材料经过水热碳化法、微波热解法和热裂解法等方法制成的生物炭。污泥生物炭表面含有羟基和羧基等含氧官能团,能提供使污染物附着的吸附点位,在进行吸附过程时污染物与生物炭表面基团形成氢键等从水中去除[6]。有研究表明,使用表面活性剂改性的生物炭可以提升对染料废水的去除效果[7]。本实验使用污水厂二沉池污泥作为碳源,通过水热法制备CTAB改性的污泥生物炭,将其用于吸附去除废水中的染料酸性橙Ⅱ。通过考察一系列影响因素对吸附的影响,探讨CTAB改性污泥生物炭吸附酸性橙Ⅱ的动力学和热力学等吸附行为,为CTAB改性的污泥生物炭的实际应用提供技术支持。
1 材料与方法
1.1 实验材料及设备
制备污泥生物炭所用污泥取自郑州市马头岗污水处理厂二沉池。CTAB(溴化十六烷基三甲铵)和酸性橙Ⅱ(质量分数>95%),购于上海阿拉丁生化科技股份有限公司,实验所用其他化学试剂均为分析纯,实验用水为去离子水。
1.2 改性污泥生物炭的制备
采用水热法制备CTAB改性污泥生物炭,分别称取CTAB 0.04、0.2、0.6、1.0、1.4 g,对应CTAB含量分别为0.2%、1.0%、3.0%、5.0%、7.0%,加入20 mL蒸馏水搅拌30 min。称取2.0 g污泥,加至不同浓度的CTAB溶液中并搅拌15 min。混合物转移至反应釜中高温高压(160 ℃、6 h)处理后冷却至室温,抽滤(压力<0.9 MPa),烘干12 h,得到实验所用改性污泥生物炭,标记为CTAB-X%/BC(X为CTAB含量)。不添加CTAB,重复上述操作制备未改性污泥生物炭,标记为BC。
1.3 吸附实验
配制1 000 mg/L酸性橙Ⅱ溶液为母液,实验时取母液稀释至所需浓度。称取20 mg污泥生物炭,量取50 mL的20 mg/L酸性橙Ⅱ溶液,在恒温振荡培养箱中以140°/min振荡24 h。振荡结束后,用0.45 μm的滤膜过滤,在480 nm波长下用紫外可见分光光度计(UV mini1240,日本岛津公司)测量酸性橙Ⅱ的吸光度。溶液pH值条件影响实验以HCl和NaOH调节pH值。动力学实验调节溶液在pH值分别为5、7、9条件下,向1 000 mL酸性橙Ⅱ溶液(20 mg/L)中加入将400 mg污泥生物炭,磁力搅拌器搅拌,在一定的时间间隔取样、过滤、测量。吸附热力学实验在298、308、318 K下进行。除了吸附等温线实验,反应温度控制在298 K。上述实验重复两次。
酸性橙Ⅱ去除率R和污泥生物炭对酸性橙Ⅱ的单位吸附量qe计算公式:
(1)
(2)
式中:c0和ce分别为溶液初始浓度和吸附平衡时浓度,mg/L;V为溶液体积,L;m为所用生物炭质量,g。
2 结果与讨论
2.1 改性污泥生物炭的吸附性能对比
在中性条件下对未改性污泥生物炭和CTAB改性污泥生物炭去除酸性橙Ⅱ进行研究,结果见图1。
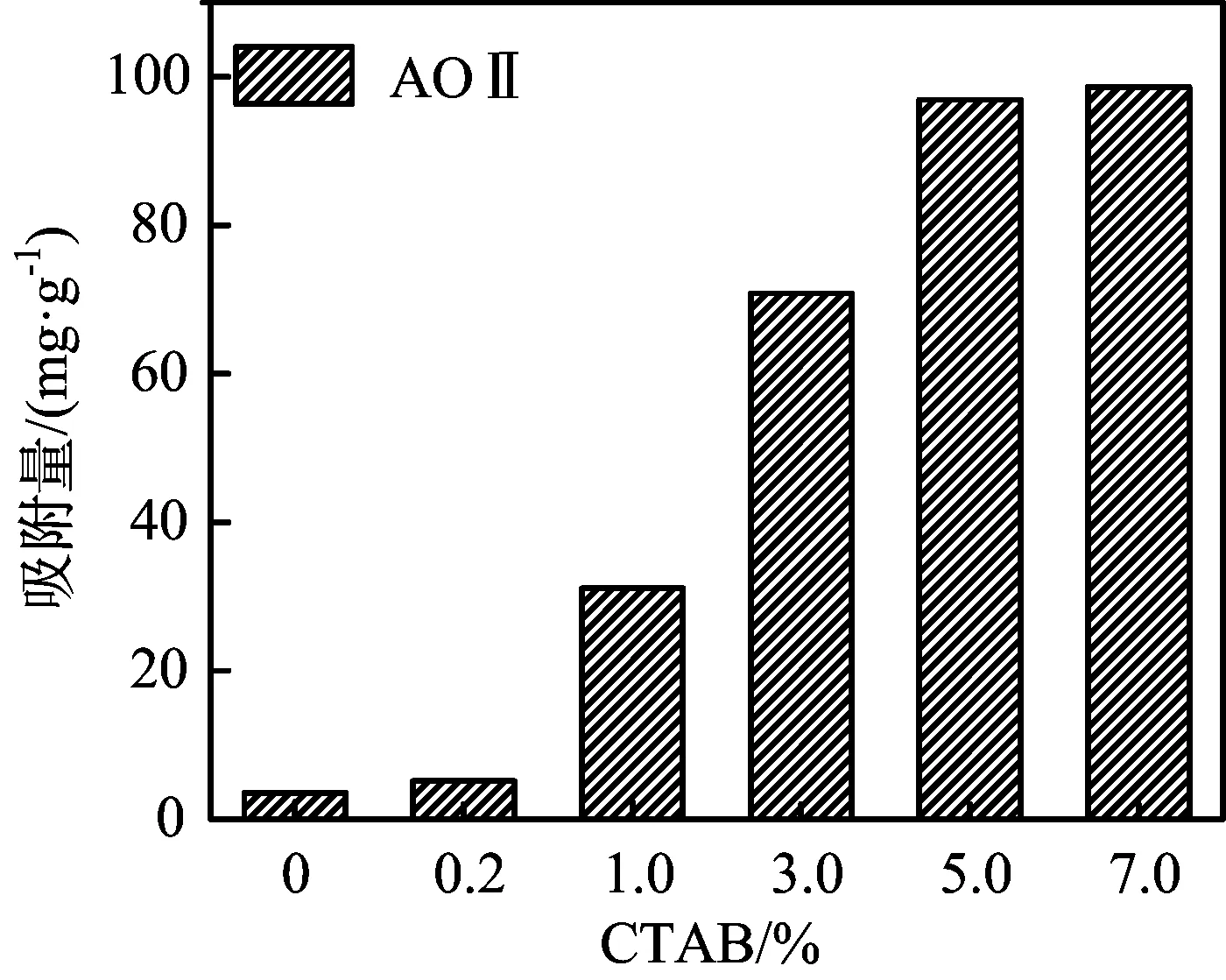
图1 中性pH值下不同改性污泥生物炭的吸附性能对比
由图1可知,经过改性后的污泥生物炭的平衡吸附量随CTAB浓度的增加而增加,这表明将CTAB负载至污泥生物炭上,可提高污泥生物炭对酸性橙Ⅱ的吸附去除能力。由于阳离子表面活性剂CTAB在污泥生物炭上的负载改变生物炭原料的表面电荷性质,促进对阴离子染料的酸性橙Ⅱ的吸附去除。浓度为7.0%的CTAB改性污泥生物炭是所选生物炭中去除效果最好的,其平衡吸附量98.6 mg/g,浓度为5.0%的CTAB改性污泥生物炭平衡吸附量96.9 mg/g。选择CTAB-5.0%/BC进行后续实验。
2.2 生物炭投加量对吸附的影响
CTAB改性污泥生物炭对酸性橙Ⅱ的吸附去除效果十分显著,在酸性橙Ⅱ浓度为20 mg/L时,改变CTAB-5.0%/BC加入量,考察其吸附效果,并和未改性污泥生物炭对比,结果如图2所示。
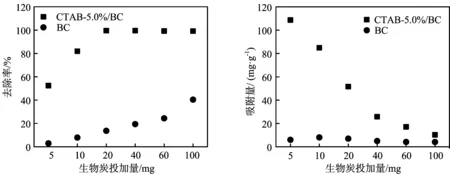
图2 生物炭投加量对酸性橙Ⅱ吸附行为对比
由图2可知,随着CTAB-5.0%/BC投加量的增大,去除率逐渐升高,同时平衡吸附量降低,去除率从投加量5 mg时的52.4%提高到投加量20 mg时的99.5%。未改性生物炭(BC)的去除率随投加量的增大而略有升高,平衡吸附量较小。在后续的实验中,选择CTAB-5.0%/BC投加量10 mg/(50 mL)溶液,酸性橙Ⅱ浓度为20 mg/L。
2.3 溶液pH值对吸附的影响
分别在初始pH值3、5、7、9和11条件下,考察CTAB改性污泥生物炭对酸性橙Ⅱ的吸附去除效果,并和未改性污泥生物炭的吸附效果对比,结果如图3所示。

图3 溶液初始pH值对改性污泥生物炭吸附能力的影响
由图3可以看出,在pH值3~5内,随着pH值的升高,CTAB-5.0%/BC对酸性橙Ⅱ的吸附去除效果提升,在pH值5时平衡吸附量最高,达到91.8 mg/g。在pH值5~11内,随着pH值的升高,生物炭的吸附量总体上在逐渐降低,从pH值5时的91.8 mg/g下降至pH值11时的59.2 mg/g。BC在不同初始pH值条件下的吸附去除效果均较低。
溶液的酸碱度可以通过改变吸附剂的表面官能团和酸性橙Ⅱ分子的解离来影响CTAB改性污泥生物炭对酸性橙Ⅱ的吸附。这是由于改性生物炭上的羧基和酚羟基等官能团对溶液酸碱度的变化敏感,改性生物炭在pH值较低时正电性增强,酸性橙Ⅱ是阴离子染料,两者静电吸引能力增强,所以吸附量较大;随着pH值升高,生物炭表面负电性增强,对阴离子染料的静电吸引能力减弱。据此,与实验中得到的结果一致,CTAB改性污泥生物炭在溶液呈酸性时对酸性橙Ⅱ的吸附能力最强。
2.4 共存离子及天然有机质对吸附的影响
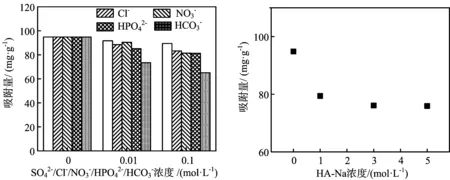
图4 共存离子及天然有机质对改性污泥生物炭吸附能力的影响
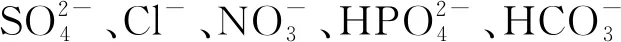
2.5 不同溶液pH值条件下的吸附动力学
在溶液pH值5、7和9的条件下进行实验,对数据进行准一级动力学模型、准二级动力学模型和Elovich模型模拟。根据模拟结果分析吸附反应的传质过程,探究吸附机理[8-11]。
准一级动力学模型描述外部传质过程,其非线性与线性表达式:
qt=qe(1-e-k1t)
(3)
ln(qe-qt)=lnqe-k1t
(4)
准二级动力学模型描述化学吸附过程,其非线性与线性表达式分别为:
(5)
(6)
Elovich模型:
qt=α+βlnt
(7)
式中:qe为平衡吸附量,qt为时刻吸附量,mg/g;t为吸附时间,min;k1和k2为准一级和准二级动力学模型的吸附常数,min-1;α和β为Elovich动力学模型吸附常数,单位分别为mg/g和g/(mg·min-1)。
吸附过程通常可分为快速反应阶段、缓慢反应阶段和反应平衡阶段三个过程。对pH值5、7和9的实验数据使用非线性回归法拟合,pH值7吸附量拟合曲线结果如图5所示。
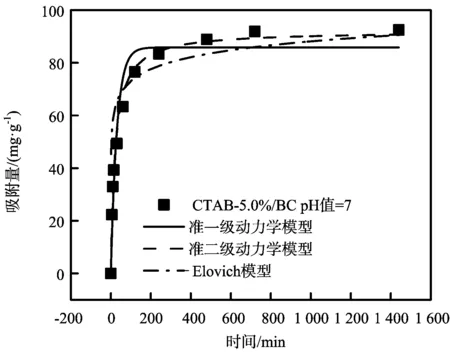
图5 CTAB改性污泥生物炭吸附酸性橙Ⅱ的非线性动力学拟合曲线图
由图5可知,在pH值为7,反应最开始的2 h是反应速率最快的阶段,2~8 h吸附反应速率有所下降,8 h后逐渐趋于反应平衡。
各非线性动力学方程的拟合参数见表1。根据拟合结果可知,准二级动力学模型拟合效果更好,相关系数R2均在0.92以上,这表明 CTAB改性污泥生物炭对酸性橙Ⅱ的吸附过程可能是化学吸附。
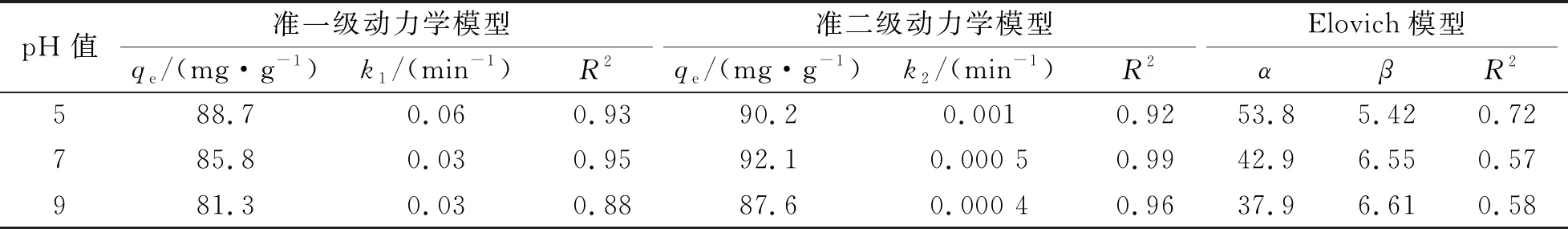
表1 不同pH值条件下CTAB改性污泥生物炭吸附酸性橙Ⅱ的动力学模型拟合参数
为了使结果更具有说服力,对动力学数值用准一级动力学和准二级动力学模型进行线性模拟,结果如图6所示;线性动力学方程的拟合参数见表2。在pH值5、7、9拟合结果中,准二级动力学模型相关系数R2值均大于0.99,证明准二级动力学模型更适合于描述该动力学吸附过程。
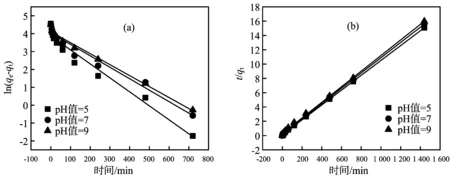
图6 CTAB改性污泥生物炭吸附酸性橙Ⅱ的动力学线性准一级(a)和准二级(b)拟合曲线
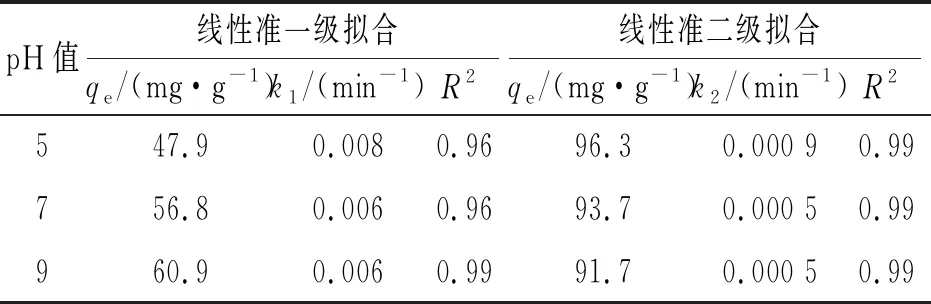
表2 CTAB改性污泥生物炭吸附酸性橙Ⅱ的线性准一级和线性准二级动力学拟合参数
2.6 吸附热力学与吸附等温线
在298、308、318 K条件下,考察吸附去除效果,结果如图7所示。
由图7可知,在所选的温度梯度中,温度越高吸附量越低,说明升温不利于吸附的进行,该吸附过程是放热过程。
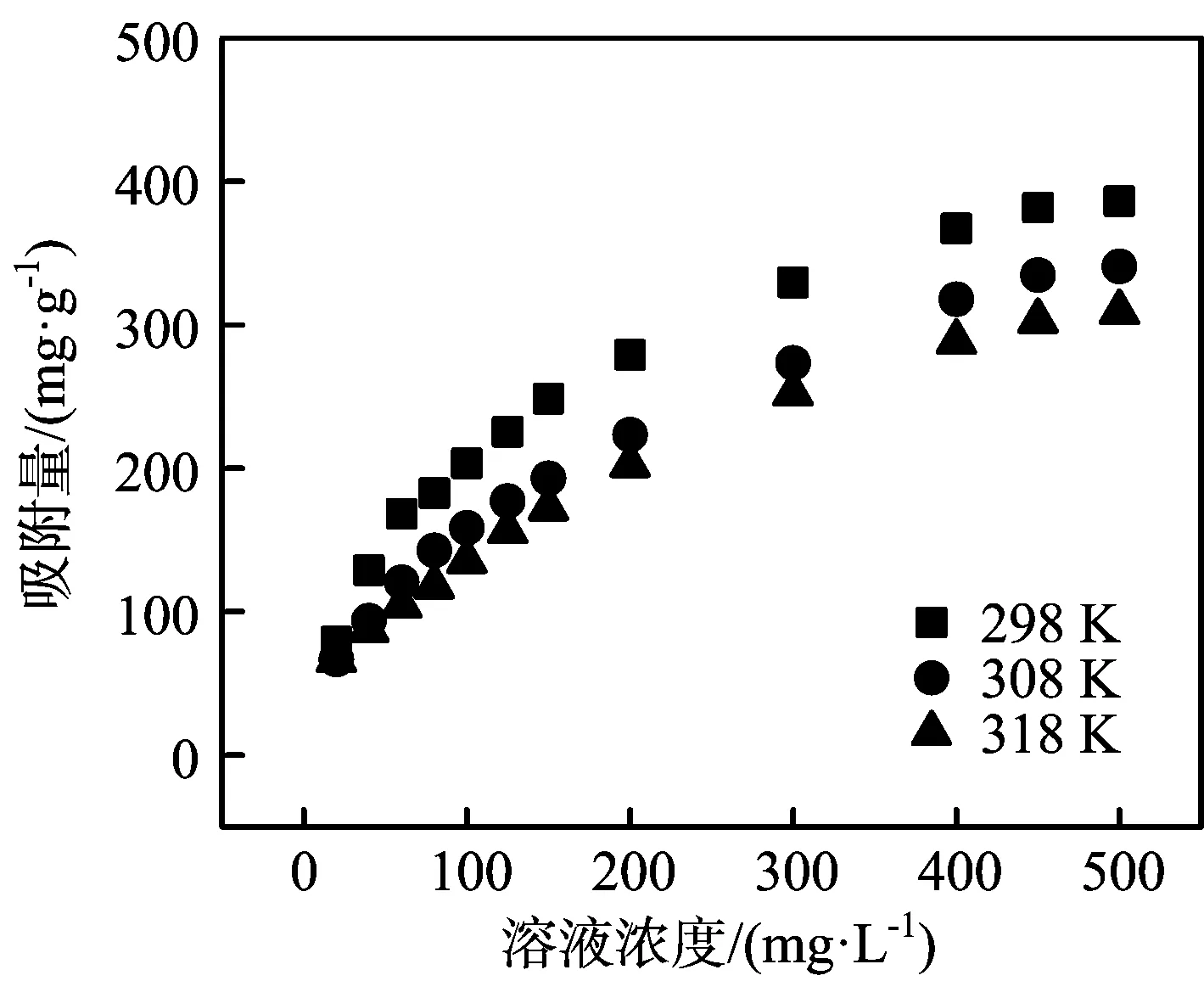
图7 不同温度下CTAB改性污泥生物炭平衡吸附量随溶液浓度变化图
为了研究吸附剂与吸附质间相互作用,分别在298、308、318 K下研究了吸附等温线。对3个温度下的实验数据分别用Langmuir、Freundlich、Temkin、Toth、Koble Corrigan和Dubinbin-Radushkevich (D-R)等温式进行拟合。
Langmuir等温式为假设吸附质在吸附剂固体表面是单分子层吸附,吸附剂表面能量均一,忽略吸附质分子之间的作用力[12]。
(8)
式中:kL为与吸附质和吸附剂之间亲和力相关的平衡常数,L/mg;qm为最大吸附量, mg/g。
Freundlich等温式为由实验规律总结得出的经验方程,通常描述多分子层吸附[13]。
(9)
式中:kF和n为Freundlich常数。
Temkin等温式:
qe=A+BlnC
(10)
式中:A和B为不均匀因子[14]。
Toth等温式是Langmuir等温式中引入不均匀能量参数t的变形式[15]。
(11)
式中:k为与吸附剂的吸附容量和强度有关的参数;t为不均匀能量参数。
Koble Corrigan等温式为Langmuir等温式和Freundlich等温式结合的公式,用于描述同时发生单分子层吸附和多分子层吸附[16]。
(12)
式中:A、B和n均为与吸附相关的常数。
D-R等温式是建立在微孔填充理论上的吸附等温方程。微孔填充理论认为,由于微孔内部孔壁间发生吸附力场的重叠,使微孔内部吸附势显著增强,因此在微孔中吸附质分子不再像在中孔和非孔性表面上发生单分子层或多分子层的吸附,而是按吸附势大小依次实现孔容积的逐步填充[17]。
qe=qme[-kln(1+1/C)]
(13)
式中:k是与吸附容量相关的参数。
吸附等温线模型拟合结果如图8和表3所示。
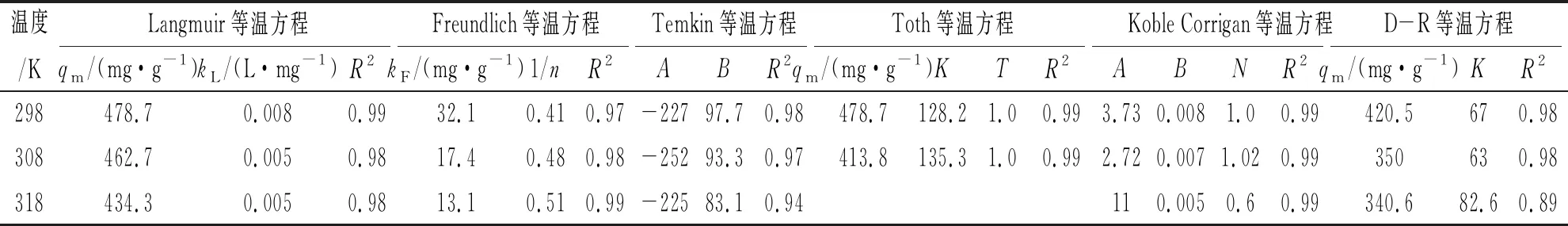
表3 不同温度下CTAB改性污泥生物炭吸附酸性橙Ⅱ的热力学拟合参数参数
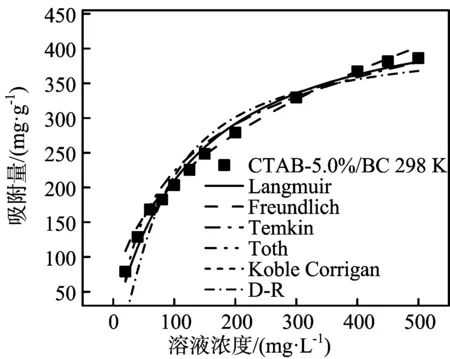
图8 298 K下CTAB改性污泥生物炭上酸性橙Ⅱ的吸附等温线
对比6种等温吸附模型可知,6种等温吸附模型均能较好的模拟酸性橙Ⅱ在CTAB-5.0%/BC上的吸附过程,其中Koble Corrigan 模型拟合效果最好,3个温度下的相关系数R2均大于0.99。说明CTAB改性污泥生物炭对酸性橙Ⅱ的吸附过程为单分子层吸附和多分子层吸附共同作用的结果,同时还伴随有微孔填充的过程。
3 结论


